作為普外科的一個主要亞專科,肝膽外科對干細胞外泌體療法治療引起了極大的關注。
首先,急性肝損傷(ALI)/急性肝衰竭(ALF)是一種罕見但具有挑戰性的綜合征,表現為肝功能障礙、凝血病、腦病和多器官衰竭。大約60%的ALF病例需要接受原位肝移植或導致死亡。
肝膽外科作為普外科的一個重要亞專業,在干細胞外泌體療法治療方面引起了極大的關注。
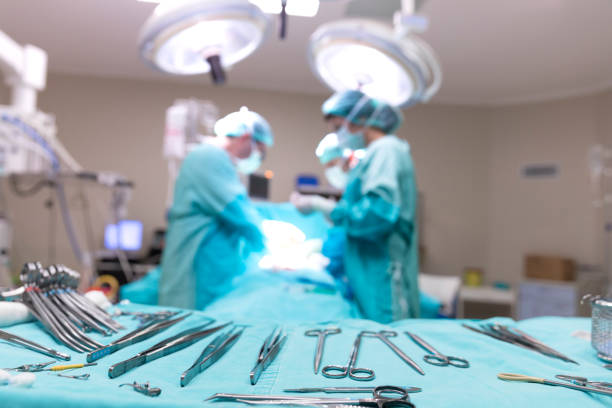
干細胞外泌體療法治療普通外科疾病
在一項研究中,Lin的團隊關注ALI的細胞死亡方面,發現間充質干細胞衍生的外泌體可通過穩定四氯化碳誘導的ALI中的SLC7A11防止鐵變態反應。
另外,Shao的研究小組關注外泌體分離前的修飾,發現臍帶間充質干細胞衍生的外泌體可通過外泌體 miR-455-3p改善IL-6誘導的ALI。其次,與ALI不同,肝纖維化發生于肝臟遭受慢性損傷時,可能發展為肝硬化、肝衰竭、肝細胞癌甚至死亡。
此外,Wang等人發現,源自三維人ESC球體的外泌體可通過外泌體miR-6766-3p使Smad通路失活,從而減弱肝星狀細胞的活化并抑制肝纖維化。對于需要進行肝移植的終末期肝纖維化患者來說,肝臟缺血再灌注損傷(IRI)是導致移植物功能障礙和器官排斥的嚴重并發癥。
最后,急性胰腺炎是一種不可預測且可能致命的疾病,其預后主要取決于是否發展為多器官功能障礙綜合征。Chen等人發現,iPSC衍生的間充質干細胞外泌體可通過Akt/Nrf2/HO-1通路改善重癥急性胰腺炎引起的心肌損傷。
作為一種無細胞療法,胎盤間充質干細胞衍生的外泌體輸注可通過激光多普勒血流分析促進小鼠耳廓缺血損傷模型中的血管生成。
- 從機理上講,間充質干細胞衍生的外泌體不僅能在體外促進管樣結構的形成,還能在體內動員內皮細胞進入皮下Matrigel塞,這主要是通過外泌體促血管生成微RNA(如miR-30b)實現的。此外,造血干細胞衍生的外泌體可修復小鼠缺血的后肢,改善肢體灌注、毛細血管密度、運動功能及其截肢情況。這很可能是內皮細胞相對于平滑肌細胞和成纖維細胞內化外泌體miR-126-3p的結果。
人類iPSC衍生的外泌體通過外泌體miR-199b-5p顯示了類似的新血管生成效應。另一方面,血管內再通術正越來越多地用于重建缺血區域的血流,恢復外周動脈疾病患者的組織損失或壞疽。
三個獨立研究小組均證明,在氣球誘導的血管損傷大鼠模型中,EPC衍生的外泌體可通過增強內皮細胞功能促進血管修復并加速血管再內皮化。此外,Kong等人通過抑制新內膜增生,證明了EPC衍生的外泌體對球囊損傷具有類似的保護作用。這種保護作用是通過促進血管再內皮化和抑制再狹窄實現的,而不是通過直接抑制平滑肌細胞的增殖和遷移實現的。
McCulloh 和他的同事發表了一項關于干細胞外泌體療法治療壞死性小腸結腸炎 (NEC) 的有趣研究,對于需要手術的早產兒來說,NEC的總體死亡率超過30%。作者比較了源自四種不同類型干細胞(即羊水MSC、骨髓MSC、羊水NSC和新生兒腸NSC)的外泌體的治療效果。當以至少4×108的濃度注射時,所有類型的 SC-exo都被證明可以像其親代干細胞一樣有效地降低實驗性NEC的發生率和嚴重程度。
膿毒癥是普外科中一種致命且可能可預防的并發癥,其中微血管功能障礙導致多器官衰竭和死亡。Zhou及其同事使用盲腸結扎穿刺 (CLP) 建立的小鼠膿毒癥模型,證明EPC衍生的外泌體可以改善膿毒癥結局。這表現為通過外泌體miR-126-5p和miR-126-3p減少了肺和腎血管滲漏、改善了器官功能并提高了存活率。
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。




 掃碼添加官方微信
掃碼添加官方微信