中樞神經系統 (CNS) 疾病,包括中風、阿爾茨海默病、帕金森病和脊髓損傷 (SCI),可導致殘疾和死亡,每年影響數百萬人 。然而,目前尚無治愈性療法來阻止或逆轉其進展。神經干細胞 (NSC) 移植由于其能夠分化為各種神經元和神經膠質細胞類型且腫瘤發生風險極小,可能成為中樞神經系統疾病的下一代治療替代方案。
近日 ,國際權威期刊雜志《Transplant Immunology》發表了一項“在腦內鑒定同種異體及異種神經干細胞的免疫原性以及減輕移植排斥的策略”的研究[1]。

在這項研究中,我們展示了同基因、同種異體和異種神經干細胞移植引發的神經炎癥反應,并評估了環孢素A(CyA)和甲潑尼龍(MP)對移植物排斥的免疫抑制作用。
研究結果顯示,異種神經干細胞移植誘導了中性粒細胞、小膠質細胞 / 巨噬細胞、CD4+和CD8+T細胞的浸潤,而同種異體移植主要觸發小膠質細胞/巨噬細胞的募集。兩種移植類型均導致移植細胞數量急劇下降。CyA和MP的聯合治療顯著減輕了異種免疫排斥反應,并顯著增加了腦內存活的移植細胞數量。同樣,MP單一療法有效降低了同種異體排斥反應,提高了移植細胞的存活率。
總體而言,同種異體神經干細胞移植主要觸發先天性免疫,而異種移植則引發先天性和適應性免疫反應。因此,異種移植需要CyA和MP聯合治療,而MP單一療法可減輕同種異體移植中的排斥反應。我們的研究結果可能為減輕腦內同種異體和異種神經干細胞移植排斥提供了一種策略,從而為各種中樞神經系統疾病的臨床前和臨床應用中基于神經干細胞的治療優化微環境。
為什么要進行這項研究?目前干細胞治療神經中樞神經系統疾病的主要挑戰是什么?
目前基礎和臨床研究發現,源自成人人體的神經干細胞(ahNSCs)在嚙齒類動物模型中對中風、阿爾茨海默病和脊髓損傷顯示出積極的治療作用。
然而,將干細胞療法應用于患者仍面臨諸多挑戰,包括細胞存活率低、人與嚙齒類動物免疫系統的差異,以及移植排斥反應。許多研究發現,免疫反應和移植排斥會導致移植物損傷并惡化其功能。此外,嚙齒類動物模型與人類患者移植后的免疫反應存在顯著差異,這可能是許多臨床前研究未能轉化為人體試驗或大型動物模型的原因。
因此,降低移植排斥可能有助于移植細胞的存活和發揮療效,并在嚙齒類動物與人類之間創造相似的免疫環境。
免疫抑制劑已成功用于預防器官移植中的同種異體排斥反應,也可能提高干細胞的存活率。在我們及其他先前的研究中,環孢素A(CyA)被用于改善移植ahNSCs的持久性,但其抑制效果并不理想。此外,許多研究表明,將作用機制不同的免疫抑制劑聯合使用,對干細胞治療的效果優于單獨使用CyA。
因此,為延長移植物存活并為移植創造一致的免疫環境,可針對每種移植類型和實驗條件選擇最佳的免疫抑制劑組合。在多種免疫抑制劑中,甲潑尼龍(MP)作為一種對先天性免疫系統具有廣泛抗炎作用的糖皮質激素,與抑制T淋巴細胞介導免疫反應的CyA,可能是理想的聯合用藥選擇。
本研究評估了同基因、同種異基因和異種神經干細胞移植入腦后在體內誘導的免疫應答的差異。基于這些免疫學差異,分別在同種異基因和異種NSCs移植中,分別單獨或聯合使用CyA和MP以最大限度延長移植物存活,并研究其對腦內移植免疫應答的影響。
什么是異種神經干細胞移植:簡單來說,異種神經干細胞移植就是“把人的神經干細胞種到動物腦子里”,用于模擬人類細胞治療,但因物種差異會引發猛烈排斥,是藥物開發和再生醫學研究中的重要工具模型。
神經干細胞的特性
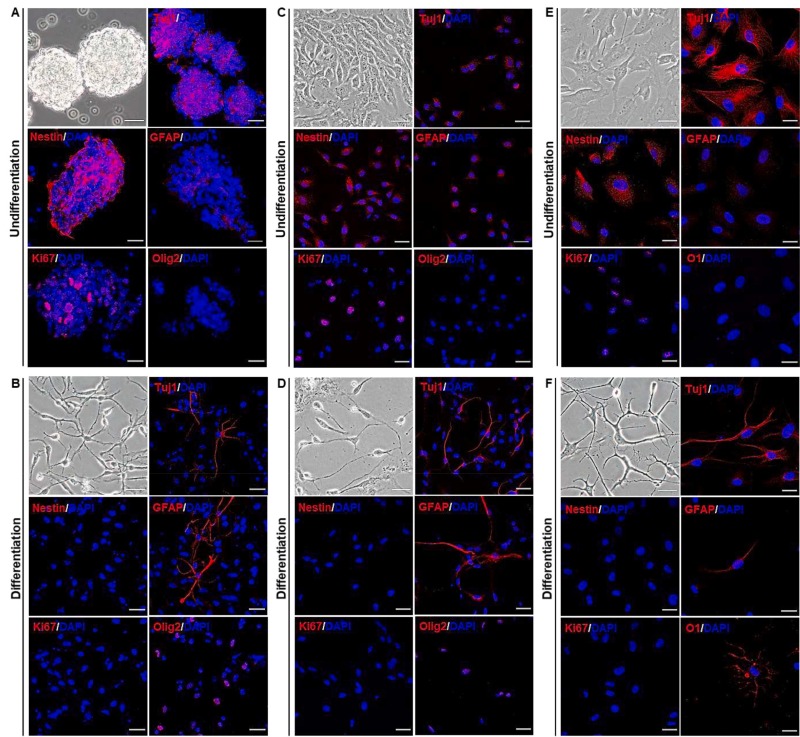
細胞來源與移植驗證:本研究使用了三種來源的神經干細胞(NSCs):C57BL/6小鼠胎腦(B6NSC,圖1A、B)、ICR小鼠胎腦(ICRNSC,圖1C、D)和成人顳葉(ahNSC,圖1E、F)。
通過H&E染色證實,這些細胞被成功移植到免疫活性C57BL/6小鼠的紋狀體內。與僅注射緩沖液(出現組織損傷且無細胞團)的對照組不同,注射了三種NSCs的組(同基因B6組、同種異體ICR組、異種ahNSC組)均在注射部位形成了明顯的細胞團。同種異體ICRNSCs和異種ahNSCs的成功移植還分別通過其特異性標志物H2Kd和STEM121分別證實移植成功,表明各組NSCs均已正確注射至紋狀體。
核心特征與分化潛能:無論來源如何,所有三種來源NSC均表達NSC特異性標志物巢蛋白和增殖標志物Ki-67(圖1A、C、E)。在未分化狀態下,一些NSC表達分化的神經細胞標志物,包括Tuj1(神經元)和GFAP(星形膠質細胞)(圖1A、C、E)。
分化后,NSC失去了巢蛋白和Ki-67的表達,而顯示出發芽和延伸的神經突,即分化神經細胞的形態(圖1B、D、F)。此外,一些細胞強烈表達Tuj1、GFAP、Olig2或O1(圖1B、D、F)。Olig2和O1是少突膠質細胞的特異性標志物。這些特征(巢蛋白/Ki-67表達、分化后特定標志物表達和形態變化)共同證實了所用細胞是具有多向分化潛能的神經干細胞。
大腦對移植神經干細胞的免疫反應
為評估大腦對不同來源移植神經干細胞(NSCs:同基因B6、同種異體ICR、異種人類NSCs分別代表自體、同種異體、異種移植)的免疫反應(圖2),研究將細胞注射到C57BL/6小鼠基底神經節,并監測至移植后6天。
免疫組化分析顯示,所有移植組均出現CD45陽性白細胞逐漸增加(圖2A),其中異種移植組在移植后第4天和第6天的白細胞數量顯著高于其他組,同種異體移植組在第6天也顯著高于對照組(僅注射緩沖液)。類似增加模式也見于中性粒細胞(圖2B)、小膠質細胞/巨噬細胞(F4/80(圖2C)+、Iba-1(圖2D))以及T細胞(CD8-(圖2E)、CD4+(圖2F)),尤其異種移植組的中性粒細胞(移植后2-4天)和T細胞(移植后4-6天)激增最為顯著。
結果表明,腦內注射本身即可激活先天免疫(如中性粒細胞、小膠質細胞/巨噬細胞),同種異體移植會加劇此反應,而異種移植則在先天免疫激活后,于移植后1周內進一步引發了適應性免疫反應。
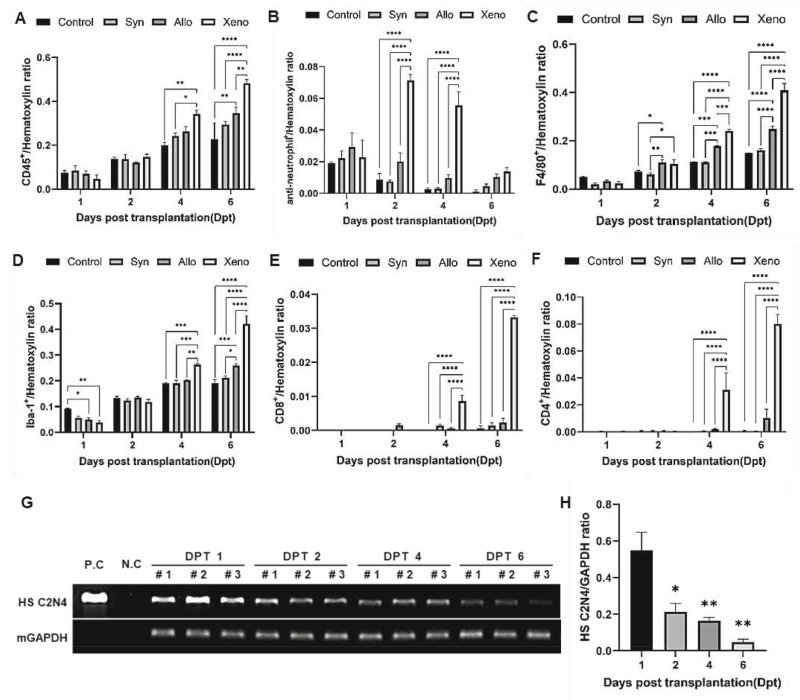
此外,當利用針對人類細胞質的免疫組織化學(IHC)檢測受體小鼠腦內的人類神經干細胞(圖S2)以及利用人類特異性序列HS C2N4的PCR檢測(圖2G、H)時,發現人類細胞逐漸減少。這與免疫系統的激活相反,提示免疫反應可能影響移植神經干細胞的存活。
免疫抑制劑對異種神經干細胞存活的影響
為評估免疫抑制劑對異種(人類)神經干細胞(NSCs)移植后免疫反應和細胞存活的影響,研究使用了靶向先天免疫的甲潑尼龍(MP)和靶向適應性免疫的環孢素A(CyA)。
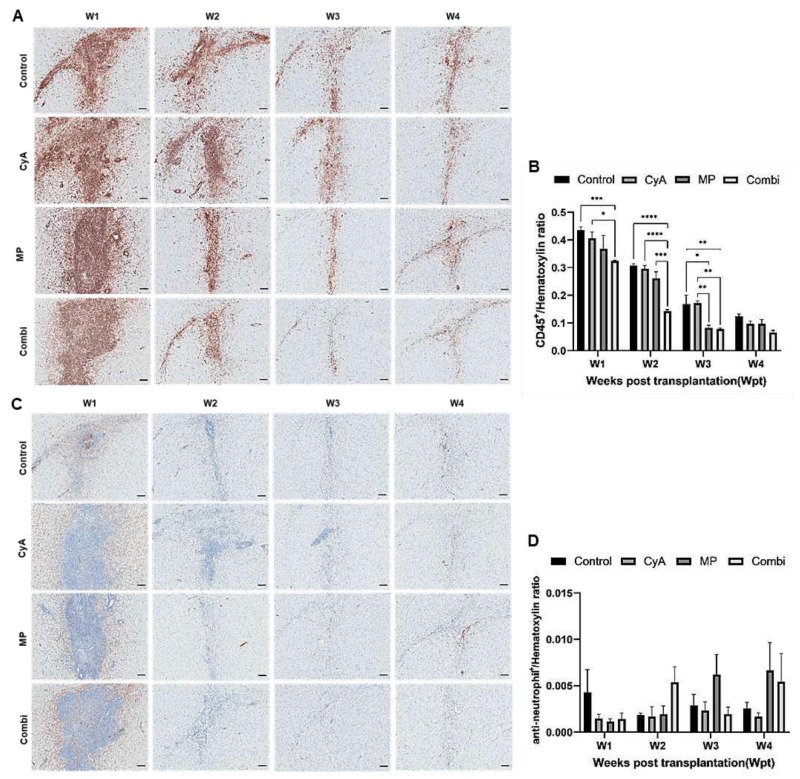
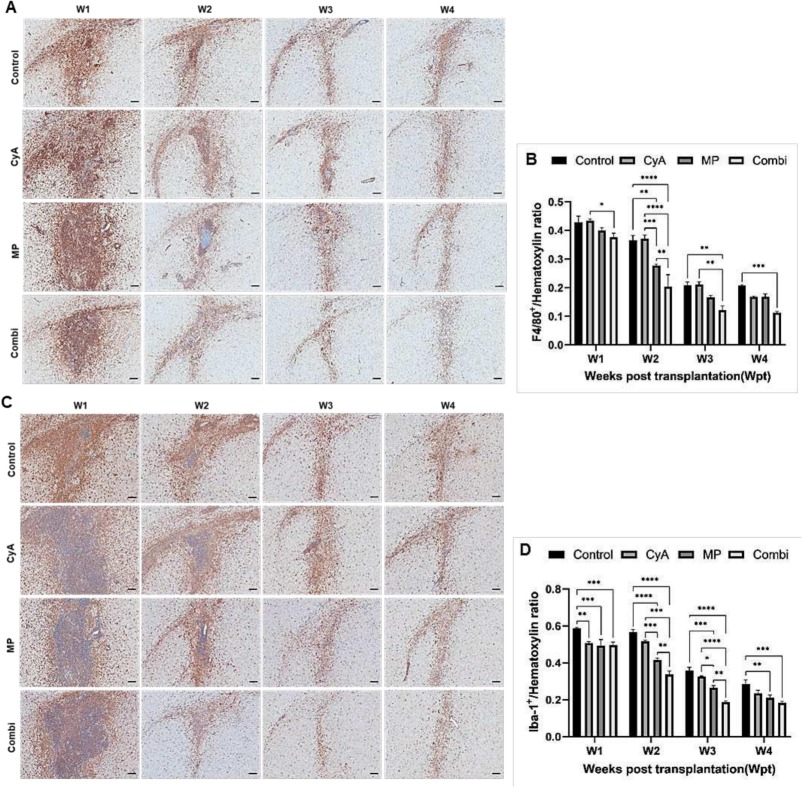
免疫組化(IHC)顯示,全身性給予MP或CyA+MP組合,在異種移植后1周至3周期間,能顯著減少大腦中CD45陽性浸潤白細胞的數量(圖3A)。然而,在CyA組中并未觀察到這種影響 (圖3A)。在異種移植后第2周,CyA+MP組與MP單一療法相比表現出明顯更高的效力 (圖3A)。雖然免疫抑制劑在中性粒細胞中的作用不明顯(圖3B),但在F4/80(圖4A、B)或Iba-1陽性的小膠質細胞/巨噬細胞(圖4C、D)以及CD8(圖5A、B)或CD4(圖5C、D)陽性T細胞群中均觀察到CyA和MP的免疫抑制作用,然而CyA組的CD8陽性T細胞數量也顯著減少(圖5A、B)。

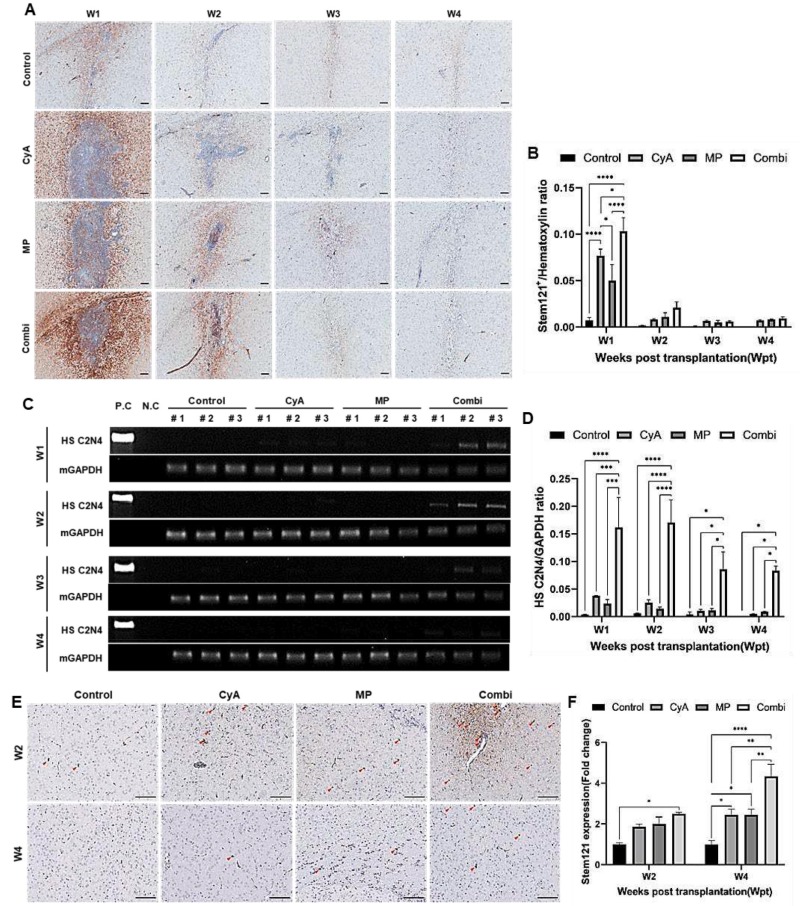
此外,研究通過免疫組化(IHC)和PCR檢測發現,聯合使用環孢素A(CyA)和甲潑尼龍(MP)進行免疫抑制治療,在移植后第1周顯著提高了受體小鼠大腦注射部位人類神經干細胞(NSCs)(圖6A、B)的存活數量及其特異性基因(HS C2N4)(圖6C、D)的表達水平;雖然在移植后2-4周,注射部位核心區細胞顯著減少,但在其周邊區域檢測到了更多人類NSCs(圖6E、F),說明移植的人NSCs遷移到附近的腦實質中。總之,結果表明,先天性和適應性免疫的雙重抑制可能為移植的異種移植細胞在腦內的存活創造更有利的環境。
免疫抑制劑對同種異體神經干細胞存活的影響
在神經干細胞(NSCs)的同種異體移植中,大腦中激活了先天免疫(圖2)。因此,通過免疫組化(IHC)分析了靶向先天免疫(MP)和/或適應性免疫(CyA)的免疫抑制劑的效果。
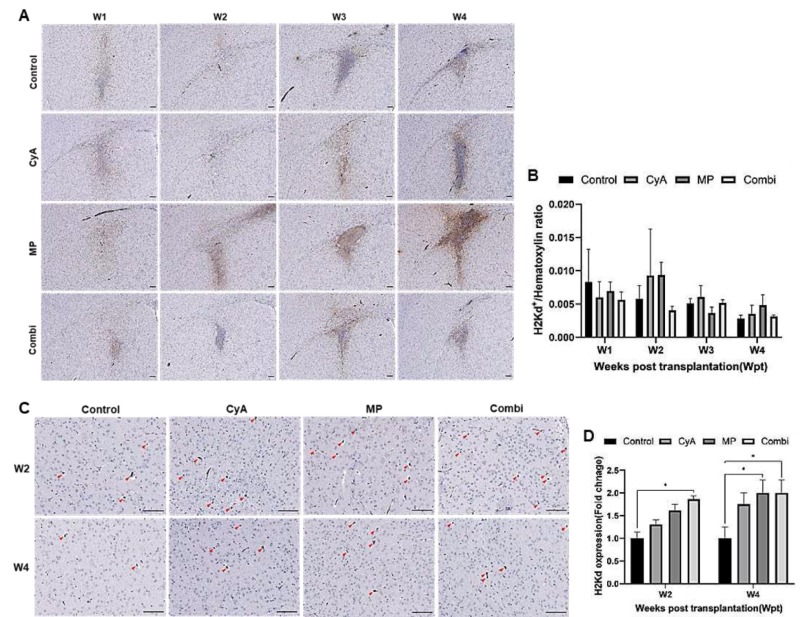
免疫抑制效果:在同種異體神經干細胞移植模型中(與異種移植不同),單獨使用靶向適應性免疫的環孢素A(CyA)、單獨使用靶向先天免疫的甲潑尼龍(MP)以及兩者聯用(CyA+MP),在移植后1-3周均能顯著減少腦內CD45陽性浸潤白細胞的數量(圖7A、B),其中聯合用藥在第2周的效果顯著優于任一單藥。
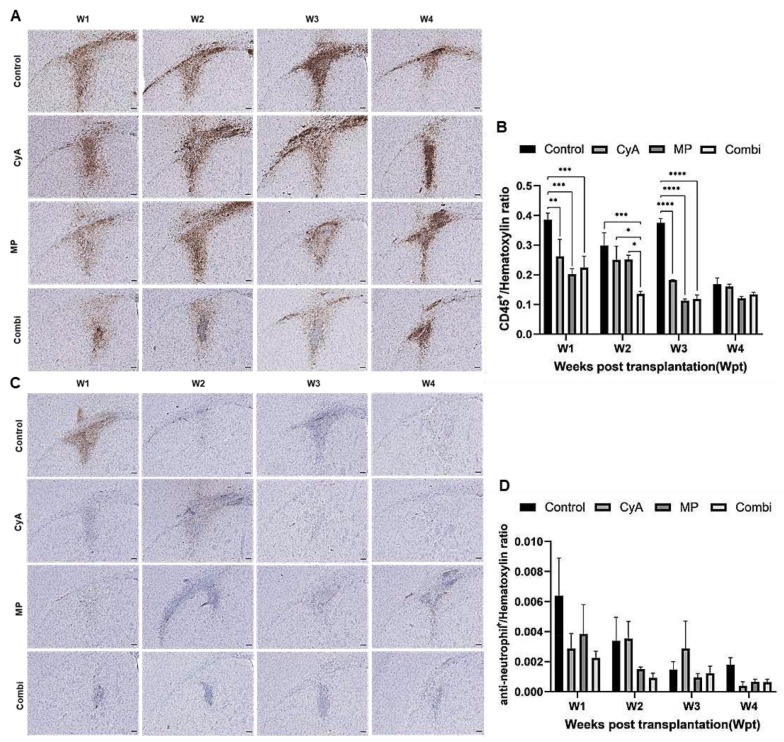
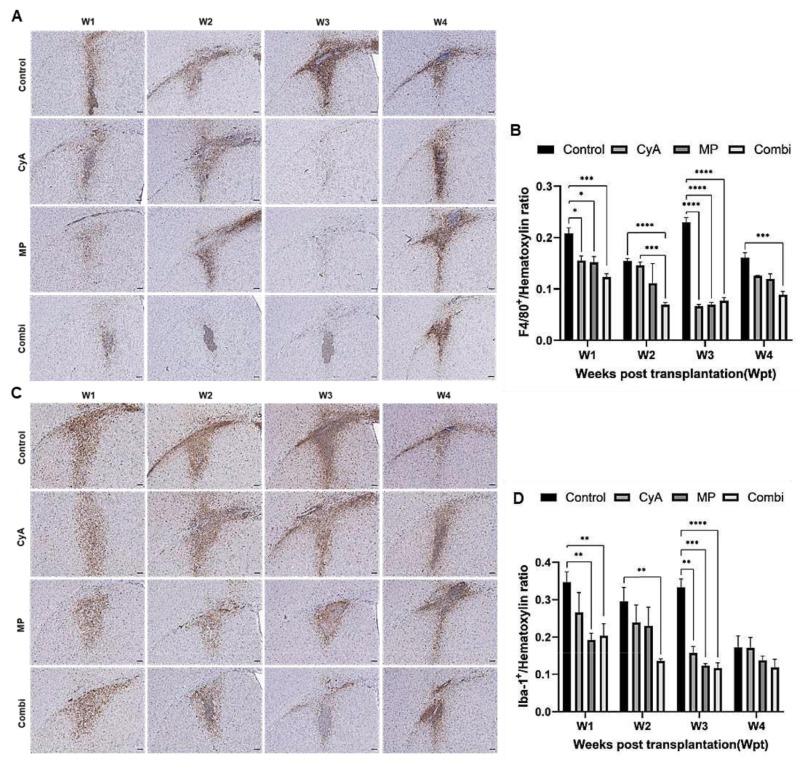
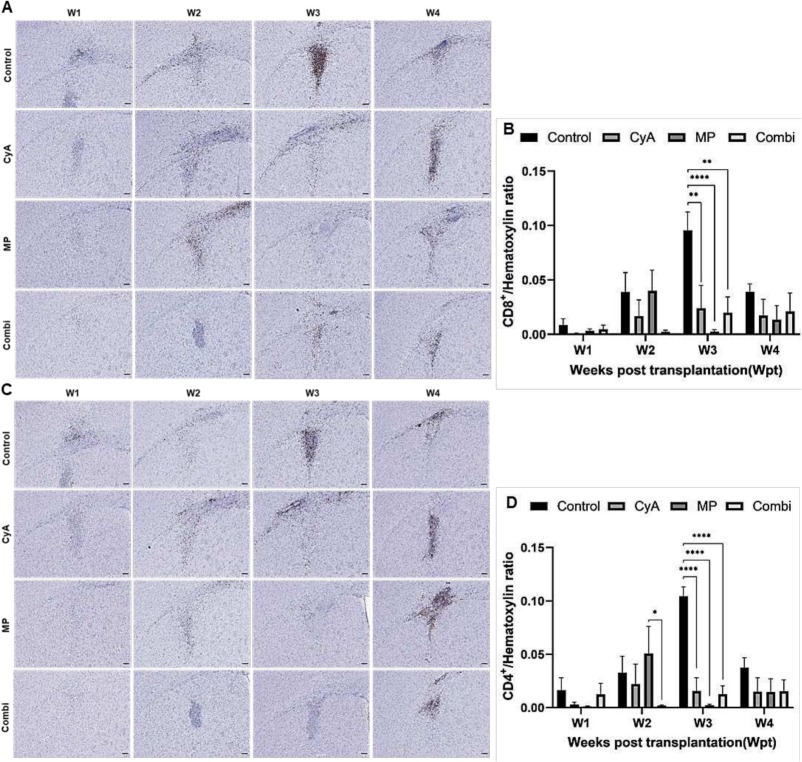
雖然中性粒細胞數量未受顯著影響,但這些免疫抑制劑也能有效抑制小膠質細胞/巨噬細胞(F4/80+(圖8A、B)、Iba-1+(圖8C、D))的激活。特別值得注意的是,移植后第3周出現了T細胞(CD8+、CD4+)數量的意外增加(圖9),而所有免疫抑制劑治療方案都能顯著抑制此反應,這表明同種異體移植引發的T細胞反應具有延遲且短暫的特點。
細胞存活與分布:免疫組化分析顯示,在注射部位核心區域,各用藥組與對照組之間存活的同種異體神經干細胞數量沒有顯著差異(圖10A、B)。然而,在注射部位的周邊區域,接受MP單藥或CyA+MP聯合治療的組中,檢測到的存活同種異體神經干細胞數量顯著多于對照組,且MP單藥與聯合用藥組在此區域的效果相當。這表明免疫抑制治療(尤其是針對先天免疫的MP)更有利于移植細胞在注射點周圍腦組織中的存活或擴散。
神經干細胞移植治療神經系統疾病的核心機制與免疫排斥挑戰
NSCs治療神經系統疾病的核心機制在于其免疫調節和神經營養旁分泌活性,這高度依賴移植細胞的存活。盡管大腦具有免疫豁免特性,但移植排斥仍是限制NSCs存活和功能的關鍵障礙。臨床前(動物模型)和臨床(患者)研究中觀察到的不同免疫反應模式,阻礙了成人源NSCs(ahNSCs)研究的轉化,凸顯了研究并抑制腦內移植排斥的重要性。
同基因、同種異體和異種NSCs體內移植會引起的腦內免疫反應差異?
免疫反應強度與模式差異:研究評估了三種神經干細胞移植(同基因、同種異體、異種)后大腦的免疫反應,發現異種移植引發最強烈的排斥反應(尤其炎癥細胞浸潤最多),同種異體移植次之。免疫細胞浸潤呈現時序性:異種移植中,中性粒細胞最早(立即至2天)并強烈浸潤,隨后巨噬細胞/小膠質細胞(4-6天)和T淋巴細胞(4-6天)依次增加,此模式與同種異體胰島移植的長期免疫反應階段劃分相似。
同種異體移植特點與基線免疫激活:與異種移植不同,同種異體移植主要激活先天免疫(顯著的小膠質細胞/巨噬細胞浸潤),而中性粒細胞和T淋巴細胞早期(6天內)浸潤與自體移植無差異;T細胞浸潤延遲至移植后第3周出現,但短暫且第4周消退。此外,陰性對照(僅注射緩沖液)和同基因組也觀察到先天免疫細胞(CD45+白細胞、中性粒細胞、小膠質/巨噬細胞)浸潤,表明注射操作本身即可觸發先天免疫反應,可能影響所有類型移植(包括同基因)細胞的存活。
同種異體移植與異種干細胞移植的免疫抑制劑效果與局限性有哪些?
同種異體移植:針對先天免疫的MP單藥或聯合CyA+MP均能有效減少CD45+白細胞及小膠質/巨噬細胞浸潤,顯著提高移植細胞在注射點周邊組織的存活率。單獨使用針對T細胞的CyA效果不佳,支持了同種排斥主要依賴先天免疫的觀點。
異種移植:需要同時抑制先天和適應性免疫。CyA+MP聯合方案在減少多種免疫細胞(CD45+白細胞、T細胞、小膠質/巨噬細胞)浸潤和提高早期(1周)細胞存活率方面效果最佳,并能促進細胞向周圍腦組織遷移。但即使聯合用藥也無法完全消除排斥,提示存在其他未被阻斷的排斥通路。
影響神經干細胞存活的其他關鍵因素與研究意義
NSCs存活還受多種非免疫因素影響,如:移植細胞形態(神經球優于單細胞)、移植部位(海馬優于紋狀體)、疾病模型/微環境(影響最佳移植時間窗)、宿主營養支持以及注射操作導致的BBB破壞(使細胞更易被識別)。免疫抑制療法被證實對提高同種和異種移植物的存活是必要且有效的。
研究結論指出:我們證明異種NSCs移植在腦內引發了最強烈的免疫反應,觸發了先天性和適應性免疫反應,而同種異體NSCs移植主要引發先天性免疫反應。鑒于此,在以異種移植為主的非臨床試驗中,CyA和MP聯合應用效果最佳;而在以同種異體移植為主的臨床試驗中,單獨使用MP的療效與聯合應用相當。
我們的研究或可為減少腦內神經干細胞移植排斥反應提供方法,并為NSCs治療各種中樞神經系統疾病后的臨床前和臨床研究創造最佳環境。
主要參考資料:
[1]:https://www.sciencedirect.com/science/article/pii/S0966327425000759?via%3Dihub#f0050
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加官方微信
掃碼添加官方微信