脊髓損傷(SCI)因神經信號傳遞中斷導致癱瘓、感覺喪失,傳統療法僅能緩解癥狀,無法實現神經再生。近年來,?神經干細胞(NSCs)移植憑借其多向分化、神經營養及免疫調節能力,成為修復脊髓損傷的焦點。
2025年3月,日本慶應義塾大學的研究團隊宣布,利用誘導多能干細胞(iPS細胞)衍生的神經干細胞治療脊髓損傷取得重大突破。研究中,4名因脊髓損傷而完全癱瘓的患者接受了200萬個iPS細胞衍生的神經干細胞移植。經過一年的觀察,1名患者能夠獨立站立并開始步行訓練,1名患者可以活動部分肢體,另外2名患者改善不明顯,但所有患者均未出現嚴重副作用。
神經干細胞干細胞移植治療脊髓損傷的長期臨床療效和安全性怎么樣?又是什么機制原理維持患者長期療效和安全性持續穩定呢?評估神經干細胞移植治療脊髓損傷長期療效和安全的指標是哪些呢?本文基于全球多項長期臨床研究,系統解析其長期療效與安全性,為患者與研究者提供科學參考。
神經干細胞移植的療效源自于哪里?
- 細胞替代與突觸重建:移植的干細胞可分化為神經元和膠質細胞,填補損傷區域,重建神經回路。
- 神經營養因子分泌:干細胞分泌BDNF、GDNF等因子,促進軸突再生和髓鞘修復。
- 免疫調節與抗炎:抑制M1型巨噬細胞活化,減少TNF-α、IL-6等炎性因子,改善損傷微環境。
神經干細胞移植治療脊髓損傷的長期臨床療效和安全性如何評估
長期臨床療效
- 肢體運動能力增強:在長期隨訪中,部分患者表現出持續的運動功能改善。
- 心理狀態改善:隨著身體功能的持續恢復,患者的心理狀態也得到改善,焦慮和抑郁等情緒障礙減輕。
- 神經病理性疼痛減輕:長期隨訪顯示,部分患者在移植后疼痛評分有所改善,神經病理性疼痛得到緩解。
- 損傷區域修復:通過磁共振成像(MRI)檢查,可以看到脊髓損傷區域的組織結構得到一定程度的修復,神經纖維的連續性得到改善。
長期安全性的評估標準
腫瘤與免疫排斥風險
- ?腫瘤發生監測:通過長期隨訪(如5年)的MRI或CT等影像學手段,評估損傷區域及全身是否存在畸胎瘤、惡性腫瘤等異常增生。
- ?免疫反應追蹤:定期檢測供體特異性人類白細胞抗原(HLA)抗體,并分析其是否針對移植細胞。例如,研究中僅1例患者檢測到非特異性HLA抗體,且未引發排斥反應。
神經功能穩定性與退化風險
- ?運動與感覺評分:采用國際標準ISNCSCI評分、SCIM評分等工具,持續追蹤患者神經功能的改善或退化。例如,兩名受試者在移植后5年仍保持穩定的神經功能改善(如肌力提升、感覺恢復)。
- ?電生理學驗證:通過肌電圖(EMG)和腦運動控制評估(BMCA),監測新出現的自主肌肉活動或神經信號傳導異常,確認神經再生效果的持久性。
影像學與脊髓結構穩定性
- ?MRI與DTI評估:定期進行脊髓MRI檢查,觀察損傷部位是否有水腫、積液或異常增強信號;彌散張量成像(DTI)用于監測白質纖維束的形態變化。結果顯示,所有患者脊髓軟化灶形態穩定,未出現結構惡化。
全身系統并發癥與代謝平衡
- ?血液與代謝指標:長期監測血常規、肝腎功能、炎癥因子(如IL-6、TNF-α)等指標,確認干細胞未引發系統性免疫紊亂或代謝失衡。
- ?感染與疼痛管理:記錄術后感染事件(如敗血癥)是否與移植相關,并評估神經病理性疼痛的長期變化。例如,兩名患者術后疼痛評分持續下降。
?生物標志物動態預警
- ?炎癥與再生標志物:定期檢測IL-1α、IL-6等炎癥因子,以及神經特異性標志物(如hNSE、GFAP),評估免疫激活與神經修復的平衡狀態。
- ?基因與表觀遺傳分析:篩查HLA-DRB1 * 04等易感基因,預測個體化風險;結合microRNA(如miR-21)動態監測,優化安全預警閾值。
神經干細胞移植治療脊髓損傷的長期臨床療效如何?安全性怎么樣?
長期臨床療效:神經損傷和運動功能得到改善(5年隨訪)
2024年,威科醫療健康的研究人員在國際期刊《Neurosurgery》上發布了一篇《2018 年神經干細胞移植治療慢性頸脊髓損傷 I 期研究的臨床和安全性結果》長達五年隨訪的研究結果。
神經干細胞移植治療慢性頸脊髓損傷 I 期研究,長達五年的隨訪,患者神經損傷水平和運動功能改善,患者對該手術的耐受性良好。

三名患者接受了雙側 NSI-566 植入,并進行了長達 60 個月的隨訪,其中包括 ISNCSCI 評分、功能和疼痛調查、肌電圖 (EMG) 和腦運動控制評估 (BMCA) 等前瞻性數據收集。
患者神經損傷水平和運動功能改善:
受試者 0202 是一名 23 歲男性,患有 C7 神經系統損傷水平 (NLI)。
- ISNCSCI 評估顯示雙側運動 (C7-C8) 在 36-60 個月時得到改善。
- BMCA 在 42 個月時顯示肘部屈曲/伸展 (F/E) 期間右側肱三頭肌出現新的反應。
- EMG 分析在 12 個月時發現右側肱三頭肌出現新的 MUAP。
受試者 0203 是一名 56 歲男性,患有 C6 NLI。
- 細胞移植后長達 54 個月,ISNCSCI 評分無變化。
- 雙側聳肩時左斜方肌的 BMCA 記錄和被動髖部 F/E 時左髖內收肌的 BMCA 記錄顯示 12 個月時出現新的活動。
- 12 個月時的 EMG 記錄發現右三角肌出現新的 MUAP。
受試者 0206 是一名 37 歲男性,患有 C6 NLI。
- 細胞移植后長達 60 個月,ISNCSCI 評分、BMCA 或 EMG 均未見變化。
安全性評估:所有患者對該手術的耐受性良好,植入 NSI-566 未導致嚴重不良事件。
結論: NSI-566 移植治療脊髓損傷5年隨訪內,患者神經損傷水平和運動功能改善得到改善,植入 NSI-566 未導致嚴重不良事件。可以達到神經干細胞移植治療脊髓損傷長期療效的目標。
2024年12月17日,加州大學圣地亞哥分校醫學院研究人員在國際期刊《Cell Reports Medicine》上發表了一篇關于《神經干細胞移植治療慢性胸椎脊髓損傷的單中心 I 期臨床研究的長期臨床和安全性結果》的研究。

神經干細胞移植治療慢性胸椎脊髓損傷的單中心 I 期臨床研究5年的隨訪結果,患者神經水平、疼痛癥狀、神經生理反應以及患者活動功能改善。
神經水平改善
神經系統反應
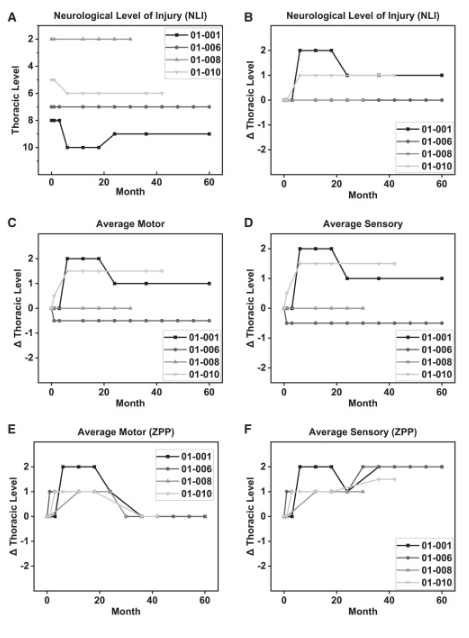
體格檢查顯示兩名患者的神經損傷水平 (NLI)、運動評分和感覺評分均有所改善。與細胞移植兩年后的神經系統評分相比,5 名受試者 001 的改善水平從兩年時的 2 個水平(改善)下降到五年時的?? 1 個水平。受試者 010 的改善在兩年和五年時均保持穩定在 1 個水平的神經系統改善。
停止免疫抑制治療
在所有四名受試者中,移植后 12 周停用他克莫司和霉酚酸酯。受試者拒絕在植入后進行額外的輸血或血液制品,當 12 個月和 18 個月出現類似的抗 HLA 抗體結果時,排除了旁觀者免疫反應。結論是患者體內存在的免疫反應與 NSC 治療無關。
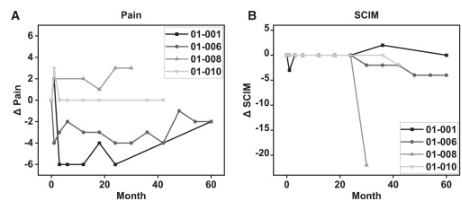
疼痛癥狀改善
疼痛和脊髓獨立性測量
四名患者中的兩名(001 和 006)術后疼痛評分總體下降,包括過渡區不適和異常性疼痛、手術部位疼痛以及其他部位的神經性疼痛和傷害性疼痛。
患者 008 的疼痛略有增加,患者 010 的疼痛評分基本保持不變。三名患者(001、006 和 010)的生活質量 SCIM 評分沒有顯著變化。患者 008 因骶骨潰瘍在 30 個月時發生 SAE,SCIM 評分大幅下降。
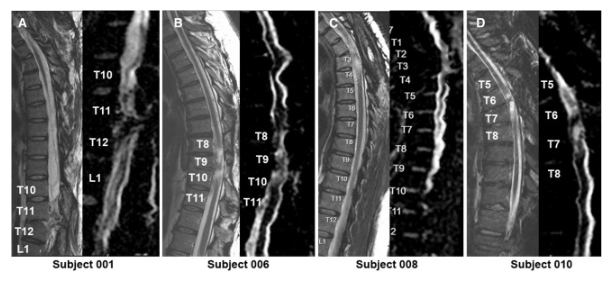
影像學評估中損傷部位未見并發癥
通過 MRI 和 DTI 成像評估動態反應
在 NSC 注射后,沒有放射學證據表明出現即時或延遲并發癥,包括術后即時或隨訪成像中沒有出現新的脊髓或軟組織水腫區域、增強或腫脹或積液。在純解剖或擴散張量序列中均未觀察到脊髓脊髓軟化癥的可見形態變化。
在所有四名患者中,彌散張量成像 (DTI) 成像顯示在損傷部位和損傷部位的前端/尾部脊髓束外觀穩定,但未顯示重塑或纖維束造影改善的廣泛證據。
神經生理反應以及患者活動功能改善
受試者 001(T8 水平損傷)
- EMG 顯示移植后四周左 T9 和右 T10 腹直肌和椎旁肌有活動。
- 27 個月時,雙側 T10 椎旁活動改善為更顯著。
- BMCA 還顯示 27 個月時下肢肌肉對強化動作有了新發展的反應。
- 60 個月時,記錄到右側脛骨前肌和右腳趾有持續的 EMG 活動,針刺 EMG 也顯示左側 T11 和 T12 雙側腹直肌有了新的自主控制。
受試者 006(T7 水平損傷)
- 2 個月的 EMG 分析顯示右側腹直肌和雙側 T6 至 T8 椎旁肌出現了新的自主活動。
- 移植后 18 個月,患者在雙側 T9 處插入 EMG 針頭時出現了感覺。
- 從 36 到 54 個月,新的 EMG 分析顯示 T10 雙側腹直肌和 T10–T11 椎旁肌的控制得到改善。
- 在 60 個月時,BMCA 顯示下肢對強化操作產生了新出現的肌肉反應。
移植后 6 到 36 個月,受試者 010(T5 損傷水平)繼續在 T7 右側淺表椎旁肌中顯示 EMG 活動,BMCA 在 42 個月時顯示下肢對強化操作產生了新出現的肌肉反應。
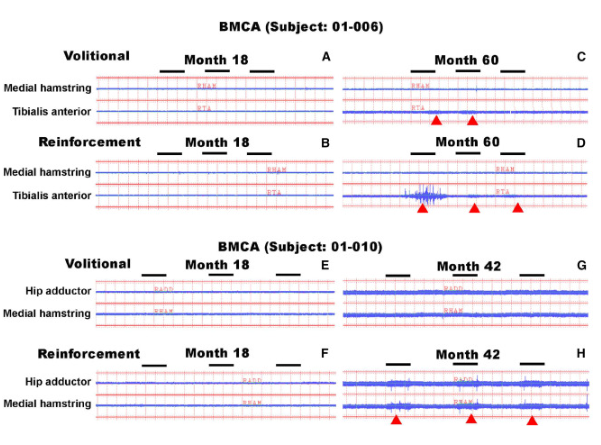
結論:兩名受試者在移植后五年有持久的肌電圖量化神經系統改善證據以及神經運動和感覺評分增加,可以達到神經干細胞移植治療脊髓損傷的長期療效的目標
長期安全性的評估
這是一項 1 期前瞻性、開放標簽、非盲、非隨機、美國食品藥品管理局 (FDA) 批準的臨床試驗 (NCT02354625),旨在評估移植 ahSC 對慢性 SCI 患者的安全性。接受試驗后,參與者連續 10 個月參與現場研究活動,并在移植后繼續接受 5 年的監測。

結論:在整個研究過程中,八名參與者共記錄了 54 起不良事件。沒有嚴重不良事件。十四起不良事件肯定或可能與研究程序有關,并與運動和康復訓練(皮膚擦傷和吊帶刺激、肌肉或關節疼痛)或移植手術(頭痛、惡心、感覺減退)有關。泌尿道感染和皮膚損傷最為常見,這與慢性 SCI 人群所經歷的問題一致。可以達到神經干細胞移植治療脊髓損傷長期安全性的目標。
影響神經干細胞移植治療脊髓損傷的因素有哪些
細胞來源與分化能力
- ?內源性NSCs:存在于脊髓中央管室管膜區,激活后可遷移至損傷部位,但再生能力有限且易分化為星形膠質細胞形成瘢痕。
- ?外源性NSCs:包括胚胎來源(倫理爭議大)、誘導多能干細胞(iPSCs)分化或體細胞直接轉分化(iNSCs)。iNSCs通過轉錄因子重編程生成,繞過多能狀態,降低致瘤風險。
- ?基因修飾NSCs:通過CRISPR等技術增強神經營養因子(如BDNF、GDNF)分泌或抵抗炎癥因子,動物模型中可提升軸突再生率30%-50%。
移植策略
- ?病灶內注射:直接靶向損傷區域,但需開顱或椎板切除,創傷大且細胞存活率僅10%-20%。
- ?鞘內/腦脊液注射:經腰椎穿刺注入蛛網膜下腔,細胞可隨腦脊液擴散至全中樞神經系統,操作簡便但靶向性差。
- ?靜脈注射:非侵入性但入脊髓效率低(<5%),需多次輸注維持療效。
患者個體差異
損傷程度與病程階段
- 不完全性損傷(AIS分級C-D級)患者神經通路保留較多,運動功能恢復概率比完全性損傷高3-5倍。
- ?窗口期選擇:亞急性期(損傷后7-14天)移植效果最佳,此時炎癥減輕且瘢痕未完全形成,細胞存活率比急性期高60%。
年齡與遺傳背景
- 年輕患者(<50歲)因神經可塑性強,UPDRS評分改善幅度可達30%-40%,而老年患者需更高劑量或聯合治療。
- 攜帶Nogo受體(NgR)基因變異者可能對NSCs響應較弱,需結合基因檢測定制方案.
神經干細胞移植治療脊髓損傷的療效受細胞質量、移植策略、宿主微環境等多因素協同影響。未來需突破基因編輯精準調控、生物材料-細胞復合體開發及個體化治療方案的優化。
總結
綜上所述,神經干細胞移植為脊髓損傷治療開辟了新路徑,其長期安全性已得到初步驗證,且對脊髓損傷患者的療效顯著。隨著2025年干細胞技術的突破及更大規模III期試驗的推進,希望這一療法在未來5-10年內成為臨床常規選項。
若想了解更多關于脊髓損傷和干細胞治療脊髓損傷的內容請點擊此處!
參考資料:
1.https://journals.lww.com/neurosurgery/abstract/2025/04001/2018_clinical_and_safety_outcomes_from_a_phase_i.627.aspx
2.https://www.cell.com/cell-reports-medicine/fulltext/S2666-3791(24)00612-8
3.Gant KL, Guest JD, Palermo AE, Vedantam A, Jimsheleishvili G, Bunge MB, Brooks AE, Anderson KD, Thomas CK, Santamaria AJ, Perez MA, Curiel R, Nash MS, Saraf-Lavi E, Pearse DD, Widerstr?m-Noga E, Khan A, Dietrich WD, Levi AD. Phase 1 Safety Trial of Autologous Human Schwann Cell Transplantation in Chronic Spinal Cord Injury. J Neurotrauma. 2022 Feb;39(3-4):285-299. doi: 10.1089/neu.2020.7590. Epub 2021 May 3. PMID: 33757304; PMCID: PMC9360180.
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。
版權說明:本文來自杭吉干細胞科技內容團隊,歡迎個人轉發至朋友圈,謝絕媒體或機構未經授權以任何形式轉載至其他平臺,轉載授權請在網站后臺下方留言獲取。



 掃碼添加微信
掃碼添加微信