近年來,干細胞治療1型糖尿病(T1D)取得了顯著進展,為患者實現“功能性治愈”提供了新的希望。
中國科研團隊通過誘導多能干細胞(iPSC)或化學重編程干細胞(CiPSC)生成胰島β細胞,并將其移植至患者體內,不僅能夠修復受損的胰島功能,還能恢復體內胰島素分泌能力,為長期依賴外源性胰島素的患者帶來全新的治療思路。
從臨床前研究到首例功能性移植,再到異體通用胰島產品獲批,中國在該領域不斷突破,技術路線日益成熟,臨床轉化加速,也為全球研究提供了寶貴經驗。
本文將帶領大家回顧中國在干細胞治療1型糖尿病的發展歷程、最新臨床成果,并結合技術創新與臨床策略,幫助讀者全面了解中國在干細胞治療1型糖尿病中的應用前景與發展趨勢。

25年回顧?|?中國干細胞治療1型糖尿病的發展歷程與技術突破
一、中國干細胞治療1型糖尿病的發展歷程
中國在干細胞治療1型糖尿病的探索始于20世紀末,其發展可大致分為四個階段,每一階段都為下一步的突破奠定了基礎。
1. 基礎研究與方法學奠基(2000–2010)
2000年代末至2010年代,中國科研機構在iPSC、胚層分化與胰島發生學方面進行了系統研究,為多能干細胞分化為功能性β細胞打下基礎。此階段主要成果包括細胞重編程、胰向分化流程優化及早期動物模型驗證,為后續臨床轉化提供了技術儲備。
2. 產業化探索與臨床前優化(2010–2020)
隨著分化效率和細胞質量控制技術成熟,中國團隊開始嘗試可放大生產、GMP制備及移植策略。通過大量動物試驗,逐步解決了細胞存活、功能成熟及免疫排斥等問題,并優化了移植位點(如腹直肌前鞘下注射),為人體給藥路徑提供了可行方案。
3. 早期臨床信號(2021–2024)
進入2020年代,中國團隊的臨床探索初見成效。以“自體再生胰島(E-islet)”為代表的個性化再生策略首次在人類中應用,程新和殷浩團隊的研究顯示,受試者在術后長期隨訪中實現了胰島功能代償和臨床改善(隨訪超過100周),為組織替代療法提供了首批人體證據。同時,多組課題在移植技術、細胞穩定性及隨訪方案上積累了可復制的經驗,為進一步放大驗證奠定基礎。
4. 里程碑性臨床試驗與產業化突破(2024–2025)
2024–2025年,中國在干細胞治療1型糖尿病領域取得多項關鍵進展:
- 首例自體再生胰島臨床報道:程新—殷浩團隊報道了首例EnSC-E-islet移植及其116周隨訪,證實體外再造胰島在安全性和功能替代上的可行性。
- 異體“貨架型”再生胰島(E-islet 01)獲臨床受理:該通用型再生胰島產品獲得國家監管部門的臨床受理,標志國產通用型細胞藥物進入規范化臨床試驗階段,可規模化、GMP放大生產。
- 多條移植路徑與工藝并行推進:肝門靜脈輸注、腹直肌鞘下植入等不同位點同步驗證,為患者提供定制化方案。
- 臨床案例積累:上海長征醫院等團隊披露的多例T1D/T2D移植案例,為多中心隨機對照試驗設計提供了現實依據。
二、政策與環境:中國干細胞研究的推動力
中國干細胞研究的快速發展得益于政策引導、資金投入和產學研合作的共同推動:
戰略規劃:干細胞治療被列入《“十四五”醫藥工業發展規劃》重點發展方向。
監管框架:國家藥品監督管理局藥品審評中心(CDE)發布《人源干細胞產品藥學研究與評價技術指導原則(試行)》,為干細胞產品研發提供技術指導。
開放創新:2024年,中國在北京、上海、廣東等地的自由貿易試驗區和海南自由貿易港試點允許外商投資人體干細胞技術開發和應用,促進了國際資本與技術的引入。
地方支持:例如四川省成立了干細胞技術與細胞治療協會,并推動干細胞領域創新平臺建設。
這些政策為干細胞技術轉化提供了制度保障,加速了臨床應用的進程。
三、關鍵臨床里程碑
E-islet 01獲批臨床:臨床治愈多位糖尿病患者
2024年5月7日,上海長征醫院殷浩教授團隊聯合中國科學院程新教授團隊在行業起來《細胞·發現》(Cell Discovery)上發表了一篇重磅研究,通過自體干細胞再生胰島移植,成功治愈一名患病25年的糖尿病患者。[1]
該患者為59歲男性,患糖尿病25年。接受干細胞療法后,隨訪116周內胰島素需求逐漸減少,并在第11周完全停用。口服降糖藥也逐步減量,第48周(阿卡波糖)和第56周(二甲雙胍)完全停用。
術后平均空腹C肽水平升至術前的3倍(0.68 nmol/L),混合餐耐量試驗(MMTT)顯示C肽和胰島素分泌顯著增加,AUC分析進一步證實了胰島功能明顯改善。
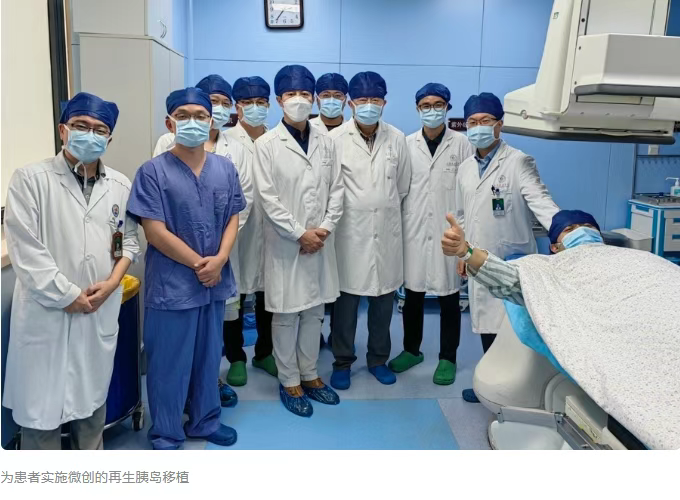
時隔一年,2025年4月18日,該團隊再傳捷報:其與中科院分子細胞科學卓越創新中心合作開發的“異體人再生胰島注射液(E-islet 01)”,正式獲得國家藥品監督管理局(NMPA)臨床試驗默示許可。[2]
這是全球第二個、中國首個獲批臨床試驗的通用型再生胰島療法,標志著我國在糖尿病再生醫學領域實現了從“跟跑”到“領跑”的跨越。這一年,在臨床上殷浩與合作團隊先后利用該自體和異體干細胞療法,成功治愈多例1型糖尿病患者!
長征醫院的臨床研究表明,E-islet 01經微創操作輸注到患者肝門靜脈內,可實現胰島功能衰竭糖尿病(1型和嚴重2型)患者的治愈。
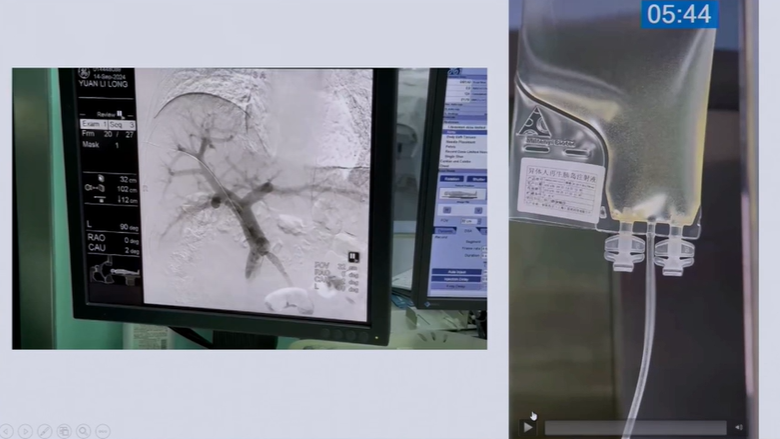
據介紹,目前E-islet 01已經實現了標準化及規模化制備,產品從生產到臨床應用全流程可追溯、質量穩定均一,為臨床試驗的高效推進及未來規模產業化落地夯實了技術基礎。
自體CiPS胰島移植里程碑:首位患者實現一年以上無胰島素生活
2024年9月25日,北京大學、昌平實驗室鄧宏魁團隊,天津市第一中心醫院沈中陽、王樹森團隊,和杭州瑞普晨創科技有限公司合作在《Cell》發表題為Transplantation of Chemically Induced Pluripotent Stem-Cell-Derived Islet Under Abdominal Anterior Rectus Sheath in a Type 1 Diabetes Patient的研究論文。[3]
該成果在國際上首次報道了利用化學重編程誘導多能干細胞制備的胰島細胞移植,治療1型糖尿病的臨床研究。首位患者在移植后恢復了內源自主性、生理性的血糖調控,移植75天后完全穩定地脫離胰島素注射治療,目前療效已穩定持續1年以上。實現了1型糖尿病的臨床功能性治愈。

研究入組的首位患者是一位病史長達11年的1型糖尿病病人,通過強化胰島素治療仍然不能有效控制血糖,為了治療糖尿病,患者于2017年5月接受了胰腺移植手術,但一年后胰腺移植失敗,并且患者群反應抗體呈現為強陽性,難以接受同種異體胰島移植,然而自體細胞移植有可能解決這個難題。
本臨床研究移植前,患者血糖在目標血糖范圍內的時間比例僅為43.18%,最近一年內多次發生嚴重低血糖,威脅患者的生命安全。2023年6月25日,患者接受了自體人CiPS細胞分化胰島移植的治療。
該研究報道了該患者臨床治療達到1年的有效性和安全性臨床終點的數據。在證明安全性的基礎上,該研究獲得了臨床有效性的關鍵數據:
1)移植后患者空腹血糖水平逐步恢復正常,外源胰島素需要量持續下降,從移植后第75天開始,實現了完全穩定地脫離胰島素注射治療,截止到論文發表時,患者完全脫離胰島素治療超過1年;
2)糖化血紅蛋白水平在移植后一年降至4.76%;
3)患者血糖達標率從基線值43.18%持續提高,移植后5個月后超過98%以上,并維持在該水平。這些結果證明了該療法實現了1型糖尿病的臨床功能性治愈。
這一案例顯示,自體CiPS細胞分化胰島移植在1型糖尿病中具備真正逆轉病程的潛力,為實現長期無胰島素生活提供了里程碑式的臨床證據。
2025年1月,鄧宏魁團隊又在《Nature》上發表了題為“A Rapid Chemical Reprogramming System to Generate Human Pluripotent Stem Cells”的最新研究成果。[4]

不僅揭示了化學重編程體系中的核心表觀遺傳障礙(KAT3A/B和KAT6A的富集表達),還進一步優化了快速化學重編程技術,將人成體細胞誘導為多能干細胞的時間從30天壓縮至最短10天,標志著該領域的重要里程碑。
此次最新的研究成果主要體現在以下幾個方面:
1.發現表觀遺傳關鍵障礙:研究團隊通過對比不同個體的體細胞,發現組蛋白修飾酶KAT3A/B和KAT6A在難誘導細胞中顯著富集,其核心作用是維持細胞身份。這一發現為突破化學重編程瓶頸提供了新靶點。
2.建立快速化學重編程體系:基于上述機制,團隊開發出新型快速重編程方法,將人CiPS細胞誘導周期從30天縮短至10-16天。在15名不同個體來源的體細胞中驗證,最高誘導效率達38%,且對難誘導樣本效率提升超20倍,顯著增強技術普適性。
3.解析機制并驗證效果:通過基因表達與表觀遺傳譜分析發現:抑制KAT3A/B和KAT6A可加速體細胞基因關閉,并預激活關鍵基因增強子區域,縮短轉錄啟動時間。單細胞測序進一步證實該機制能快速打破原基因程序,抑制異常激活,促進目標基因高效表達。
這一成果不僅為干細胞治療(如I型糖尿病)提供了高效、低成本的細胞來源,也為破解細胞命運調控難題提供了新靶點,標志著我國科研團隊在干細胞領域邁入國際領先行列,加速了再生醫學向臨床轉化的步伐。
相關閱讀:我國干細胞技術又迎新突破:10天從體細胞到多能干細胞,1型糖尿病治愈提速,更多復雜疾病有望被治愈
這些里程碑事件標志著中國在干細胞治療糖尿病領域已進入世界領先行列。
四、國內干細胞的技術路線與特色
中國團隊在干細胞治療糖尿病領域實現了多項技術創新:
- 化學重編程技術:鄧宏魁團隊開發的化學小分子重編程法,取代了傳統的病毒載體方法,避免了基因組整合風險,更安全且易于標準化生產。
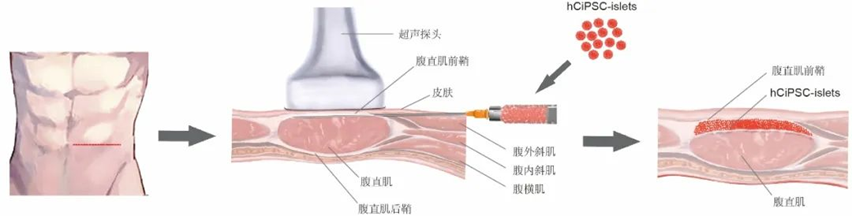
- 新型移植部位:團隊創新性地將胰島移植到腹直肌前鞘下,替代傳統的肝門靜脈移植。這一部位創傷更小、易于成像觀察,且能提高細胞存活率。
- 高效分化方案:研究團隊建立了高效優化的分化方案,成功生成了特征與天然人類胰島相當的CiPSC來源的胰島樣細胞(CiPSC-islets)。
- 異體通用型產品:上海長征醫院與中科院團隊開發了利用健康供體來源的血液細胞轉化為內胚層干細胞,再定向制備再生胰島的技術路線,實現了標準化和規模化制備。
這些創新點共同構成了中國在該領域的技術優勢,為臨床轉化奠定了基礎。
五、國內什么時候能夠上市?
2025年11月,由浙江省數理醫學學會主辦、浙江大學醫學院附屬第二醫院協辦的“2025廣濟內分泌代謝論壇”上海軍軍醫大學上海長征醫院殷浩教授就干細胞治療1型糖尿病的最新進展進行系統解讀。
其中提到該團隊計劃于2026年初進入二期研究階段,若一切順利,預計在未來3至5年內,有望實現國產化產品的臨床應用與上市。
相關閱讀:11.11-11.17干細胞治療一周熱點:糖尿病、紅斑狼瘡新療法等8大前沿動態速覽
六、國內干細胞治療1型糖尿病的費用是多少?
據了解,國內相關產品的定價預計在50萬至80萬人民幣之間,而美國同類產品定價約為100萬美元。
當然隨著生產工藝優化和產能提升,產品價格有望進一步降低。未來可能通過醫保、商業保險及個人共付等方式降低患者負擔。
七、面臨的挑戰與未來方向
盡管進展顯著,但從“功能性個例”走向“廣泛可及的臨床產品”仍面臨若干關鍵挑戰:
- 長期安全性:需大樣本、多中心長期隨訪以監測腫瘤風險與免疫并發癥;
- 免疫管理:如何減少或避免長期免疫抑制(基因免疫化、局部耐受誘導或封裝技術的結合);
- GMP放大生產與質量一致性:實現穩定批次與可追溯的生產體系;
- 可及性與定價:把高度復雜的細胞療法轉化為患者可支付的醫療服務,是產業化必須解決的問題。
針對這些問題,下一步需以多中心隨機對照臨床試驗為主線,加速標準化生產體系建設,并同步完善監管與支付制度保障。
結語
中國在干細胞治療T1D的臨床轉化中,已經從理論與動物驗證走入了首例人體移植和異體產品申報階段,展現出“個性化自體再生”與“通用貨架型產品”并行推進的獨特優勢。
未來幾年,隨著多中心驗證、監管審批與產業化落地,中國有望在全球干細胞糖尿病治療版圖中占據重要席位,為T1D患者帶來真正可及的功能性替代治療方案。
參考資料:
[1]Wu, J., Li, T., Guo, M.?et al.?Treating a type 2 diabetic patient with impaired pancreatic islet function by personalized endoderm stem cell-derived islet tissue.?Cell Discov?10, 45 (2024). https://doi.org/10.1038/s41421-024-00662-3
[2]https://www.thepaper.cn/newsDetail_forward_30703516
[3]Transplantation of chemically induced pluripotent stem-cell-derived islets under abdominal anterior rectus sheath in a type 1 diabetes patientWang, Shusen et al.Cell, Volume 187, Issue 22, 6152 – 6164.e18
[4]Wang, Y., Peng, F., Yang, Z.?et al.?A rapid chemical reprogramming system to generate human pluripotent stem cells.?Nat Chem Biol?21, 1030–1038 (2025). https://doi.org/10.1038/s41589-024-01799-8
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。




 掃碼添加微信
掃碼添加微信