近年來,干細(xì)胞治療作為再生醫(yī)學(xué)的重要分支,為慢性腎病(CKD)、急性腎損傷(AKI)、糖尿病腎病等腎臟疾病的治療提供了全新思路。干細(xì)胞通過分化為功能性腎細(xì)胞、分泌生長因子、調(diào)節(jié)免疫反應(yīng)及抗纖維化等機(jī)制,展現(xiàn)出修復(fù)受損腎臟組織的潛力。本文結(jié)合最新臨床證據(jù)與技術(shù)進(jìn)展,系統(tǒng)解析干細(xì)胞治療腎病的技術(shù)成熟度與發(fā)展前景。

干細(xì)胞治療腎病:技術(shù)成熟度評估與未來臨床應(yīng)用前景
一、干細(xì)胞治療腎病的核心機(jī)制
干細(xì)胞治療腎病基于其自我更新、多向分化和免疫調(diào)節(jié)等特性,通過以下機(jī)制發(fā)揮作用:
- 細(xì)胞替代與組織修復(fù):干細(xì)胞可分化為腎小球上皮細(xì)胞、腎小管細(xì)胞等,直接修復(fù)受損組織。
- 旁分泌效應(yīng):分泌生長因子(如VEGF、FGF9)和抗炎因子,促進(jìn)血管生成、抑制炎癥反應(yīng),改善腎臟微環(huán)境。
- 免疫調(diào)控:調(diào)節(jié)Th1/Th17等促炎性免疫反應(yīng),減輕自身免疫性腎病的損傷。
相關(guān)閱讀:干細(xì)胞治療腎臟疾病的6大原理機(jī)制,您都了解嗎?
二、臨床進(jìn)展與技術(shù)成熟度
2.1 臨床驗證其療效和安全性
多項隨機(jī)對照試驗(RCT)驗證了干細(xì)胞治療的安全性與有效性:
慢性腎病:2025年3月,BMC腎臟病學(xué)期刊上的一篇關(guān)于間充質(zhì)干細(xì)胞治療慢性腎病的文獻(xiàn)表明:間充質(zhì)干細(xì)胞輸注可以改善腎小球濾過率、尿蛋白、血清肌酐和血尿素氮等腎功能指標(biāo),同時通過增加調(diào)節(jié)性T細(xì)胞來抑制免疫反應(yīng)。

我們回顧了自2010年以來18篇涉及間充質(zhì)干細(xì)胞治療慢性腎病中的已發(fā)表研究。
核心療效
- 減少尿蛋白:對狼瘡性腎炎(LN)效果明確(多數(shù)研究顯示1-9個月見效)。
- 穩(wěn)定腎功能:可延緩腎小球濾過率(GFR)下降,尤其對早期患者(基線GFR≥30ml/min/m2)更有效。
其他改善
- 血液指標(biāo):降低血肌酐、提升血紅蛋白/血小板(部分LN患者),改善腎臟血流和氧合。
- 腎臟結(jié)構(gòu):可能逆轉(zhuǎn)萎縮,增加腎臟體積(部分研究)。
安全性:十年臨床研究證實MSC在CKD患者中安全性良好,常見不良反應(yīng)輕微且可控。但是年齡、細(xì)胞類型、疾病類型、給藥方式等可能影響AE發(fā)生風(fēng)險。
綜上所述,臨床研究證實干細(xì)胞療法可顯著降低腎臟疾病患者的尿蛋白水平、穩(wěn)定腎小球濾過率(GFR),并調(diào)節(jié)免疫平衡(如增加調(diào)節(jié)性T細(xì)胞/Tregs),且10年隨訪顯示長期安全性良好。
急性腎損傷:2021年12月,杜克大學(xué)醫(yī)學(xué)院在《干細(xì)胞轉(zhuǎn)化醫(yī)學(xué)》期刊上發(fā)表了一項《體外間充質(zhì)干細(xì)胞免疫治療對急性腎損傷和潛在全身炎癥患者的藥理作用》的研究,該研究是一項精心設(shè)計的多中心臨床試驗,在美國12個研究中心同步開展。

本次研究納入了16名受試者按2:1的比例隨機(jī)分配到有效低劑量的SBI-101(250×106MSCs)或假治療(無 MSCs)。研究結(jié)果表明:
SBI-101通過調(diào)節(jié)免疫系統(tǒng)和減少炎癥,顯著改善急性腎損傷。治療后,血液中的促炎因子(如TNFα、IFNγ)明顯下降,而抗炎因子(如IL-10)上升,尤其在治療早期(第3天)效果最明顯。這種從“促炎”到“抗炎”的轉(zhuǎn)變,有助于緩解腎臟損傷。
免疫細(xì)胞方面,部分單核細(xì)胞數(shù)量減少,與炎癥相關(guān)的趨化因子(如MCP-1)水平也同步降低,進(jìn)一步抑制炎癥反應(yīng)。同時,B細(xì)胞、T細(xì)胞等部分免疫細(xì)胞亞群比例發(fā)生變化,可能參與修復(fù)過程。
此外,SBI-101還能降低腎損傷標(biāo)志物(如KIM-1),表明腎臟功能得到保護(hù)或恢復(fù)。與傳統(tǒng)藥物不同,它通過多靶點(diǎn)作用(抗炎、免疫調(diào)節(jié)、護(hù)腎)實現(xiàn)治療效果,且長期安全性良好,未見嚴(yán)重副作用。
綜上所述,間充質(zhì)干細(xì)胞療法為急性腎損傷提供了一種全新的治療思路——通過調(diào)節(jié)全身免疫平衡和直接修復(fù)腎臟,有望成為傳統(tǒng)藥物之外的有效補(bǔ)充,尤其適用于難以控制的重癥患者。
狼瘡性腎炎:?2023年6月,哈薩克斯坦阿斯塔納國家科學(xué)醫(yī)學(xué)中心在期刊《腎臟病透析移植》上發(fā)表了一篇關(guān)于《間充質(zhì)干細(xì)胞移植治療狼瘡性腎炎的免疫矯正新焦點(diǎn)?》的臨床研究結(jié)果。

本次研究總共納入了15名對傳統(tǒng)免疫抑制療法有抵抗力的SLE(ACR標(biāo)準(zhǔn))患者。
對患者自體干細(xì)胞移植效果的監(jiān)測顯示,12個月后,SELENA-SLEDAI評分活動性顯著下降2倍,從 14.67±1.15分降至7.33±1.15分。在對照組中,盡管持續(xù)進(jìn)行免疫抑制治療,但該指標(biāo)保持不變,為15.0±0.87分。
所有接受高劑量免疫抑制療法(HIST)和骨髓間充質(zhì)干細(xì)胞(MSC)移植的患者均表現(xiàn)出臨床療效,其表現(xiàn)為:
- 每日蛋白尿量從2.48±0.77降至1.06±0.56g/l
- DNA抗體值(從443.28±547.53降至187.8±146.60)
- 血液細(xì)胞因子(TNF-Α顯著降低)降低,
- 補(bǔ)體水平升高(盡管不顯著)。
根據(jù)腎活檢數(shù)據(jù),在接受HIST的MSC移植后,積極的動態(tài)包括腎小球血管環(huán)中網(wǎng)狀纖維的數(shù)量增加,以及通過對抗體譜的免疫熒光分析發(fā)現(xiàn)腎小球血管環(huán)中的免疫炎癥過程減少。
研究表明,根據(jù)臨床和實驗室數(shù)據(jù),MSC移植與HIST相結(jié)合對SLE的療效明顯優(yōu)于傳統(tǒng)的免疫抑制療法。該方法安全,可以減少自身免疫攻擊的跡象,可用于SLE標(biāo)準(zhǔn)療法無效、療效低或不耐受的情況。
糖尿病腎病:2024年11月,江西贛南醫(yī)科大學(xué)研究人員在國際期刊《medRxiv》上發(fā)表一篇有關(guān)《干細(xì)胞治療糖尿病腎病的療效和安全性:系統(tǒng)評價與薈萃分析》的綜述,該綜述總結(jié)了江西贛南醫(yī)科大學(xué)研究人員整合的3,528項研究,并且在3528項研究篩選了4項高質(zhì)量研究,并對這四項高質(zhì)量研究進(jìn)行了系統(tǒng)評價與薈萃分析。[3]

這四項研究,涉及90名糖尿病腎病患者,其中53名(58%)接受了干細(xì)胞移植。
臨床研究結(jié)果:
1.干細(xì)胞移植對eGFR的影響:eGFR是腎功能的重要指標(biāo)。腎臟疾病飲食調(diào)整和慢性腎臟病流行病學(xué)協(xié)作公式通常用于估算GFR。
- 四項研究表明,干細(xì)胞移植顯著改善了eGFR水平。
- 森林圖數(shù)據(jù)分析(圖2)顯示,與對照組的結(jié)果相比,干細(xì)胞移植作為干預(yù)措施顯著改善了eGFR水平。
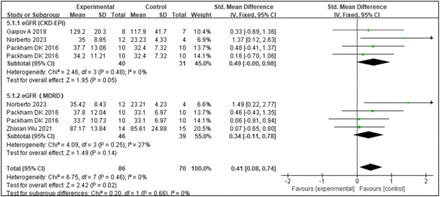
2.干細(xì)胞移植對SCr的影響:SCr水平可用于監(jiān)測糖尿病腎病。在糖尿病腎病早期,SCr可維持在正常范圍,但隨著病情進(jìn)展,其水平逐漸升高,因此監(jiān)測SCr水平糖尿病腎病的早期診斷和病情監(jiān)測有重要意義。
- 3項研究報道了SCr水平,其相關(guān)的I2值為0%,因此本研究采用固定效應(yīng)模型。
- 森林圖分析結(jié)果(圖3)顯示,SCT治療與SCr水平的顯著變化相關(guān),以干細(xì)胞注射為干預(yù)措施的試驗組糖尿病患者的SCr水平顯著降低。
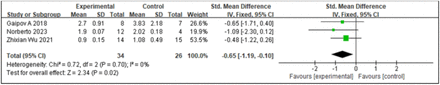
3.干細(xì)胞移植對MAU的影響:MAU是糖尿病腎病的早期標(biāo)志。持續(xù)性MAU與糖尿病患者發(fā)生臨床蛋白尿的風(fēng)險呈顯著正相關(guān),提示MAU對預(yù)防糖尿病腎病發(fā)展至關(guān)重要。
- 兩項研究對MAU進(jìn)行了綜合分析,如圖6A所示。SCT與MAU水平的顯著變化相關(guān),研究間異質(zhì)性較低,I2值為41,提示研究結(jié)果一致性較高。
- 森林圖數(shù)據(jù)分析顯示,干細(xì)胞移植組的MAU水平顯著低于對照組。

4.干細(xì)胞移植對UACR的影響:UACR是尿蛋白排泄指標(biāo),是早期篩查DKD的關(guān)鍵參數(shù)。UACR升高預(yù)示腎臟損傷的存在,尤其對于糖尿病患者。此外,研究間異質(zhì)性較低。試驗組和對照組之間的UACR無顯著差異。
綜上所述,這項系統(tǒng)評價與薈萃分析,首次通過高證據(jù)等級的研究整合了干細(xì)胞治療糖尿病腎病的臨床數(shù)據(jù),明確證明了干細(xì)胞移植在改善腎功能(eGFR、SCr)、降低尿蛋白(MAU、UACR)方面的顯著療效。
lga腎病:2025年2月,韓國首爾腎臟中心在《KIREPORTS》上發(fā)表了一篇關(guān)于《WCN25-482 間充質(zhì)干細(xì)胞可能成為CKD嚴(yán)重IgA腎病的急救療法》的臨床研究成果。
本研究首次報道甲基強(qiáng)的松龍(MP)沖擊療法聯(lián)合自體脂肪源性干細(xì)胞(SVF/MSC)治療重癥IgA腎病的長期隨訪結(jié)果(2015年ASN會議首次發(fā)布),并拓展至10年以上療效分析。

患者分組:根據(jù)估算腎小球濾過率(eGFR)將病理確診的重度IgA腎病患者分為兩組:A組(n=7,eGFR>45 ml/min):平均年齡60歲;B組(n=3,eGFR<45 ml/min):平均年齡30.6歲。
臨床結(jié)果:
1.腎功能長期維持:
- A組(eGFR>45 ml/min):初始eGFR平均29 ml/min,8.1年隨訪后升至37 ml/min,顯著優(yōu)于自然病程;
- B組(eGFR<45 ml/min):初始eGFR平均106 ml/min,10.3年隨訪后穩(wěn)定在106 ml/min,避免進(jìn)展至終末期腎病(ESRD);
- 對照組(僅ARB治療):2年內(nèi)全部進(jìn)入血液透析。
2.腎活檢證實:
- A組與B組均顯示系膜增生減輕、上皮足突恢復(fù)及IgA沉積消失(免疫熒光鏡下);
- 電子致密物沉積(EDD)完全清除,提示病理活動性顯著降低。
3.安全性:全程未觀察到嚴(yán)重不良事件(SAEs),僅偶見短暫性低鉀血癥(發(fā)生率<10%)。
本研究證實,甲基強(qiáng)的松龍(MP)聯(lián)合自體脂肪源性干細(xì)胞(SVF/MSC)治療重癥IgA腎病可顯著延緩腎功能惡化,10年隨訪中A組eGFR從29 ml/min提升至37 ml/min,B組穩(wěn)定于106 ml/min,且組織學(xué)顯示病理活動性完全緩解,安全性良好。該療法為高危IgA腎病患者提供了非透析替代方案。
2.2 臨床轉(zhuǎn)化進(jìn)展
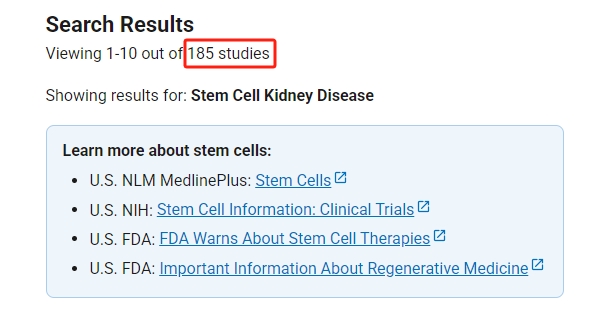
截止2025年5月16日,在美國國立衛(wèi)生研究院的最大臨床試驗注冊庫clinicaltrials.gov網(wǎng)站上注冊的有關(guān)干細(xì)胞治療腎病的臨床研究項目達(dá)到185項,已完成的達(dá)到97項,其余88項處于進(jìn)行中或招募階段。從試驗階段分布來看:
- Ⅰ期(安全性與劑量探索):90項(48.6%),主要評估干細(xì)胞治療的安全性、耐受性及最佳給藥方案。
- Ⅱ期(療效初步驗證):81項(43.8%),聚焦不同干細(xì)胞類型(如間充質(zhì)干細(xì)胞、誘導(dǎo)多能干細(xì)胞)對腎功能指標(biāo)(如eGFR、尿蛋白)的改善效果。
- Ⅲ期(大規(guī)模療效確認(rèn)):10項(5.4%),通過多中心隨機(jī)對照試驗驗證長期療效與安全性,推動療法標(biāo)準(zhǔn)化。
- Ⅳ期(長期隨訪或適應(yīng)癥擴(kuò)展):6項(3.2%),探索治療長期獲益及潛在新適應(yīng)癥。
三、未來發(fā)展方向
3.1 發(fā)展方向:
精準(zhǔn)化與聯(lián)合治療策略
- 個體化治療:結(jié)合基因檢測和生物標(biāo)志物篩選,針對不同腎病亞型(如糖尿病腎病、狼瘡性腎炎)制定個性化干細(xì)胞治療方案。
- 聯(lián)合傳統(tǒng)療法:干細(xì)胞治療與藥物治療(如RAAS抑制劑)、透析或腎移植結(jié)合,可能增強(qiáng)療效。例如,上海長征醫(yī)院的數(shù)據(jù)顯示,干細(xì)胞聯(lián)合胰島素治療的糖尿病腎病患者,肌酐值平均下降明顯。
技術(shù)創(chuàng)新驅(qū)動突破
- 基因編輯技術(shù):利用CRISPR-Cas9修飾干細(xì)胞,增強(qiáng)其抗炎能力或免疫兼容性。例如,有的研究提出通過基因編輯優(yōu)化MSCs的抗纖維化功能,有望提升治療效果。
- 生物材料輔助移植:開發(fā)可降解支架或水凝膠載體,提高干細(xì)胞在腎組織的滯留率。研究顯示,腎包膜下注射干細(xì)胞結(jié)合膠原蛋白支架,可使腎功能恢復(fù)率提高。
3.2 挑戰(zhàn)與解決策略:
建立統(tǒng)一標(biāo)準(zhǔn):需制定干細(xì)胞治療腎病的細(xì)胞制備標(biāo)準(zhǔn)、移植劑量及療效評估體系。?
推動多中心 RCT 研究:目前多數(shù)研究為單中心、小樣本,需開展 III 期臨床試驗驗證療效。
政策與支付體系支持:參考韓國、日本對干細(xì)胞療法的審批經(jīng)驗,建立 “風(fēng)險分級管理” 制度,對已完成Ⅱ期試驗的療法加速審批。同時,探索醫(yī)保支付創(chuàng)新,如將干細(xì)胞治療納入商業(yè)保險覆蓋范圍,提升可及性。
結(jié)語
干細(xì)胞治療腎病已從實驗室研究邁向臨床驗證階段,其在改善腎功能、延緩疾病進(jìn)展方面展現(xiàn)出顯著潛力。未來需通過多學(xué)科協(xié)作(如基因編輯、材料科學(xué))、大規(guī)模臨床試驗及個體化策略優(yōu)化,推動這一療法從實驗室走向廣泛臨床應(yīng)用。患者在選擇時應(yīng)基于專業(yè)評估,權(quán)衡潛在獲益與風(fēng)險,同時關(guān)注治療機(jī)構(gòu)的合規(guī)性與科學(xué)性。隨著技術(shù)突破與監(jiān)管完善,干細(xì)胞治療有望成為腎病精準(zhǔn)醫(yī)療的核心支柱,重塑疾病管理范式。
相關(guān)閱讀:間充質(zhì)干細(xì)胞治療腎病:不同劑量與給藥途徑會影響療效嗎?
參考資料:
Li, J., Wu, M. & He, L. Immunomodulatory effects of mesenchymal stem cell therapy in chronic kidney disease: a literature review.?BMC Nephrol?26, 107 (2025). https://doi.org/10.1186/s12882-025-04029-y
Madhav Swaminathan, Nelson Kopyt, Mohamed G. Atta, Jai Radhakrishnan, Kausik Umanath, Sunny Nguyen, Brian O’Rourke, Ashley Allen, Natalie Vaninov, Arno Tilles, Elizabeth LaPointe, Andrew Blair, Chris Gemmiti, Brian Miller, Biju Parekkadan, Rita N. Barcia, Pharmacological Effects of Ex?Vivo Mesenchymal Stem Cell Immunotherapy in Patients with Acute Kidney Injury and Underlying Systemic Inflammation,?Stem Cells Translational Medicine, Volume 10, Issue 12, December 2021, Pages 1588–1601,?https://doi.org/10.1002/sctm.21-0043
Natalya Krivoruchko, Lina Zaripova, Manarbek Askarov, Abay Baigenzhin, Temirlan Karibekov, Galiya Shaimardanova, Saltanat Bekturganova, #2733 TRANSPLANTATION OF MESENCHYMAL STEM CELLS – NEW FOCUS OF IMMUNE CORRECTION IN TREATMENT OF LUPUS NEPHRITIS,?Nephrology Dialysis Transplantation, Volume 38, Issue Supplement_1, June 2023, gfad063b_2733,?https://doi.org/10.1093/ndt/gfad063b_2733
Lixin Liu, Yiman Chen, Xuan Li, Juan Wang, Lina Yang,Therapeutic potential: The role of mesenchymal stem cells from diverse sources and their derived exosomes in diabetic nephropathy,Biomedicine & Pharmacotherapy,Volume 175,2024,116672,
ISSN 0753-3322,https://doi.org/10.1016/j.biopha.2024.116672.WCN25-482 Mesenchymal Stem Cell might be a rescue therapy in severe IgA nephropathy with CKDCho, Byoung Soo et al.Kidney International Reports, Volume 10, Issue 2, S633 – S634
免責(zé)說明:本文僅用于傳播科普知識,分享行業(yè)觀點(diǎn),不構(gòu)成任何臨床診斷建議!杭吉干細(xì)胞所發(fā)布的信息不能替代醫(yī)生或藥劑師的專業(yè)建議。如有版權(quán)等疑問,請隨時聯(lián)系我。



 掃碼添加官方微信
掃碼添加官方微信