萬字長文!NK細胞療法的生物機制和臨床進展
NK細胞作為一類無需抗原預先致敏即可非特異性殺傷腫瘤細胞的先天淋巴細胞,不少研究者和創業團隊已躬身入局推進基于NK細胞的創新療法,特別是CAR-NK細胞療法;據Market Research Guru咨詢機構的調研,全球NK細胞療法市場規模2021年達到3.40億美元,預計2028年將增長至10.09億美元,年均復合增長率(Compound Annual Growth Rate, CAGR)將達16.8%。
當下NK細胞療法多數仍處于臨床前及臨床研究階段,雖然挑戰多多但卻充滿希望,本文以NK細胞療法為主題,觀今朝以望未來,以享諸君。
一、NK細胞及其生物學特征、功能和調控
(一)NK細胞概述
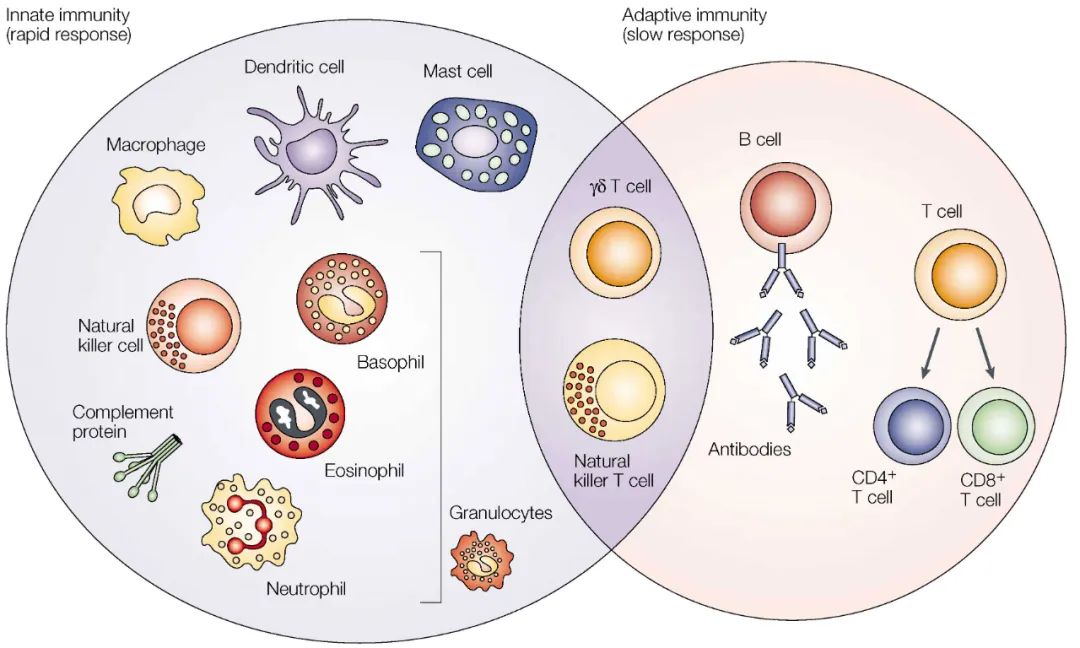
NK細胞是一種固有淋巴樣細胞(Innate Lymphoid Cell, ILP),是緊隨T細胞、B細胞之后的第三大類淋巴細胞;其形體較大,含有胞漿顆粒,通常采用“麻子臉”呈現NK細胞這種特征形態(圖1)。NK細胞是一個與生俱來的殺手,無需抗原預先致敏即可快速反應并非特異性產生殺傷效果,由此冠名“自然殺傷”。
NK細胞源自CD34+造血祖細胞(Hematopoietic Progenitor cells, HPCs),發育為淋巴樣祖細胞(Common Lymphoid Progenitor, CLP)后,逐漸下調CD34、上調CD56,進而發育為NK細胞(圖2)。NK細胞主要存在于淋巴結、骨髓、外周血、肺、脾臟、肝臟等器官內;根據CD56在細胞表面表達密度的多少,NK細胞包括CD56bright和CD56dim兩個亞群,其中CD56dim NK細胞占體內NK細胞數量的90%以上(圖3)。
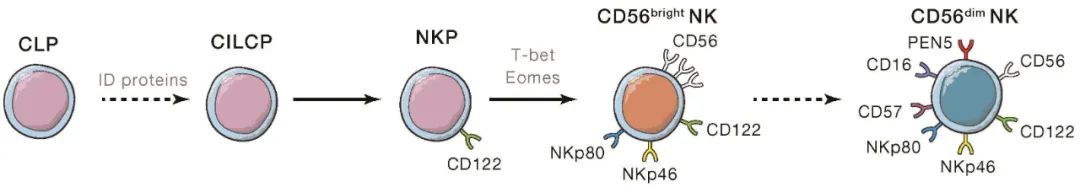
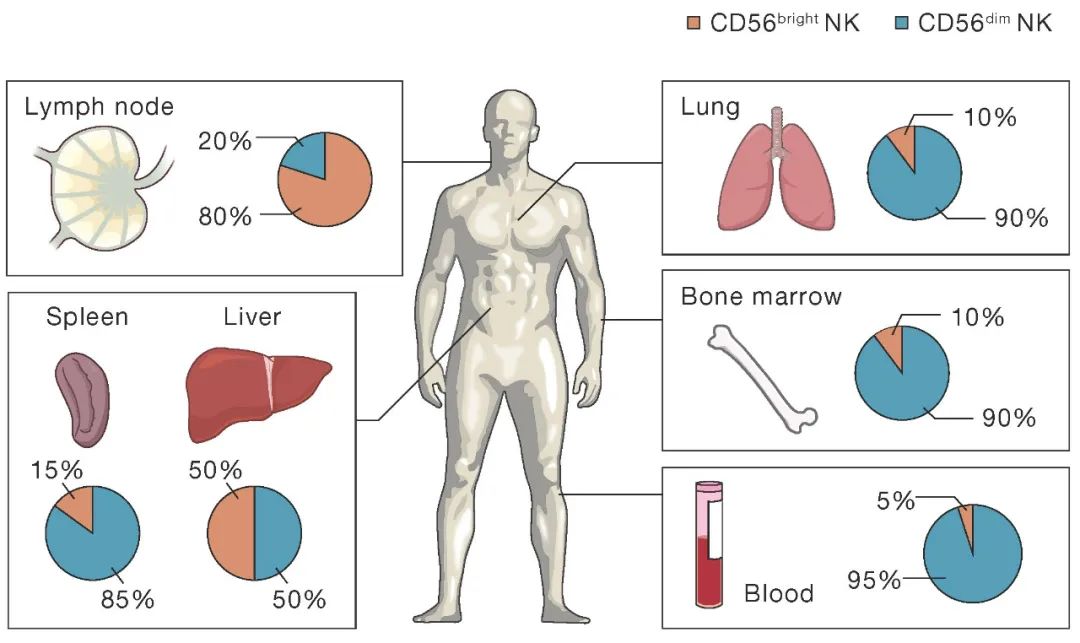
(二)NK細胞的表型及特征
基于細胞表面蛋白表達對細胞進行免疫分型是生物醫學研究中的常用方法,實踐中多采用流式細胞技術(Flow Cytometry),分型依據是免疫熒光檢測信號的有無(采用“+/-”或“positive/negative”表示)以及相對強度(采用“+/++/+++”或“bright/moderate/dim/variable”表示)。對于NK細胞一般采用CD56(有的研究會同時采用CD56和CD16)進行免疫分型,根據熒光亮度差異,將其分為CD56bright和CD56dim兩個亞群;進一步的研究表明,CD56bright亞群的細胞表面CD56高表達、CD16和殺傷細胞抑制受體(Killer-Cell Immunoglobulin-Like Receptors, KIRs)低表達,而CD56dim亞群則反之,呈現CD56低表達、CD16和KIRs高表達的特征(圖4)。由于表型不同,NK細胞的CD56bright和CD56dim亞群具有不同的生物學功能。
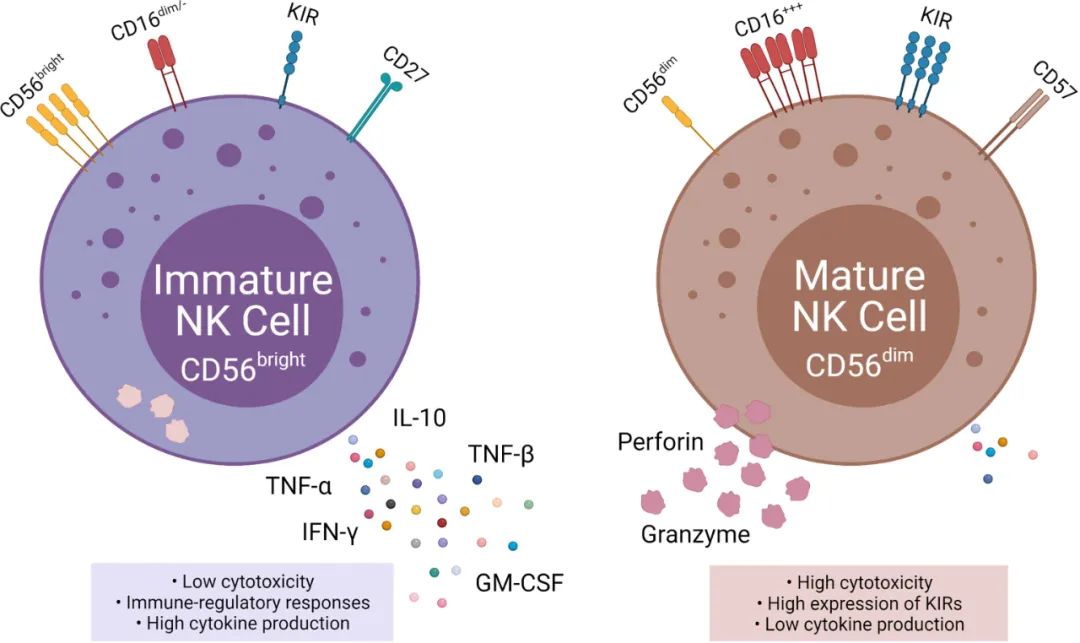
圖片來源:Front. Immunol., doi: 10.3389/fimmu.2021.732135; 康橙投資
CD56bright NK細胞是未成熟的NK細胞,其生物學功能有兩方面,不僅是CD56dim NK細胞的祖細胞,同時也是效應細胞。CD56bright NK細胞的細胞毒作用較弱,主要依靠分泌細胞因子(Cytokines)、生長因子(Growth Factor)、趨化因子(Chemokine)等發揮其免疫調節作用,例如干擾素γ(Interferon-γ, IFN-γ)、腫瘤壞死因子α(Tumor Necrosis Factor-α, TNF-α)、TNF-β、白細胞介素10(Interleukin-10, IL-10)和粒細胞巨噬細胞刺激因子(Granulocyte-Macrophage Colony-Stimulating Factor, GM-CSF)。CD56dim NK細胞的細胞因子分泌能力較弱,但是具備天然細胞毒作用和抗體依賴細胞介導的細胞毒作用(Antibody Dependent Cellular Cytotoxicity, ADCC),具有更強的殺傷力。
(三)NK細胞的功能及調控
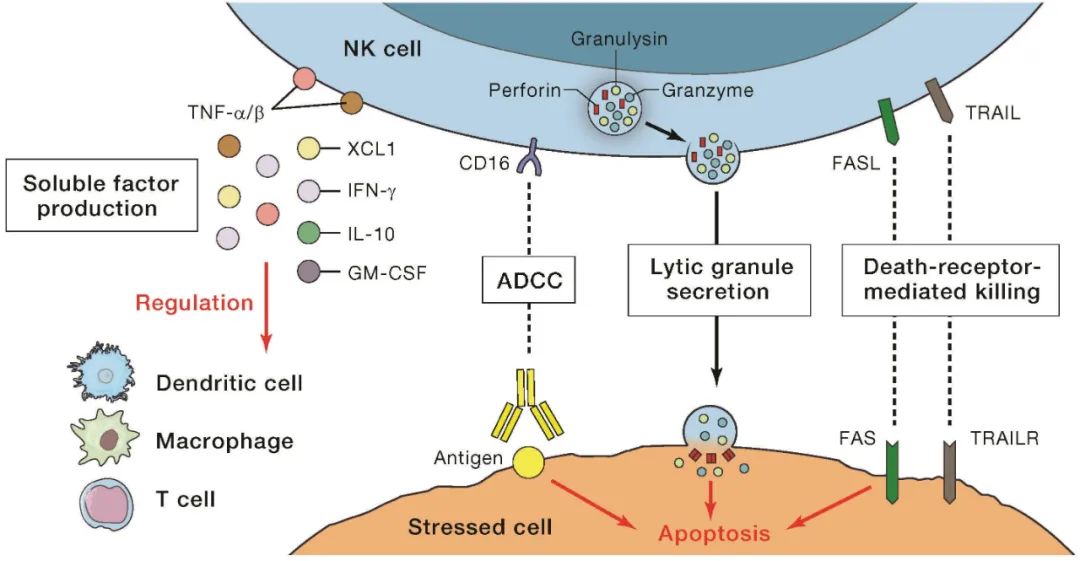
作為人體抗擊癌癥的第一道防線,NK細胞在防線中的作用主要包括(圖5):
- (1)NK細胞分泌穿孔素(Perforin)、顆粒酶(Granzyme)、顆粒溶素(Granulysin)等具有細胞毒性的溶解性顆粒,誘導靶細胞凋亡。
- (2)NK細胞表達TNF超家族成員結合相應受體誘導靶細胞凋亡,例如FAS結合FAS配體(FAS Ligand, FASL),腫瘤壞死因子相關凋亡誘導受體(TNF-related Apoptosis-Inducing Ligand, TRAIL)結合TRAIL受體(TRAIL Receptor, TRAILR)。
- (3)NK細胞分泌大量細胞因子(e.g. IFN-γ、TNF-α、TNF-β、IL-10),生長因子(e.g. GM-CSF)和趨化因子(e.g. CCL3、CCL4、CCL5、XCL1),招募巨噬細胞、樹突狀細胞、T細胞等友軍協同抗戰。
- (4)表達Fc受體(CD16),介導ADCC效應。
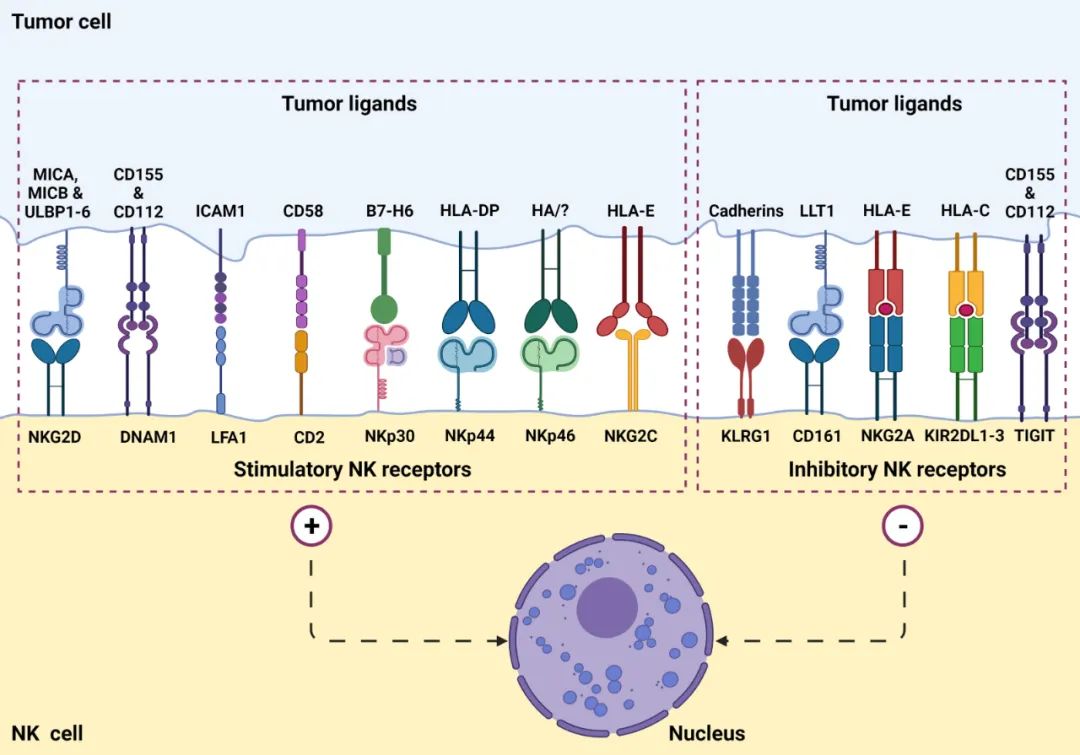
由于NK細胞缺乏特異性抗原識別受體,在防線中如何做到不誤傷“隊友”,其“防誤傷機制”與T細胞、B細胞不同。NK細胞功能的調控依賴于表面殺傷活化受體和殺傷抑制受體,兩者結合靶細胞相應的表面配體后分別起到激活NK細胞殺傷與抑制NK細胞殺傷的作用(圖6)。
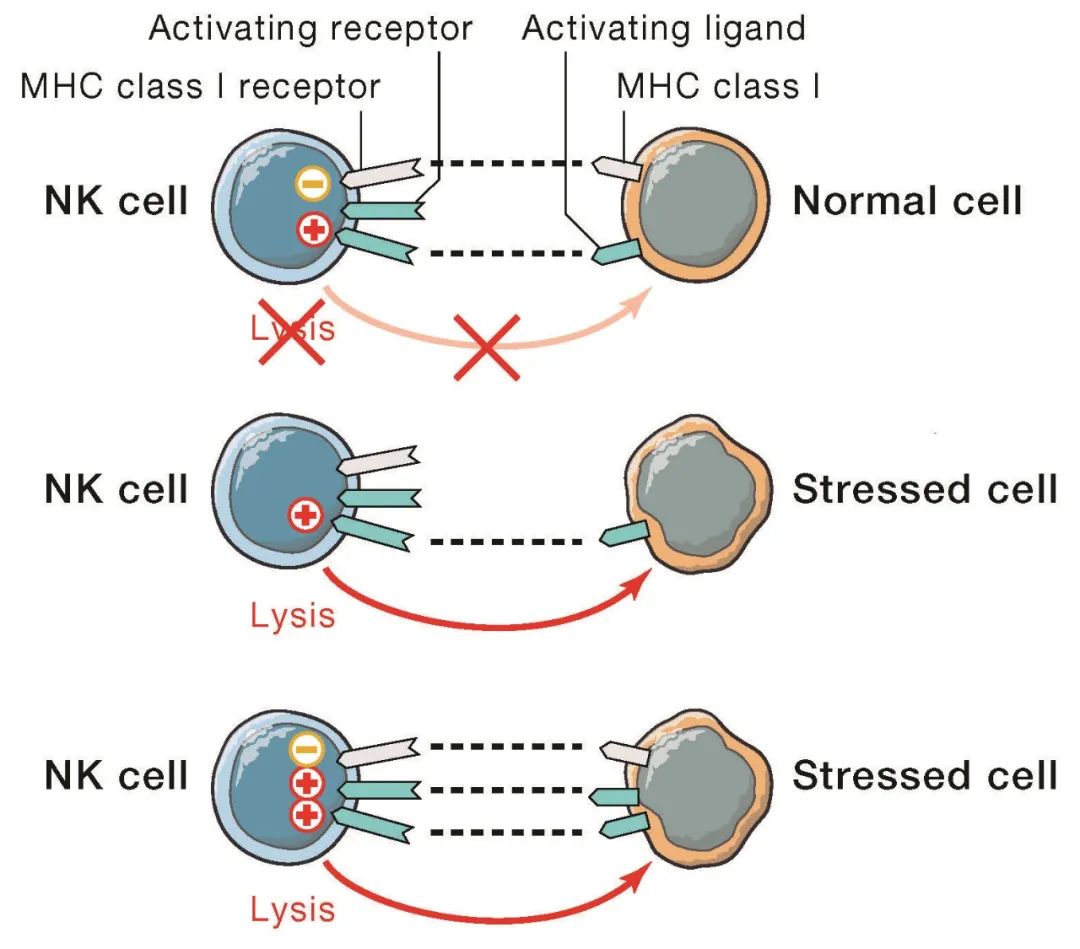
在正常生理情況下,兩個受體同時與正常細胞表面配體主要組織相容性復合體(Major Histocompatibility Complex, MHC)I類分子(MHC-I)結合,此時抑制信號占主導,NK細胞不殺傷正常細胞;在感染或腫瘤的病理情況下,MHC-I缺失或下調,非MHC-I異常表達或上調,此時抑制信號缺失,活化信號占主導,從而激活NK細胞殺傷靶細胞(圖7)。形象地理解,NK細胞基于“有罪推論”:首先假定靶細胞有問題,若靶細胞可以出示“良民身份證”,則將其判定為正常細胞,不予以殺傷;若靶細胞不能出示正確有效的證件,則將其判定為感染或腫瘤細胞,NK細胞便投入戰斗。
二、基于NK細胞的創新療法
(一)基于NK細胞的創新療法策略概述
NK細胞最早發現于上世紀七十年代,至今人們對其生理學機制及應用仍在不斷探索。近年來腫瘤免疫療法、細胞療法、基因編輯等新技術不斷獲得突破,其中基于NK細胞的創新療法也顯現巨大的臨床轉化潛力。根據設計思路的不同,基于NK細胞的創新療法分為激活殺傷活化受體和阻斷殺傷抑制受體兩條路徑,細分為五種策略(圖8)。
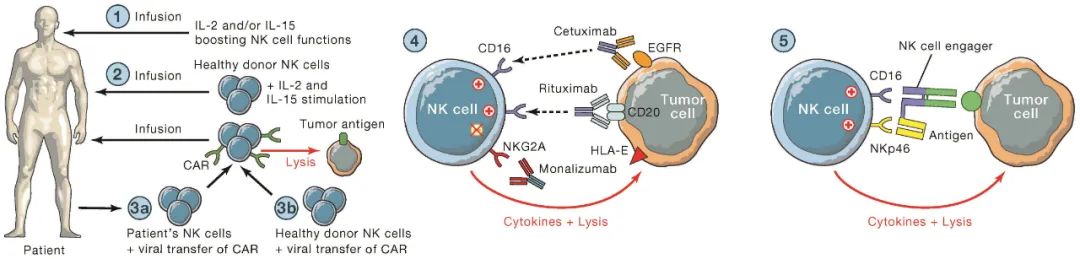
(1)細胞因子療法。向患者輸注IL-2、IL-15等細胞因子以激活體內NK細胞活性。
(2)NK細胞的過繼性細胞療法(Adoptive Cell Therapy, ACT)。向患者輸注健康的經活化的NK細胞,其中回輸的NK細胞在體外經過IL-2、IL-15等細胞因子的活化處理。
(3)基因工程化NK細胞療法。向患者輸注基因改造的NK細胞,例如CAR修飾的NK細胞(CAR-NK)。
(4)單克隆抗體(Monoclonal Antibody, mAb)療法。根據抗體的靶向不同,可以分為兩類:i. 采用靶向腫瘤相關抗原的治療性抗體,例如靶向表皮生長因子受體(Epidermal Growth Factor Receptor, EGFR)的西妥昔單抗(Cetuximab)、靶向CD20的利妥昔單抗(Rituximab),通過NK細胞誘導ADCC效應達到治療目的;ii. 采用直接靶向NK細胞抑制受體的抗體,例如靶向NKG2A的莫那利珠單抗(Monalizumab),活化NK細胞對腫瘤細胞進行殺傷。
(5)NK細胞銜接器(Engager)。銜接器一般是雙特異性抗體或三特異性抗體(e.g. 德國生物技術公司Affimed),可以同時靶向腫瘤細胞抗原以及NK細胞活化受體,將NK細胞和腫瘤細胞“拉攏”在一起,進而引發NK細胞殺傷腫瘤細胞。
根據輸注有效物質的屬性進行分類,策略(1)、(4)和(5)歸為生物藥,策略(2)和(3)歸為細胞療法,本文以下內容對NK細胞療法重點展開介紹。
(二)NK細胞療法
1. NK細胞療法技術流程及要點
NK細胞療法與其他免疫細胞療法的技術流程相似,概括起來主要包括三大環節(圖9):獲得細胞、擴增生產、臨床使用。
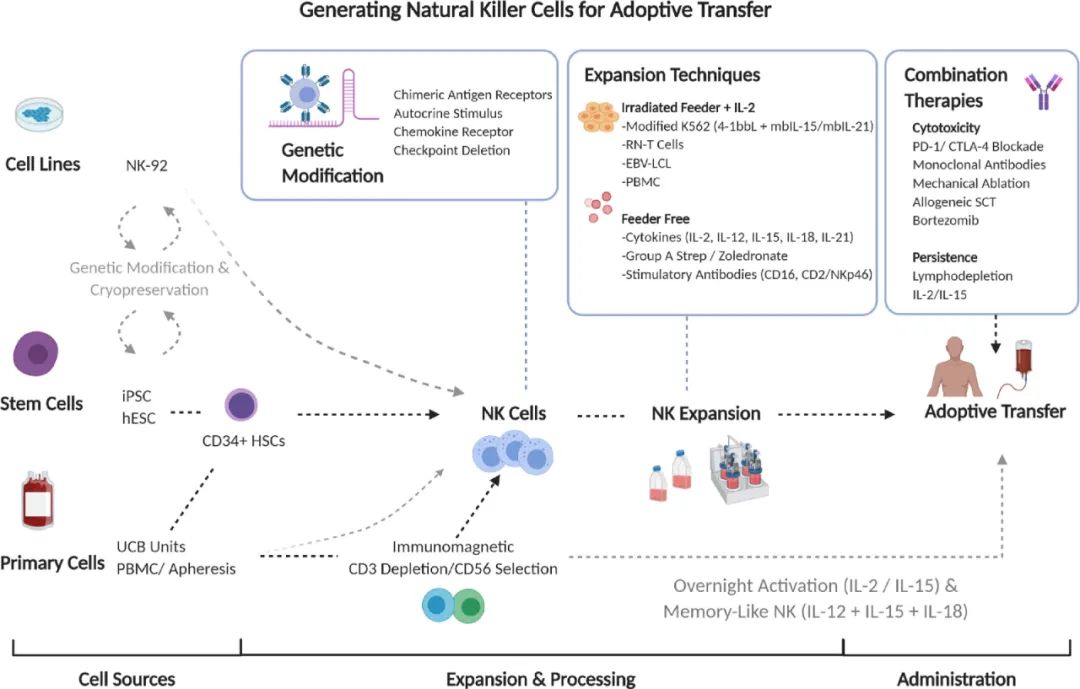
(1)獲得細胞
獲得細胞這個環節還涉及NK細胞來源、分離富集、活化、改造等若干步驟,本小節僅對NK細胞來源和CAR-NK細胞展開討論。
i. NK細胞來源
如何獲得合適的NK細胞是NK細胞療法的萬里長征第一步,目前主要來源于以下三類細胞,優劣各有不同:
(i)原代NK細胞,主要通過采外周血(Peripheral Blood, PB)、臍帶血(Umbilical Cord Blood, UCB或CB)后分離獲得。外周血來源的NK細胞(PB-NKs)細胞具有安全性高、殺傷活性強的優點,但是細胞純度低且難以大量擴增、低溫保存會影響細胞活性,給規模化生產帶來較大挑戰;臍帶血來源的NK細胞(CB-NKs或UCB-NKs)可分化擴增且獲得不錯的臨床數據(e.g. MD Anderson癌癥中心),但是缺點在于未完全分化、殺傷力有限、且有致瘤性風險。
(ii)NK細胞系,NK細胞有許多成熟的細胞系,包括NK-92、NKG、YT、NK-YS、HANK-1、YTS、NKL等,目前臨床試驗中主要采用NK-92細胞系,是從一位患有急進性非霍奇金淋巴瘤的50歲白人男性外周血單核細胞衍生來的一株IL-2依賴型NK細胞株。NK-92細胞系相較于原代NK細胞最大的優勢在于不涉及分選純化步驟、體外擴增得到的細胞群體一致性更好、其表面的殺傷抑制受體表達很低從而具有更優異的殺傷能力,但是NK-92細胞系的缺點也很明顯,主要表現在需要輻照處理、存在致瘤性以及體內存活時間極短。
(iii)由干細胞定向分化所得的NK細胞,目前臨床試驗中選用的干細胞為人胚胎干細胞(Human Embryonic Stem Cell, hESC)和誘導性多能干細胞(Induced Pluripotent Stem Cell, iPSC)。iPSC定向分化的NK細胞(iNKs)的研究熱度很高,是目前國內外眾多公司主要采用的一個NK細胞來源。iNKs綜合了原代NK細胞和NK-92細胞系的優點,表型與原代NK細胞更為接近,生長能力強,有利于獲得充足且同質的細胞,更容易滿足臨床應用要求。不過iNKs技術難度較高,安全性和臨床有效性仍需面臨監管挑戰;也存在潛在的致癌風險,已有大量研究從表觀遺傳修飾、染色質組織、代謝重編程等途徑來抑制其致癌潛能。另外,也有研究采用CD34+ HPC向NK細胞定向誘導分化的方式獲得NK細胞。
ii. CAR-NK細胞
CAR-NK細胞需要在NK細胞基礎上“加裝”CAR(圖10),對于原代NK細胞、NK細胞系而言,僅需對其直接改造“加裝”CAR;對于源于干細胞定向分化的CAR-NK細胞,其技術路徑還可以分為兩種,一種是對干細胞改造“加裝”CAR,然后定向分化為可以表達CAR的NK細胞;另一種是干細胞先定向分化為NK細胞,然后再改造“加裝”CAR。
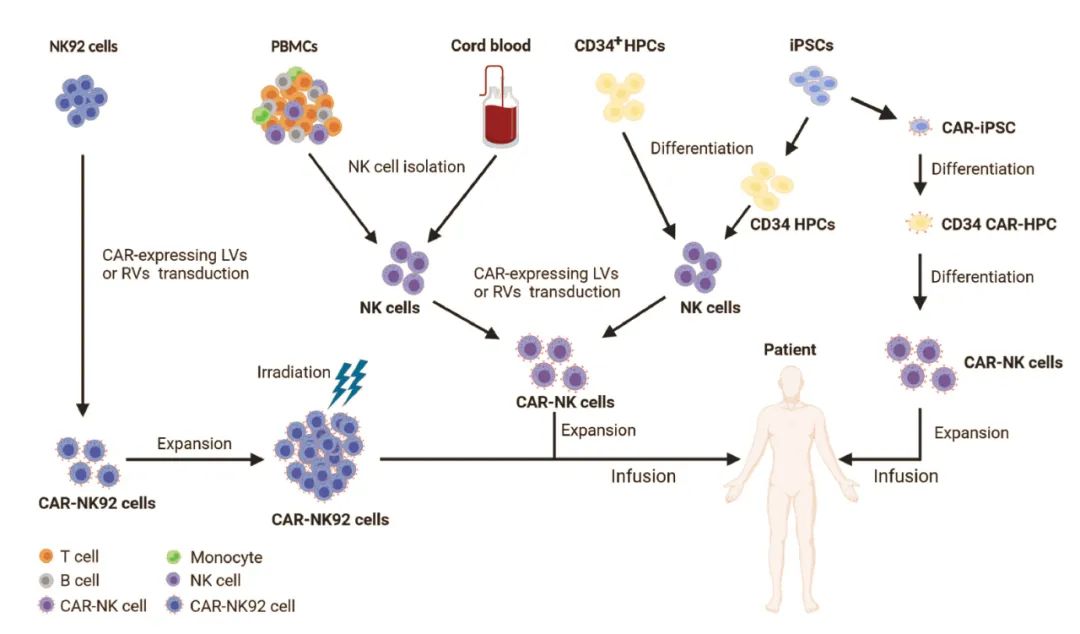
給NK“加裝”CAR的目的可以使得NK細胞具有靶向性,同時新建一條活化NK細胞的激活通路并增強其抗腫瘤效應。CAR結構的設計以及轉導對于CAR-NK的治療功效至關重要。
CAR-NK借鑒傳承了CAR-T的基本結構框架和轉導方式,早期的CAR-NK構建更多基于參與T細胞激活的共刺激域(Costimulatory Domain),現在人們越來越重視NK特異性信號轉接器,例如一些研究發現DAP10、DAP12和2B4發揮著特別重要的作用,這些細胞內信號轉接器在與它們各自的上游受體結合后介導NK細胞活化。
基因轉導(Gene Transduction)的穩定性是實現效應細胞穩定表達CAR的前提。當前常用的CAR-NK轉導技術包括病毒載體和非病毒載體兩類(圖11),其中常用的病毒載體包括逆轉錄病毒(Retrovirus)、慢病毒(Lentivirus)和腺相關病毒(Adeno-Associated Virus, AAV),常用的非病毒載體包括利用電穿孔(Electroporation)、睡美人轉座子(Sleeping Beauty Transposon)、脂質體(Liposome)等方式轉導DNA、mRNA。與CAR-T類似,CAR-NK的基因轉導也面臨效率低的技術困境,開發具有更高轉導效率和安全性的載體是CAR-NK未來走向臨床應用的關鍵。
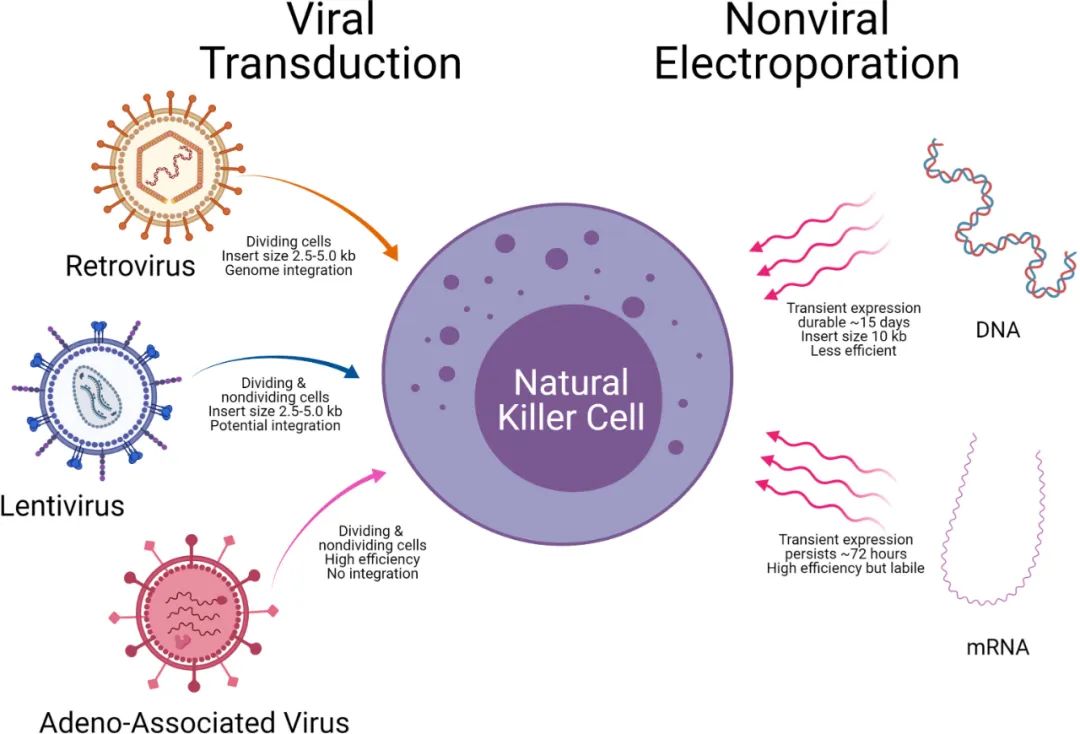
圖片來源:Front. Immunol., doi: 10.3389/fimmu.2021.732135; 康橙投資
(2)擴增生產
細胞療法在臨床應用時需要大量效應細胞,有研究表明適合臨床應用的NK細胞數量范圍在5×106-1×108 細胞數量/體重(kg)。在獲得NK細胞(包含CAR-NK細胞)后,如何在體外高效擴增成為產業轉化中需要面臨的又一挑戰,需要考察擴增能力、適配NK/CAR-NK細胞的生長特點、安全性、便捷性、生產周期、生產成本等諸多因素,同時還要考慮生產工藝不能引致效應細胞發生非預期或異常的變化。
目前不同研究機構或開發企業各自擁有不同的NK細胞擴增技術,根據培養工藝的特點,概括起來主要分為兩類(圖9):
i. 滋養細胞(Feeder Cell)+細胞因子的培養工藝(Feeder-Dependent)
該類方法廣為采用的滋養細胞為K562細胞或經基因改造的K562細胞,該細胞表面可以穩定表達多種細胞因子受體,在多種細胞因子協同作用下,外周血單個核細胞中的自然殺傷細胞得到定向激活和擴增。
該類培養工藝的優點在于細胞擴增活率高、速度快,CD56bright NK細胞純度高,CD16等受體表達比例高,所收獲的NK細胞具有較強的殺傷性。有研究報道,經過這樣的培養方式可以收獲擴增超過300倍的NK細胞。不過該方法引入的細胞為腫瘤細胞,其潛在風險難以完全消除;將正常細胞與腫瘤細胞共培養,然后將收獲所得的NK細胞回輸體內存在難以克服的倫理障礙;引入滋養細胞后,對細胞來源、歷史培養情況、安全性等方面需要建立管理標準和質控體系,進一步增加了NK細胞產品的報批難度。
ii. 純因子培養工藝(Feeder-Free)
該類培養工藝使用IL-2、IL-12等細胞因子刺激,向NK細胞方向誘導或激活,同時配合相應的細胞培養基,使NK細胞大量增殖。
該類培養工藝的優點在于安全性,其所用的細胞因子在體內原本就存在,整個培養過程相當于在體外模擬體內環境;由于無活細胞成分,較添加滋養細胞的培養方法而言,降低了產品報批難度。但是純因子培養技術的生產效率較低,在培養過程中需要消耗大量的細胞因子,細胞因子研發成本及價格都很高,所以導致該類工藝的生產成本居高不下;另外,該類工藝所收獲的NK細胞純度不及添加滋養細胞的培養工藝,存在脫靶效應,殺傷效果偏弱。
在以上的分類基礎上,根據培養基是否含有血清和動物源成分,可以作進一步地細分。
(3)臨床使用
NK細胞產品的凍存(Cryopreservation)復蘇(Thaw)是回輸人體前的最后一個技術環節,對該環節工藝的摸索是NK細胞產品走向大規模臨床應用的必修課。有研究發現,NK細胞對凍存復蘇極為敏感,復蘇后的NK細胞存活率和細胞毒作用顯著降低;進一步研究發現加入IL-2等細胞因子孵育后可以再次激活NK細胞功能(圖9)。
凍存復蘇環節一般遵循“慢凍快融”原則。慢凍可使細胞逐步脫水,以避免細胞內產生大量冰晶;快融則是使凍存時產生的胞外冰晶迅速融化,避免其緩慢融化后進入細胞再結晶而造成的損害(圖12)。在凍存環節,冰晶結構與降溫速率密切相關,有研究結果表明1°C/分鐘或更慢的降溫速率對NK細胞是較為合適的;而在復蘇環節,合適的復蘇速率對最終回輸人體的NK細胞狀態至關重要。
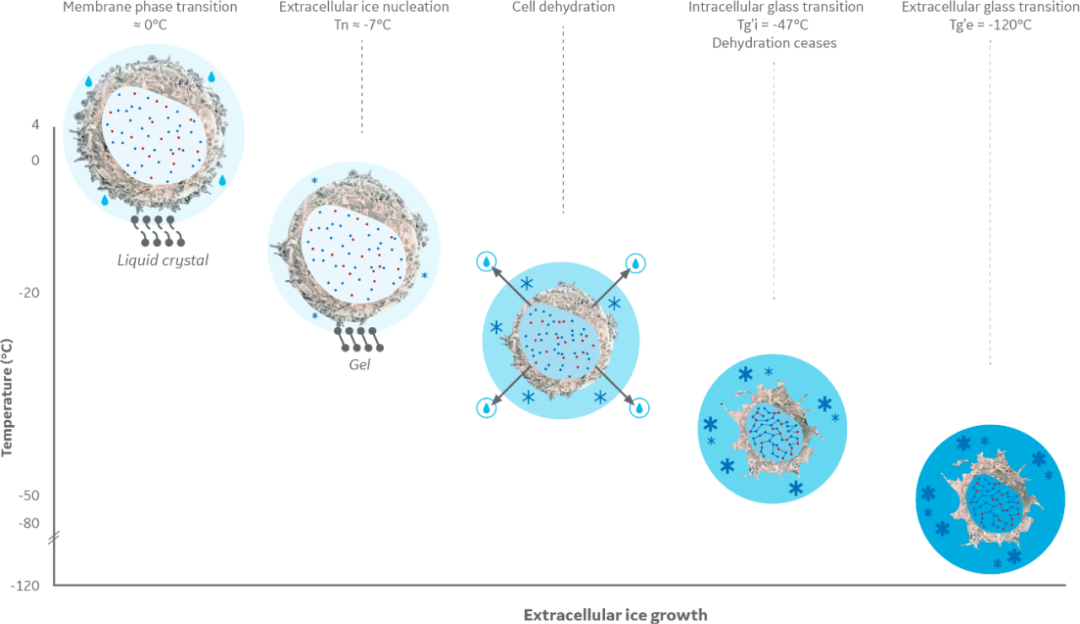
2. NK細胞療法的優勢
T細胞療法是各類細胞療法中發展較為成熟的,從2017年開始美國食品藥品監督管理局(Food and Drug Administration, FDA)已經陸續批準了6款CAR-T與1款TCR-T細胞療法產品,國家藥品監督管理局(National Medical Products Administration, NMPA)也批準了兩款CAR-T細胞療法產品。T細胞療法給血液腫瘤患者帶來了痊愈的希望,但是脫靶效應(Off-Target Effect)、細胞因子風暴(Cytokine Storm; 也稱為細胞因子釋放綜合征, Cytokine Release Syndrome, CRS)、對實體瘤效果有限、治療費用十分昂貴等缺陷,也制約了T細胞療法的應用。
相對T細胞療法而言,NK細胞療法具有以下幾個優勢。
(1)更廣泛的細胞來源。與T細胞療法目前主要依賴患者自體T細胞不同的是,NK細胞療法可以采用多種不同來源的NK細胞。截至目前,進入臨床階段的NK細胞療法的細胞來源主要包括外周血、臍帶血、NK-92細胞系、iPSC和hESC。
(2)更廣泛的適應癥。NK細胞療法被廣泛用于各種癌癥治療,包括血液腫瘤(Hematological?Malignancy)和實體瘤(Solid?Tumor),其中CAR-NK療法有望突破CAR-T療法難以治療實體瘤的瓶頸。
(3)更多的殺傷途徑。NK細胞療法具有更多的腫瘤殺傷途徑,包括分泌穿孔素、顆粒酶,激活凋亡途徑以及介導ADCC。
(4)更好的安全性。異體NK細胞不會引起移植物抗宿主病(Graft-versus-Host?Disease,?GvHD),供者NK細胞KIR與受者人白細胞抗原(Human?Leukocyte?Antigen,?HLA)不匹配而誘導的異體反應(Alloreactivity)亦可改善腫瘤治療或干細胞移植的治療效果。對于CAR-NK細胞療法而言,其安全性主要體現在CAR-NK細胞不分泌炎癥因子(Inflammatory?Cytokines),一般不誘發細胞因子風暴;同時體內存活周期短,不易產生長期毒性。
(5)可作為通用(Universal)即用(Off-the-Shelf)產品。基于NK細胞的高安全性,NK細胞療法的一個巨大價值在于可作為通用即用產品,適用于不同個體、可長期凍存,能為危重患者提供及時的治療,同時還能有效降低生產成本和終端售價,進而降低患者自費以及醫保支付壓力。
3. 注冊路徑分析
(1)目前的監管情況
目前中國對于細胞治療采用“雙軌制”:一種軌道是將細胞療法產品作為藥品管理, NMPA及其下屬部門對臨床試驗以及產品注冊進行監管審批;另一種軌道則是將細胞療法作為醫療技術管理,由國家衛生健康委員會(National Health Commision, NHC)及其下屬部門進行監管審批,準予在醫療機構實現臨床技術應用。
(2)監管政策動態
2019年3月,NHC發布了《體細胞治療臨床研究和轉化應用管理辦法(試行)》征求意見稿,該辦法表明對體細胞臨床研究進行備案管理,并允許臨床研究證明安全有效的項目經過備案在相關醫療機構進入轉化應用。相比藥品注冊,醫療技術備案更為簡單快捷,由此也吸引研發機構與醫療機構聯合開展研究者發起的臨床試驗(Investigator-Initiated Trial, IIT)。然而時至今日,該辦法仍未落地,意味著細胞治療通過第三類醫療技術進入臨床應用的路線暫未獲得官方支持。
2021年2月和12月,NMPA藥品審評中心(Center?for?Drug?Evaluation,?CDE)分別發布了《免疫細胞治療產品臨床試驗技術指導原則(試行)》和《基因修飾細胞治療產品非臨床研究技術指導原則(試行)》這兩部技術指導原則,分別對免疫細胞治療產品和基因修飾細胞治療產品的開發做了規范。2021年2月,NHC在官網上發布了《對十三屆全國人大三次會議第4371號建議的答復》,答復函中明確提出:“我委一直鼓勵和支持干細胞、免疫細胞等研究、轉化和產業發展。
干細胞、免疫細胞等細胞制劑具有明顯的藥品屬性。國家藥品監管部門已經為相關制劑通過藥品審批制定配套政策,審批后可以迅速廣泛應用,既有利于保障醫療質量安全,又有利于產業化、高質量發展。”2022年1月,NMPA發布《藥品生產質量管理規范-細胞治療產品附錄(征求意見稿)》和《嵌合抗原受體T細胞(CAR-T)治療產品申報上市臨床風險管理計劃技術指導原則》兩項與細胞治療產品密切相關的法規。
基于以上一系列政策和意見的頒布,將細胞療法產品作為藥品管理“似乎”更契合我國監管的發展方向,也許在未來可能從“雙軌制”變為以藥品管理的“單軌制”,與以美國、歐盟為代表的國際主流做法接軌。
(3)當前NK細胞療法注冊的建議
NK細胞與T細胞均為免疫細胞,由此NK細胞療法可以模仿CAR-T的注冊路徑,按照新藥方式在國內注冊申報。
2021年11月11日,CDE批準了第一款我國自主研發的針對“晚期上皮性卵巢癌治療的靶向間皮素(Mesothelin,MSLN)嵌合抗原受體NK細胞(CAR-NK)注射液”的臨床試驗申請。通過眾多CAR-T與CAR-NK項目的審評審批,CDE專家在細胞治療領域也逐步積累了豐富經驗,建議NK細胞療法的開發者與CDE保持緊密溝通,爭取獲得更多協助與指導。
三、NK細胞療法的臨床在研格局及融資進展
目前海內外已有多家科研機構及初創企業布局NK細胞療法賽道,其中NK細胞ACT療法用于腫瘤治療的效果相對有限,而用于增強免疫力以及抗衰老方向的研究較多;相比之下,CAR-NK療法在腫瘤治療領域表現了更好的潛力,已有多家藥企的CAR-NK管線進入臨床試驗階段。以下我們主要針對CAR-NK療法的臨床在研格局與融資進展進行簡要介紹。
(一)臨床在研格局
目前,MD Anderson癌癥中心(合作方Takeda武田制藥)與Fate Therapeutics(NASDAQ: FATE)公布了CAR-NK的相關臨床數據。
2020年2月,MD?Anderson癌癥中心在知名醫學期刊The?New?England?Journal?of?Medicine上公布了關于CAR-NK治療CD19陽性淋巴瘤的I/II期臨床研究(NCT03056339)數據(圖13)。
臨床試驗結果顯示,對11例復發性/難治性非霍奇金淋巴瘤(Non-Hodgkin?Lymphoma,?NHL)患者和慢性淋巴細胞性白血病(Chronic?Lymphocytic?Leukemia,?CLL)患者分別給予不同劑量的臍帶血HLA不匹配的抗CD19?CAR-NK細胞,大多數患者顯現出臨床療效,而且未觀察到重大毒性反應。
參與該研究的11名患者中,有8名(73%)對治療有反應,其中7名(4名NHL患者和3名CLL患者)達到了完全緩解,5名有反應的患者緩解后繼續接受治療。治療反應迅速,且注入的CAR-NK細胞擴增并以低水平持續至少12個月。該療法安全性良好,受試者未出現細胞因子釋放綜合征、神經毒性以及移植物抗宿主病,并且IL-6、TNF-α等炎癥細胞因子與基線水平相比均未見升高。
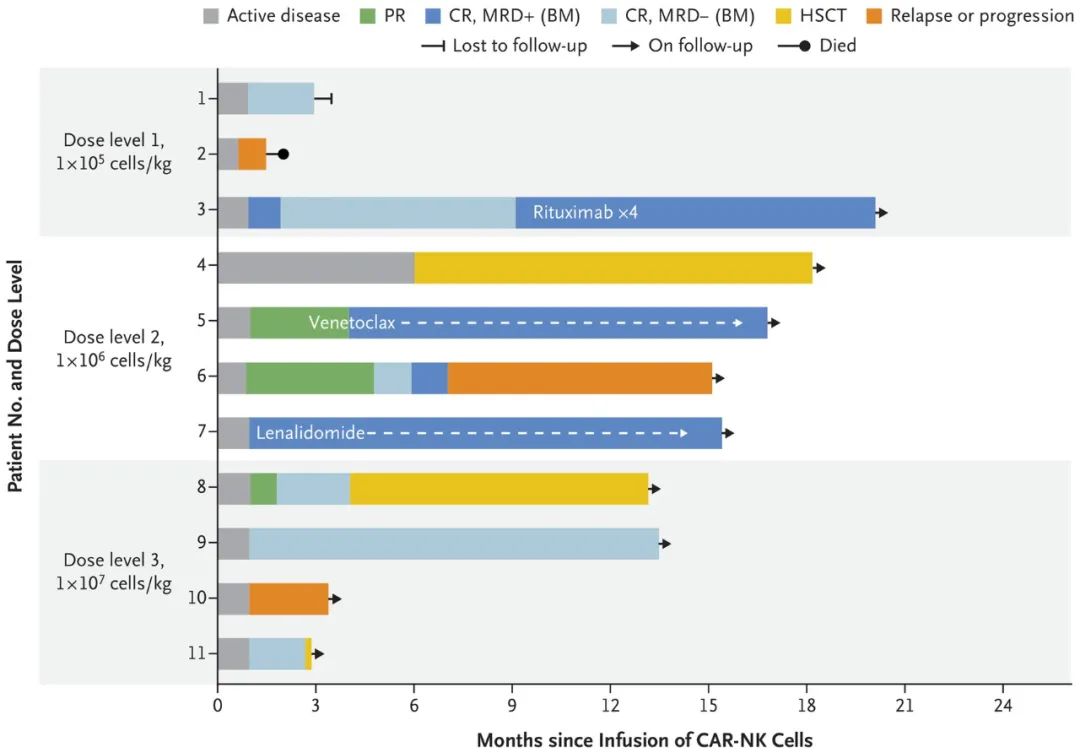
該產品(編號TAK-007)已于2019年由MD Anderson癌癥中心與Takeda達成獨家許可和研究協議,Takeda于2021年11月啟動了一項關鍵的II期開放標簽多中心臨床研究(NCT05020015)來評價TAK-007在治療成人復發/難治性B細胞非霍奇金淋巴瘤中的安全性和有效性。該試驗將在全球范圍內進行,預計將招募約242名患者。
Fate Therapeutics是NK細胞療法的全球引領者,目前有多款NK細胞療法產品進入臨床試驗階段,Fate關于CAR-NK療法最新的臨床數據報道是在2021年12月美國血液學會(American Society of Hematology, ASH)年會上。Fate展示了針對復發/難治性B細胞淋巴瘤(B-Cell Lymphoma, BCL)患者FT596項目的臨床I期中期數據,FT596是該公司多抗原靶向、iPSC源性的CAR-NK候選產品。
摘要展示了截至2021年10月11日的臨床數據,包含了來自三個劑量隊列(分別為3000萬、9000萬和3億細胞)的25名可評估患者(單藥組n=12;聯合組n=13;聯合給藥利妥昔單抗),其中24名患者的療效也可評估(單藥治療組n=12;聯合治療組n=12),這25名患者的前期中位治療線數為四線。在ASH報告的數據截止日期之后,聯合組第三個單劑量隊列中的另一名患者出現了初始抗腫瘤反應。
在共26名患者的單藥治療和聯合治療的高于9000萬劑量隊列中,18名患者(69%)在第29天實現了客觀反應,其中12名患者(46%)單劑量FT596后實現了完全緩解。其中9名之前接受過自體CD19靶向CAR-T細胞療法的患者中有6名在單劑量FT596治療后的第29天達到了客觀反應(67%)。在總共包括12名患者的聯合組中,9名患者(75%)在單次給藥后的第29天實現了客觀緩解,其中包括7名患者(58%)實現了完全緩解。
FT596表現出良好的安全性,所有患者沒有觀察到免疫效應細胞相關神經毒性綜合征(Immune Effector Cell–Associated Neurotoxicity Syndrome, ICANS)與GvHD,僅有3次細胞風暴報告(均為一、二級)。主要的不良反應是中性粒細胞計數下降、嘔吐、貧血、白細胞數減少、疲勞和血小板減少等,未觀察到B細胞或T細胞介導的排異反應。
除了以上已公布的CAR-NK臨床結果以外,還有多家企業也在積極推進,我們對目前已經進入臨床研究階段的代表企業和CAR-NK管線進行了梳理(表1)。
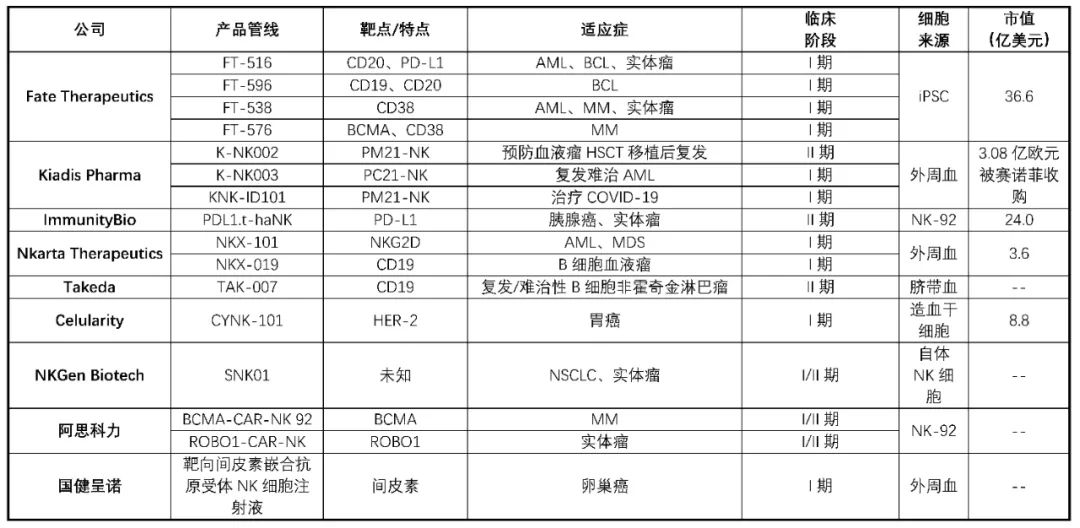
GBM:多形性膠質母細胞瘤;AML:急性髓系白血病;MM:多發性骨髓瘤;MDS:骨髓增生異常綜合癥;BCL:B細胞淋巴瘤;CLL:慢性淋巴細胞白血病;ALL:急性淋巴細胞白血病;NSCLC:非小細胞肺癌;BCMA:B細胞成熟抗原。
數據來源:康橙投資
(二)重磅交易與融資進展
MD Anderson癌癥研究中心與Fate Therapeutics臨床數據的公布,進一步堅定了大家開發CAR-NK產品的信心。CAR-NK在腫瘤治療領域的巨大潛力,獲得了科學界和資本市場的廣泛認可,海外已有Fate Therapeutics、Century Therapeutics(NASDAQ: IPSC)、Caribou Biosciences(NASDAQ: CRBU)、Cytovia Therapeutics(NASDAQ: CYTX)等多家CAR-NK技術公司登陸納斯達克,此外多家跨國藥企也積極參與布局該賽道,達成了多筆重磅合作協議(表2)。
表2 CAR-NK領域重磅交易
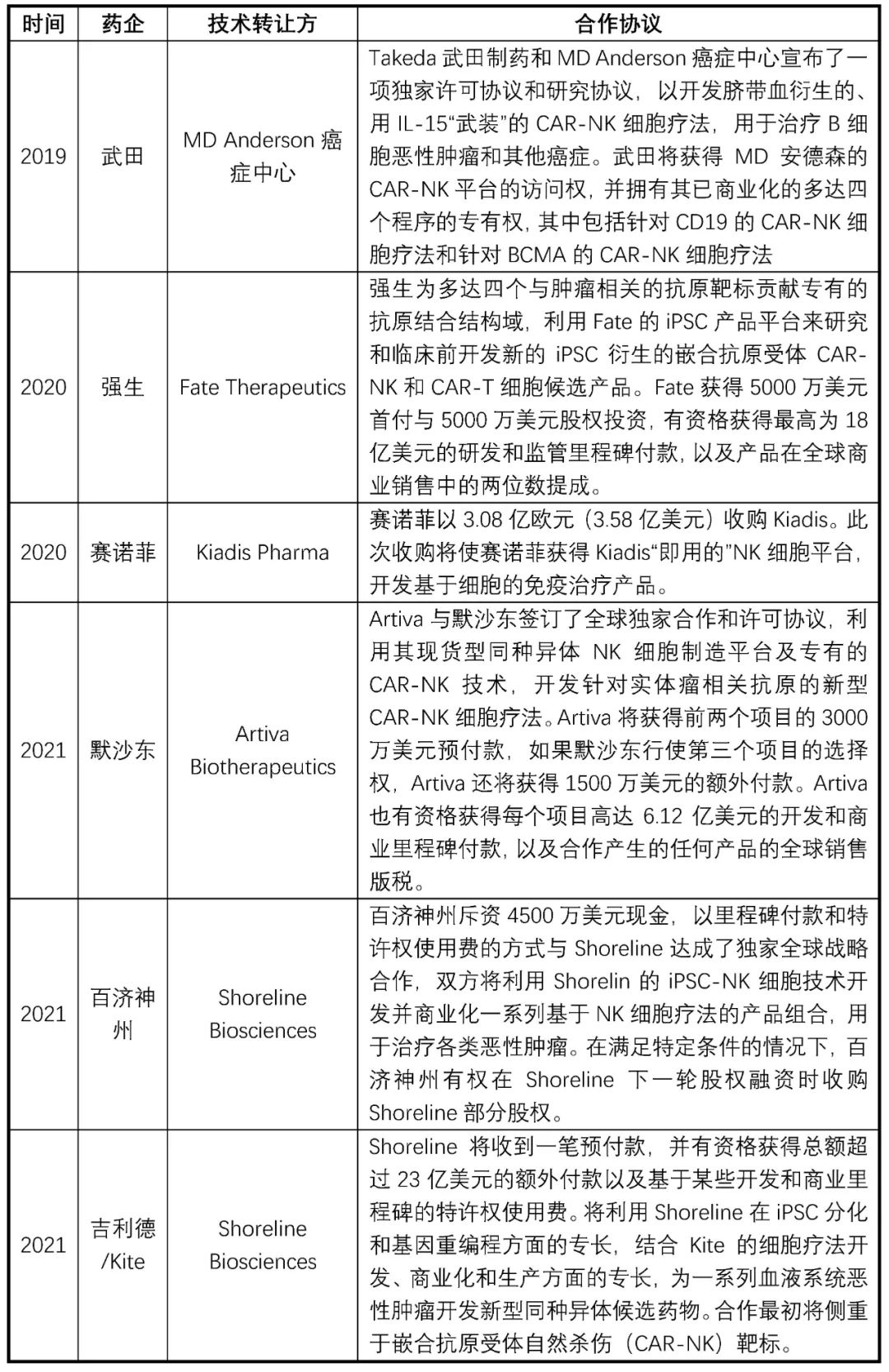
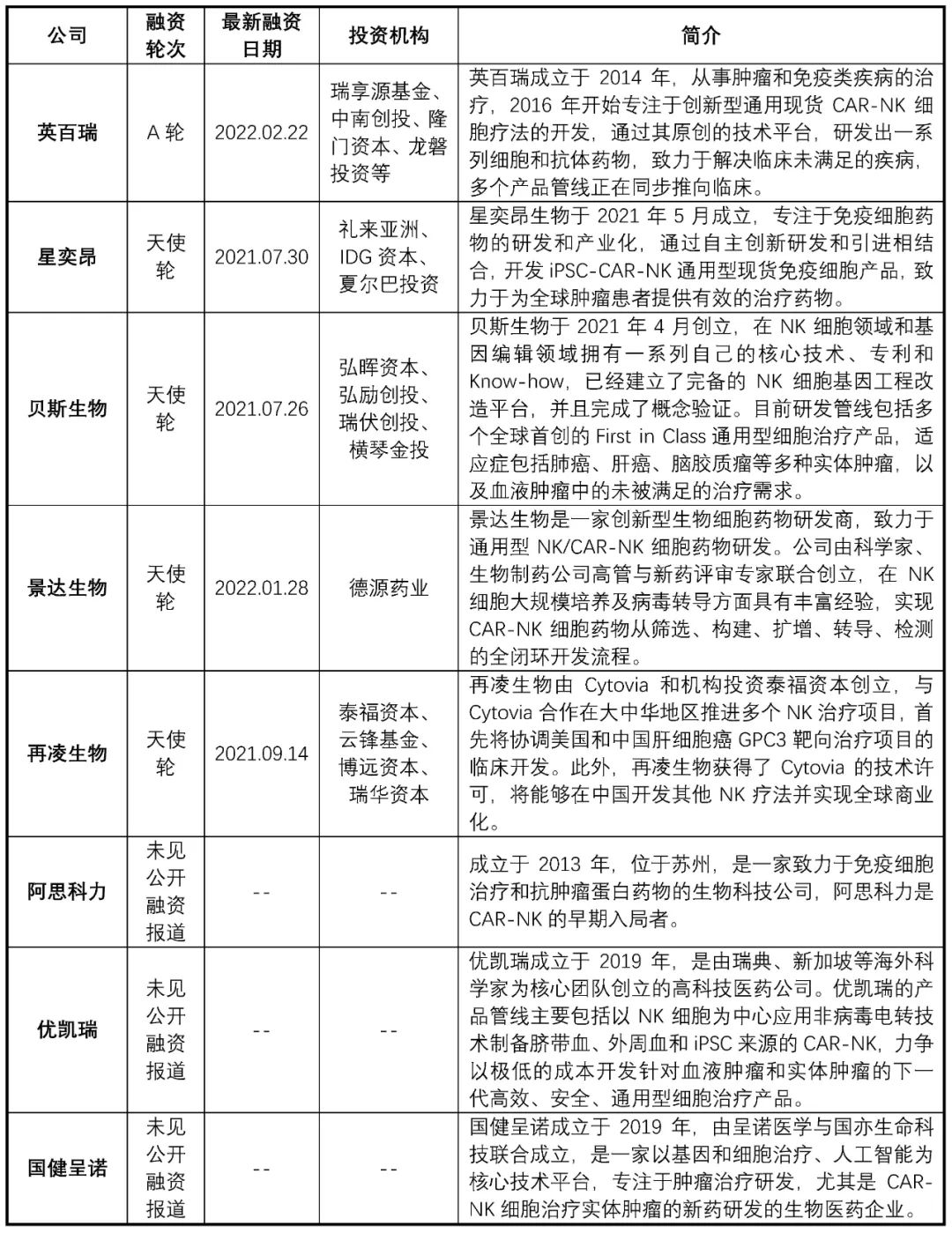
2021年NMPA連續批準了兩款CAR-T療法上市,大大鼓舞了國內細胞治療企業。近兩年,國內的CAR-NK療法開發呈現百舸爭流的景象,投融資進展也十分活躍,多家初創Biotech公司都獲得大手筆的早期投資(表3)。
隨著資本的涌入,相關產品研發工作得以進一步提速,其中國健呈諾的CAR-NK產品已順利獲得IND批件,多家企業的產品也進入IIT臨床研究階段。另有多家主要從事CAR-T療法開發的公司也有CAR-NK管線的布局如科濟生物(2171.HK)、恒潤達生、博生吉等。加科思藥業(1167.HK)通過投資Hebecell,百濟神州(688235.SH)通過與Shoreline?Biosciences達成戰略合作也都快速實現在該領域的布局。
四、小結及展望
NK細胞療法作為細胞療法領域的一名老兵,隨著相關技術領域的突破和資本的大力加持,正在煥發“第二春”的路上高歌猛進,特別是以Fate Therapeutics為代表的iPSC源NK療法逐步進入主賽道,市場對NK療法的熱情也進一步高漲,使得CAR-NK賽道成為了當下國內投融資市場的一個風口。
人們往往傾向于高估一項新技術的短期效應,而低估它的長期影響。近幾年,隨著CAR-T與TCR-T為代表的T細胞療法的陸續獲批,細胞療法在腫瘤治療領域表現的“可能根治”的巨大潛力誘惑者諸多的從業者和資金向該領域涌進,但是T細胞療法存在的CRS反應、實體瘤療效欠佳、治療費用昂貴等大大限制了其應用。
NK細胞療法相比于T細胞療法在某些方面確實有著天然的優勢,因而也成為了細胞治療領域的一根“救命稻草”,眾多細胞治療研究機構和企業都快速將目光向CAR-NK領域靠攏,當然也包括多家從事T細胞療法開發的企業。
MD?Anderson癌癥中心與Fate?Therapeutics臨床數據的公布,對行業有很大的鼓舞,但是我們必須注意到這些都是小樣本的、短期的數據,大樣本、長期的安全性和有效性結論才是決定成敗的關鍵,我們需要一直保持客觀謹慎的態度。
我們也需要注意到NK治療領域存在的眾多技術問題,如NK細胞來源、NK細胞體外擴增、凍融對NK細胞的損耗、NK細胞治療的持續時間、CAR-NK細胞中CAR的轉導等,這些問題都足以構成NK療法發展的限速步驟或技術瓶頸,都需要投入大量的人力、資金和時間來解決。
同時對于從事NK細胞療法的國內企業而言,在新冠疫情導致全球供應鏈短缺的不確定形式下,對國產供應鏈的重視必須提上戰略高度,尤其是影響產品工藝、報批和轉化的上游試劑耗材、生產純化設備和相關生命科學工具。
參考文獻
1. Heipertz E. L., Zynda E. R., Stav-Noraas T. E., et al. Current perspectives on “off-the-shelf” allogeneic NK and CAR-NK Cell Therapies. Front. Immunol., 2021, 12: 732135
2. Dranoff G. Cytokines in cancer pathogenesis and cancer therapy. Nat. Rev. Cancer, 2004, 4(1):11-22
3. Crinier A., Narni-Mancinelli E., Ugolini S., et al. SnapShot: natural killer cells. Cell, 2020, 180(6): 1280-1281
4. Kundu S., Gurney M., O’Dwyer M. Generating natural killer cells for adoptive transfer: expanding horizons. Cytotherapy, 2021, 23(7): 559-566
5. Xie G. Z., Dong H., Liang Y., et al. CAR-NK cells: A promising cellular immunotherapy for cancer. EBioMedicine, 2020, 59: 102975
6. Meneghel J., Kilbride P., Morris J. G., Fonseca F. Physical events occurring during the cryopreservation of immortalized human T cells. Plos One, 2019, 14(5): e0217304
7. Liu E. L., Marin D., Banerjee P., et al. Use of CAR-Transduced Natural Killer Cells in CD19-Positive Lymphoid Tumors. N. Engl. J. Med., 2020, 382(6): 545-553
8. Wu S. Y., Fu T., Jiang Y. Z., et al. Natural killer cells in cancer biology and therapy. Mol. Cancer, 2020, 19(1): 120
9. Caligiuri M. A. Human natural killer cells. Blood, 2008, 112(3): 461-469
10. Koehl U., Kalberer C., Spanholtz J., et al. Advances in clinical NK cell studies: donor selection, manufacturing and quality control. OncoImmunology, 2016, 5(4): e1115178
8. 方芳, 肖衛華, 田志剛. NK細胞腫瘤免疫治療的研究進展. 中國免疫學雜志, 2019, 35(9): 1025-1030
9. 殷書磊, 于益芝, 曹雪濤. CAR-NK抗腫瘤研究的現狀與發展趨勢. 中國腫瘤生物治療雜志, 2016, 23(1): 1-10
10. 免疫細胞治療產品臨床試驗技術指導原則(征求意見稿)-CDE
11. 免疫細胞治療產品臨床試驗技術指導原則(征求意見稿)-CDE
12. CAR-T細胞治療產品質量控制檢測研究及非臨床研究考慮要點-CDE
版權聲明:本文轉自康橙投資,如不希望被轉載的媒體或個人可與我們聯系,我們將立即刪除




 掃碼添加微信
掃碼添加微信