內源性修復失效是神經系統疾病的主要特征,無法恢復受損組織并導致功能障礙。目前,神經系統疾病的治療方案范圍有限,雖有經批準的藥物用于治療神經系統疾病,但療效仍不理想。
近年來,不同的研究發現,神經干細胞(NSCs)在治療神經系統疾病方面取得了令人振奮的成就。神經干細胞具有自我更新和分化的潛能,在替代內源性細胞治療神經系統疾病方面具有廣闊的前景,拓寬了細胞治療的新途徑。有鑒于此,我們全面探討了神經干細胞移植在神經系統疾病中的應用和價值。
神經干細胞移植在神經系統疾病中的治療作用
簡介
神經系統疾病,包括阿爾茨海默病 (AD)、帕金森病 (PD)、肌萎縮側索硬化癥 (ALS) 和亨廷頓病 (HD),是影響全世界數百萬人的嚴重致殘和致命疾病。
神經系統疾病的病理機制主要是由于神經元結構或功能進行性喪失,導致不同程度的癱瘓、認知、感覺和運動功能障礙,甚至永久性殘疾。重要的是,神經系統疾病的組織修復和再生能力是有限的,并且沒有根治方法可以阻止或逆轉其發展。

臨床上使用藥物來緩解或控制患者的癥狀,但藥物治療的效果有限,仍不能達到理想的效果。重要的是,藥物不能修復受損的神經并重建神經網絡。此外,由于藥物開發過程復雜且昂貴,這些疾病的臨床治療受到限制。因此,迫切需要探索有效的治療方法。
近年來,隨著對神經損傷修復的不斷探索,細胞移植/細胞治療進入了人們的視野,在神經系統疾病中得到了廣泛的應用,拓寬了新的治療策略。細胞療法在神經系統疾病中的治療價值在于模仿神經系統細胞修復和發育的正常過程,從而消除致病原因,改善功能障礙,修復受損組織。
神經干細胞在中樞神經系統的發育中發揮著重要作用。神經干細胞在治療神經系統疾病中的功能包括促進神經再生、細胞分化、分泌神經營養因子、神經保護和免疫調節,以及產生修復組織損傷和改善功能的藥理特性。重要的是,神經干細胞療法可以替代內源性缺失細胞來重建神經網絡的功能。
神經干細胞移植可以通過在神經損傷部位分化為神經元來替代受損或缺失的神經元,產生保護性神經元并維持神經元數量,這為神經系統疾病的治療提供了另一種有吸引力的治療策略。
目前,不同的研究已經證實了神經干細胞在神經系統疾病中的治療作用和應用價值,并取得了很大進展。它揭示了神經干細胞可用于治療神經系統疾病的事實。
神經干細胞及其在神經再生修復中的生物學特性
NSCs作為一種自我更新的多能細胞,可以產生建立中樞神經系統所需的各種類型的細胞。NSCs通過多個過程產生新神經元和神經膠質細胞的可塑性,并在胚胎發育和成體神經發生中發揮重要作用。
近年來,NSCs移植在組織損傷修復、神經再生等方面的應用獲得了廣泛的認可和應用價值。將神經干細胞移植到受損的脊髓中可以通過替換丟失的神經元或少突膠質細胞來增加再生的可能性。
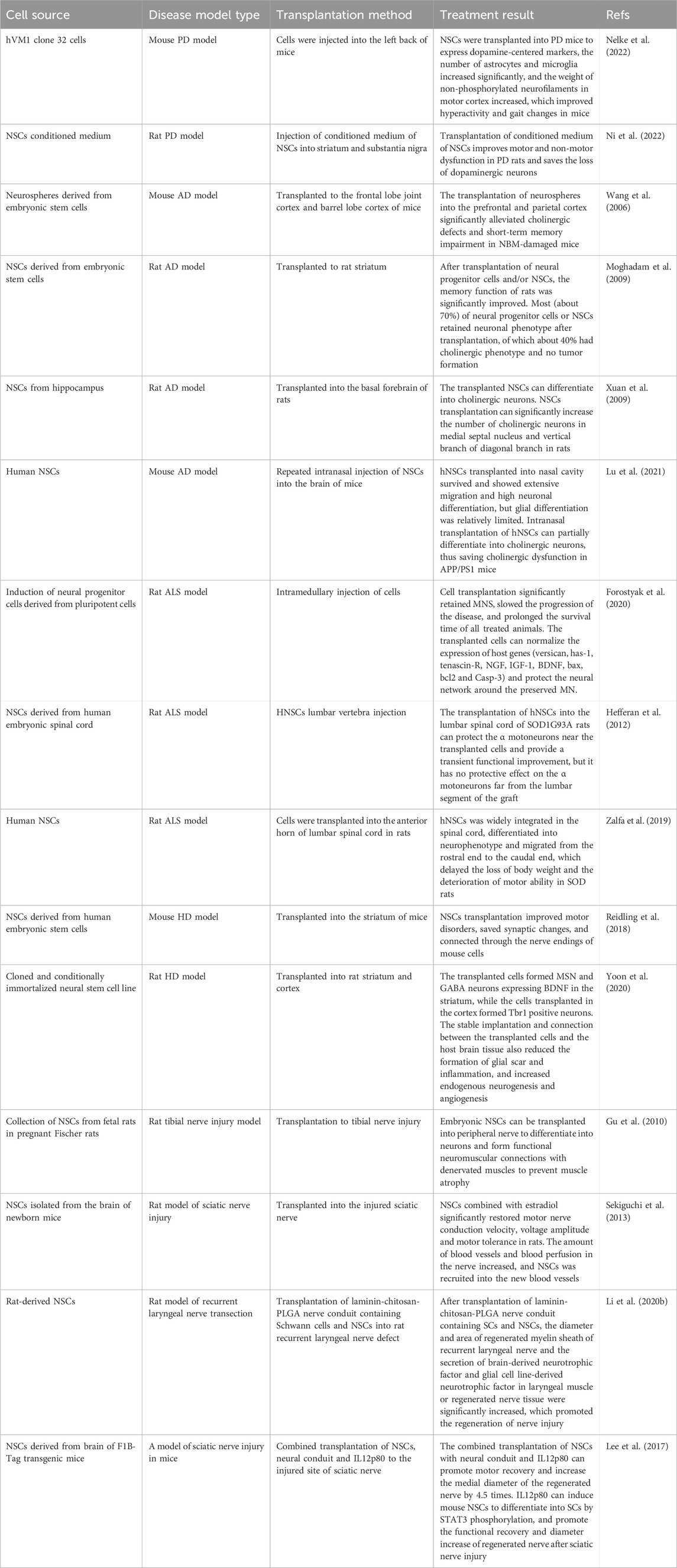
除了NSCs的分化和自我更新特性外,NSCs在神經損傷修復和再生中發揮多種功能特性,包括免疫調節(免疫細胞與NSCs/神經祖細胞及其后代之間的相互作用似乎決定了神經損傷修復和再生的有效性)它還決定移植神經干細胞的命運和功能整合、神經營養因子(如GDNF和BDNF)的分泌、抗炎調節、血管生成、軸突再生和髓磷脂形成以及神經膠質疤痕形成的抑制 (表1)。

此外,在周圍神經系統疾病中,植入的NSCs可以分化為雪旺細胞(SCs)并維持富含生長因子的微環境,從而促進神經再生。鑒于這些特點,NSCs在神經系統疾病中的應用價值具有廣闊的前景。
神經干細胞的來源
NSC主要來源于內源性NSC(人胚胎干細胞和人胎腦NSC/祖細胞)、誘導多能干細胞(iPSC)和直接重編程。這些為NSCs的起源及其在組織修復和再生領域的發展提供了堅實的基礎。
神經干細胞與神經系統疾病
神經系統疾病包括PD、AD、HD和ALS。這些疾病的特點是特定神經元亞群的喪失,導致感覺、認知和運動神經元逐漸喪失和癱瘓。這種疾病影響著全世界數以千萬計的人。
隨著世界人口老齡化,此類疾病的發病率持續上升,給患者帶來巨大的精神、身體和經濟負擔。盡管人們對這些疾病的發病機制的了解日益加深,但仍然缺乏有效可行的治療方法。臨床上使用一些藥物來減緩這些疾病的進展,但長期使用藥物會帶來依賴性、副作用和短期獲益,因此不可能替代和恢復丟失的神經元并重建神經功能網絡。
因此,隨著研究人員的不斷研究和探索,細胞治療的策略被提出。人們將功能活性細胞移植到神經損傷部位以起到治療作用。細胞療法通過生成特定的神經元來維持和替換丟失的宿主神經元,在受影響區域周圍建立輔助連接神經網絡,并創造一個支持宿主神經元生存的新環境來治療神經系統疾病。NSCs作為一種特殊的干細胞,在神經再生領域得到了廣泛的研究,它通過不同的機制發揮著有益的作用,如產生神經營養因子、減少神經炎癥、神經保護和免疫調節等。
此外,NSCs必須正確遷移到受損的神經系統并整合到宿主神經元回路中,以重建疾病中丟失的神經網絡并增強神經可塑性。盡管NSCs在神經系統疾病中的應用還處于初步探索階段,但它是一種可行的新治療策略(表2)。
01神經干細胞和帕金森病
帕金森病(PD)是一種常見的神經退行性疾病,其特征是紋狀體多巴胺低表達和黑質致密部多巴胺能神經元變性,導致各種運動和非運動癥狀。抑制或替換變性神經元一直被認為是一種有效且標準化的治療方法。盡管目前有多種治療方法用于治療PD,如左旋多巴治療、深部腦刺激手術和康復治療,但這些治療已被確定為當前的治療策略。這些方法雖然具有一定的治療作用,但不能預防多巴胺耗竭引起的功能缺陷和紊亂。
幸運的是,細胞療法可能是退行性/退行性神經元真正恢復的關鍵。PD的細胞療法始于1979年,通過移植胎鼠體內含有多巴胺的神經元來改善PD大鼠的運動異常。結果發現移植的細胞存活且軸突生長良好。
PD患者的室管膜下區、顆粒下區和嗅球的神經前體細胞/NSCs數量在死亡后有所減少,提示PD患者神經前體細胞/NSCs的產生受損,這是多巴胺能的結果神經喪失。這表明NSC/神經祖細胞與PD之間存在密切關系。
因此,神經干細胞移植可能成為治療PD的一種新的神經功能恢復策略。神經干細胞移植可以融入中樞神經系統周圍環境,建立適當的微環境,增強多巴胺能神經傳遞。神經干細胞可以通過識別微環境中靶標的細胞和非細胞區域來分化為多巴胺能細胞。通過將分化的多巴胺能神經元整合到現有的黑質紋狀體多巴胺能通路中,可以緩解PD的癥狀。
02神經干細胞和阿爾茨海默病
阿爾茨海默病(AD)可以說是我們這個時代嚴重的社會、經濟和醫療危機。AD發病機制的核心在于以下幾個方面。
- Tau是神經元中的一種微管相關蛋白,對于結構支持和軸突運輸非常重要。它被過度磷酸化,導致微管塌陷并聚集成神經纖維纏結。
- 其次,β-淀粉樣蛋白(A-β)碎片在細胞外積累和積累。而活化的小膠質細胞與β-淀粉樣蛋白聚集和淀粉樣蛋白斑形成密切相關。
- 第三,大量神經元和突觸的喪失是AD早期認知能力下降最密切相關的因素。AD的特點是進行性神經變性,主要是神經元變性/變性和突觸喪失。
因此,逆轉和改善神經元變性和軸突丟失對于AD的治療非常重要。隨著細胞療法的出現,它不僅可以阻止疾病的發展,還可以逆轉癥狀,在AD的應用中取得了一些成果。
AD進展過程中淀粉樣前體蛋白的病理變化可能會阻礙神經干細胞的神經元分化,而減少淀粉樣前體蛋白則可促進神經干細胞的神經元分化并遷移分化為海馬和皮質神經元。這也意味著神經干細胞在AD過程中發揮著重要作用。神經干細胞移植通過分化神經元、替代和改善丟失的神經元,在AD的應用中發揮著重要的治療作用。神經干細胞可以通過補償機制增強AD的神經元連接和代謝活動,從而挽救AD的認知。
神經干細胞移植改善AD癥狀的機制可能是通過上調β-淀粉樣蛋白酶、胰島素降解酶和腦啡肽酶的表達來減少β-淀粉樣蛋白的積累。神經干細胞和骨髓MSCs的移植減少了AD小鼠海馬中β-淀粉樣蛋白斑的數量,并增加了M2小膠質細胞的極化,表明干細胞移植具有抗炎作用。這些研究強調了神經干細胞在治療AD方面的潛在益處。
03神經干細胞和漸凍癥
肌萎縮側索硬化癥(ALS)是一種以運動神經元持續性變性為特征的致命性疾病,通過影響運動皮層、腦干和脊髓的運動神經元而導致癱瘓和死亡。目前,一些研究提出了ALS誘導的運動神經元死亡的幾種病理機制,包括谷氨酸誘導的興奮性毒性、細胞骨架異常、蛋白質聚集、氧化應激、線粒體功能障礙和細胞外SOD1毒性。這種毀滅性的疾病沒有有效的治療方法。
隨著對ALS治療的探索,研究人員移植了不同類型的功能細胞來替代丟失和退化的神經元,產生了治療效果。鑒于神經干細胞可以分化為神經元的獨特特性,在ALS的治療應用中取得了令人興奮的結果。移植到ALS動物體內的NSC可以優先定植于運動皮層、海馬和脊髓。它們的分化特征是巢蛋白、MAP2、GFAP、O4和CD68陽性細胞的表達降低,以及與腫瘤壞死因子相關的NSC的分化和存活增加。
神經干細胞移植可以減緩ALS癥狀的發生和進展,延長生存時間。這種有益作用似乎是通過產生營養因子、保護神經肌肉功能、減少星形膠質細胞增殖、改善炎癥和增強突觸可塑性來實現的。
04神經干細胞和亨廷頓病
亨廷頓病 (HD) 是一種由亨廷頓蛋白 (HTT) 基因CAG擴增引起的神經退行性疾病。該疾病的特點是紋狀體和皮質的神經元變性,導致功能變性和障礙,包括認知障礙和運動障礙。隨著疾病的發展,神經元的喪失會更廣泛地影響大腦的許多區域。自從發現HTT基因以來,預防或減緩HD進展的治療策略的開發并沒有取得重大進展,也沒有有效的治療方法。隨著干細胞的生物挖掘及其在神經退行性疾病中的應用,一些新的、令人興奮的結果已經出現。
隨著神經干細胞的生物挖掘及其在神經退行性疾病中的應用,一些新的、令人興奮的結果已經出現。神經干細胞的獨特特性為HD的應用和治療提供了基礎。神經干細胞移植治療亨廷頓病的基礎是替代或防止細胞損失。隨著神經干細胞的生物挖掘及其在神經疾病中的應用,一些新的、令人興奮的結果已經出現。神經干細胞的獨特特性為HD的應用和治療提供了基礎。
神經干細胞移植在亨廷頓病治療中的作用主要是通過分化為神經元表型、增強神經元可塑性和細胞替代。
神經干細胞在神經系統疾病中的臨床應用
近年來,細胞替代療法的出現,為神經系統疾病的治療開辟了光明的前景。神經干細胞獨特的生物學特性及其在神經系統疾病治療中的巨大潛力受到了眾多研究者的青睞。前面提到,在不同的基礎研究領域,神經干細胞移植對神經系統疾病具有治療作用,可以逆轉和改善疾病進展和修復功能。鑒于基礎研究的實質性成果,研究人員已從基礎研究上升到臨床試驗的探索階段,進一步探索神經干細胞在臨床試驗中的有效性、安全性和可行性。
雖然神經干細胞在神經系統疾病臨床試驗中的報道有限,但一些臨床試驗報道了神經干細胞在神經系統疾病治療中的潛在價值,并取得了一些令人鼓舞的結果。在一項1期臨床試驗中,12名ALS患者接受了椎管內注射NSC。隨訪30個月后,這些患者接受了MRI評估、標準臨床評估和定期功能評估,包括ALSFRS-R、坐位用力肺活量、握力評估、手測力計、電阻抗肌電圖和膀胱超聲。結果顯示了良好的耐受性以及細胞移植的可行性和安全性,延緩了疾病的進展。
另一項臨床試驗發現,胎兒神經干細胞被移植到6名ALS患者的脊髓中。主要成果指標是短期和長期安全。死亡率和任何原因的嚴重不良反應,而次要結果指標是ALS-FRS-R量表和用力肺活量 (FVC) 測量。移植后18個月的隨訪期間未發現疾病進展增加。兩名患者的ALS-FRS-R量表(從1到2)顯示步行能力短暫改善。一名患者的脛骨前肌MRC評分改善了7個月。兩名患者拒絕接受PEG和有創呼吸機,術后8個月因呼吸衰竭死亡,證實死亡與病情進展有關。這表明神經干細胞移植是一種安全的細胞治療方法。
一項臨床試驗報告了神經干細胞移植對PD患者的效果。將人神經祖細胞/未分化的神經干細胞移植到8名中度PD患者的背殼核中。術前及術后1年、2年、4年對患者進行神經病學、神經心理學和腦影像學評估。證明細胞移植是安全的,移植過程中沒有出現免疫反應,也沒有不良反應。患者的神經心理學評分并未受到移植的影響。除一名患者外,其余患者的運動功能均有不同程度的改善,其中五名患者對左旋多巴的反應顯示出更好的療效。PET成像顯示細胞移植后中腦多巴胺能活性有增加的趨勢。
其他臨床試驗報告稱,神經干細胞被移植到21名PD患者的紋狀體中。采用統一帕金森病評定量表(UPDRS)、Hoehn-Yahr、PDQ-39和Schwab-England評分來評估帕金森患者的神經功能。從四個方面評估移植可能產生的副作用:
a)腫瘤形成,
b)免疫排斥和免疫抑制劑的使用,
c)移植并發癥和
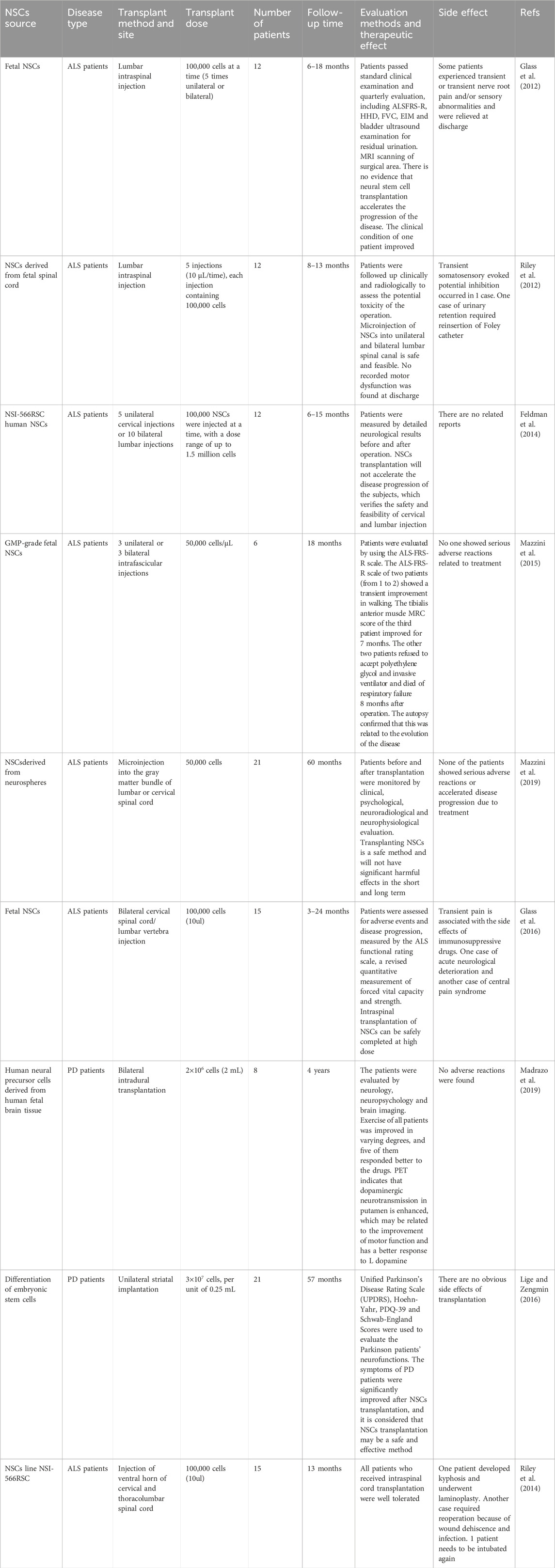
d)與分娩相關的副作用。所有PD患者的癥狀均明顯改善,且未出現明顯的移植后致瘤、免疫排斥和并發癥等副作用(表3)。
結論
鑒于神經干細胞的分化潛力及其在神經損傷再生和修復方面的獨特特性,神經干細胞在神經系統疾病的治療中具有巨大的潛力。神經干細胞移植在神經系統疾病的治療方面取得了巨大進展,揭示了它們可以成為神經系統疾病的候選細胞替代療法。
然而,神經干細胞尚未做好臨床移植的準備。盡管一些臨床試驗報道神經干細胞在治療神經系統疾病患者方面是可行且安全的,但其廣泛應用仍受到很大阻礙,需要更直接的證據來支持。雖然目前需要解決的問題還有很多,但并不會阻礙研究者探索的步伐,最終這些問題都會得到很好的解決。總之,神經干細胞是一種很有前景的治療神經系統疾病的細胞移植療法。
參考資料:Yang L, Liu S-C, Liu Y-Y, Zhu F-Q, Xiong M-J, Hu D-X and Zhang W-J (2024) Therapeutic role of neural stem cells in neurological diseases. Front. Bioeng. Biotechnol. 12:1329712. doi: 10.3389/fbioe.2024.1329712
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請及時跟本公眾號聯系,我們將在第一時間處理。



 掃碼添加微信
掃碼添加微信