概述:本文通過分析總結4項關于干細胞在漸凍癥中的應用的文獻,從而評估干細胞移植作為漸凍癥患者的潛在治療方法的安全性和有效性,重點介紹了干細胞治療漸凍癥的臨床效果。
漸凍癥(Amyotrophic Lateral Sclerosis, ALS),又稱肌萎縮側索硬化。是一種慢性進行性神經系統變性疾病,主要影響控制肌肉運動的神經細胞(運動神經元)。這種疾病會導致肌肉逐漸萎縮和無力,最終可能導致完全癱瘓。
肌萎縮一詞指的是肌肉逐漸衰弱。這種衰弱是由于神經緩慢而逐漸地被破壞(神經退化)造成的。最終,患者可能無法進食、說話、走動或呼吸。
相關閱讀(肌萎縮側索硬化癥體征和癥狀是什么?及其治療方法)
漸凍癥的治療方法
漸凍癥的早期診斷面臨挑戰,患者從癥狀出現到確診通常需要9-15個月。
治療方面,目前由于漸凍癥尚無有效藥物,大約80%的患者會在發病后5年內死亡。雖然ALS的臨床和病理特征逐步被闡明,但醫學界一直無法徹底揭開其發病原因和機制,更沒有找到有效的藥物來阻斷疾病的發展。
因此,尋找更高效、更安全的新療法成為醫學界持續努力的方向。
干細胞治療漸凍癥:78例患者的安全性與有效性驗證
近年來,隨著再生醫學的發展,干細胞治療漸凍癥作為一種新興的治療方法,利用干細胞的自我更新和分化潛能,為漸凍癥患者提供新的修復策略。
臨床試驗一:間充質干細胞移植治療漸凍癥患者的安全性和效果
2010年10月?,神經內科、神經免疫學實驗室和Agnes Ginges神經遺傳學和多發性硬化癥中心在行業期刊《JAMA Neurology》上發表了一篇關于《多發性硬化癥和肌萎縮側索硬化癥患者間充質干細胞移植的安全性和免疫學效果》的研究成果。[1]

共招募了15名MS患者(平均[SD]擴展殘疾狀態量表[EDSS]評分,6.7[1.0])和19名ALS患者(平均 [SD] 肌萎縮側索硬化癥功能評定量表[ALSFRS]評分,20.8[8.0])。
有效性評估
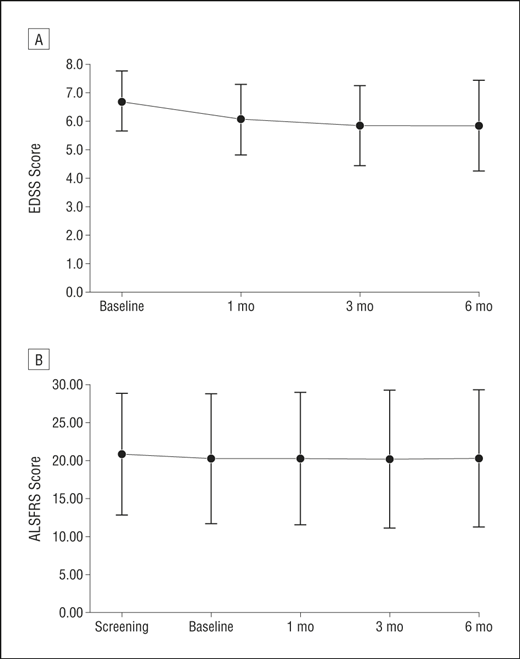
- 在MS患者中,平均EDSS評分逐漸下降(表明功能改善),從治療前的6.7(1.0)下降到MSC注射后1個月的 6.1(1.2),3個月的5.9(1.4)和6個月的5.9 (1.6)(圖A)。
- 在患有ALS的患者中,平均ALSFRS評分在篩選訪問和MSC注射當天之間的2個月內略有下降,隨后在6個月的隨訪期間保持穩定。
磁共振成像顯示腦室枕角中的MSCs,表明氧化鐵標記細胞可能在腦膜、蛛網膜下腔和脊髓中遷移。免疫學分析顯示,在干細胞移植后24小時,CD4+CD25+調節性T細胞比例增加,淋巴細胞增殖反應降低,以及髓系樹突狀細胞上CD40+、CD83+、CD86+和HLA-DR的表達。
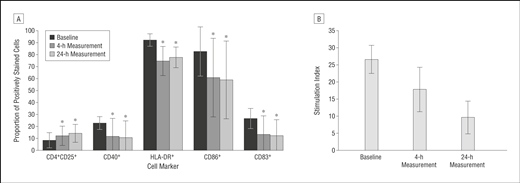
安全性評估:34名患者中,有21名在干細胞注射后出現輕度自限性發熱反應(體溫 ≤ 37.5°C),持續時間為8至24小時。15名患者報告出現頭痛,持續時間最長為7天,主要與腰椎穿刺有關。在長達25個月的隨訪期間,沒有任何患者報告出現重大不良反應。
研究表明,間充質干細胞移植治療MS和ALS患者在臨床上是一種可行且相對安全的手術,可立即誘導免疫調節作用。
臨床試驗二:干細胞移植治療漸凍癥癥的安全性及臨床效果
2016年3月?,希伯來大學醫學中心神經內科在行業期刊《JAMA Neurology》上發表了一篇關于《間充質干細胞移植治療肌萎縮側索硬化癥的安全性及臨床效果1/2期和2a期臨床試驗結果》的研究成果。[2]

以色列耶路撒冷哈達薩醫療中心于2011年6月至2014年10月招募了26名漸凍癥患者。
有效性評估
- 在2項連續開放標簽研究中,發現使用自體 MSC-NTF 細胞通過鞘內 (IT)、肌肉內 (IM) 或聯合 (IT+IM) 給藥治療漸凍癥患者是安全且耐受性良好的。
- 在試驗的2a期階段,MSC-NTF細胞移植后觀察到ALS-FRS-R評分和FVC每月下降率更顯著改善(分別從 -1.4到-0.6和從-2.6%到0.86%。
- 分析顯示,FVC進展率有統計學顯著改善,并且ALS-FRS-R評分進展率有改善趨勢對于接受完整隨訪的患者。
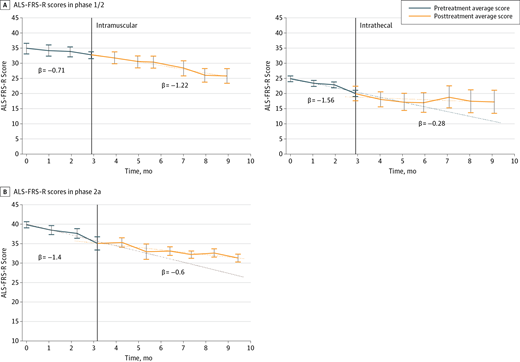
接受IT(或IT+IM)治療的患者用力肺活量和漸凍癥功能評定量表修訂評分的進展速度降低。
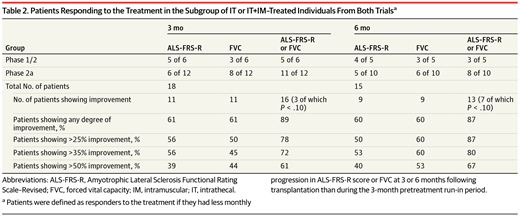
安全性評估:觀察到的大多數不良事件為I級和II級,且為短暫性,與MSC-NTF細胞的給藥密切相關。這些不良事件主要包括頭痛、發燒、嘔吐、腿部和背部疼痛以及頸部僵硬。
結果表明,在漸凍癥患者中對MSC-NTF細胞進行IT和IM給藥是安全的,并提供了臨床益處的跡象,將在即將到來的臨床試驗中得到證實。
臨床試驗三:骨髓間充質干細胞移植治療漸凍癥癥的安全性和有效性
2021年12月,伊朗馬什哈德醫科大學免疫學研究中心在行業期刊《Regenerative Therapy》上發表了一篇關于《骨髓間充質干細胞移植治療肌萎縮側索硬化癥的安全性和有效性》的研究成果。[3]

參與者年齡在18至75歲之間,患有漸凍癥病史至少1年。15名患者(n=15)符合ElEscorial標準,確診患有漸凍癥,被選為本研究對象。
有效性評估
在應用骨髓間充質干細胞后,各個患者的ALSFRS-R值在3個月內保持穩定(圖B). 所有患者的ALSFRS-R評分回歸分析表明,與植入前評分相比,骨髓間充質干細胞移植1個月和3個月后ALSFRS-R斜率無顯著降低(圖A–B)。
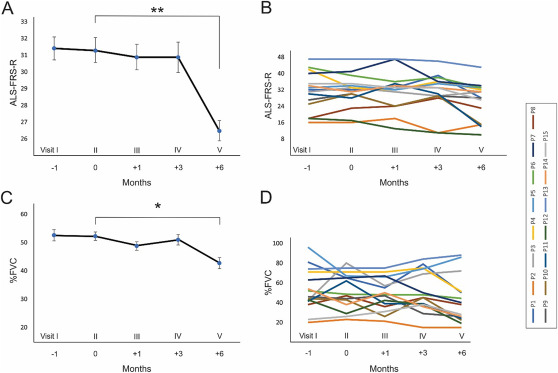
此外,還評估并比較了移植前后的FVC評分。與植入前相比,BM-MSCs移植后1個月和3個月的FVC斜率之間沒有顯著差異(圖C–D)。個體患者在接受細胞治療的3個月內,FVC 的平均值保持穩定(圖D).
安全性評估:本次臨床試驗的15名患者在隨訪期間均未出現嚴重不良反應。
結果表明,ALS患者的BM-MSCs的IT和IV移植是一種安全的手術,可以減緩疾病的進展。
臨床試驗四:人類神經干細胞移植到漸凍癥患者的脊髓中的效果
2022年9月5日,美國加利福尼亞州洛杉磯雪松西奈脊柱中心在國際期刊《Nature Medicine》上發表了一篇關于《將分泌GDNF的人類神經祖細胞移植到ALS患者的脊髓中:一項1/2a期臨床試驗》的研究成果。[4]
21名患者被選中進行篩選,18名符合條件的患者被隨機分配參加本次試驗,條件包括根據El Escorial標準診斷為ALS,患病時間≤3年,臨床或肌電圖顯示腰椎運動神經元受累,仰臥用力肺活量>60%。
有效性評估
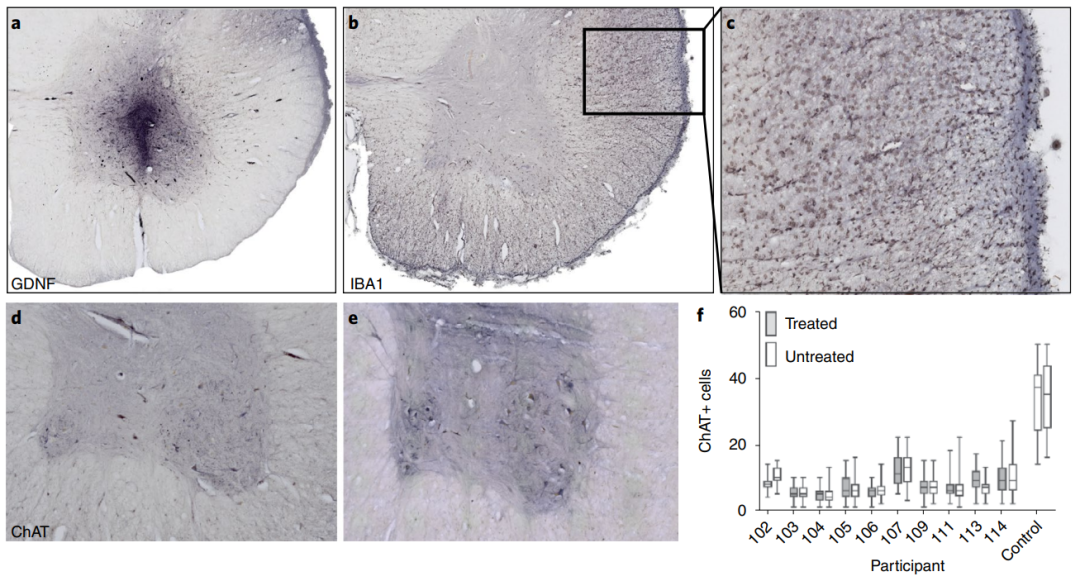
- 在注射移植后,研究團隊對患者進行了一年的隨訪,以測量治療和未治療腿的力量,結果顯示,與未治療的腿相比,細胞移植治療沒有對腿的肌肉力量產生負面影響。此外,研究團隊對13名因疾病進展而去世的參與者的檢測中發現這些移植的細胞持續存在且有GDNF蛋白的產生。
- 研究表明,一次工程神經祖細胞的注射可以在移植后長達42個月內為漸凍癥患者脊髓提供新的支持細胞和 GDNF輸送。
- 參與者的漸凍癥功能評定量表修訂版 (ALSFRS-R) 評分平均進步速度為每月1.2分(每月-1.5至-0.9分),這是漸凍癥試驗參與者的典型特征。
安全性評估:術后即刻,89%的低劑量組患者和67%的高劑量組患者報告在手術部位神經支配的區域出現感覺減退和/或感覺異常和/或疼痛/不適,大約在L2-L4皮節,對應于大腿前部,這可能是由于注射過程中針頭經過所致。試驗期間沒有嚴重不良事件歸因于該產品。
這項研究表明了,一次工程神經干細胞給藥可以在移植后長達42個月內為ALS患者脊髓提供新的支持細胞和GDNF遞送。并達到1年時的主要安全性終點,與未治療的腿相比,移植對治療腿的運動功能沒有負面影響。
干細胞治療漸凍癥的臨床研究進展
截止2024年8月26日,在美國國立衛生研究院的最大臨床試驗注冊庫clinicaltrials.gov網站上注冊的有關干細胞治療漸凍癥臨床研究項目有52項,已完成的有22項。
結論
臨床研究結果顯示干細胞治療漸凍癥是具有臨床價值的,可以分化為運動神經元樣細胞,替換退化或死亡的神經元并且能夠減緩漸凍癥的進展并提高患者的存活率。
盡管干細胞治療總體上安全,仍存在一些潛在風險,例如,低熱和頭暈和輕微不適反應。因此,患者在接受干細胞治療前需要進行詳細的檢查和評估,并在專業醫生的指導下進行治療。
隨著研究的深入和技術的成熟,我們期待干細胞治療能夠在漸凍癥治療中發揮更大的作用。
相關閱讀:了解更多關于干細胞治療漸凍癥的新聞資訊!
參考資料:
[1]Karussis D,?Karageorgiou C,?Vaknin-Dembinsky A, et al. Safety and Immunological Effects of Mesenchymal Stem Cell Transplantation in Patients With Multiple Sclerosis and Amyotrophic Lateral Sclerosis.?Arch Neurol.?2010;67(10):1187–1194. doi:10.1001/archneurol.2010.248
[2]Petrou P,?Gothelf Y,?Argov Z, et al. Safety and Clinical Effects of Mesenchymal Stem Cells Secreting Neurotrophic Factor Transplantation in Patients With Amyotrophic Lateral Sclerosis:?Results of Phase 1/2 and 2a Clinical Trials.?JAMA Neurol.?2016;73(3):337–344. doi:10.1001/jamaneurol.2015.4321
[3]Safety and efficacy of bone marrow derived-mesenchymal stem cells transplantation in patients with amyotrophic lateral sclerosis https://doi.org/10.1016/j.reth.2021.07.006
[4]Baloh, R.H., Johnson, J.P., Avalos, P.?et al.?Transplantation of human neural progenitor cells secreting GDNF into the spinal cord of patients with ALS: a phase 1/2a trial.?Nat Med?28, 1813–1822 (2022). https://doi.org/10.1038/s41591-022-01956-3
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。
版權說明:本文來自杭吉干細胞科技內容團隊,歡迎個人轉發至朋友圈,謝絕媒體或機構未經授權以任何形式轉載至其他平臺,轉載授權請在網站后臺下方留言獲取。




 掃碼添加微信
掃碼添加微信