盡管經過100年的研究,1型糖尿病仍無法治愈,但供體和干細胞衍生的同種異體胰島可能是答案,但卻受到監管阻力的阻礙。
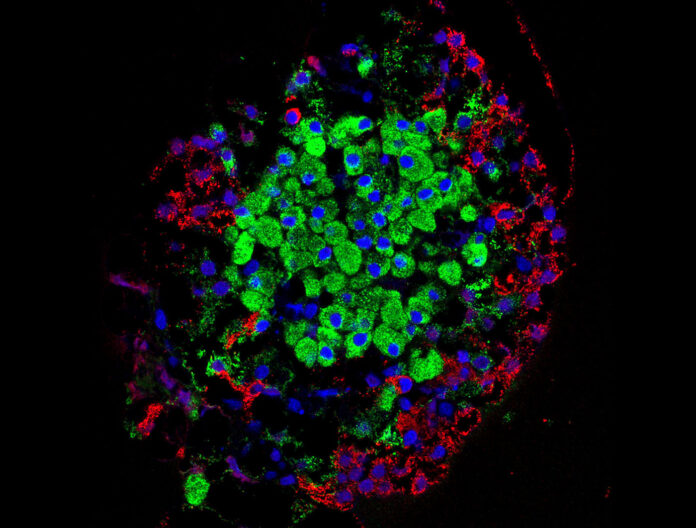
芝加哥大學醫學中心的醫療中心有一支團隊隨時待命,全天候24小時接收已故捐獻者的胰腺,并將其加工成分離的胰島,然后注入1型糖尿病患者體內。結果令人震驚。一些十多年前接受過同種異體胰島移植的患者至今仍無法使用胰島素。
治療1型糖尿病的細胞療法在哪里?
芝加哥大學醫學院外科教授兼胰腺和胰島移植項目主任醫學博士Piotr Witkowski表示:“那些在小時候患上糖尿病、完全不知道沒有糖尿病的生活會怎樣的人,在得知可以停止使用胰島素后,都欣喜若狂,難以置信。”
然而,對于美國約200萬1型糖尿病患者來說,這種看似廣泛適用、簡便易行且非侵入性的治療方法每年只使用幾次。而且,1型糖尿病患者并沒有像2型糖尿病患者一樣,因semaglutide(Ozempic)和tirzepatide(Mounjaro)而得到福音。相反,1型糖尿病患者仍未痊愈,必須通過每日注射、胰島素泵或胰島素自動給藥系統終生服用胰島素。這種情況已經持續了一個多世紀。
胰島移植是藥物嗎?
20世紀80年代末和90年代初,阿爾伯塔大學的一組研究人員開發了從已故捐獻者身上移植同種異體胰島的技術,該技術于2000年發表在《新英格蘭醫學雜志》上。
這并不是最復雜的方案:將捐獻的胰腺切成小塊,輕輕地用酶分離成小細胞簇,離心分離細胞,然后準備注射。這會在移植接受者體內產生胰島簇,從而重建門靜脈的血管。
從2000年到2014年,美國一直在進行臨床試驗,以證明死者供體來源的胰島移植是安全有效的。在長達14年的努力接近尾聲時,美國食品及藥物管理局的立場是,異體胰島移植需要通過已獲批準的生物制品許可申請(BLA)才能獲得批準。
因此,維特科夫斯基等人建議,器官共享聯合網絡、器官獲取與移植網絡以及衛生資源和服務管理局應該對人類胰島進行監管,其監管途徑應與美國目前對其他人體器官的監管途徑類似。然而,FDA一直拒絕這些提議,主要原因是對于由死亡捐獻者制成的胰島是否應被視為器官或可制造的藥物存在分歧。

維特科夫斯基不同意這種觀點,而且他并不是唯一一個認為來自尸體捐贈者的胰島可以作為器官的人。
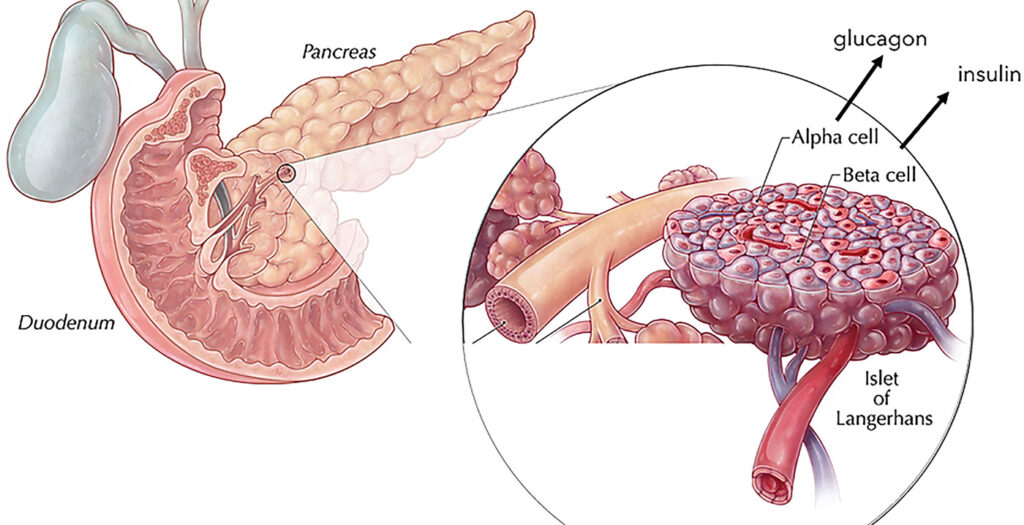
領導Imagine Pharma胰島項目的Rita Bottino博士同意Witkowski的觀點,認為胰島與移植器官具有許多共同特征,例如它們在人體內自然存在、無需制造、結構保存完好、能夠融入接受者的血管系統。

博蒂諾解釋說:“如果單獨培養單個胰腺β胰島細胞,它們甚至不能產生良好的胰島素。它們必須與其他細胞協同工作,形成一個調節網絡。我們將這些微型器官交給病人,因此我們實際上并不制造任何東西。它們有別于疫苗、藥片和化學品等藥物實體。它們是微型器官”。
重要的是,來自已故捐獻者的同種異體胰島與任何其他移植器官的行為相似,因為它們無法承受零度以下的溫度,只能在室溫下保存很短的時間。此外,用于移植的胰島和器官不能儲存在商業器官庫中,需要有效力證書,并且只能根據成功的臨床結果在移植后評估其有效性。
因此,器官移植項目,而不是制造商,對胰島移植的成功負有責任。此外,由于人類胰島與器官一樣,本質上是多種多樣的,因此它們不能像藥物一樣標準化。
“自2014年以來,我們一直處于迷茫之中,因為我們擁有可以使用的療法,而這種療法并沒有被美國食品及藥物管理局批準為藥物,維特科夫斯基說。”同種異體胰島移植正在發揮作用,保險公司愿意支付,但他們不能支付未經批準的藥物。
新一代1型糖尿病療法
維特科夫斯基似乎是美國最后一批從事1型糖尿病胰島移植手術的人之一。他已經獲得了一些資金,幫助他向BLA邁進,盡管這使他每年只能做大約20例手術。但這并不意味著維特科夫斯基等人開發1型糖尿病療法的工作已經完全停滯,相反,它正開始蓬勃發展。
去年,一個團隊終于突破了美國食品及藥物管理局對異體胰島細胞療法的要求。CellTrans遵照美國食品及藥物管理局的要求,成功獲得了Lantidra?治療1型糖尿病的批準。

然而,Lantidra也并非沒有問題。從捐贈的胰腺組織中提取的胰島β細胞被移植到成年患者的肝臟中,這些患者在接受強化胰島素治療后血糖仍會急劇波動。在對30名接受一至三次輸注的參與者進行的臨床研究中,有21人至少在一年內不需要額外的胰島素,其中11人在五年多的時間里一直不需要胰島素。
不過,Lantidra似乎不會在短期內壟斷1型糖尿病市場,尤其是在獲得BLA批準一年后,患者仍無法獲得這種藥物。
另一種不同的方法是完全放棄人體捐獻和移植的環節,轉而采用更久經考驗的細胞療法。近年來,從干細胞中提取、在實驗室中培育胰島的方法受到了廣泛關注,盡管這種方法無疑成本更高、更復雜,而且可能更有利可圖。
2021年10月,美國食品和藥物管理局(FDA)批準的首家基于CRISPR技術的療法提供商頂點制藥公司(Vertex Pharmaceuticals)成為頭條新聞,因為該公司披露,一名1型糖尿病患者的異體干細胞(VX-880)已完全分化為可產生胰島素的胰島細胞。

Vertex公司的一位發言人告訴Inside Precision Medicine:“Vertex公司已經有效地破解了按需制造完全分化胰島細胞的密碼,這種細胞在早期臨床結果中顯示出了療效,并且可以擴大規模以滿足需求”。
2022年5月,在兩名患者死亡后,FDA暫停了VX-880的I/II期臨床研究,最初的承諾似乎好得不像真的。然而,FDA在2022年7月解除了監管暫停,因為審查顯示研究暫停是 “協議指定的”,而且死亡與正在研究的治療 “無關”。

2024年6月21日,Vertex宣布正在進行的VX-880治療1型糖尿病的1/2期研究取得積極結果,并于美國糖尿病協會第84屆科學會議上發表。
- 所有12名接受單次輸注全劑量VX-880的患者均在第90天內表現出胰島細胞植入和葡萄糖反應性胰島素產生
- 所有患者均達到ADA推薦的目標HbA1c水平<7.0%且>70%時間處于范圍內 (70-180mg/dL),12名患者中有11名減少或停止使用外源性胰島素
- 3名患者經過至少12個月的隨訪,因此可評估,達到了消除嚴重低血糖事件 (SHE) 的主要終點(HbA1c<7.0%)和胰島素依賴性的次要終點
- 隨著公司向關鍵發展階段邁進,試驗范圍擴大到招募約37名參與者

這些更新的數據涉及12名在試驗B部分和C部分接受單次輸注全劑量治療的患者,與之前報告的VX-880試驗的積極結果一致,并加強了這種療法的變革潛力。
抑制移植物排斥反應或對胰島進行免疫保護
無論采用哪種異基因方法,無論是來自已故患者還是干細胞,移植物排斥反應的問題依然存在,目前主要有兩種方法:免疫保護性封裝和免疫抑制。
Vertex公司利用VX264,將其從干細胞中提取的完全分化的胰島細胞放入一個類似膠囊的裝置中,通過手術植入體內,保護胰島細胞免受免疫系統的侵害。

Vertex公司使用的免疫保護裝置(由Viacyte公司首創)并不是全新的想法,一些生物制藥公司和研究人員已經進行了探索,其中包括加拿大生物技術公司Sernova,該公司正在開發一種免疫保護 “細胞袋系統”,用于治療各種慢性疾病,如1型糖尿病。
一年前,Sernova公司公布了他們正在進行的1/2期臨床試驗的首批患者數據,首批完成方案定義的胰島移植的五名患者在六到三十八個月的時間里實現了胰島素獨立。
Eledon Pharmaceuticals公司采用了更為傳統的方法,通過免疫抑制來解決宿主-移植物排斥反應。雖然Eledon公司的主要業務是腎移植,但該公司于2024年1月宣布,由研究者主導的臨床試驗的第一位參與者接受了胰島細胞移植,并正在接受其新型免疫抑制方案的治療,其中包括該公司的新型抗CD40L抗體tegoprubart。
人體臨床試驗和非人靈長類動物臨床前研究表明,Tegoprubart有可能提供更好的療效和更高的安全性,包括減少與降鈣素抑制劑等標準免疫抑制劑相關的致糖尿病副作用。Tegoprubart目前正處于利用人體尸體細胞進行胰島細胞移植的二期臨床試驗階段。
“Tegoprubart可作為胰島細胞移植技術的輔助療法,包括來自豬的細胞(異種移植)、使用或不使用隱形技術的人造細胞,以及與封裝袋等給藥裝置的組合,”Gros告訴《精準醫療》(Inside Precision Medicine)。”
因此,我們相信tegoprubart是充分釋放胰島細胞移植作為1型糖尿病功能性療法潛力的關鍵。
基因組編輯角度稀缺
基于基因編輯的1型糖尿病療法的開發,無論是自體編輯方法還是體內編輯方法,都幾乎沒有引起任何熱議。
對于后者,除了在小鼠身上進行試驗外,還沒有其他研究更進一步。
2022年,澳大利亞加文醫學研究所(Garvan Institute of Medical Research)掀起了最大的浪潮,該研究所宣布,一項使用腺相關病毒(AAV)的體內基因治療計劃已獲得資助和批準,可以開始臨床試驗。該療法名為GARV-AAV2-A20,是基于加文研究所移植免疫學實驗室主任Shane Grey博士的研究成果。

他的團隊發現了一種名為A20的關鍵蛋白,這種蛋白與炎癥和自身免疫性疾病有關。這種蛋白質可用于基因工程胰島細胞,減緩或阻止免疫系統的損害。關于GARV-AAV2-A20的最新消息稱,”將于2024年中期通過阿德萊德皇家醫院招募患者”。
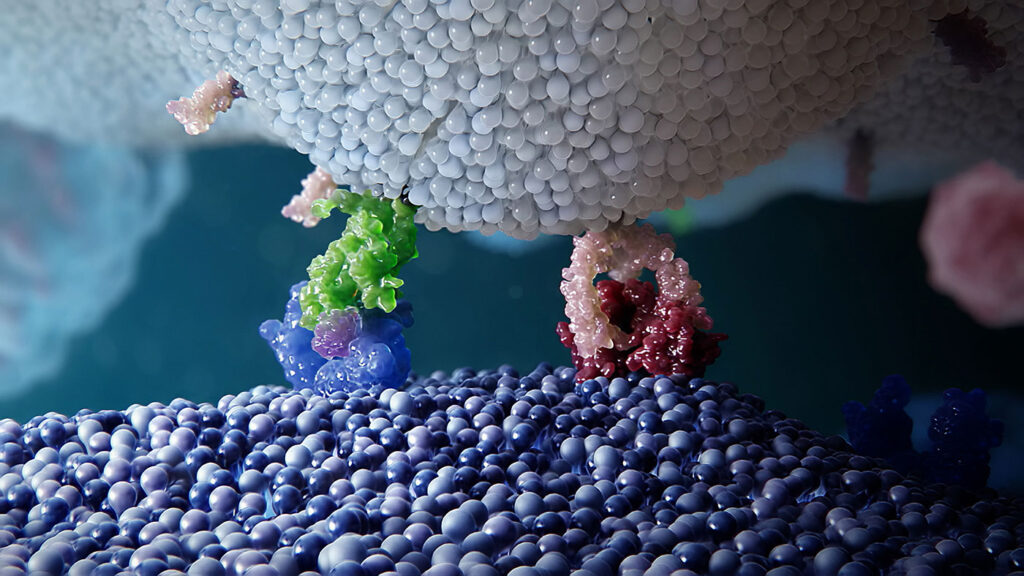
抗原呈遞細胞(白色)上的CD40(粉色)與免疫細胞上的CD40L(紫色)相互作用,導致克隆擴增、抗體產生和促炎細胞因子分泌,從而增強免疫反應。Tegoprubart(未顯示)靶向CD40L,以抑制與CD40的相互作用,從而控制移植引起的免疫反應。
基因編輯干細胞療法的最新進展發生在今年早些時候,Vertex公司與CRISPR Therapeutics公司就基因編輯干細胞衍生細胞療法治療1型糖尿病分道揚鑣。下一代前景藥物和VCTX210(初始候選藥物)均于2022年開始臨床試驗。
一旦完成退出,CRISPR將完全擁有這些資產,它打算在沒有Vertex協助的情況下,繼續進行下一代候選藥物(現名CTX211)的I期臨床試驗。該臨床試驗計劃于2025年完成。
Vertex公司在這一領域的基因編輯工作還沒有全部結束,但它不必通過基因組工程策略直接治療1型糖尿病。Vertex公司確實有一個低免疫細胞計劃,該計劃涉及使用CRISPR-Cas9對VX-880和VX-264計劃中使用的相同干細胞衍生、完全分化的胰島進行基因編輯,使細胞不受免疫系統的影響。
該計劃正處于研究階段。當被問及Vertex公司是否有針對1型糖尿病的基因療法時,該發言人表示:”Vertex公司目前正在開發針對1型糖尿病的細胞療法。
對干細胞治療1型糖尿病正確基因療法的探索仍在繼續,首先是如何對體內某些細胞進行重新編程,使其能夠制造胰島素,而不會出現免疫系統反應。
但現在看來,1型糖尿病領域的下一個批準最有可能不是基于基因編輯,而是基于未經修飾的異源干細胞衍生胰島。
不管誰先出手,身為Vertex、Sernova和Eledon顧問的Witkowski都將參與其中。雖然他可能無法獲得已故捐贈者異體胰島移植的批準,但維特考斯基正竭盡全力推進所有胰島細胞移植臨床試驗,以確保1型糖尿病患者獲得治療,甚至治愈,從而挽救和改變他們的生命。
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加微信
掃碼添加微信