腎臟疾病(如慢性腎病、急性腎損傷和終末期腎病)發病率持續攀升,已成為全球性的重大健康負擔,傳統治療手段面臨諸多局限。干細胞療法憑借其獨特的再生與修復潛力,為突破這些瓶頸帶來了新的希望,相關研究近年來呈現出蓬勃發展的態勢。
在此背景下,近期,上海中醫藥大學附屬曙光醫院腎內科聯合上海中醫藥大學中醫腎病研究所等機構團隊,在國際權威期刊《Frontiers in Immunology》上發表了題為“近十年全球腎臟疾病干細胞治療熱點與趨勢:2015年至2024年的文獻計量與可視化分析”的研究綜述。
該研究旨在通過系統性文獻計量分析,全面概述腎臟疾病干細胞療法的研究現狀、核心力量、知識基礎及前沿動向。
腎臟疾病負擔與干細胞療法的機遇挑戰
腎臟疾病(包括慢性腎病[CKD]、急性腎損傷[AKI]和終末期腎病[ESRD])是全球重大健康挑戰,影響數億人群,死亡率和醫療成本居高不下。現有主流療法如透析和腎移植雖可延緩疾病進展,但面臨器官短缺、免疫排斥、長期并發癥及患者生活質量下降等嚴峻限制。尤其終末期腎病依賴透析的患者,5年生存率不足50%,凸顯傳統治療模式的不可持續性。

干細胞療法(以間充質干細胞[MSCs]為核心)通過組織再生、免疫調節及旁分泌機制修復腎損傷,為替代傳統療法提供新路徑。臨床前研究證實其可改善腎小球濾過率、降低蛋白尿并抑制纖維化。然而,其轉化應用仍存關鍵瓶頸:安全性風險(如輸注后發熱)、療效異質性(不同來源干細胞功能差異)、缺乏標準化治療方案,且長期效果及機制尚未明確。這些挑戰正是推動該領域研究持續深入的動力。
文獻計量研究的目標與方法
本研究旨在通過文獻計量學方法,系統回答核心問題:腎臟疾病干細胞治療研究的當前趨勢、知識基礎、研究差距以及未來發展方向是什么?如何利用這些分析指導未來的研究工作?
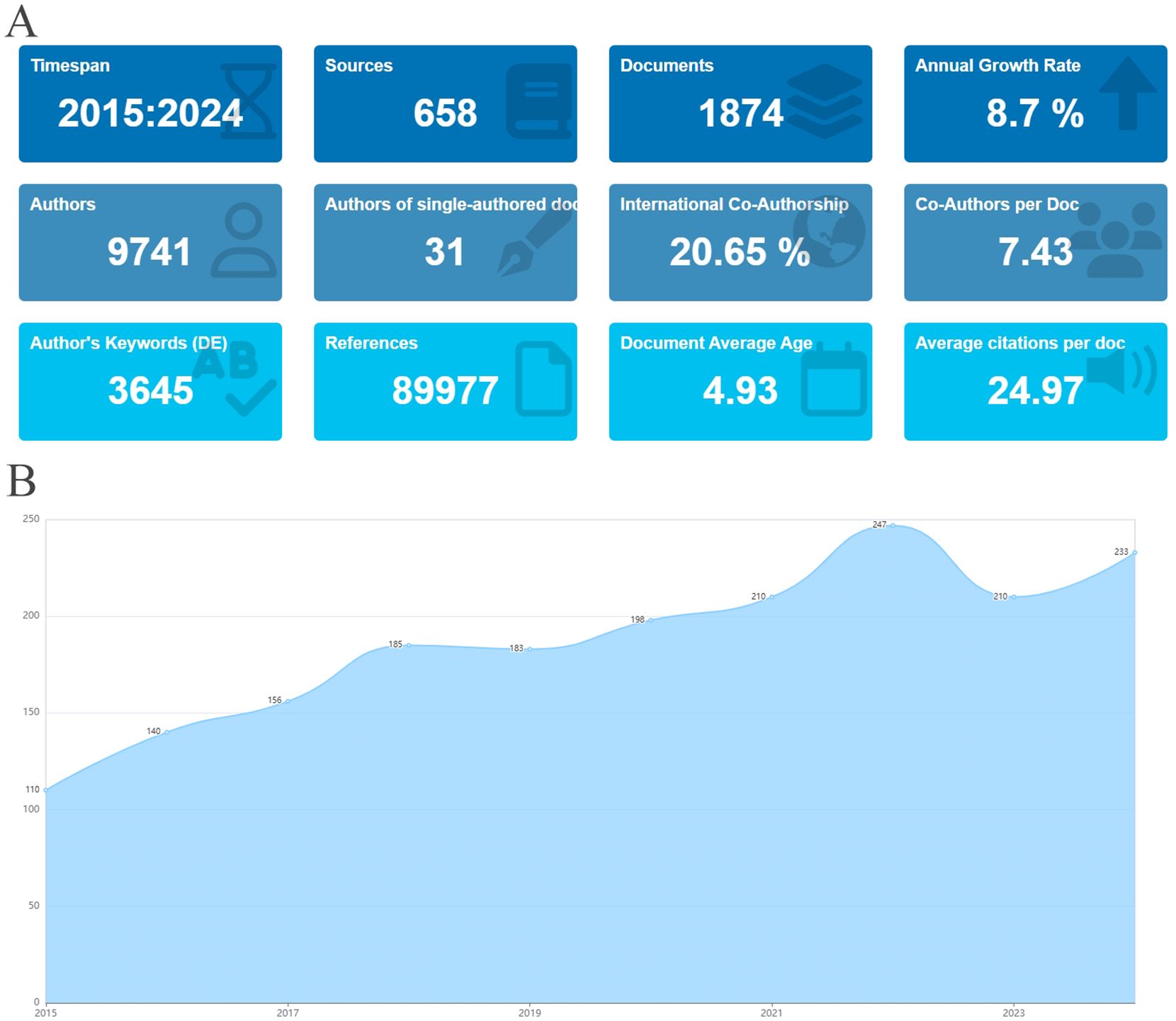
研究納入了2015年至2024年間Web of Science核心合集收錄的1,874篇關于腎臟疾病干細胞治療的文獻(圖1)。

運用CiteSpace、VOSviewer、R-Bibliometrix和文獻數據治理與分析系統等工具,對出版物數量與趨勢、國家/地區與機構貢獻及合作網絡、學科分布與期刊影響力、核心作者及其合作、高被引文獻與知識基礎、關鍵詞共現與演化等進行了全面的定量分析和可視化呈現。
納入文獻的基本信息及出版年份
本研究對1,874篇關于腎臟疾病干細胞治療的文獻進行了分析。基本信息如圖2A所示。圖2B顯示了過去十年該領域的出版趨勢。文獻產量從2015年到2022年穩步增長,過去兩年產量異常高。2022年,出版物數量達到頂峰,凸顯了人們對該領域研究的日益關注。
地理分布和機構分析
地理分布:文獻分布于83個國家和地區,呈現明顯的區域集中性。中國(592篇,31.6%)和美國(497篇,26.5%)是絕對的領導者,貢獻了超過一半的出版物,其次是意大利、日本和韓國(見圖3A, B)。主要研究中心集中在亞洲、歐洲、北美洲和澳大利亞,區域間合作廣泛。美國在國際合作網絡中處于核心地位(見圖3C, D, F)。值得注意的是,盡管早期(約2015-2017年)加拿大和土耳其顯示出一定的先驅性,但近年來的研究重心明顯向中國、美國以及部分歐洲和亞洲國家傾斜(見圖3E)。
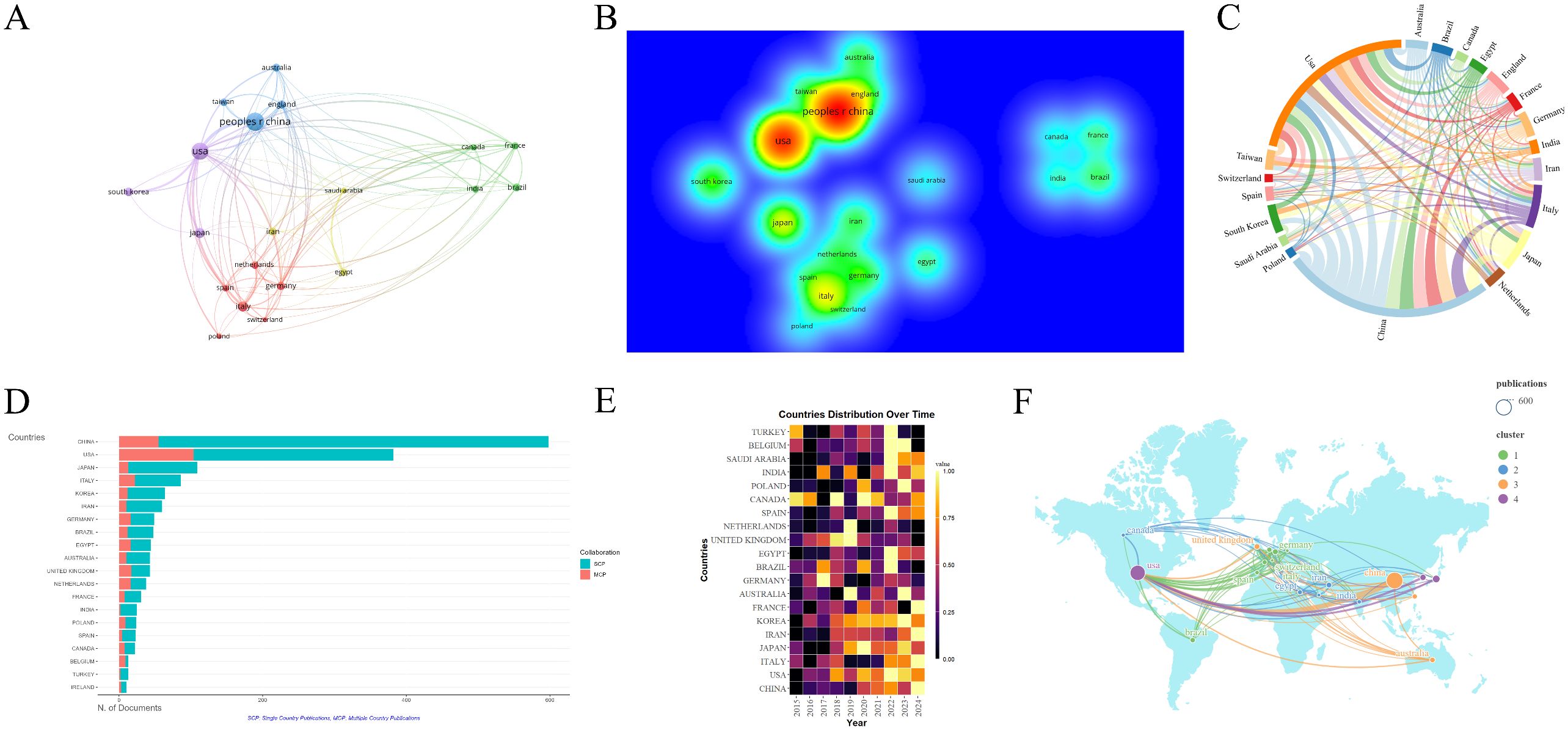
(A)貢獻國家/地區的分布。(B)國家/地區的密度可視化。(C)國家/地區的合作弦圖。(D)前20個國家/地區的出版物數量圖表。(E)按國家/地區劃分的出版物年度分布。(F)國家/地區合作地圖。
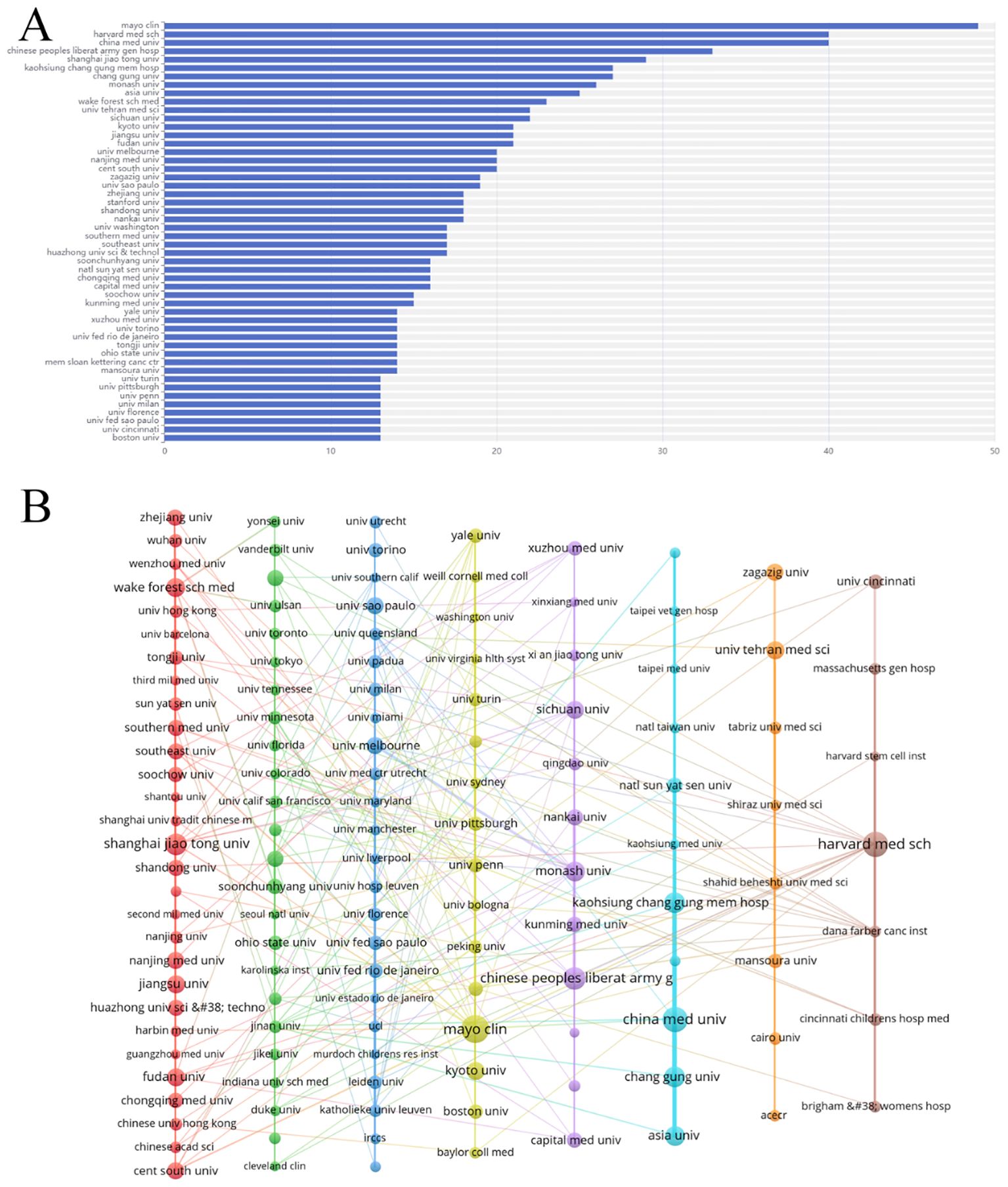
機構貢獻與合作:全球共有335個機構參與研究。梅奧診所(49篇)、哈佛醫學院(40篇)、中國醫科大學(40篇)、中國人民解放軍總醫院(33篇)和上海交通大學(29篇)是發表論文數量最多的前五機構(見圖4A)。
發表量前十機構中,美國、中國大陸和中國臺灣各占三席。合作網絡分析揭示了機構間的緊密聯系,如中國醫科大學與臺灣機構、莫納什大學與中國研究中心、以及部分中國機構與哈佛醫學院的合作(見圖4B)。
然而,中美頂尖機構間的直接合作相對有限,存在地理距離、政策監管差異(美國更寬松、中國在規范中發展)、倫理法律框架及研究優先級不同等潛在障礙,突破這些瓶頸需要建立互認標準、協調數據規范并規劃互補方向。
學科與期刊分析
學科與期刊:文獻來源于658種期刊,顯示出顯著的跨學科性(圖5A)顯示。分析表明,分子/生物學/遺傳學以及健康/護理/醫學領域的研究常被分子/生物學/免疫學期刊和醫學/臨床期刊引用(期刊疊加圖譜)。發文量超過20篇的期刊有8種,其中《Stem Cell Research & Therapy》、《International Journal of Molecular Sciences》等位列前五。

作者分析
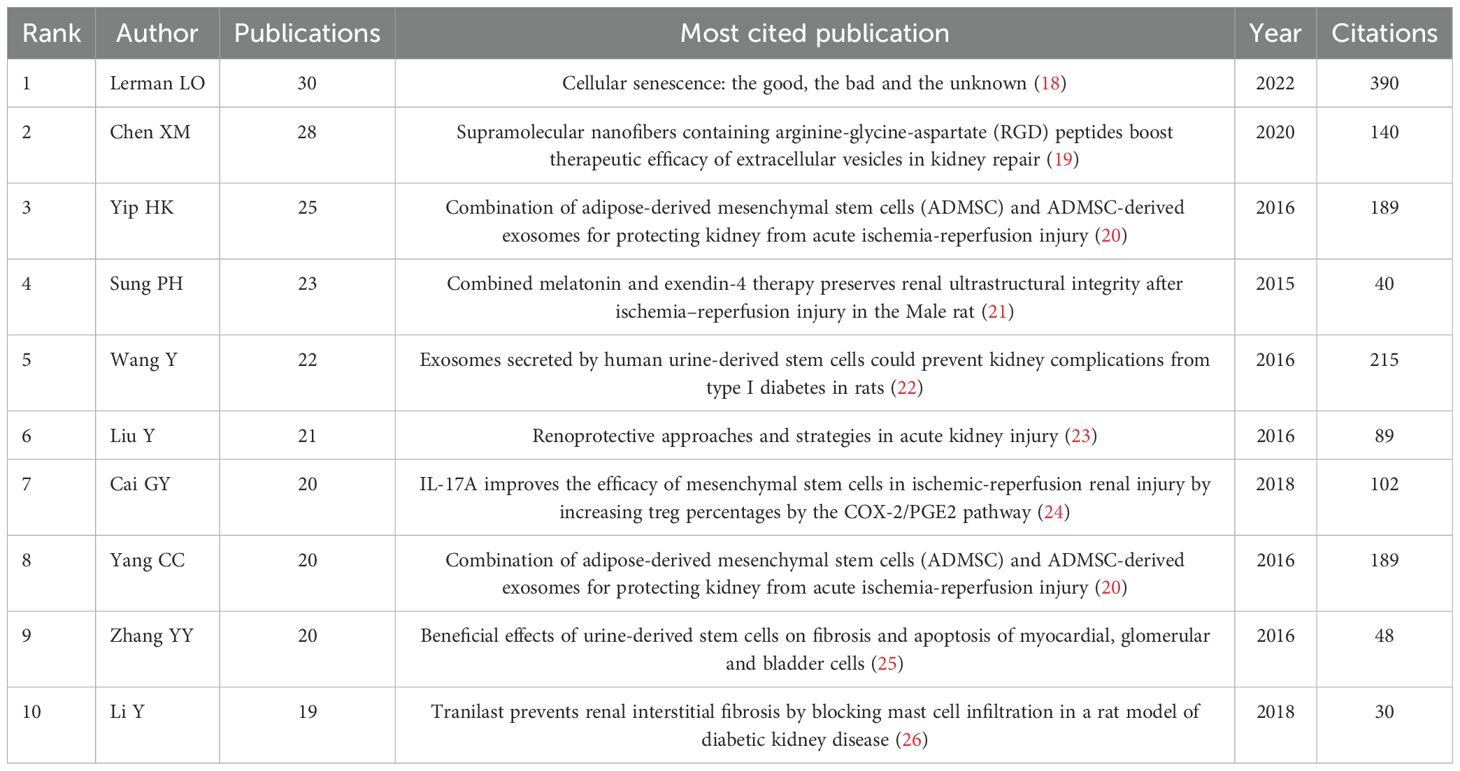
核心作者:研究共涉及9,741名作者。Lerman LO以30篇出版物位居榜首,其次是Chen XM、Yip HK、Sung PH和Wang Y(見圖6A,表1)。作者合作網絡(見圖6B)揭示了幾個重要的合作集群,例如由Yip HK、Yang CC和Sung PH形成的緊密團隊。值得注意的是,不同集群間的互動相對有限。Lerman LO展現了持續的研究產出(見圖6C)。
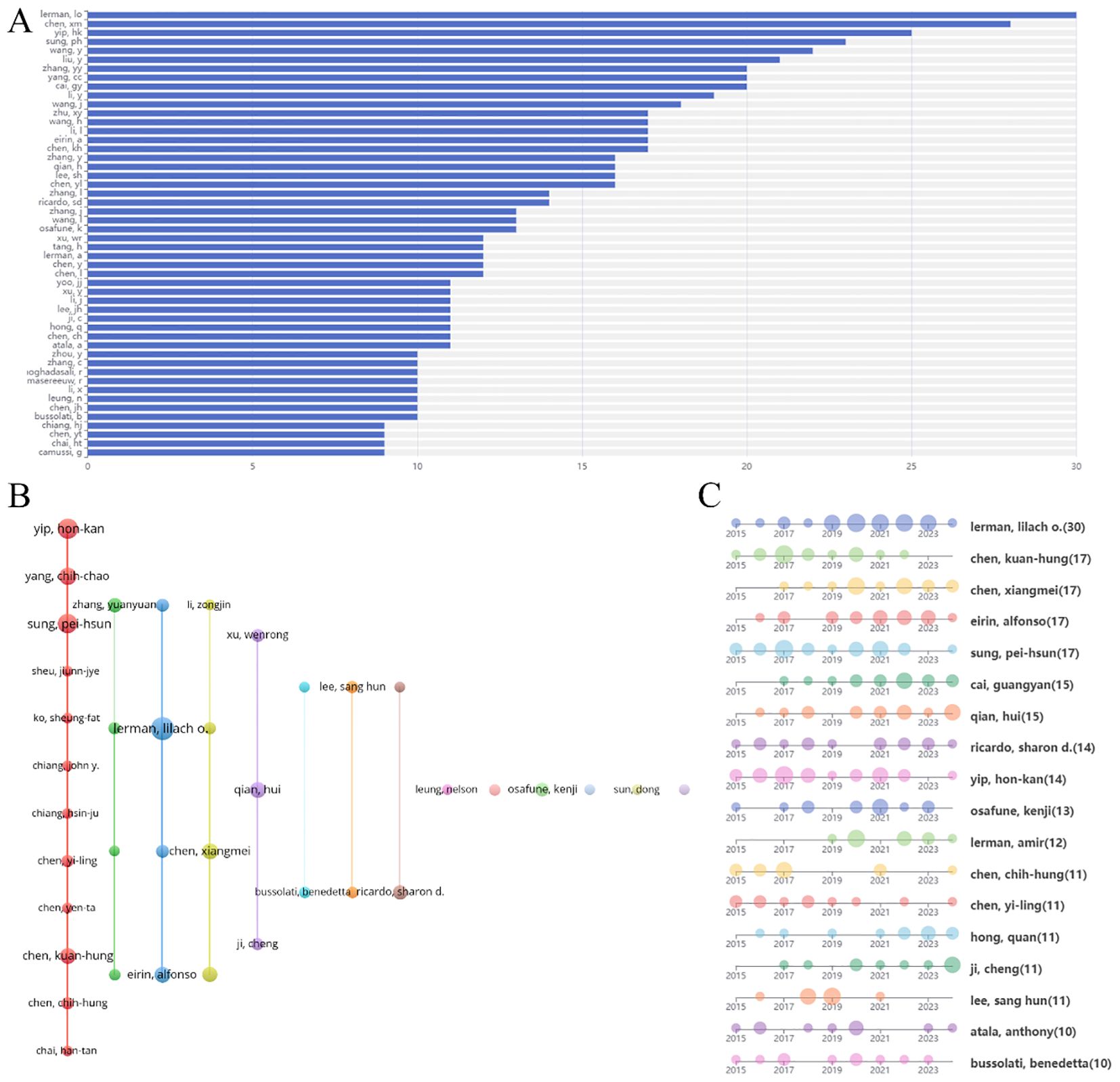
引用文獻及參考文獻分析
核心文獻與學術影響力:分析納入的1,874篇文獻發現,引用次數是衡量學術影響力的關鍵指標。
其中,SquillaroT等人發表在《細胞移植》上的文章“間充質干細胞臨床試驗:更新”被引用次數最多,引用密度也最高(圖7A-C)。該文全面評述了間充質干細胞(MSC)的再生潛力、臨床應用(涵蓋多種疾病)、當前面臨的挑戰(如細胞異質性),并分析了大量臨床試驗,突顯了MSC的治療前景和持續性問題。研究領域內引用最熱門的10篇文獻信息見表2。
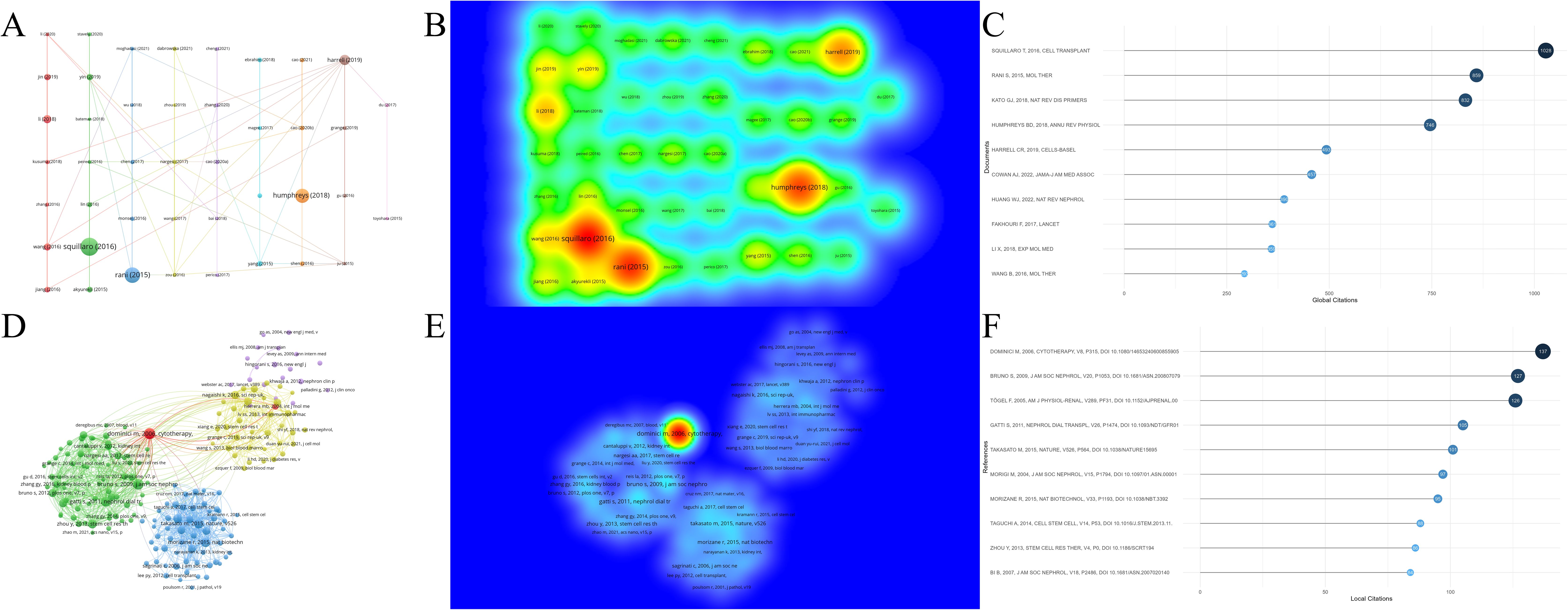
(A)被引文獻網絡圖。(B)被引文獻密度可視化。(C)被引文獻Top10量圖。(D)被引參考文獻網絡圖。(E)被引參考文獻密度可視化。(F)被引參考文獻Top10量圖。
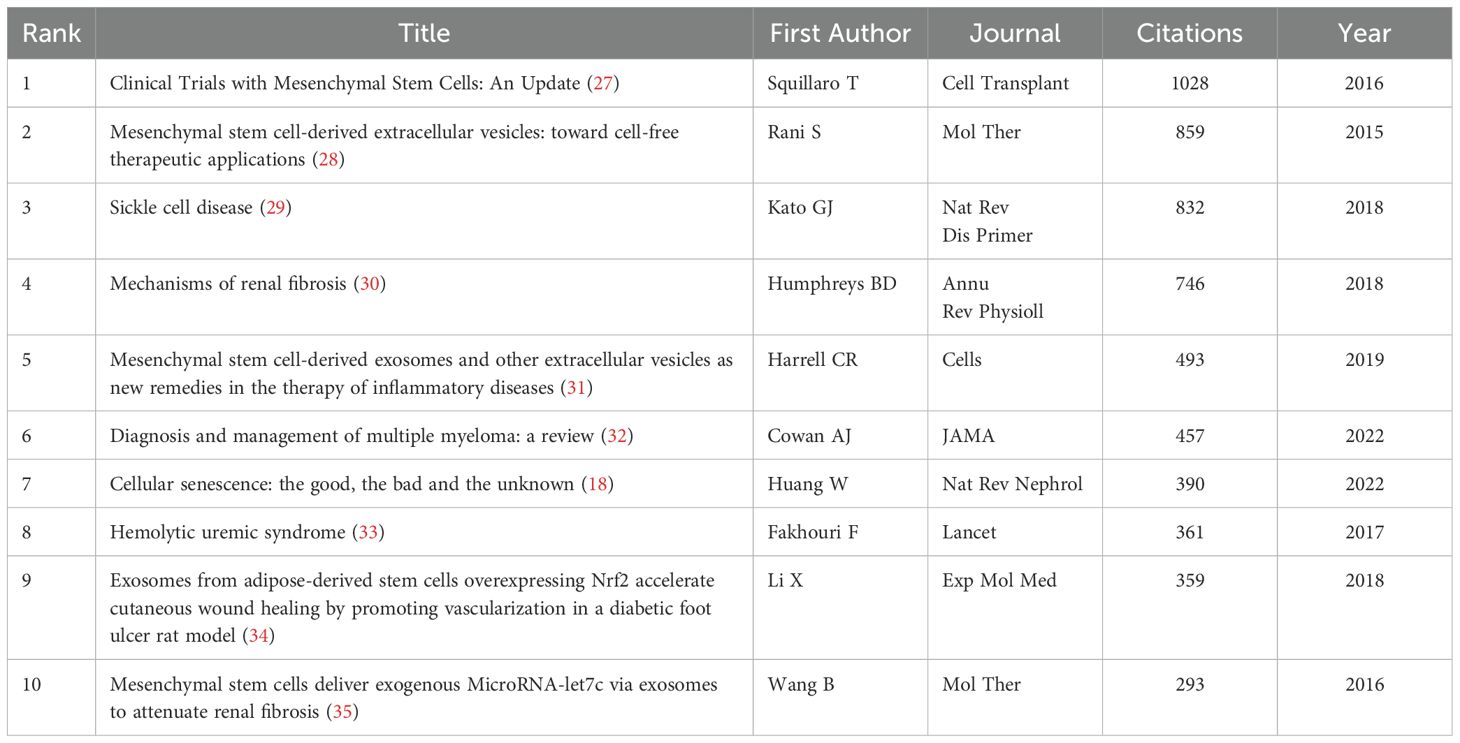
關鍵參考文獻與奠基性工作:在分析所有文獻的參考文獻時,Dominici M等人2006年發表于《細胞治療》的論文“定義多能間充質基質細胞的最低標準:國際細胞治療學會的立場聲明”最為突出。這篇具有里程碑意義的論文提出了標準化定義人類MSC的最低標準,旨在統一研究規范、促進細胞表征和增強數據可比性,對該領域的發展產生了深遠影響。該領域被引用次數最多的前10篇參考文獻信息見表3。
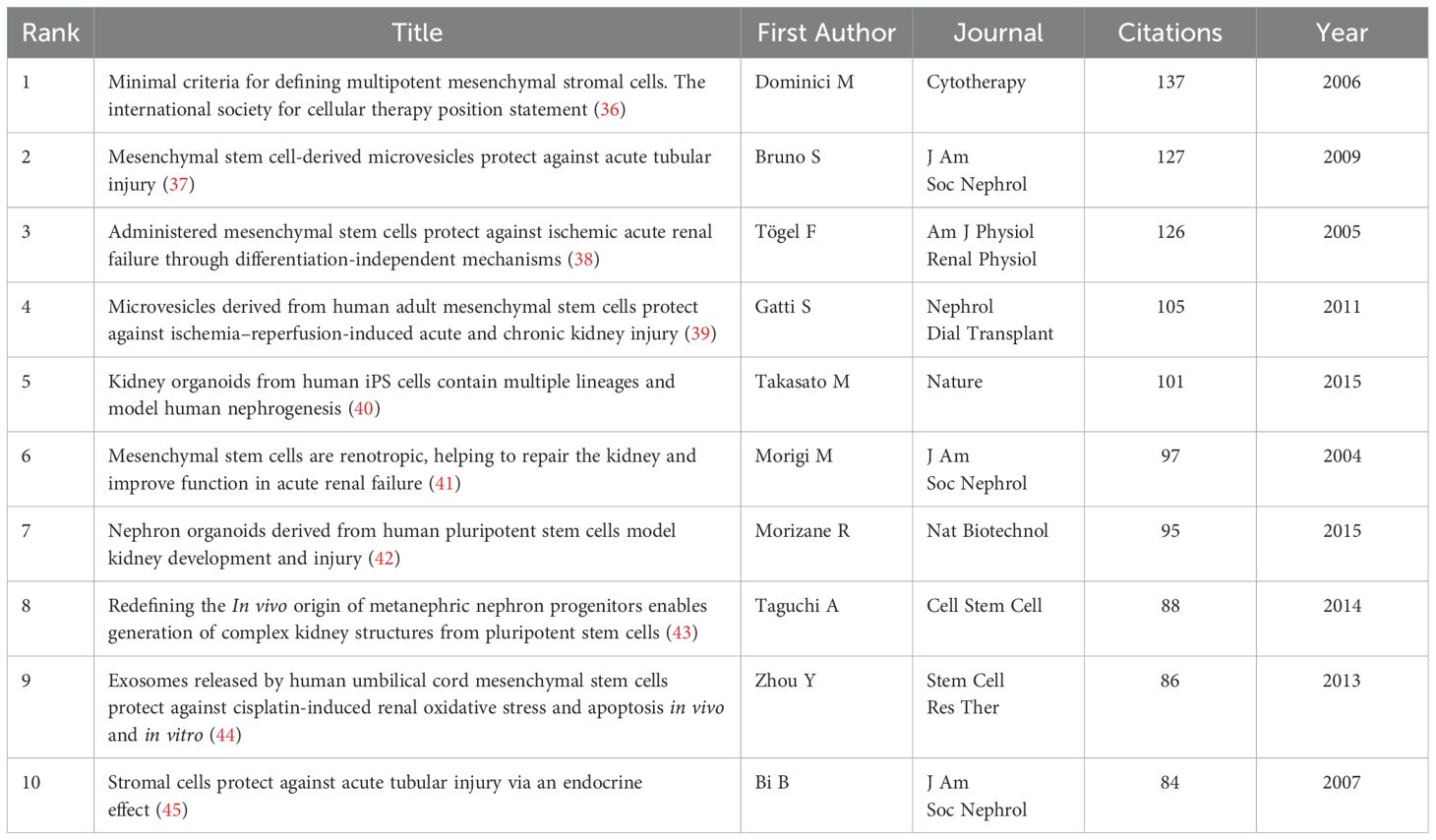
引用激增與前沿熱點:通過CiteSpace軟件識別出引用量激增的前30篇參考文獻)(圖8),揭示了特定時期的研究熱點。這些文獻的引用量在標注為紅色的年份段內出現顯著高峰,最早可追溯到2011年。最近一次是在2021年。
其中,Taguchi A等人2014年發表的“重新定義后腎腎元祖細胞的體內起源使得能夠從多能干細胞生成復雜的腎臟結構”展現了最強的引用激增(2015-2019年,強度=13.13)。該研究通過重新定義腎臟祖細胞的起源,成功利用多能干細胞在體外生成了復雜的腎臟結構,為腎臟發育研究和再生醫學提供了突破性的新見解。
干細胞治療腎病的研究熱點與前沿趨勢
關鍵詞分析是洞察領域核心主題和新興趨勢的關鍵窗口。共現圖譜(見圖9A, B)顯示高頻關鍵詞包括“MSCs”、“AKI”、“移植”、“基質細胞”和“CKD”。K均值聚類識別出10個主題集群,如“造血干細胞移植”、“多能干細胞”、“細胞外基質”等(見圖9C),勾勒出研究的基本框架。

(A)關鍵詞出現情況。(B)關鍵詞密度可視化。(C)關鍵詞聚類圖。(D)關鍵詞時間軸。(E)關鍵詞年度熱力圖。(F)關鍵詞云圖。(G)腎臟疾病干細胞治療研究中引用爆發性最強的Top20個關鍵詞。
時間軸圖譜(見圖9D)和年度熱圖(見圖9E)清晰展示了研究熱點的動態遷移:早期聚焦“MSCs”、“細胞凋亡”、“氧化應激”等基礎機制;近期熱點顯著轉向“糖尿病腎病(DN/DKD)”和“腎移植”,標志著向臨床轉化方向的深化。關鍵詞云圖(見圖9F)再次確認“MSCs”與“CKD”的主導地位。爆發詞檢測(見圖9G)則精準捕捉到兩大最強勁的前沿:
細胞外囊泡(EVs)療法:以最高爆發強度(7.88)在2021-2022年涌現。EVs攜帶miRNA、蛋白質等活性物質,通過靶向遞送發揮治療作用。其核心機制之一是抑制TLR4/NF-κB信號軸(見圖10),例如miR-125b通過下調TRAF6阻斷NF-κB驅動的TGF-β通路,減輕DKD的炎癥與纖維化。EVs規避了活細胞移植風險,穩定性高,可規模化生產,全球已有超過20項臨床試驗聚焦其在膜性腎病(MN)和DKD中的應用。

糖尿病腎病(DKD):緊隨其后(強度7.82),預計2022-2024年達峰值,成為轉化研究的核心戰場。
具體熱點方向與技術進展:間充質干細胞(MSCs):仍是絕對核心。其療效主要通過旁分泌生物活性分子介導,調節腎臟纖維化、炎癥和免疫穩態,而非直接分化為腎細胞。研究熱點集中于其在AKI、CKD、腎纖維化、特定腎病(如DKD, MN)及腎移植免疫調節中的應用。
多能干細胞(iPSCs)與基因編輯:
- 定向分化:患者特異性iPSCs分化為腎前體細胞(如足細胞、腎小管上皮細胞)用于修復損傷。中國REGEND003制劑(尿液來源腎前體細胞)已獲NMPA批準開展I/II期臨床試驗,治療2型糖尿病合并CKD。
- 基因修飾:CRISPR等技術編輯iPSCs增強其治療特性(如過表達HO-1基因增強抗炎和抗氧化應激能力)。
新型干細胞來源與聯合策略:
- 無創來源細胞:尿液干細胞(USCs)因采集便捷、增殖力強,成為修復DKD足細胞損傷的新興選擇。
- 聯合療法:探索干細胞與傳統藥物(如免疫抑制劑)或創新療法的聯合。例如,南京中醫藥大學研究證實,黃酮類中藥成分可改善腎臟微環境,提升MSCs存活率,協同減少蛋白尿和腎纖維化。
臨床轉化突破案例(佐證熱點方向):
重癥腎病:
- IgA腎病:韓國采用自體脂肪SVF/MSC聯合甲潑尼龍治療,患者eGFR顯著改善并長期穩定(隨訪10年未透析),腎活檢顯示系膜增生減少。
- 狼瘡性腎炎:同種異體MSCs輸注使75%難治性患者獲得緩解,尿蛋白下降,調節性T細胞(Treg)比例升高。
糖尿病腎病(DKD):
- MSCs穩定腎功能:II期試驗顯示,早期DKD患者(GFR>60mL/min)經MSCs治療后eGFR保持穩定,強調了早期干預的重要性。
- 腎移植免疫調節:腎移植后輸注第三方MSCs,術后早期eGFR顯著提高(較對照組+50%),并通過上調Treg細胞降低排斥反應風險。
政策與產業化:中國國家衛健委將干細胞療法納入《腎臟病學領域十大創新方向》,上海長征醫院報道MSCs修復腎小球有效率達75%,肌酐顯著下降。全球首款自體腎前體細胞藥物REGEND003(中國)已進入多中心臨床試驗,目標2026年上市。
總結與未來展望
本研究通過對近十年(2015-2024)全球腎臟疾病干細胞治療研究的系統性文獻計量分析,清晰描繪了該領域的全景圖:研究產出持續快速增長,中國和美國是主導力量,機構間合作廣泛但中美頂尖機構互動有待加強。Lerman LO等學者和《Stem Cell Research & Therapy》等期刊貢獻卓著。間充質干細胞(MSCs)及其旁分泌機制(尤其是細胞外囊泡[EVs])是研究的核心焦點和知識基礎。
分析揭示了顯著的研究趨勢:從早期的基礎機制探索(凋亡、氧化應激)轉向以解決重大臨床需求為導向的研究,特別是針對糖尿病腎病(DKD)和膜性腎病(MN)等難治性疾病的創新療法開發。EVs療法和基于iPSCs的再生策略(包括基因編輯)是當前最具爆發力的前沿方向。
臨床案例的成功(如IgA腎病、狼瘡性腎炎、DKD早期干預、腎移植免疫調節)和政策支持(如中國創新方向、REGEND003藥物進展)為該領域的轉化注入了強心劑。
未來研究應著力于:深入解析EVs等治療載體的作用機制與優化策略;推進iPSC來源細胞治療的安全性與有效性評估;加強針對DKD、MN等特定疾病的綜合治療方案開發;深化跨機構、跨國界的合作,尤其需彌合中美研究體系差異;建立標準化流程并探索長期療效。
本研究提供的定量證據和可視化圖譜,為科研人員、資助機構和政策制定者把握領域脈搏、識別關鍵挑戰、規劃未來研究路徑提供了重要依據,有望加速干細胞療法在腎臟疾病領域的臨床轉化進程。
參考資料:[1]:iao S, Zhang X, Zhou Y, Wang L, Chen C, Ye C, Zhou Y and Wang C (2025) Worldwide hotspots and trends in stem cell therapy for kidney disease in the last decade: a bibliometric and visualization analysis from 2015 to 2024. Front. Immunol. 16:1619291. doi: 10.3389/fimmu.2025.1619291
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加微信
掃碼添加微信