慢性腎臟病(Chronic Kidney Disease, CKD)是指由各種原因引起的腎臟結構或功能異常,且持續時間超過三個月的健康狀況。根據改善全球腎臟病預后組織(KDIGO)的臨床指南,符合以下任一情況即可診斷為CKD:腎小球濾過率(eGFR)持續低于60 mL/(min·1.73m2),或存在腎損傷標志,如蛋白尿、電解質紊亂、尿沉渣異常、影像學或組織學提示腎臟結構異常。
CKD可由多種疾病及危險因素引起,導致腎功能出現進行性、不可逆的下降。高血壓和糖尿病是其主要病因,其他還包括單基因或多基因遺傳因素、表觀遺傳改變以及不良環境影響等。據統計,全球CKD的患病率約為3%至18%,可發生于各年齡段,尤其在老年人群中更為常見。
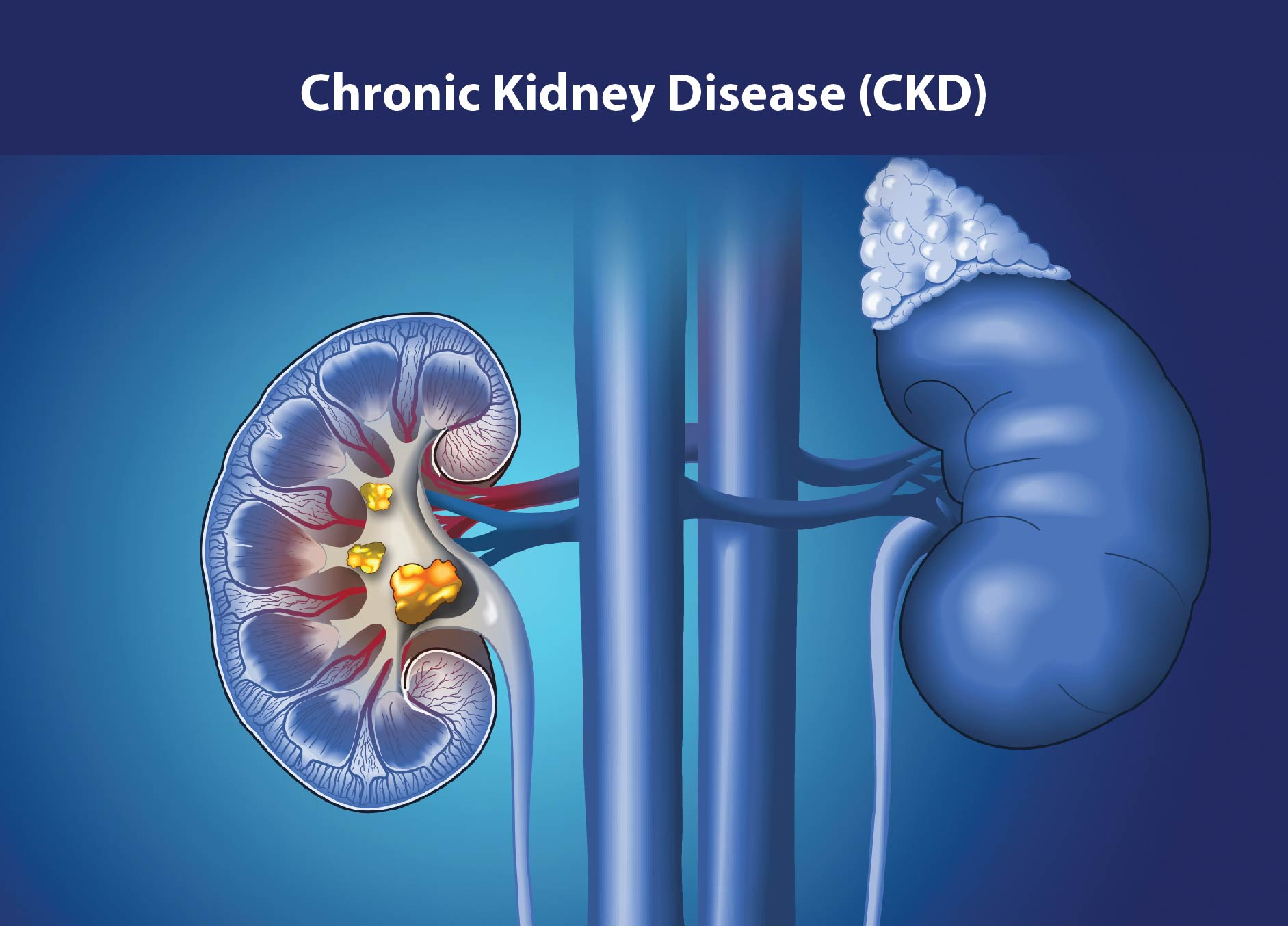
CKD早期常無明顯癥狀,容易被忽視,而一旦出現顯著臨床表現,往往已進展至中晚期。多數患者會逐漸發展至終末期腎病(ESKD),此時通常需依靠腎臟替代治療,如透析或腎移植。雖然透析可延長患者生存時間,但高昂的費用及對生活質量的影響仍是巨大挑戰。腎移植雖是有效手段,卻受限于器官供體短缺,且移植后患者需長期服用免疫抑制劑,增加了感染及其他并發癥的風險。因此,探索更有效、更安全的CKD治療方案成為當前醫療研究的重點。
近年來,隨著再生醫學的快速發展,干細胞治療為CKD患者提供了新的希望。研究表明,干細胞不僅具有多向分化潛能,還可通過旁分泌機制發揮腎臟保護作用,從而為治療CKD開辟了新途徑。
間充質干細胞(MSCs)在CKD治療中的潛力
有研究發現間充質干細胞(MSCs)能定位于受損組織器官部位,定向分化為器官特異性細胞,修復受損組織或者通過旁分泌和內分泌作用產生生物活性因子,如細胞因子、趨化因子、生長因子等,能發揮促細胞增殖、抗纖維化、抗炎、抗凋亡、多向分化和調節免疫反應等作用。這些功能使MSCs在治療CKD方面顯示出強大的潛力。
大量研究表明MSCs在一定條件下可以分化為腎小球細胞、腎小球系膜細胞、腎小管上皮細胞等腎臟實質細胞,并發現MSCs可以選擇性地修復外髓質部的部分腎小管,恢復腎小管結構及功能。
臨床試驗驗證
Cinzia Rota等人曾在《International journal of molecular sciences》雜志發表了一篇文獻,描述了全球16項關于干細胞療法在慢性腎病領域的臨床試驗結果,總結了當前的研究進展和進入臨床應用的前景。[1]

Machiguchi等人將MSCs誘導培養成腎小管上皮細胞,然后將其移植入免疫缺陷大鼠的腎皮質,可檢測到新生的腎小球和腎小管結構。
Choi等人納入30例CKD患者,通過靜脈途徑輸注臍帶來源的MSCs,結果發現細胞移植后第1、3、6個月,移植組血清肌酐清除率明顯高于對照組,且2例患者蛋白尿消失。
Shekarchian等人進行了一個為期1年的單臂臨床實驗,給7例不同原因導致的CKD患者單次輸注自體骨髓MSC,1年后隨訪發現6例患者血肌酐水平、腎小球濾過率(eGFR)較移植前無明顯改善,也未發現細胞輸注的不良反應,證明了干細胞移植的安全性和耐受性。
總 結:MSCs作為治療CKD的一種潛在方式,引起了許多學者的關注和研究。比起傳統的治療方法,具有不可替代的優勢,一方面可用于移植的MSCs來源廣泛,不同來源的MSCs在CKD中均能發揮治療作用。另一方面MSCs無免疫排斥反應,移植后不用長期服用抗免疫排斥藥物。
參考資料:
[1]Rota, C.; Morigi, M.; Imberti, B. Stem Cell Therapies in Kidney Diseases: Progress and Challenges.?Int. J. Mol. Sci.?2019,?20, 2790. https://doi.org/10.3390/ijms20112790
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加微信
掃碼添加微信