腦卒中是全球發病率和死亡率的主要原因,而有效恢復神經功能的治療方法卻很有限。細胞療法已成為促進中風后神經再生和功能恢復的突破性方法。
細胞療法治療腦卒中:神經重塑的革命性突破與臨床轉化
首先,本章全面概述了細胞療法在腦卒中臨床前的應用,使用的各種細胞類型包括神經干細胞間充質干細胞和骨髓源性單核細胞,每種細胞都有不同的作用機制,如神經保護和神經發生、免疫調節和血管生成。
其次,本章還概述了中風患者細胞療法的適應癥和禁忌癥,以及細胞來源和劑量、給藥途徑。
第三,本章還討論了相關副作用、潛在并發癥以及近期試驗中觀察到的臨床結果。
最后,通過整合臨床前和臨床研究的結果,本章旨在全面概述腦卒中細胞療法的現狀,并討論未來的研究和臨床應用方向,強調標準化方案、嚴格臨床試驗和先進研究的必要性,以優化腦卒中患者細胞療法的安全性和有效性。
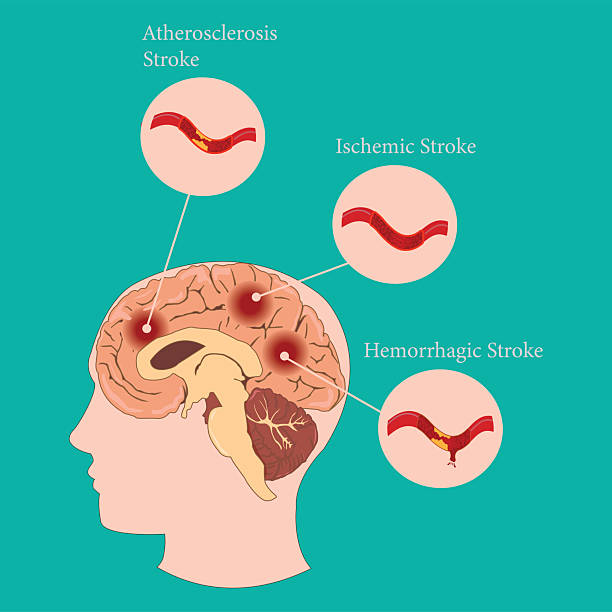
腦卒中疾病的本質與流行病學負擔
腦卒中是一種危重疾病,發生在腦部血液供應中斷時,導致腦功能突然受損。這種中斷可能是由血管阻塞(缺血性中風,圖1)或血管破裂(出血性中風,圖2)引起的,這兩種情況都會導致大腦特定區域缺氧和營養。缺血性中風是最常見的中風類型,占所有中風病例的87%。
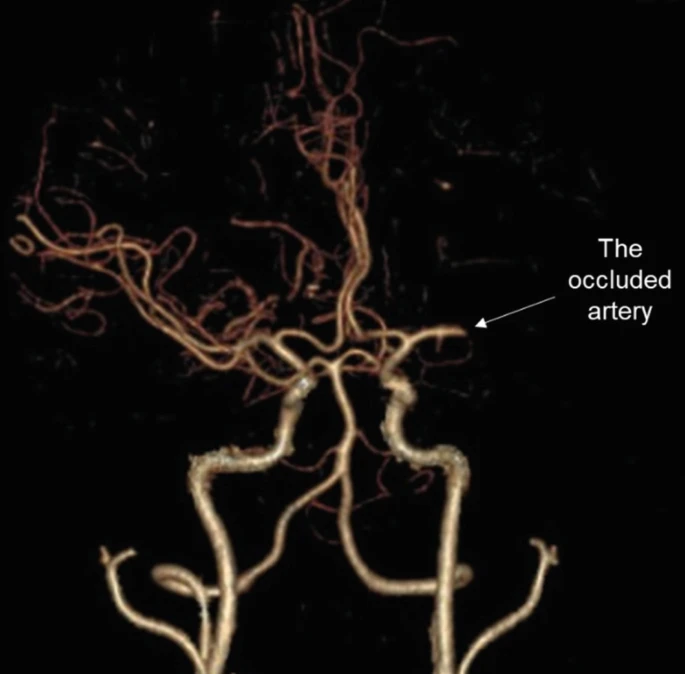
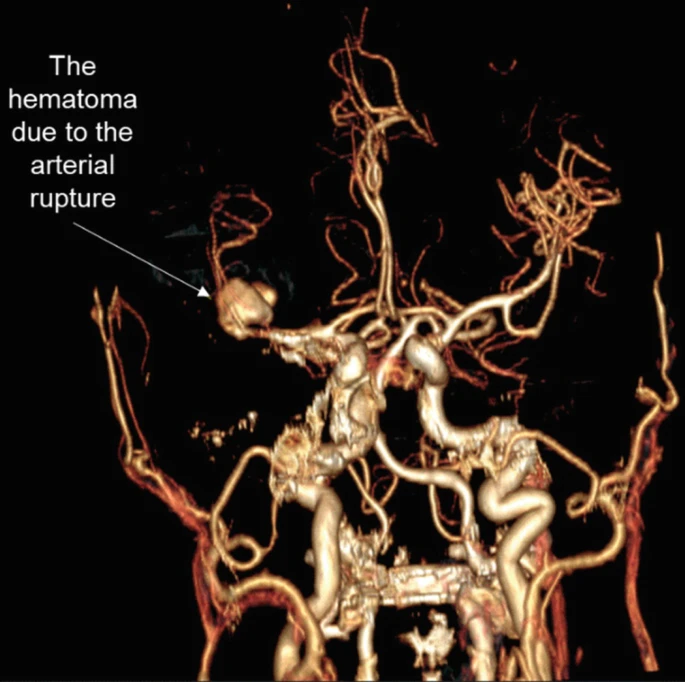
作為美國致殘首因,其發病率呈上升趨勢:
- 死亡率:2021年達41.1人/10萬(較2020年↑5.9%)
- 發病率:每40秒新增1例,年發病人數超79.5萬
- 經濟負擔:2018-2019年直接醫療成本+生產力損失達560億美元
腦卒中的分型治療策略與局限性
治療方案因中風病因而異。
對于缺血性中風,早期干預包括進行血栓溶解療法,該療法使用組織型纖溶酶原激活劑 (tPA) 等藥物。這種靜脈注射療法旨在溶解血栓并恢復血流,在中風發作后的最初4.5小時內最有效。然而,由于時間有限和潛在的并發癥,只有一小部分(約 3-5%)中風患者接受tPA治療。血管內血栓切除術是通過介入放射學使用導管進行的,可與血栓溶解療法相結合,以有效消除特定血管內的大血栓 。
對于出血性中風,當血管破裂導致出血時,需要進行手術干預。手術的目的是修復血管、去除血栓并減輕腦部壓力。此外,也可使用介入放射學方法利用線圈封堵出血部位。雖然慢性卒中護理需要強化康復,但功能恢復的程度仍然有限。報告顯示,56.7%的患者在卒中一年后可以恢復工作,兩年后這一比例上升至66.7%。
因此,當務之急是找到能夠增強患者處理卒中后心理健康和神經系統后果能力的補充治療方法。細胞療法是卒中治療的一個有希望的方向,因為它們可能兼具神經保護和再生作用。2000年,Kondziolka等人首次將培養的人類神經元細胞移植到卒中患者體內。此后,已開展了許多卒中細胞療法試驗。
細胞療法治療腦卒中的突破性前景
因此,當務之急是找到能夠增強患者處理卒中后心理健康和神經系統后果能力的補充治療方法。細胞療法是卒中治療的一個有希望的方向,因為它們可能兼具神經保護和再生作用。2000年,Kondziolka等人首次將培養的人類神經元細胞移植到卒中患者體內。此后,已開展了許多卒中細胞療法試驗。
細胞療法在治療中風的細胞類型有哪些?
細胞療法使用不同的細胞,包括神經干細胞 (NSC)/神經祖細胞 (NPC)、間充質干細胞 (MSC)、多向分化耐壓細胞 (Muse)、誘導性多能干細胞 (iPSC) 以及骨髓來源的單核細胞 (BMMNC),代表著一種頗具吸引力的中風治療途徑,并已取得令人欣喜的療效。各種類型的細胞已被用于不同劑量、不同注射途徑,每種途徑都通過多種機制發揮作用。
神經干細胞/神經祖細胞
神經干細胞(NSC)/神經祖細胞(NPC)被認為是治療中風的有希望的療法。據報道,NSC主要通過腦局部注射給藥。一項研究表明,NSC和NPC在治療中的主要作用機制是通過釋放血管內皮生長因子(VEGF)來誘導血管生成,以及通過星形膠質細胞和神經元的分化來促進神經發生,這有可能改善中風后的神經功能。
研究表明,NSC/NPC能夠在選擇性神經元死亡區域存活(約占移植NSC/NPC的8%),并在移植后28天分化為成熟的神經元和神經膠質細胞,從而有助于改善局灶性缺血模型蒙古沙鼠的神經系統結果。將表達VEGF的人類修飾 NSC 注射到腦出血 (ICH) 中風模型小鼠體內,可發揮神經保護、血管生成和功能恢復的作用,因為人類NSC分化為神經元和星形膠質細胞,從而刺激宿主微血管增殖,下調促凋亡蛋白,上調抗凋亡蛋白和促進細胞存活的分子。
間充質干細胞
MSCs具有神經再生潛力,能夠促進遷移、分化、血管生成、免疫調節、旁分泌信號傳導和神經保護,因此可用于治療中風。
MSCs治療中風的靶點可能取決于病理缺血過程的不同階段。用于治療中風的MSCs主要來源包括骨髓 (BM)、臍帶 (UC) 和脂肪組織 (AD)。雖然MSCs可在早期減輕梗死周圍區域的炎癥反應和損傷,并調節動態環境以抵抗毒性,但晚期 MSC 移植可通過血管生成和神經發生來調節修復過程。在臨床前試驗中,MSCs可通過不同途徑給藥,包括動脈內、靜脈內和腦內注射。
最近,間充質干細胞 (MSC) 產品也被用于治療中風。注射胚胎干細胞衍生的MSC (ESC-MSC) 的培養基 (CM) 可減輕體重、降低死亡率、減少梗死體積,促進突觸恢復,并改善MCAO大鼠的神經功能缺損。UC-MSC的細胞外囊泡 (EV) 通過增強短暫性MCAO大鼠模型的神經發生和神經可塑性,改善功能恢復。干細胞衍生的EV的可能機制包括維持干細胞特性、神經保護、新血管形成、生物標志物應用和神經炎癥免疫調節。
骨髓來源的單個核細胞(BMMNC)
多項研究已證明BMMNC對腦缺血動物具有神經保護作用。在缺血性中風動物模型中,BMMNC移植已顯示出良好的效果。Yang等人使用栓塞性中風大鼠模型證明BMMNC降低了BBB通透性和tPA誘發的出血性轉化的嚴重程度。
細胞療法治療中風的的臨床應用
治療適用性與禁忌范圍
干細胞治療適用于全階段(急性/亞急性/慢性)與全類型(缺血性/出血性)中風后神經功能障礙患者。
絕對禁忌癥包括:
- ??昏迷狀態
- ??進行性腦水腫
- ??嚴重血液系統疾病
- ??活動性細菌/病毒感染
- ??循環呼吸功能失代償
核心原則:治療需在生命體征穩定后實施
細胞來源與劑量差異
臨床常用四類細胞:BMMNC(骨髓單核細胞),BM/AD/UC-MSC(骨髓/脂肪/臍帶間充質干細胞)。
劑量尚未標準化,關鍵發現:
- BMMNC劑量跨度大:單次輸注1×10?細胞(Ghali等)至1.59×10?細胞(Moniche等),差異達159倍;
- MSC基準方案:多數研究采用?1×10?細胞/kg體重(如de Celis-Ruiz團隊);
- 特殊案例:華通氏膠MSC采用固定劑量3×10?細胞/患者(Milczarek等);
- UC-MSC現行實踐:按1×10?細胞/kg體重給藥。
矛盾點:療效與劑量非線性相關,需個體化調整
細胞輸送途徑
將細胞輸送到體內主要有三種途徑:靜脈輸注、動脈輸注和病灶周圍注射。為了評估通過各種給藥途徑進行細胞治療的療效,Fauzi等人對21篇已發表的文章進行了薈萃分析。他們的研究結果表明,腦內途徑與其他途徑相比,療效更佳,盡管由于該操作的侵入性,不良事件的發生率更高。我們選擇鞘內途徑進行細胞給藥,因為它有助于將細胞輸送到腦部,而不會遇到靜脈輸注中觀察到的諸如肺部包封等問題。此外,與直接注射到腦部相比,鞘內途徑是一種侵入性較小的替代方法。
副作用和并發癥
Chumnanvej等人對九項研究進行了薈萃分析,以評估中風患者接受細胞療法相關的不良事件。研究人員比較了細胞療法組和對照組的不良事件發生情況。研究結果表明,接受細胞療法的患者與對照組患者發生各種副作用(包括部分性癲癇發作、低燒、感染、復發性血管發作和腫瘤發展)的風險并無顯著差異。此外,兩組的死亡風險也相當。
干細胞治療腦卒中的臨床應用結果
治療結果評價指標
已經使用了多種測量量表來測量細胞治療期間的臨床結果,例如功能獨立性清單 (FIM) 、美國國立衛生研究院卒中量表 (NIHSS) 、Barthel 指數 (BI) 和改良Rankin量表 (mRS) 評分。
2010年,Lee等人報道了52例接受細胞療法治療的患者的結果;其中16例患者接受了MSC治療,對照組36例患者。隨訪期間,MSC組4例(25%)患者死亡,對照組21例(58.3%)患者死亡。
MSC治療后未觀察到明顯的副作用。兩組出現副作用(包括癲癇發作和復發性血管發作)的患者數量并無差異。與對照組相比,MSC組的隨訪mRS評分較低,而mRS評分為0-3的患者數量較多。作者得出結論,靜脈自體MSC移植對卒中患者在長期隨訪中是安全的,并且可能改善卒中后的康復,具體取決于患者的具體特征。
2015年,Sharma及其同事報道了將自體BMMNC輸注至24例慢性卒中患者脊髓腔的結果。

結果顯示,24例患者中,12例步行功能改善,10例手部功能改善,6例站立平衡改善,9例行走平衡改善。作者還提到,治療結果與患者年齡存在相關性。60歲以下患者的預后優于60歲以上患者。
2023年,Fauzi等人進行了一項“干細胞治療缺血性卒中給藥途徑的比較:臨床結果和安全性的系統評價與薈萃分析”。其中對21篇研究進行了薈萃分析,以評估細胞治療治療卒中的安全性和有效性。

他們發現,接受干細胞治療的患者在12和24個月后,NIHSS和mRS評分有下降的趨勢,BI評分有上升的趨勢,表明臨床結果更好。6個月后,腦內組NIHSS評分下降至6.96±2.36,動脈組下降至2.2±1.92,靜脈組下降至7.25±5.31。6個月后,腦內組mRS評分下降至3.34±0.63,動脈組下降至2.33±0.86,靜脈組下降至2.63±0.90。 6個月后,BI評分改善顯著,腦內組為26±16.80,靜脈組為76.85±21.41。動脈組數據未提及。
2020年,Chumnanvej等人進行的自體骨髓單核干細胞治療卒中患者:比較研究的薈萃分析顯示,隨訪3個月后,NIHSS、BI或mRS評分無顯著差異。

然而,接受BMMNC治療的患者的BI評分在6個月后顯著改善。作者得出結論,細胞療法的效果僅在6個月后才顯著。
我們已開展一項1/2期臨床試驗,以評估臍帶間充質干細胞(UC-MSCs)在改善中風后神經系統后遺癥方面的安全性和有效性。10例患者參與了該試驗的1期,其中5例接受靜脈注射UC-MSCs,5例接受鞘內注射UC-MSCs。兩組均未觀察到嚴重不良事件。該研究的2期正在進行中。
爭議與未來方向
研究結果表明細胞療法治療中風患者的安全性和有效性,但仍需要進一步研究以確定細胞療法輸注的理想劑量、給藥方法和時間。
參考資料:Liem, N.T., Nguyen, Q.T. (2025). Cell Therapy for Cerebral Stroke. In: Liem, N.T., Forsyth, N.R., Heke, M. (eds) Cell Therapy. Springer, Singapore. https://doi.org/10.1007/978-981-96-1261-1_12
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加微信
掃碼添加微信