原發性扭轉肌張力障礙(PTD)是由基因突變引起的,并且通常逐漸進展。目前,尚無能夠抑制進展的療法。神經干細胞移植(NSC)正在被研究作為神經退行性疾病(如中風和創傷)的潛在療法。
肌張力障礙涉及主動肌和拮抗肌同時收縮,導致不自覺的持續和重復姿勢以及定向運動。原發性扭轉肌張力障礙 (PTD) 的發病機制與多種基因突變有關。PTD常常導致患者嚴重殘疾。PTD的傳統療法包括口服抗帕金森病藥物、肉毒桿菌神經毒素、蒼白球切開術和深部腦刺激 (DBS) 。然而,這些療法通常無法有效預防 PTD 進展,可能會引起嚴重的副作用,并且成本高昂(例如DBS設備)。神經干細胞(NSC)療法在帕金森病、小腦萎縮、中風和其他神經系統疾病領域取得了一些臨床進展。這種方法的臨床療效為其抑制PTD 進展帶來了希望。

神經干細胞移植治療原發性扭轉肌張力障礙:一例報告
本研究探討了通過立體定向手術對一名原發性扭轉肌張力障礙患者進行神經干細胞移植的有效性,該患者在手術后4年的隨訪中表現出部分神經功能恢復。據我們所知,這是首次報道神經干細胞移植用于治療原發性扭轉肌張力障礙。
方法:患者的基因檢測顯示扭轉肌張力障礙1 (DYT1) 基因 (907-909delGAG) 存在突變。通過立體定向手術將神經干細胞植入患者雙側蒼白球。
結果:術前,患者的(Burke-Fahn-Marsden)肌張力障礙運動評分(BFMDMS)為21分,術后逐漸下降,術后1、2、3、4年分別降至18、17、15、13分。術后4年,BFMDMS改善了38.1%。盡管計算機斷層掃描和磁共振成像檢查顯示手術前后沒有顯著變化,但術后腦部正電子發射斷層掃描顯示移植區域的葡萄糖代謝增加。神經干細胞移植在該患者中的臨床療效表明其治療原發性扭轉肌張力障礙患者的潛力。
患者選擇
本研究選擇的患者為18歲男性,患有PTD,預產期剖宮產出生,無任何遺傳病家族史,無腦炎、黃疸、腦腫瘤病史或外傷。他在5歲時首次出現左下肢不自主痙攣和扭轉,沒有任何誘發因素。臨床特征從5歲至9歲逐漸擴展到全身。18歲時,患者無法書寫、抓握、站立或行走。他吞咽固體食物有些困難,但沒有癲癇癥狀。患者智力正常。頭部計算機斷層掃描(CT;圖1a)和磁共振成像(MRI;圖2a)提示大腦輕度萎縮。PTD是根據上述數據診斷的。
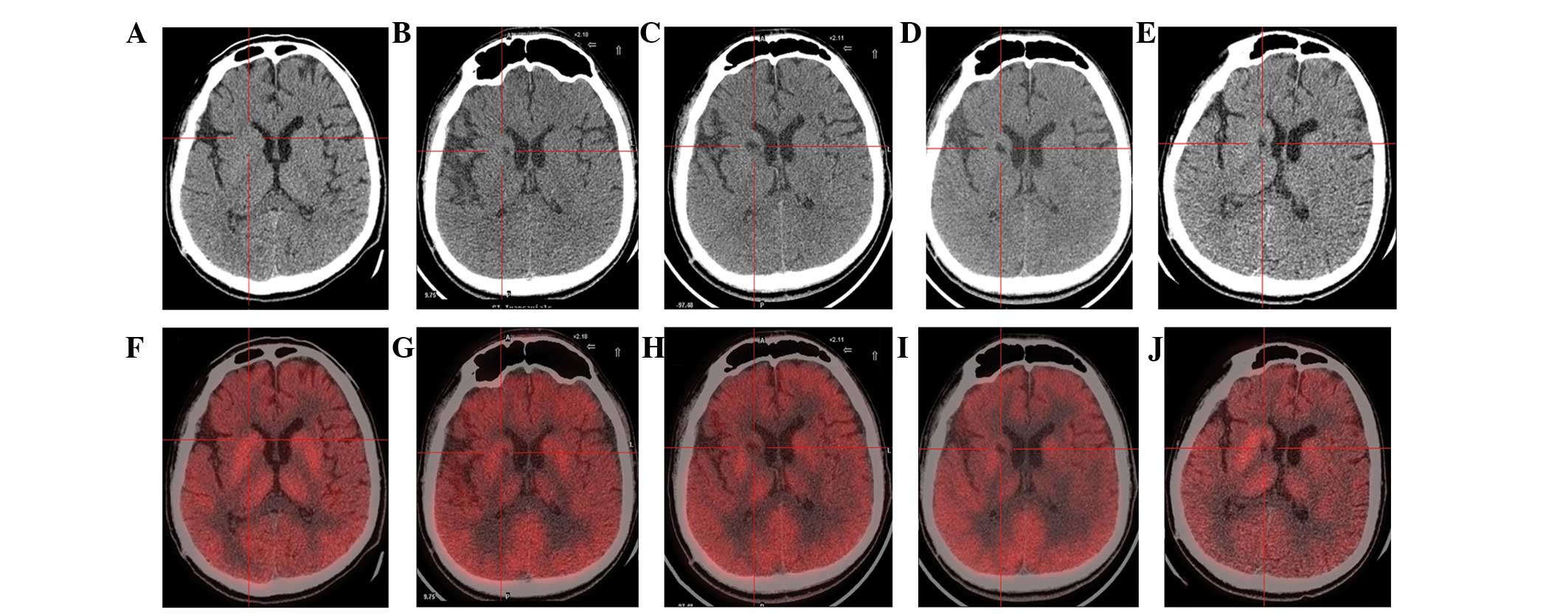
(A) 術前CT顯示腦萎縮。
(BE)術后1年、2年、3年、4年CT與術前相比均無明顯變化。
(F)術前18F-氟脫氧葡萄糖 (FDG) PET 掃描顯示,整個大腦皮層FDG攝取彌漫性減少,細胞核FDG攝取相對高于其他區域。術前1天,豆狀核和丘腦的標準化攝取值 (SUV) 平均值/最大值分別為4.3/5.8和3.3/4.5。
(GJ) 神經干細胞移植治療后分別 1、2、3 和 4 年的 18F-FDG PET 掃描顯示,雙側植入部位的豆狀核和丘腦對 18F-FDG的攝取增加(紅十字)與植入前相同部位進行比較。 豆狀核和丘腦的SUV*平均值/最大值在 1、2、分別是術后3年和4年。 該結果表明移植后葡萄糖代謝比移植前稍高。
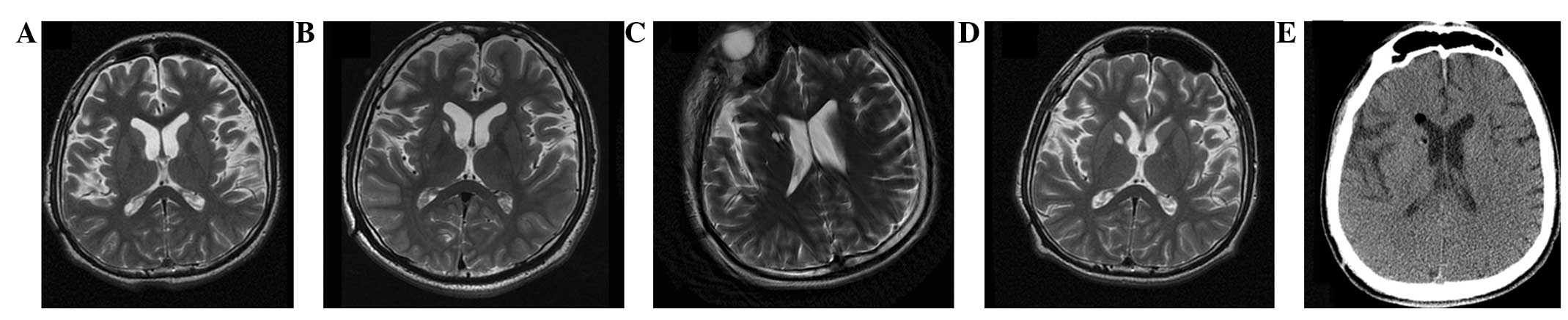
(A) 術前 MRI 顯示腦萎縮。 (BD)術后1年、3年、4年MRI與術前MRI相比無明顯變化。 (E) 術后3天,計算機斷層掃描顯示沒有出血或水腫。
遺傳分析、影像觀察和隨訪
遺傳分析發現患者DYT1 ( TOR1A )第五外顯子存在突變 (907-909 delGAG) 。他對神經外科手術表現出良好的耐受性,并于4點出院。沒有與細胞植入或外科手術相關的嚴重不良事件。POD時的CT掃描顯示沒有出血或水腫(圖2e)。術后1個月,患者的PTD癥狀開始改善。BFMDMS逐漸增加,從術前的21分別增加到術后1、2、3和4年的18、17、15和13,術后4年改善38.1%(表1)。
BFMDMS,Burke-Fahn-Marsden 肌張力障礙運動評分。
CT(圖1b-e)和MRI(圖2b-d)掃描顯示4年隨訪期間沒有顯著變化。 手術前1天(圖1f)和手術后1、2、3和4年(圖1g-j) 獲得18F-FDGPET掃描。術后雙側植入部位豆狀核和丘腦18F-FDG攝取值較術前增加。這一結果表明,自移植以來,葡萄糖代謝逐年略有增加。
討論
作為遺傳性原發性扭轉肌張力障礙最常見和最嚴重的形式之一,DYT1的特點是兒童期發病的進行性肌張力障礙,通常以節段性(主要是手臂或腿部)肌張力障礙開始,隨后普遍化。病理主要表現為基底節尾狀核和殼核小神經細胞變性,蒼白球變性,小腦齒狀核細胞缺失。本研究中,患者的臨床表現與DYT1表型一致,基因檢測結果證實其為DYT1陽性。腦CT和MRI檢查顯示腦萎縮。腦部PET掃描顯示,大腦皮層的葡萄糖代謝普遍下降。總之,這些發現支持上述病理退化模式。
原發性扭轉肌張力障礙的傳統治療包括各種藥物、腦內核損傷和DBS。盡管DBS在一定程度上是有利的,但它無法抑制PTD進展。神經干細胞研究的最新進展使得神經干細胞移植能夠用于治療原發性扭轉肌張力障礙。在某些條件下,神經干細胞可以增殖、遷移并分化為特定位置的神經細胞,以替代局部受損的細胞。通過這些過程,神經干細胞修復異常的神經通路,分泌神經營養因子并保護受損的神經元。
因此,神經干細胞移植可能能夠補充因衰老、損傷或疾病而損失的細胞。由于NSCs的免疫原性較低,移植后的免疫排斥反應非常輕微,為NSCs的存活提供了有利的條件。神經干細胞移植已用于治療成人帕金森病、小腦萎縮和中風后遺癥。神經干細胞在這些情況下的效用為它們用于治療PTD提供了理論基礎。研究人員動員腦室下區的內源性神經干細胞來替代黑質中的多巴胺能細胞,從而恢復紋狀體多巴胺水平并改善帕金森病患者的運動癥狀。
總結
據我們所知,這是第一項使用神經干細胞移植治療原發性扭轉肌張力障礙患者的研究。該患者表現出腦組織惡化,術前CT和MRI掃描顯示腦萎縮,PET掃描顯示腦葡萄糖代謝下降。經過4年的隨訪,患者沒有出現神經干細胞移植引起的并發癥。他的BFMDMS持續下降,在手術后4年內改善了38.1%。NSC治療后1個月內患者病情開始好轉,6個月后病情穩定。移植部位葡萄糖攝取增加,表明NSCs可能在細胞更替和神經通路修復中發揮作用。
在本研究中,NSC移植是使用無框架立體定向手術技術完成的。立體定向手術是一項成熟且可靠的技術,多年來已廣泛應用于神經外科臨床。立體定向手術的使用確保了定位準確且創傷最小。將NSC直接移植到基底神經節附近。NSC治療后患者沒有表現出出血。
神經干細胞移植治療原發性扭轉肌張力障礙患者目前正處于早期臨床探索階段,在成為標準的臨床治療之前仍有一些問題需要解決。
- 首先,神經干細胞的致瘤性仍然是一個主要問題,一些研究已經分析了腫瘤生成的可能性。本研究中的患者在4年的隨訪期間沒有出現任何神經系統腫瘤,但評估NSC治療的安全性需要更長的觀察時間。
- 其次,神經干細胞的免疫排斥是一個相關問題。大多數研究人員認為,由于血腦屏障的完整性和NSC的輕微免疫原性,很少發生免疫排斥反應。本研究中的患者未接受長期免疫抑制治療,NSC移植后未出現免疫排斥反應。
DYT1陽性原發性扭轉肌張力障礙患者的在神經干細胞移植4年后隨訪期內顯示出一定的臨床療效。盡管如此,仍需要對更多患者進行治療評估并進行更長時間的隨訪,以證實結果并確定神經干細胞分化的機制。
參考資料:Ren, W., Yin, F., Zhang, J., Lu, W., Liang, Y., Adlerberth, J., & Tian, Z. (2016). Neural stem cell transplantation for the treatment of primary torsion dystonia: A case report. Experimental and Therapeutic Medicine, 12, 661-666. https://doi.org/10.3892/etm.2016.3392
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加微信
掃碼添加微信