腦性癱瘓(Cerebral Palsy, CP)是兒童期最常見的運動功能障礙性疾病,主要由發育中的腦組織損傷引發,目前尚無根治性療法。傳統康復治療雖能部分改善癥狀,但對神經修復的局限性促使研究者將目光轉向再生醫學領域。
干細胞療法因其潛在的神經再生、抗炎及血管生成能力,成為腦癱治療的新希望。然而,干細胞的異質性(如來源、分化潛能及免疫特性)導致不同細胞類型在臨床應用中的安全性差異顯著。
本文基于近些年的臨床研究數據,系統對比間充質干細胞(MSCs)、神經干細胞(NSCs)、臍帶血干細胞(UCB)?等主流細胞類型在腦癱患者治療中的安全性差異,旨在為臨床選擇提供循證依據,并探討未來優化方向。

干細胞治療腦癱:臍帶血、間充質干細胞與神經干細胞哪個更安全?
一、間充質干細胞治療腦癱患者
間充質干細胞(MSCs)是目前腦癱治療中研究最廣泛、安全性數據最充分的干細胞類型,主要包括骨髓、脂肪和臍帶間充質干細胞。
1.1 臍帶間充質干細胞治療腦癱的安全性
臍帶間充質干細胞(UC-MSCs)來源廣泛、免疫調節能力強,其安全性表現突出:
2021年,伊朗德黑蘭醫科大學在行業期刊《干細胞研究與治療》上發表了一篇關于《臍帶組織間充質干細胞鞘內注射治療腦癱的臨床及影像學結果:一項隨機雙盲假手術對照臨床試驗》的臨床結果。

該研究納入了72名腦癱參與者進行分析。從基線到干預后12個月,在參與者中發現了5起不良事件。UCT-MSC組中有2 例(2/36或5.5%)在鞘內細胞注射后24小時內出現發燒(38至38.7o?C),但自行緩解,且未診斷出感染(例如腦膜炎)。其他術后24小時內報告的不良事件包括:
- 輕度至中度煩躁:對照組3例(8.3%),UCT-MSC組6例(16.7%);
- 頭痛:對照組1例(2.8%),UCT-MSC組5例(13.9%);
所有癥狀均未發展為嚴重不良事件(SAE),且通過對癥處理后完全緩解。隨訪期間未發現與治療相關的長期并發癥。
1.2 脂肪間充質干細胞治療腦癱的安全性
2012年,東京干細胞研究所在期刊《Journal of Medical Research》上發表了一篇關于《自體人脂肪組織衍生的間充質干細胞治療腦癱:病例報告》的臨床研究成果。

患者在自體脂肪間充質干細胞靜脈輸注期間在靜脈輸注過程中及24小時內未出現發熱、過敏反應或其他急性不良事件,此外后續隨訪期內(隨訪時長未明確)未報告與干細胞輸注相關的慢性毒性、免疫排斥或神經系統并發癥。
局限性:作為單例病例報告,樣本量過小,無法通過統計學方法驗證安全性,患者需謹慎考慮。
1.3 骨髓間充質干細胞治療腦癱的安全性
?2016年,國際干細胞雜志上發表了一篇關于《干細胞治療腦癱17例報告》的臨床研究結果。該研究對17名患有腦性癱瘓 (CP) 的患者進行了骨髓間充質干細胞的治療。

研究報告的不良事件(圖1)僅限于輕度頭痛(2例,占12%)、短暫性發熱(1例,占6%)或嘔吐(2例,占12%),或未報告任何不良事件(12例,占70%)。所有副作用均在幾天內消退。未發現癲癇發作、躁動、腦膜炎、注射部位疼痛或其他嚴重事件的報告。

二、神經干細胞移植治療腦癱患者
神經干細胞(NSCs)因具備定向分化為神經細胞的潛力,成為腦癱治療的重要研究方向。
2.1 鼻內給藥革新降低風險
我國科研人員首創的NSCs鼻腔貼片技術有效突破了血腦屏障的限制,為非侵入性干細胞治療中樞神經系統疾病提供了新的途徑,減少侵入性操作風險,為腦癱治療帶來了新的希望。其臨床結果在2024年發表在國際知名期刊《frontiers》上。

安全性:本次研究22例腦癱患兒住院及隨訪期間,患兒均未出現免疫排斥相關不良反應,但1例患兒鎮靜后出現頭暈、惡心、嘔吐等癥狀。3例患兒出現少量鼻黏膜出血,2例患兒在移植后24 h內及2 d內體溫升高(≤38.5 ℃)。所有患兒均未出現畏寒及全身感染。1例患兒有復雜部分性癲癇(CPS)病史,其類型及發作頻率在接受NSC治療3個月后發生改變。(見圖2)

研究表明,所有患兒未出現免疫排斥或嚴重不良事件(SAE),僅少數出現鼻黏膜出血、鎮靜后短暫不適及低熱,且均通過對癥處理緩解,表明該技術具備良好的耐受性。
2.2 鞘內注射的潛在風險
2013年,武警總醫院在國際期刊《轉化醫學雜志》上發表了一篇關于《自體骨髓間充質干細胞來源的神經干細胞樣細胞用于治療腦癱患者》的臨床研究結果。

本次研究在鞘內注射(腰椎穿刺)前患者禁食禁水。采集骨髓前根據劑量和用法給患者注射苯巴比妥鈉、阿托品和氯胺酮。待患者睡著后,將局麻藥浸潤皮下,將脊椎穿刺針插入腰椎L3/L4或L4/L5之間,推進直至穿刺針穿過硬腦膜和薄蛛網膜進入蛛網膜下腔。
安全性:本研究中的所有患者在治療后均接受了超過6個月的觀察。60名患者均未出現與實驗操作相關的發燒、頭痛、異常性疼痛、嘔吐或其他嚴重不良事件。后續MRI評估未顯示任何可能提示不良事件的顯著解剖或結構變化。未發現任何新的缺血性、出血性或腫瘤性病變的證據。
然而,一名患者報告哭鬧頻率增加,但在治療后2天自行緩解,無需任何干預。對照組和移植組還評估了其他可能的不良反應或并發癥,但兩組間新發疾病的發生率無差異。
2.3 兩種技術的安全性對比
綜上所述,神經干細胞(NSCs)治療腦癱的兩種給藥途徑各具特點:
- 鼻腔貼片技術通過非侵入性方式突破血腦屏障,顯著降低傳統侵入性操作風險,安全性良好。在22例患兒中,僅出現輕微不良反應(如鼻黏膜出血、短暫不適及低熱),未發生免疫排斥或嚴重并發癥,且與康復治療結合可改善神經功能。
- 而鞘內注射(腰椎穿刺)雖需侵入性操作,但通過精準給藥實現了局部高濃度細胞分布,60例患者未出現嚴重不良事件,MRI評估顯示安全性可靠,但依賴專業操作且可能引發短暫不適(如哭鬧增多)。
兩種技術均驗證了NSCs治療腦癱的安全性,鼻腔途徑以低風險、易操作為優勢,適合兒童及需多次治療的患者;鞘內注射則以精準性為特點,適用于復雜病例。未來需進一步優化技術(如鼻腔貼片的靶向性、鞘內注射的鎮靜方案),并探索長期療效及聯合治療策略,以推動腦癱治療的個體化發展。
三、臍帶血干細胞治療腦癱患者
臍帶血干細胞(UCBSCs)富含多能祖細胞,臨床應用中分為自體移植和異體移植兩種方式。其中,自體臍帶血干細胞移植因來源與受體基因完全一致,可避免免疫排斥反應,安全性較高,而異體輸注則需警惕免疫相關風險:
2015年,廣東省中醫院在國際期刊《Stem Cells International》上發表了一篇關于《異基因臍帶血干細胞治療重度腦癱患者的安全性:一項回顧性研究》的臨床研究成果。

安全性:異基因UCBSCs輸注后不良事件發生頻率的分析表明存在一些非致命性不良事件。在最初的靜脈輸注中沒有不良事件。所有不良事件均發生在鞘內注射的休息期間。47名患者中有26名(55.3%)報告了不良事件,但未發生人員傷亡。發熱和嘔吐是最常見的不良事件,發生率分別為42.6%和21.2%。
此外在出院后的第一個月、第二個月和第六個月通過電話或電子郵件對每位患者進行隨訪。隨訪6個月,47例患者共發生15例不良事件,包括上呼吸道感染7例、腹瀉4例、發熱3例、癲癇發作1例,但沒有證據表明這些常見疾病與細胞移植治療。所有患者均未出現嚴重不良事件。(見圖3)
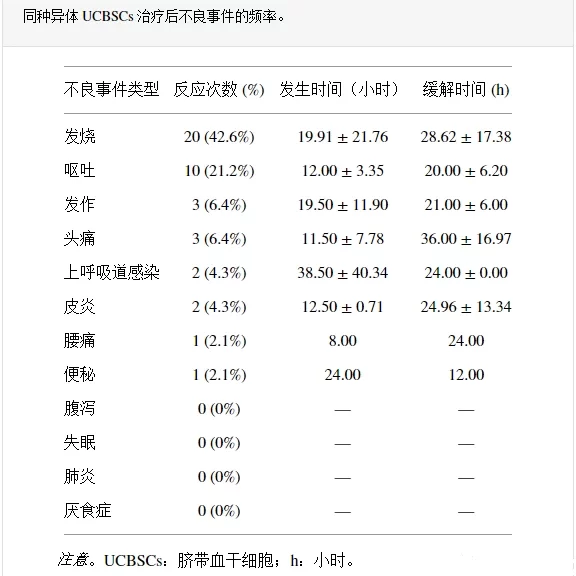
四、安全性對比總結
目前用于腦癱治療的干細胞療法中,間充質干細胞(MSCs)和神經干細胞(NSCs)均展現出良好的安全性。
- 臍帶間充質干細胞通過鞘內注射治療的臨床試驗顯示,不良事件以輕度發熱、煩躁、頭痛為主,均未發展為嚴重事件;
- 脂肪間充質干細胞的單例研究未報告不良反應,但需更大樣本驗證;
- 骨髓間充質干細胞治療僅出現短暫頭痛、發熱等輕微癥狀。
- 神經干細胞的鼻腔貼片技術(22例)以零侵入性操作實現低風險,僅鼻黏膜出血、低熱等局部反應,而鞘內注射僅1例短暫哭鬧,MRI未見結構異常。
- 異體臍帶血干細胞輸注雖55.3%患者出現發熱、嘔吐等AE,但均為非致命性且無免疫排斥。
總體而言,所有療法未引發嚴重并發癥,不良事件可控且可通過對癥處理緩解。不同干細胞類型及給藥途徑各有特點:臍帶/脂肪來源MSCs安全性高且來源廣泛,鼻腔NSCs貼片以低侵入性優勢適合兒童,鞘內注射需權衡精準性與操作風險,異體UCBSCs需警惕免疫風險但未觀察到嚴重事件。這些進展為腦癱患者提供了個性化治療選擇,但需結合患者年齡、病情及醫療條件優化方案,并通過標準化流程推動臨床轉化。
結語
干細胞治療為腦癱患兒帶來了修復神經損傷的希望,但其安全性與療效的實現需基于細胞類型、給藥方式及個體差異的精準匹配。目前,臍帶間充質干細胞的非侵入性給藥、鼻內神經干細胞移植的低風險技術已成為臨床主流選擇,而異體UCBSCs及鞘內NSCs需通過個體化評估與規范操作規避風險。
未來,隨著技術優化與長期數據的積累,干細胞治療有望為腦癱患者提供更安全、持久的神經修復方案。患者及家屬應理性看待技術潛力,在專業團隊指導下權衡利弊,避免盲目追求“一勞永逸”的療效,而是通過科學、漸進的治療路徑為患兒爭取最佳康復機會。
相關閱讀:自體vs異體:不同來源的干細胞治療腦癱患者的安全性有區別嗎?
參考資料:
Amanat, M., Majmaa, A., Zarrabi, M.?et al.?Clinical and imaging outcomes after intrathecal injection of umbilical cord tissue mesenchymal stem cells in cerebral palsy: a randomized double-blind sham-controlled clinical trial.?Stem Cell Res Ther?12, 439 (2021). https://doi.org/10.1186/s13287-021-02513-4
Please Cite this Article at: Jeong Chan Ra, Journal of Medical Research, 1 (1), Nov- Dec 2012, 01-09
DOI:https ://doi.org/10.15283/ijsc.2016.9.1.90
Li Xiaoyan , Li Mengyao , Qin Xixian , Li Ying , Wang Yachen , Han Chao , Ni Shiwei , Sun Xuna , Dong Peipei , Liu JingProviding holistic care to children with cerebral palsy treated with transnasal neural stem cell transplantationFrontiers in PediatricsVolume 11 – 20232024https://www.frontiersin.org/journals/pediatrics/articles/10.3389/fped.2023.1297563
Chen, G., Wang, Y., Xu, Z.?et al.?Neural stem cell-like cells derived from autologous bone mesenchymal stem cells for the treatment of patients with cerebral palsy.?J Transl Med?11, 21 (2013). https://doi.org/10.1186/1479-5876-11-21
Feng,?Mei,?Lu,?Aili,?Gao,?Hongxia,?Qian,?Caiwen,?Zhang,?Jun,?Lin,?Tongxiang,?Zhao,?Yuanqi,?Safety of Allogeneic Umbilical Cord Blood Stem Cells Therapy in Patients with Severe Cerebral Palsy: A Retrospective Study,?Stem Cells International,?2015, 325652, 7 pages,?2015.?https://doi.org/10.1155/2015/325652
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加微信
掃碼添加微信