腦癱(Cerebral Palsy, CP)作為兒童期最常見的運動功能障礙性疾病,主要由圍產期腦損傷引發,全球發病率約為1.5%-4%。傳統康復手段如物理治療、肉毒素注射等雖能部分緩解癥狀,但難以逆轉神經結構性損傷。近年來,以干細胞為核心的再生醫學療法,憑借其神經修復、免疫調節與血管再生的多維度干預機制,為腦癱治療開辟了新路徑。
本文將從病理分型角度,系統探討干細胞在各種類型腦癱中的治療原理與研究進展,以期為臨床轉化提供理論依據。

從痙攣到共濟失調:干細胞可以治療哪些類型的腦癱患者?
一、按運動障礙類型分類的適用性
1.1 痙攣型腦癱
定義:痙攣型腦癱是最常見的類型,約占腦癱患者的70%,主要表現為肌肉僵硬、運動受限,尤其是下肢痙攣導致行走困難。其病理機制與皮質脊髓束損傷、神經元死亡及炎癥反應相關。
2021年,伊朗德黑蘭科研人員在行業期刊《干細胞研究與治療》上發表了一篇關于《臍帶組織間充質干細胞鞘內注射治療腦癱的臨床及影像學結果:一項隨機雙盲假手術對照臨床試驗》的研究成果。
本研究評估了臍帶組織間充質干細胞(UCT-MSC)鞘內注射治療患有痙攣性腦性癱瘓的安全性和有效性。

經過12個月的UCT-MSC治療,實驗組在運動功能、日常生活能力及生活質量方面均顯著優于基線組和對照組:
- 運動功能方面,GMFM-66評分較基線組提升10.65分,較對照組差異達8.07分,且MAS痙攣評分降低1.0分,提示粗大運動能力和肌張力顯著改善;
- 日常生活能力顯著提升,PEDI總評分較基線提高8.53分,較對照組差異達6.87分;
- 生活質量中,CP-QoL量表顯示“社交互動”“活動參與”等領域的改善程度顯著優于對照組;
- 影像學驗證顯示,實驗組白質完整性顯著修復:皮質脊髓束(CST)和皮質投射纖維(PTR)的FA值分別增加0.032和0.024,MD值分別降低0.035×10?3和0.045×10?3,均顯著優于對照組。
這些結果表明,UCT-MSC通過促進神經結構修復與功能重建,為痙攣型腦癱患兒提供了顯著且多維度的臨床獲益。
1.2 運動障礙型腦癱
定義:以不自主運動或肌張力波動為特征,約占腦癱的10%-20%。患者表現為舞蹈樣動作、手足徐動或震顫,常因基底節或錐體外系損傷導致神經遞質失衡(如多巴胺、乙酰膽堿異常)。
2013年,武警總醫院曾在國際期刊《轉化醫學雜志》上發表了一篇關于《自體骨髓間充質干細胞來源的神經干細胞樣細胞用于治療腦癱患者》的臨床研究結果。

本研究于2010年6月至2011年6月入選60例運動功能嚴重受限的運動障礙型腦癱患兒,粗大運動功能分類系統平均Ⅲ-Ⅴ級。
經6個月隨訪,臍帶間充質干細胞移植組在粗大運動功能改善方面呈現顯著療效:
- 運動功能提升:治療后3個月,粗大運動功能測量評分較基線顯著提高42.6分;6個月時進一步增至58.6分,均顯著優于對照組。
- 語言功能:兩組在治療后1、3、6個月的語言商評分均未見顯著提升。
- 安全性:全部60名患者存活,且無嚴重不良事件或治療相關并發癥發生,證實該療法的安全性。
研究表明,神經干細胞移植可顯著改善運動障礙型腦癱腦癱患兒的粗大運動功能,且在6個月內未觀察到嚴重不良反應,為該療法的臨床應用提供了有效性和安全性的支持證據。
1.3 共濟失調型腦癱
定義:以協調功能障礙和平衡失調為主,約占5%-10%。患者步態不穩、動作笨拙,多因小腦或小腦通路損傷導致運動協調能力受損。
2012年,解放軍干細胞治療中心牽頭在《中國組織工程研究》上發表了一篇關于《臍血干細胞聯合神經生長因子和物理康復治療小兒腦性癱瘓》的臨床研究成果。本次研究納入了共濟失調型腦癱患兒5例。

臍血干細胞聯合鼠神經生長因子及物理康復治療顯著改善腦癱患兒的粗大運動功能:治療后3個月,臍血干細胞組與常規治療組(僅神經生長因子+康復)的GMFM量表A、B、D能區評分均較基線顯著提升,且臍血干細胞組A、B能區評分顯著高于常規治療組;對照組(未治療)評分無變化。
研究證實,臍血干細胞聯合療法在改善共濟失調型腦癱患兒運動功能(尤其姿勢控制與移動能力)方面優于單純神經生長因子聯合康復治療,為腦癱患兒提供了更有效的干預方案。
1.4 混合型腦癱
定義:混合型腦癱指患者同時具備兩種或以上運動障礙類型的臨床表現(如痙攣型與運動障礙型并存),約占腦癱患者的10%-15%。其病理機制復雜,可能涉及多腦區損傷(如皮質脊髓束、基底節及小腦聯合損傷),導致肌張力異常、不自主運動及協調功能障礙并存。
2018年,土耳其伊斯坦布爾伊斯坦尼耶大學在國際期刊《國際干細胞雜志》上發表了一篇關于《臍帶間充質干細胞移植治療腦癱患者療效觀察:病例報告》的臨床研究成果。
本次研究是納入了一名6歲混合型男性腦癱患兒,患者同時患有肌張力障礙型和痙攣型,接受4次1×106/kg臍帶間充質干細胞(UC-MSCs)鞘內及靜脈注射治療。

經干細胞治療后,患者通過軀干控制測量量表(TCMS)評估的坐姿平衡與功能獨立性顯著改善:
- 靜態坐姿平衡從2/20提升至10/20,表明患者在無外部支持下維持穩定坐姿的能力大幅增強(初始幾乎無法獨立坐立,治療后顯著改善);
- 選擇性運動控制從2/28增至17/28,提示軀干精細運動的精準性顯著提升(能夠更獨立地控制軀干運動,減少多余動作);
- 平衡反應從1/10提高至4/10,雖仍處于較低水平,但對外界干擾的動態平衡調節能力有所恢復;
- 總成績從5/58躍升至31/58,綜合反映了軀干控制能力、坐姿穩定性和運動協調性的全面進步。
這些結果表明,干細胞治療通過改善核心肌群控制與平衡功能,顯著提升了混合型腦癱患兒的坐姿功能獨立性及生活質量。
二、按病因分類的針對性干預
2.1 缺氧缺血性腦損傷(HIE)相關腦癱
定義:由圍產期缺氧缺血(如胎兒窘迫、新生兒窒息)引發的腦損傷,導致腦組織壞死、神經元凋亡及膠質瘢痕形成。
2023年,國內三甲醫院在國際期刊《Stem Cell Research & Therapy》上發表了一篇關于《腦癱患者鼻腔內注射神經干細胞的安全性和有效性結果:一項隨機1/2期對照試驗》的研究成果。
研究中納入了24例腦癱患者,入選受試者年齡3至12歲,臨床表現為中度至重度癱瘓,以缺血缺氧誘發的痙攣性腦性癱瘓為特征。

本研究通過基線與24個月終點數據對比發現,接受神經干細胞(NSCs)鼻腔注射的治療組在多項功能評估中顯著優于對照組。
- 治療組在自理能力(ADL量表)和粗大運動功能(GMFM-88量表)方面改善尤為顯著,且部分指標(如站立、步行/跑步/跳躍)在治療后1個月內即出現統計學意義的進步;
- 至3個月時,表達能力與粗大運動整體功能進一步提升;
- 6個月時社交技能增強,且前期改善得以維持。盡管精細運動(FMFS)、部分GMFM-88子項(如B部分)及社交技能(SS、LAS、EAS)的改善未達統計學意義,但整體趨勢積極。
- 此外,治療組睡眠質量(SDSC評分)改善而對照組無變化。
- 值得注意的是,復雜的手部精細動作功能在24個月后才顯現顯著改善,提示NSCs對不同功能的干預存在時間梯度差異,且療效呈現持續性和穩定性。
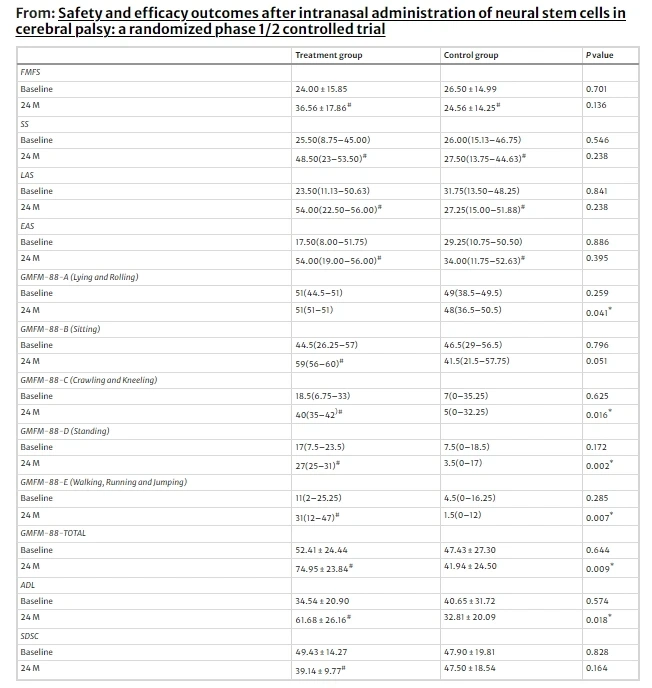
綜上所述,本研究表明,鼻腔內施用NSCs復合貼劑是一種安全有效的治療方法,它能夠在保持腦癱患者長期安全性的情況下,顯著提高缺血缺氧誘發的痙攣性腦癱患兒的生活質量和運動功能,特別是在早期粗大運動能力的恢復方面具有特別的優勢。
2.2 早產兒腦白質損傷(WMI)相關腦癱
定義:因早產兒腦白質發育不成熟,易受缺氧、感染或機械通氣損傷,導致白質軟化、髓鞘形成障礙及神經傳導異常。
2017年,越南科研人員在國際期刊《BMC Pediatrics》上發表了一篇關于《自體骨髓單核細胞治療腦癱的療效:一項開放標簽非對照臨床試驗》的臨床研究成果。
本研究對40名2至15歲腦癱患者進行了一項開放標簽、非對照臨床試驗。腦癱嚴重程度如下:III 級 2 名(5%),IV 級 14 名(35%),V 級 24 名(60%)。其中納入最常見的三種腦癱患兒類型是:基底神經節損傷、皮質/皮質下損傷和腦室周圍白質損傷腦癱患兒。

本研究顯示,自體骨髓單核細胞移植在腦癱患兒中具有顯著療效與安全性:
- 治療后3–6個月,患者粗大運動功能(GMFM-88總分及各維度評分、GMFM-66百分位數均顯著提升)、肌肉痙攣程度均顯著改善,且療效不受性別、年齡或基線GMFCS分級影響;
- 安全性方面,僅12例出現一過性非感染性發熱、9例輕微嘔吐(藥物可控制),無嚴重并發癥發生,證實該療法安全有效且具有廣泛適用性。
研究表明,自體骨髓單核細胞移植在改善腦室周圍白質損傷腦癱患兒運動功能、緩解痙攣及安全性方面表現突出,且療效不受患者基線特征限制,為該療法的臨床推廣提供了重要依據。
三、治療窗口期與療效差異
最佳干預時間:嬰幼兒期(2-6歲)腦組織可塑性強,干細胞易遷移至損傷區域。
療效影響因素:
- 損傷范圍:局灶性損傷比彌漫性損傷更易靶向;
- 并發癥:合并癲癇或嚴重認知障礙者需謹慎評估。
相關閱讀:為何兒童更受益?解析年齡對干細胞治療腦癱的核心影響
四、挑戰與未來方向
- 精準分型治療:需結合基因檢測和影像學定位,匹配最佳干細胞類型(如MSCs適用于炎癥環境,NSCs適于神經元替代)。
- 遞送技術優化:納米材料介導的干細胞靶向遞送或可提高病灶區域駐留率。
- 長期安全性:大規模臨床試驗仍需跟蹤致瘤性和免疫排斥風險。
結語
腦癱作為兒童運動功能障礙的常見病因,傳統療法難以修復神經損傷。干細胞治療憑借其多向分化與再生修復能力,為不同類型及病因的腦癱患兒提供了突破性方案:通過改善神經結構、調節遞質失衡、促進血管新生等機制,顯著提升運動功能與生活質量(如GMFM評分顯著提高),且安全性良好。盡管療效存在個體差異,但其臨床潛力已獲驗證,未來需進一步優化精準分型、靶向遞送技術及長期安全性監測,以推動神經再生醫學向更精準、長效方向發展,為腦癱患兒帶來更優治療選擇。
相關閱讀:低劑量VS高劑量:不同劑量的干細胞治療腦癱哪個更加安全?
參考資料:
Amanat, M., Majmaa, A., Zarrabi, M. et al. Clinical and imaging outcomes after intrathecal injection of umbilical cord tissue mesenchymal stem cells in cerebral palsy: a randomized double-blind sham-controlled clinical trial. Stem Cell Res Ther 12, 439 (2021). https://doi.org/10.1186/s13287-021-02513-4
Chen, G., Wang, Y., Xu, Z. et al. Neural stem cell-like cells derived from autologous bone mesenchymal stem cells for the treatment of patients with cerebral palsy. J Transl Med 11, 21 (2013). https://doi.org/10.1186/1479-5876-11-21
邢利和,張麗欣,張麗麗,孫麗芳,董燕慧,劉 影,郭立杰. 臍血干細胞聯合神經生長因子和物理康復治療小兒腦性癱瘓[J]. 中國組織工程研究, 2012, 16(41): 7777-7781.
https://synapse.koreamed.org/articles/1159131
Lv, Z., Li, Y., Wang, Y. et al. Safety and efficacy outcomes after intranasal administration of neural stem cells in cerebral palsy: a randomized phase 1/2 controlled trial. Stem Cell Res Ther 14, 23 (2023). https://doi.org/10.1186/s13287-022-03234-y
Nguyen, L.T., Nguyen, A.T., Vu, C.D. et al. Outcomes of autologous bone marrow mononuclear cells for cerebral palsy: an open label uncontrolled clinical trial. BMC Pediatr 17, 104 (2017). https://doi.org/10.1186/s12887-017-0859-z
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加微信
掃碼添加微信