小兒腦性癱瘓(Cerebral Palsy,CP ),簡稱腦癱。是一組由出生前或分娩過程中腦損傷引發的非進行性中樞神經系統障礙,主要表現為運動功能障礙、肌肉張力異常及協調能力受損,常伴隨智力缺陷、癲癇、行為異常、視聽語言障礙等多系統并發癥,是全球兒童常見致殘性疾病之一。
在全球范圍內,腦癱的發病率大約為每1000名兒童中有2到3人被確診患有這種疾病。然而,不同地區的具體患病率有所差異,例如在中國,《中國實用兒科臨床雜志》上一項針對12個省市的研究顯示,中國腦癱的發病率為2.48%,而在1-6歲的兒童中,患病率為2.46%。
該疾病不僅造成患兒終身護理需求(需24小時看護、長期康復訓練及持續醫療支出),還可能因部分患兒在出生后數周死亡或壽命縮短至8-9歲而加劇家庭經濟與心理壓力。
腦癱這種疾病的治療是很復雜的,通常都是以對癥康復為主,幫助患兒改善運動功能,比如說進行物理療法、康復訓練、藥物治療和手術治療等,但是治療的效果都不是很理想。但近年來,間充質干細胞移植治療在神經系統疾病取得了令人鼓舞的進展,許多針對腦癱的臨床研究項目也取得了階段性成果。
接下來本文結合近年臨床研究及案例,系統闡述間充質干細胞治療腦癱核心機制以及臨床療效證據。

間充質干細胞治療腦癱療效如何?249例患者告訴你答案
一、間充質干細胞:生物醫學的 “多面手”
間充質干細胞(MSC)是一類具有自我更新和多向分化潛能的成體干細胞,廣泛存在于骨髓、脂肪、臍帶、胎盤等多種組織中 。正是由于其來源廣泛、易于獲取和體外擴增的特性,使其成為干細胞研究和臨床應用的熱點。在治療腦癱的過程中,間充質干細胞發揮著 “多重角色”。?
- 從分化能力來看,間充質干細胞具備向神經細胞分化的潛力。當將其移植到受損的腦組織后,在特定的微環境誘導下,間充質干細胞能夠分化為神經元、神經膠質細胞等,補充因損傷而缺失的神經細胞,修復受損的神經通路。
- 此外,間充質干細胞強大的免疫調節和抗炎能力也在腦癱治療中發揮關鍵作用。腦癱患者腦部受損后,局部會發生炎癥反應,炎癥因子的持續釋放會進一步加重神經細胞的損傷。而間充質干細胞能夠通過分泌多種細胞因子,如轉化生長因子 -β(TGF-β)、白細胞介素 – 10(IL-10)等,調節免疫細胞的功能,抑制炎癥反應,減輕腦部組織的二次損傷,為神經修復創造有利的微環境。?
- 同時,間充質干細胞還具有旁分泌作用。它可以分泌大量的生物活性分子,包括神經營養因子(如腦源性神經營養因子 BDNF、神經生長因子 NGF)、血管內皮生長因子(VEGF)等。這些因子能夠促進內源性神經干細胞的增殖和分化,刺激神經細胞的存活、生長和突觸形成,同時還能促進腦部血管的新生,改善腦部的血液循環,為受損神經組織提供充足的營養和氧氣,加速神經功能的恢復。
二、臨床療效:多維度功能改善
2.1 臍帶間充質干細胞治療腦癱患者
2020年,南方醫科大學附屬東莞市人民醫院在《Stem Cells International》上發表了一篇關于《人類間充質干細胞移植治療腦癱的證據:隨機對照試驗的薈萃分析》的研究成果。

本分析納入4項研究,共189名受試者,研究均采用臍帶間充質干細胞(hUC-MSC)治療。結果顯示:
1.粗大運動功能(GMFM)評分:治療組在3個月、6個月和12個月時均顯著高于對照組,整體加權效應值達1.10,表明hMSC治療對腦癱患兒粗大運動功能有持續改善作用。(見圖1)
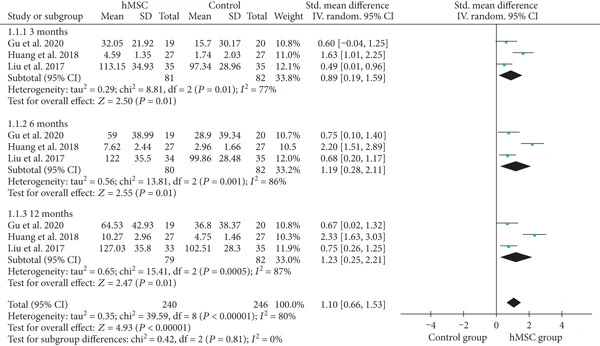
2.綜合功能評估(CFA):2項RCT研究的CFA評分分析同樣顯示:治療組3個月和6個月時CFA評分均顯著優于對照組,加權效應值為1.30,提示hMSC治療對整體功能恢復具有積極作用。(見圖2)
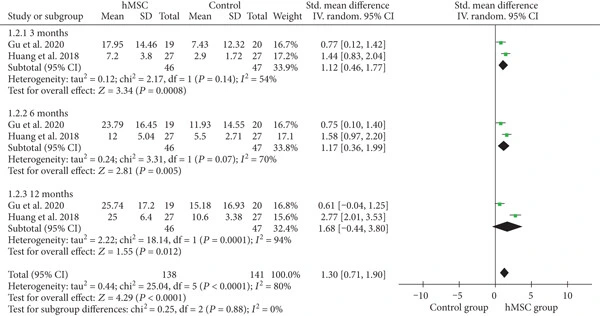
安全性評估:不良事件(AE)的meta分析表明治療組與對照組無顯著差異。
綜上所述,臍帶間充質干細胞療法在改善腦癱患兒運動功能(GMFM/CFA評分)方面效果顯著且安全性良好,為臨床應用提供了可靠依據。
2.2 臍帶間充質干細胞治療腦癱兒童安全性和有效性的進一步證據
同年,根據《干細胞研究與治療》報道,我國研究團隊開展的研究,通過隨機、雙盲、安慰劑對照試驗為人臍帶間充質干細胞治療腦癱的安全性和有效性進一步提供證據。

本次研究工納入了40例腦癱患者,其中1名患者在未接受任何治療的情況下撤回知情同意并失訪。因此,39名患者完成了所有研究評估。最后一名患者的最后一次訪視于2018年2月完成。研究發現:
ADL(日常生活能力)評分和CFA(精細動作功能)評分在3個月隨訪時hUC-MSC組較對照組改善更顯著。(見圖3)
斷層掃描/計算機斷層掃描評估腦代謝活動:發現相比于對照組,間充質干細胞治療組中五分之三的患者在3個月中觀察到葡萄糖標準攝取值顯著增加,較基線提升超過50%。這表明腦糖代謝的改善可能在間充質干細胞移植誘導的功能改善中起到重要作用。

綜上所述,hUC-MSC治療可顯著改善腦癱患者的功能障礙,并揭示其作用機制可能與腦代謝活性的增強相關,為干細胞治療腦癱提供了新的治療方向和循證依據。
2.3 脂肪間充質干細胞移植治療五例腦癱兒童療效觀察
2022年3月1日,贛南干細胞臨床研究中心牽頭在國際期刊《美國轉化醫學雜志》上發表了一篇關于《脂肪間充質干細胞移植治療腦癱五例療效觀察:病例報告》的研究成果。

共5名腦癱患者在常規體格檢查后,每14天靜脈輸注一次脂肪間充質干細胞(ADMSC),3次輸注為1個療程。同時進行常規康復訓練,并隨訪6個月至1年。
治療后,兒童粗大運動功能量表(GMFM-88)、腦癱兒童綜合功能評估量表和精細運動功能量表(FMFM)的評分均得到改善。1名既往有結核性胸膜炎病史的受試者在治療期間復發,但經過適當的醫療干預后癥狀消失。其余4名受試者的常規血液參數均正常。(見圖4、5)
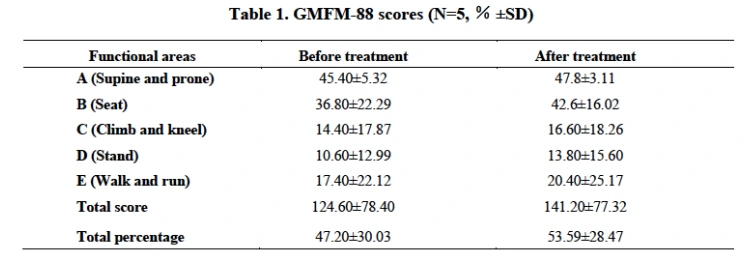
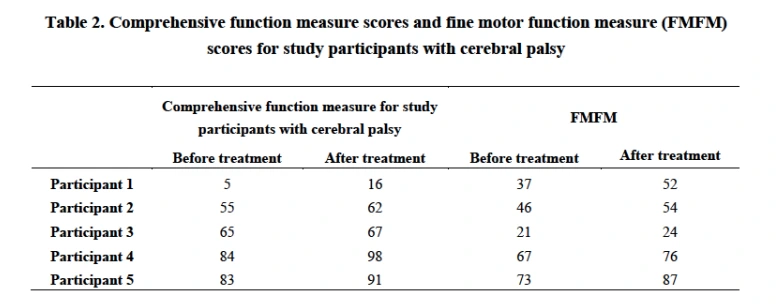
綜上所述,研究表明靜脈注射ADMSCs后,腦癱兒童的運動功能和言語功能得到改善,尤其是重度腦癱兒童。沒有觀察到明顯的安全性問題。
2.4 骨髓間充質干細胞多次注射治療腦癱患者的療效
2025年,伊朗德黑蘭科研人員在國際期刊《神經修復學雜志》上發表了一篇關于《反復鞘內注射自體骨髓間充質干細胞治療痙攣性腦癱:單組安全性和初步療效臨床試驗》的臨床研究結果。

本研究對16名2至12歲痙攣型腦性癱瘓(CP)患兒進行了一項前瞻性、單組、開放標簽的I期臨床試驗。患者接受4次鞘內MSC注射,每次間隔一個月。研究結果發現:
1.運動功能改善(GMFCS分級):
12個月隨訪中,50%(8/16)患者GMFCS分級提升。
具體而言,GMFCS II 級患者比例從6.2%上升至18.75%,III 級患者比例從12.5%上升至18.75%。GMFCS V級患者比例從62.5%下降至43.75%。總體比例變化具有統計學意義,表明參與者的運動功能得到了顯著改善。所有IV級和III級患者以及30%的V級患者的GMFCS分級均有所改善。(見圖6)
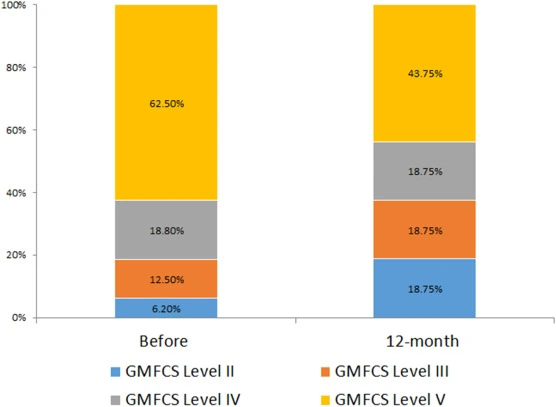
2.粗大運動功能(GMFM-88評分):
12個月后總分顯著提高,各領域均改善。平均從47.01±21.45提高至54.69±22.62。
具體來說,躺著從70.47提升到81.37;坐著從56.77提升到67.92;爬行/站立/行走,分別提升7.6%、6.7%、3.8%。這些結果表明,干預后運動能力有統計學上顯著的提高。(見圖7)
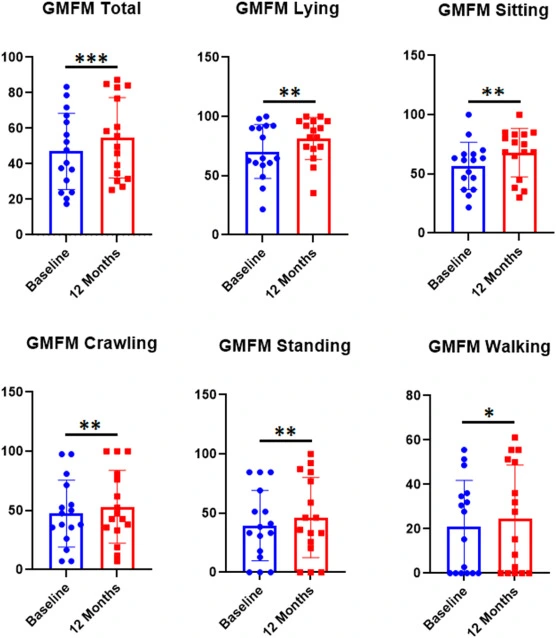
3.平衡與痙攣控制(BBS&MAS)
治療后12個月,BBS評分從平均值6.75提高至9.88,表明參與者的平衡能力和穩定性得到了增強。通過MAS評估,肌肉痙攣明顯減少,平均評分從2.25降至1.62,表明肌肉緊張度降低,運動控制改善。(見圖8)
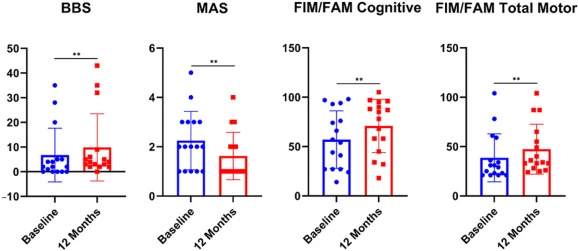
4.功能獨立性(FIM/FAM)
使用FIM/FAM評估功能獨立性。運動分量表得分從38.63提高至47.44,提示運動獨立性有所提高。認知分量表得分也顯著提高,從57.06提高至70.88,提示干細胞治療后認知功能有所改善。(見圖8)
綜上所述,這些結果表明,MSC療法可改善功能結局和生活質量,并且反復鞘內注射自體MSC是安全的,能夠顯著改善痙攣型腦性癱瘓患兒的運動功能、平衡能力和痙攣狀態。
三、間充質干細胞治療腦癱療效總結
綜上所述,間充質干細胞(MSCs)治療腦癱在運動功能、平衡能力、痙攣控制及認知功能等方面均展現出顯著療效,且安全性良好。
臍帶間充質干細胞(hUC-MSC)的薈萃分析顯示,治療組在粗大運動功能(GMFM)和綜合功能評估(CFA)評分上持續優于對照組,且腦代謝活性增強;
脂肪間充質干細胞(ADMSC)治療則顯著改善重度腦癱兒童的運動與言語功能,未見明顯不良反應;
伊朗團隊的I期臨床試驗進一步證實,反復鞘內注射自體骨髓MSC可顯著提升痙攣型腦癱患兒的GMFCS分級、平衡能力(BBS評分)及肌肉痙攣控制(MAS評分),同時認知功能獨立性(FIM/FAM)亦顯著提高。
這些研究共同表明,不同來源的MSCs均能有效促進腦癱患者的功能恢復,為臨床治療提供了多樣化的選擇與循證支持。
四、挑戰與未來方向
個體化治療方案:需根據腦癱類型(如痙攣型、共濟失調型)和損傷部位選擇最佳細胞來源(臍帶、胎盤)及輸注途徑(鞘內、靜脈)。
長期安全性評估:需建立10年以上隨訪機制,監測遲發性風險(如免疫耐受性變化)。
技術優化:
- 基因編輯:增強MSCs的歸巢能力或神經營養因子分泌。
- 外泌體療法:MSCs分泌的外泌體攜帶修復因子,可減少細胞移植風險
結語
間充質干細胞治療腦癱展現出顯著的臨床潛力,通過神經修復、免疫調節和血管新生等多機制改善運動功能與生活質量。現有數據支持其安全性與有效性,但需進一步通過大規模隨機對照試驗驗證長期療效。未來,隨著工程化外泌體與基因編輯技術的突破,MSCs有望成為腦癱精準治療的核心手段,為全球數百萬患兒帶來康復希望。
相關閱讀:臍帶、脂肪、骨髓和胎盤:哪種來源的間充質干細胞更適合治療腦癱?
參考資料:
Xie, Baocheng, Chen, Minyi, Hu, Runkai, Han, Weichao, Ding, Shaobo, Therapeutic Evidence of Human Mesenchymal Stem Cell Transplantation for Cerebral Palsy: A Meta-Analysis of Randomized Controlled Trials, Stem Cells International, 2020, 5701920, 10 pages, 2020. https://doi.org/10.1155/2020/5701920
Gu, J., Huang, L., Zhang, C. et al. Therapeutic evidence of umbilical cord-derived mesenchymal stem cell transplantation for cerebral palsy: a randomized, controlled trial. Stem Cell Res Ther 11, 43 (2020). https://doi.org/10.1186/s13287-019-1545-x
Hu, K., Wang, R. ., Xiao, B. ., Xiao, B. ., Gu, Y. ., Liu, F. ., … Wen, Y. . (2022). Effect of adipose-derived mesenchymal stem cell transplantation in five patients with cerebral palsy: A case report. American Journal of Translational Medicine, 6(1), 33–40. Retrieved from https://journals.publicknowledgeproject.org/default3/index.php/ajtm/article/view/2253
Mohammadhosein Akhlaghpasand, Maede Hosseinpoor, Bardia Hajikarimloo, Atieh Hajarizadeh, Maryam Golmohammadi, Roozbeh Tavanaei, Ida Mohammadi, Nastaran Ansari Noghlebari, Niloofar MohammadEbrahim, Alireza Zali, Saeed Oraee-Yazdani,Repeated Intrathecal Injections of Autologous Bone Marrow-Derived Mesenchymal Stem Cells for Spastic Cerebral Palsy: Single-Arm Safety and Preliminary Efficacy Clinical Trial,Journal of Neurorestoratology,2025,100207,ISSN 2324-2426,https://doi.org/10.1016/j.jnrt.2025.100207.
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加微信
掃碼添加微信