型糖尿病(T1D)是一種自身免疫性疾病,其特征是胰腺中分泌胰島素的β細胞遭到破壞。盡管胰島素療法和β細胞替代治療取得了進展,但針對疾病根本原因(即機體對β細胞免疫耐受的喪失)的根治性療法仍未實現。當前免疫重塑策略聚焦于胰腺自身抗原特異性干預,通過過繼轉移體外擴增的調節性細胞——包括間充質干細胞(MSCs)、調節性T細胞(Tregs)及樹突狀細胞(DCs),統稱調節性細胞療法。
免疫調節新范式:三系細胞療法攻克1型糖尿病的進展與突破
近期,歐洲免疫學雜志主頁發表了一篇“1型糖尿病調控細胞療法的進展:新興戰略與未來方向”的文獻綜述[1]。

本綜述旨在概述當前正在開發的基于調節性細胞的1型糖尿病治療方案。多項臨床試驗已證實向T1D患者體內輸注調節性細胞的安全性,但僅報告了輕微的有效性跡象。在病程較短且殘余β細胞量較高的患者中觀察到最具前景的療效,這表明早期干預可能帶來臨床獲益。該療法仍面臨重大挑戰,包括輸注產品的長期療效和穩定性。
未來,將調節性細胞療法與免疫調節劑或胰島β細胞修復策略相結合,可能成為實現T1D功能性治愈的關鍵。
什么是1型糖尿病,目前治療1型糖尿病主流方式有哪些?
1型糖尿病(T1D)是一種慢性自身免疫性疾病,其特征是主要由自身反應性T細胞驅動選擇性破壞胰島素分泌β細胞,導致胰島素缺乏和高血糖。
當前臨床管理依賴外源性胰島素治療,但需持續監測血糖水平并逐步增加劑量。臨床試驗表明,Teplizumab短期療程可顯著延緩T1D患者高風險非糖尿病親屬的臨床發病進程,并顯著提升新診斷T1D患者的刺激后C肽水平。這些成果促成Teplizumab成為首個獲批治療T1D的藥物,通過保護β細胞功能延緩疾病進展,為改變病程提供了新治療選擇。

替代受損胰島素分泌細胞的策略主要包括胰島移植或胰島素聯合降糖藥物改善代謝控制。自2000年代初埃德蒙頓方案實施以來,胰島移植已成功應用于血糖控制不穩定的患者,其安全性和有效性得到廣泛證實。但該技術受限于供體胰腺稀缺、胰島提純效率低及需終身免疫抑制等問題。為突破這些限制,新型胰島移植位點、封裝系統及自體誘導多能干細胞(iPSC)源胰島移植等研究已取得積極進展。
最近有報道稱,一名長期患有1型糖尿病 (T1D) 的患者在移植自體iPSC衍生胰島后,經過1年的隨訪,血糖水平仍維持正常。
為保護β細胞功能并改善代謝控制,胰高血糖素樣肽-1受體激動劑(如利拉魯肽)作為胰島素輔助治療,可降低胰島素需求量并優化血糖控制。
盡管上述療法為T1D治療開辟了新途徑,但均未針對疾病根源——即自身反應性T細胞介導的β細胞免疫攻擊。因此,重建胰腺抗原免疫耐受仍是未滿足的醫療需求。在此背景下,多種基于調節性細胞的療法已在臨床試驗中開發驗證。

本綜述將重點闡述基于過繼轉移免疫調節細胞(包括干細胞樣細胞、T淋巴細胞及抗原呈遞細胞)的最新治療進展(圖1),這些療法旨在逆轉T1D自身免疫反應。此類策略有望與β細胞替代/保護方案形成互補:在T1D早期階段阻斷對殘余功能β細胞的免疫攻擊,或在長期患者中保護新重建的胰島素分泌細胞。
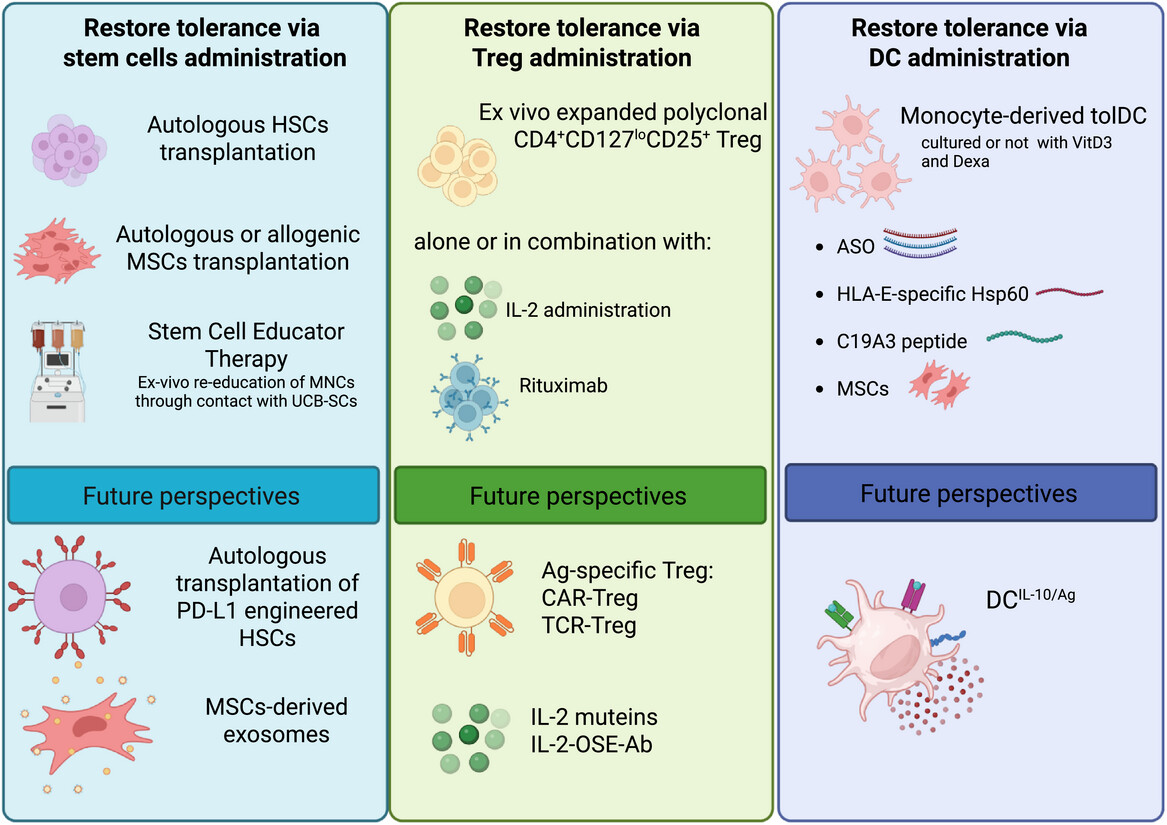
目前正在臨床試驗(上圖)或臨床前開發(下圖)中研究的策略,基于干細胞(左圖)、Tregs(中圖)或DCs(右圖)。
1、干細胞療法通過免疫調節治療1型糖尿病:阻斷β細胞破壞
自體造血干細胞療法:基于”在重建初始免疫耐受系統前清除自身反應性免疫細胞”的理論基礎,結合造血干細胞(HSCs)已知的免疫調節活性,自體HSC移植已應用于T1D患者治療。
該療法在短中期內可維持良好代謝控制,顯著提升胰島素非依賴性。但長期隨訪數據有限,且存在不同程度的自身免疫復發率。盡管療效確切,由于存在致命并發癥風險及需精準篩選獲益患者亞群,其風險獲益比仍存爭議。
為降低自體HSC移植后疾病復發風險,目前正研究改造HSCs使其表達共抑制分子程序性死亡配體1(PD-L1)的新策略。該創新療法可能通過PD1-PD-L1抑制軸作用于自身反應性T細胞,從而規避T1D患者自體HSC移植后的復發風險。
創新間充質干細胞療法:目前學界亦在探索替代性干細胞方案以規避HSC移植風險。間充質干細胞(MSCs)作為成纖維細胞樣多能基質細胞,可從多種組織中分離。MSCs通過釋放可溶性因子或細胞間接觸機制重塑免疫反應,抑制效應T細胞功能。
異體HSC移植后直接注射MSCs治療移植物抗宿主病的實踐已顯示免疫調節效應,進而推動其在實體器官移植及類風濕關節炎、克羅恩病、多發性硬化癥和系統性紅斑狼瘡等自身免疫/炎癥疾病中的應用。多項研究證實其雖效果短暫但具臨床獲益。
對T1D而言,MSCs兼具促進β細胞再生與免疫調節雙重潛力。臍帶血(UCB)或骨髓源MSCs的直接體內給藥已在T1D不同病程(新發/長期)患者中測試(表1)。
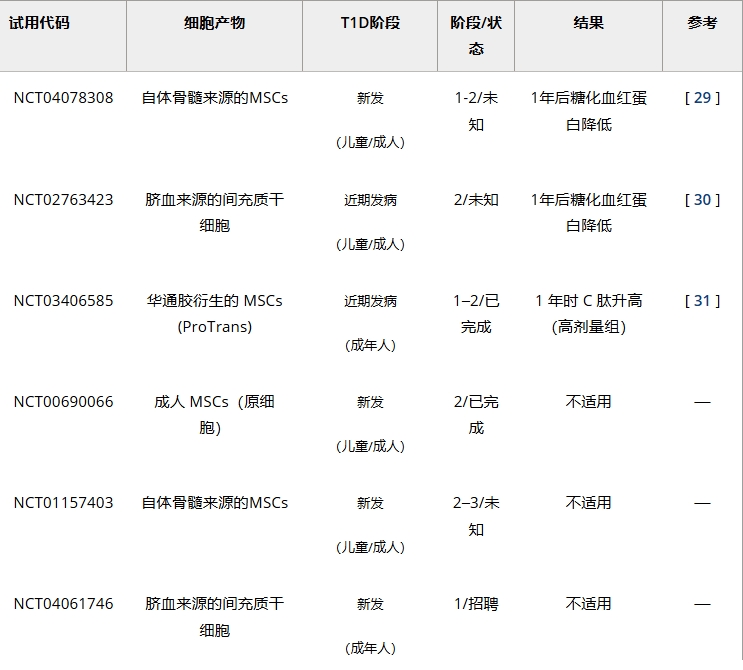
目前有限數據表明其安全性良好,干細胞治療1型糖尿病且在保護β細胞功能方面具治療潛力,但仍需更廣泛長期試驗驗證持續獲益。
干細胞教育療法應用:免疫調節MSCs的應用正向體外方向拓展:通過單核細胞與貼壁UCB-MSCs共培養實現免疫重編程。
這種”干細胞教育療法”(SCE)已在涵蓋兒童/成人、不同病程的T1D患者臨床試驗中驗證(表1)。結果證實SCE安全性及其重塑外周T細胞區室的能力:增加調節性T細胞(Tregs)與CD4+初始T細胞,恢復細胞因子平衡。短期代謝控制僅輕微改善,而β細胞保護效應僅見于治療時具殘余β細胞功能的患者。
外泌體療法拓展:基于MSCs旁分泌活性的胞外囊泡(如外泌體)療法,經炎癥性疾病驗證具臨床潛力,現正于T1D臨床試驗(NCT02138331)評估其應用價值。該策略規避了活細胞移植風險,為免疫調節提供新路徑。
大量正在進行的臨床試驗的結果可能會揭示基于干細胞的療法治療1型糖尿病的潛力。
2、調節性T細胞療法:重建1型糖尿病的免疫耐受性
調節性T細胞(Tregs)——包括表達叉頭框P3的Tregs(FOXP3+Tregs)和分泌IL-10的1型調節性T細胞(Tr1)——被公認為維持健康與疾病狀態下外周免疫耐受的關鍵細胞。在T1D患者中,研究顯示存在Tregs穩定性、功能及數量的缺陷,或效應細胞對抑制作用的抵抗。
體外擴增的自體多克隆CD4+CD127loCD25+Tregs是首個應用于T1D兒童及成人患者的Treg療法(臨床試驗號:ISRCTN0612846, NCT01210664, Treg-TID研究)(表2)。
結果證實該方法安全性良好,但療效僅見于兒童隊列:隨訪1年時β細胞功能得以維持,且病程較短患兒代謝改善更顯著。然而2年后所有患者疾病進展均需依賴胰島素治療。
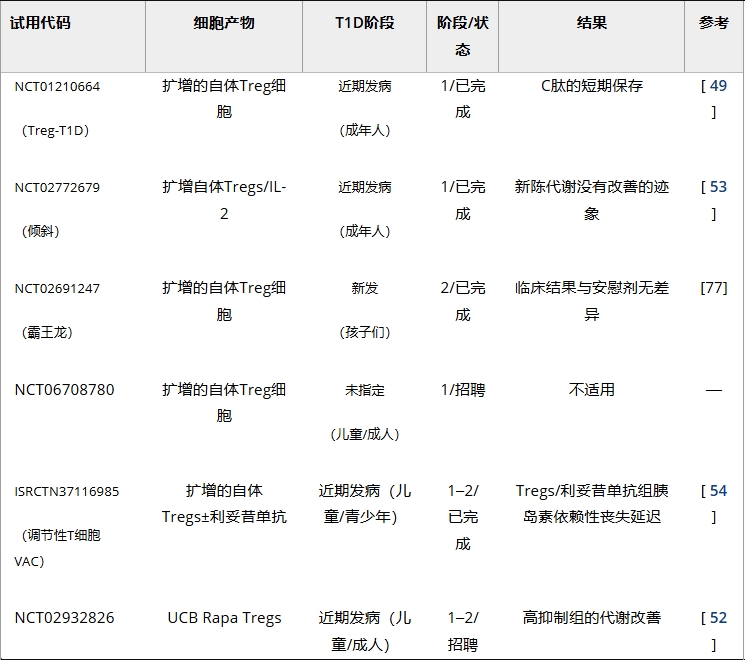
近期開展的Trex研究(NCT02691247,表2)將體外擴增Treg療法應用于更大規模的新發T1D兒童隊列。結果顯示:無論輸注劑量高低,Treg均未能保護殘余β細胞功能。值得注意的是,體外增殖率較低的細胞產品與C肽下降減緩相關,提示Treg療效可能與其增殖特性呈負相關。
臍帶血Tregs與IL-2聯用挑戰
臍帶血源Tregs試驗(NCT02932826/NCT03011021)顯示病程較短者療效更優。輸注Tregs因體內IL-2不足快速衰減,IL-2聯合療法(TILT試驗,NCT02772679)雖維持Tregs數量卻未能保護胰島功能。新型嵌合IL-2構建體(TiilT項目)通過靶向炎癥位點增強Tregs存活與控制炎癥能力。
B細胞清除聯合療法突破
Tregs聯合利妥昔單抗清除B細胞(ISRCTN37116985)實現部分患者2年胰島素非依賴,亞組治療12年后仍處臨床緩解期。針對癥狀前期T1D的聯合療法試驗(NCT06688331)有望揭示病程對療效影響。?
工程化Tregs成為調節性T細胞療法治療1型糖尿病的新方向
總體而言,目前的結果表明輸注的Treg缺乏長期療效,因此對該領域提出了新的挑戰。為了改進Treg療法,正在研究增強Treg功能的策略,包括利用轉基因T細胞受體 (TCR) 進行工程改造。事實上,已經從胰島浸潤的致病T細胞中分離出3種TCR。
- 01、ARTiDe聯盟結合機器學習方法、體外和體內臨床前研究以及臨床級流程,旨在開發新型TCR工程化Treg,以在針對1型糖尿病 (T1D) 患者的I期臨床試驗中進行測試。與此同時,
- 02、Abata Therapeutics開發了HLA-DR4限制的胰島素原靶向TCR工程化 Treg,可在體外直接或通過感染耐受機制微調自身免疫反應。
- 03、ABA-201產品預計預計2025年啟動I期臨床試驗
關鍵瓶頸:靶點選擇(如HPi2-CAR因Tregs自身表達靶抗原導致失敗)
總體而言,在1型糖尿病 (T1D) 研究中,Treg療法旨在通過改善其特異性并提高體內強度和存活率來增強注入的Treg產品。
3、耐受性樹突狀細胞:逆轉1型糖尿病的自身免疫
樹突細胞(DCs)是主導適應性免疫應答的專業抗原呈遞細胞(APCs)。耐受性DC(TolDCs)作為特定DC亞群,其特征為低表達共刺激分子、分泌抗炎細胞因子,并能調節效應T細胞應答、誘導T細胞失能或促進Tregs分化。TolDCs可從循環單核細胞體外誘導生成,使其成為”反向疫苗接種”策略的理想工具。
近20年前,T1D成為首個接受過繼性TolDC療法的自身免疫病。該研究中(NCT00445913),通過靶向CD40-CD80-CD86的反義寡核苷酸維持DC未成熟狀態,輸注至完全確診的T1D患者(表3)。
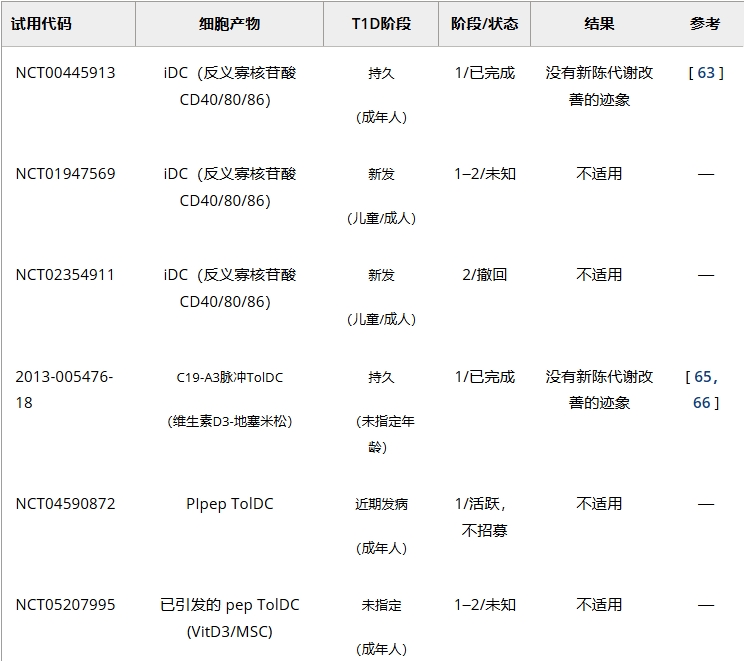
治療耐受性良好,但未觀察到血糖控制改善。鑒于該方案的安全性,后續在近期發病及新發T1D患者中啟動兩項試驗(NCT01947569, NCT02354911),結果尚未公開(表3)。
新型耐受性樹突狀細胞制備技術與初步驗證
耐受性樹突細胞(TolDCs)還可通過以下流程制備:在單核細胞向DC分化階段,使用維生素D3(VitD3)和地塞米松(Dexa)處理,隨后負載自身抗原(即VitD3/Dexa TolDC)。
該方案曾用于治療類風濕關節炎(AutoDECRA試驗,NCT01352858),并成功抑制類風濕關節炎進展。
應用于T1D時,負載HLA-DR4限制性前胰島素肽(C19-A3)的該方案雖安全性良好,但因患者β細胞功能嚴重衰竭未改善血糖,但顯著降低抗原特異性T細胞應答并誘導長效IL-10分泌細胞。
創新聯合療法與靶向突破
兩項進行中試驗探索:1)PipepTolDC在新近診斷成人患者中測試肽負載TolDCs(NCT04590872);2)MSC-tolDCs療法將VitD3致耐受DC與MSCs共培養后輸注(NCT05207995),結果尚未公布。
突破性進展來自AVT001——新發T1D患者接受AVT001(負載HLA-E限制性熱休克蛋白60衍生肽的自體單核細胞源DC)治療后(NCT03895996)。該肽段此前被證實可與CD8+調節性T細胞亞群互作——而該亞群在多數T1D患者中存在缺陷(表3)。
AVT001治療組1年內C肽水平較基線值下降幅度更小,盡管整體血糖控制及胰島素需求未改善。這表明特異性靶向Tregs的TolDC治療1型糖尿病的策略目前成效最為顯著。
結論
盡管已有大量臨床試驗報道,逆轉T1D自身免疫反應仍面臨挑戰。過繼性轉移免疫調節細胞為下一代細胞療法指明了關鍵方向:
- 治療時機前移:需在疾病早期(理想狀態為癥狀前期)干預。為此,除胰島自身抗體外,亟需更優生物標志物識別T1D患者高風險一級親屬;
- Treg療法局限性:依賴FOXP3的調節性T細胞因體內適應能力不足,僅產生輕微療效;
- 新型耐受策略:體內誘導非FOXP3依賴的抗原特異性Tregs(如過繼性TolDC療法或MHC-抗原納米顆粒),可能實現更持久、自我延續的免疫耐受。
唯有跨越單一療法局限,構建”免疫穩態重置-β細胞再生”的協同網絡,方能在攻克T1D的征途上實現從血糖控制到功能性治愈的歷史性飛躍。
主要參考資料:
[1]https://onlinelibrary.wiley.com/doi/10.1002/eji.202451722
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加官方微信
掃碼添加官方微信