間充質基質細胞 (MSC;又稱間充質干細胞) 可促進愈合并減少炎癥。許多后期臨床試驗都顯示出有希望的治療反應,但其他一些試驗尚未達到其主要終點,這使得將MSC轉化為臨床實踐變得困難。這些不一致可能與MSC輸送途徑、缺乏產品優化或臨床試驗中接受的背景療法隨時間變化有關。因此,隨著間充質干細胞治療的研究越來越廣泛并且可能在臨床上可用,必須考慮和優化給藥途徑和作用機制。
本文主要闡述討論間充質干細胞輸送的不同途徑,重點介紹治療作用的擬議機制以及潛在的安全問題[1]
為什么說干細胞不同的給藥途徑,會成為影響干細胞治療疾病療效的關鍵因素?
干細胞不同的給藥途徑成為影響細胞改善疾病的關鍵因素,主要基于以下幾個方面:
- 細胞分布和歸巢性:干細胞具有主動歸巢到損傷部位的功能,不同的給藥途徑會影響干細胞在體內的分布,從而影響其歸巢效率。例如,靜脈注射的干細胞可能會在肺部被大量截留,而局部給藥則可以直接將細胞送達至損傷部位,提高治療效果。
- 藥代動力學和生物學特性:干細胞的給藥方式會影響其進入體內后的行為,包括藥代動力學和生物學特性。注射點部位、注射器、載體材料和緩沖液等因素都會影響細胞的給藥效果。
- 治療效果的差異性:不同的給藥方式會導致治療效果產生顯著差異。例如,局部給藥可以更精準地引導干細胞到達病灶,提高療效,而全身給藥可能因為細胞無法有效到達目標組織而影響治療效果。
- 安全性和創傷風險:局部給藥雖然可以提高療效,但也存在造成新的創傷或并發癥的風險。選擇合適的給藥方式可以減少這些風險。
- 細胞存活和保留時間:局部給藥后,細胞在給藥部位的保留時間和存活率是一個挑戰,這影響治療效果。不同的給藥途徑可能會影響細胞的存活時間和數量。
- 免疫介導的損傷和細胞凋亡:局部給藥后,免疫介導的損傷和細胞凋亡也會影響細胞的存活,從而影響治療效果。
- 治療方案的個體化:不同的適應癥、病程和治療訴求需要不同的給藥方式。例如,在治療缺血性卒中慢性期階段的方案中,局部給藥比全身給藥更有效。
- 旁分泌作用:MSCs的旁分泌作用,包括分泌細胞外囊泡和細胞因子以及免疫應答修飾等,與全身用藥比較而言,MSCs以靶向局部注射的給藥方式注射到機體病灶區可以有效的增加MSCs的旁分泌活性,從而延長/增強干細胞療法的治療潛力。
01間充質干細胞的給藥途徑有哪些?
給藥途徑的選擇似乎是影響細胞療法分布、保留、存活和療效的最關鍵因素之一。目前尚未建立黃金標準,需要進一步研究。對于目前的細胞療法,途徑包括直接局部給藥至組織和器官,以及通過動脈內、靜脈內 (IV) 和腹膜內 (IP) 注射進行全身給藥,盡管關于最后一種途徑的數據非常有限。
這些方法大致可分為兩類:全身給藥和局部給藥(圖1,說明了MSC注入心臟的全身和局部途徑)。
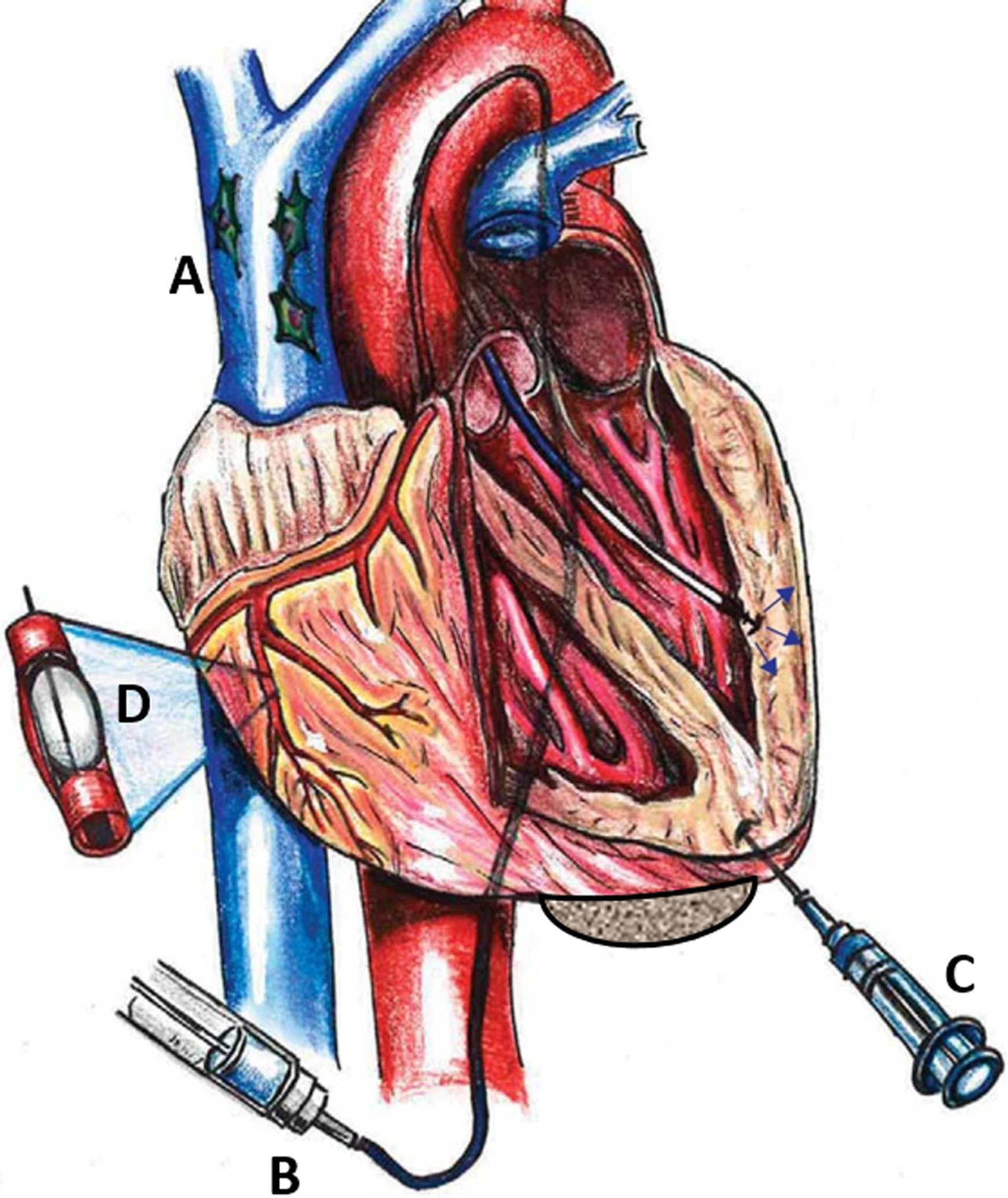
(A) 靜脈 (IV) 輸注間充質干細胞 (MSCs;未顯示外周IV) (Sys)。
(B) 通過經心內膜注射 (TESI) 施用MSCs (Loc)。
(C) 直接心外膜注射MSCs (Loc)。
(D) 通過冠狀動脈內輸注輸送MSCs (Sys)。
其中間充質干細胞(MSCs)的全身給藥方式主要包括以下幾種:
1、靜脈注射:這是全身MSC輸送的主要方法,被認為是人體臨床試驗中常規且安全的方法。靜脈輸注允許MSCs通過血液循環到達全身各個部位,包括關節的炎癥區域。
2、動脈注射:與靜脈注射相比,動脈內(IA)注射方法更有效,因為它減少了肺中的細胞捕獲,并誘導目標組織損傷部位的移植細胞遷移。
3、腹膜內注射:盡管腹膜內(IP)給藥在臨床試驗中并不像靜脈注射那樣常用,但臨床前研究已證實它們在各種疾病康復中的治療作用。
這些全身給藥方式各有其優勢和局限性,選擇最合適的給藥途徑需要根據具體的疾病狀況和治療目標來決定。
間充質干細胞靜脈給藥
間充質干細胞(MSCs)靜脈注射的特點主要包括以下幾個方面:
- 操作簡便、侵襲性小:靜脈輸注因其操作簡便、侵襲性小、可重復性強,成為臨床試驗中優先選擇的給藥方式。
- 歸巢能力:靜脈注射的MSCs會歸巢到炎癥部位和組織損傷部位。MSCs具有很好的趨化特性,能穿透血管壁,故靜脈或局部注射均能自動趨化到損傷的組織部位。
- 劑量要求:靜脈注射MSCs的劑量通常是≥1×10^6細胞/kg,且多次給藥比單次注射更有益。
- 免疫調節作用:MSCs具有免疫調節功能,能通過細胞間相互作用及產生細胞因子抑制T細胞的增殖及其免疫反應,從而發揮免疫重建的功能。
- 抗炎作用:通過調節各類炎癥因子,如IL-6等,MSCs可抑制炎癥發生發展,改善全身炎癥反應和提高患者生活質量。
- 促進細胞組織修復:MSCs因其多向分化能力、免疫調節和抗炎作用、損傷部位的歸巢和遷移能力以及對內源性組織祖細胞的刺激作用,促進細胞修復和組織再生。
- 安全性和有效性:許多接受了靜脈滴注間充質干細胞治療的病人都有一個很好的身體感覺,代謝改善,增強肌肉和關節強度。間充質干細胞治療具有安全可靠、無免疫排斥、不產生疤痕以及更自然的感觀等優點。
- 快速清除問題:由于“首過效應”,靜脈注射的間充質干細胞主要滯留在肺部,注射后迅速消失。這可能會影響治療效果,最終成藥進入臨床應用的很少。
- 治療多種全身性疾病:系統注射的MSCs可以到達全身,可以治療多種全身性疾病,但缺點是趨化效率低,只有非常少的細胞真正到達受損部位發揮治療作用。
這些特點綜合了MSCs靜脈注射的優勢和局限性,為臨床應用提供了重要的參考依據。
間充質干細胞動脈給藥
間充質干細胞(MSCs)動脈給藥的特點主要包括:
在某些治療適應癥中,動脈內 (IA) 輸送可能被證明是最有效的方法。
- 提高療效:相較于其他給藥方式,動脈注射方式可見更為明顯的療效。研究表明,動脈注射組改善最迅速且最明顯,并明顯增強梗死側胼胝體區髓鞘的重建。
- 更多的細胞聚集:動脈移植組在注射后早期有更多聚集于梗死灶周圍,這可能有助于提高治療效果。
- 繞過肺系統:動脈注射可以繞過肺系統,更有效地將細胞導向大腦的缺血部位,這對于治療腦卒中等疾病尤為重要。
- 安全性:有研究指出動脈注射安全且具有更好的治療效果。
- 減少腦損傷風險:盡管有研究表明動脈注射與靜脈注射相比有可能增加腦損傷的風險,但也有研究未能明顯改善神經功能,這表明動脈給藥的安全性需要根據具體情況評估。
- 提高趨化效率:經動脈注射可以相對提高MSCs向損傷組織的趨化效率。
- 微血栓產生風險:體積較大的MSCs經動脈注射后易在微動脈聚集,可能產生微血栓,提示經動脈注射MSCs存在較高的治療風險。
- 靶向性:動脈給藥可以更精確地將MSCs輸送到特定的組織或器官,如心臟或大腦,這對于治療局部缺血性疾病特別有用。
- 技術挑戰:盡管動脈給藥具有上述優勢,但也存在技術挑戰,如需要精確的注射技術和對血管的精確定位。
綜上所述,動脈給藥在提高MSCs治療效果、靶向性和趨化效率方面具有明顯優勢,但同時也伴隨著一定的風險和技術挑戰。在實際應用中,需要根據患者的具體情況和疾病特點來選擇最合適的給藥途徑。
間充質干細胞腹腔給藥
腹腔注射間充質干細胞(IP)有一定的益處,但這種方法的命運、益處和局限性尚未得到很好的研究。IP注射可降低細胞從腹腔移出的速度,從而避免可能致命的肺血管快速栓塞,并允許注射更多細胞。
與靜脈注射相比,IP注射間充質干細胞在多種疾病的臨床前模型中具有相似甚至更深遠的效果。
與靜脈注射相比,IP注射的MSC在多種疾病的臨床前模型中具有相當甚至更深遠的效果。MSC在這些和其他疾病模型中的有益作用與其改變先天和獲得性免疫系統的能力有關。
間充質干細胞局部給藥
局部給藥包括:包括鞘內注射、病灶內注射和心內膜注射等,適用于特定區域或器官的治療。
將MSCs局部注射到靶組織或損傷部位附近具有重要優勢,包括反應快速、局部化。細胞可以被注射到精確的目標位置,從而增加植入機會(與組織再生相關)并延長其治療潛力(直接旁分泌支持)。
與生物材料/支架一起局部注射到損傷部位可以降低肺梗塞或心肌梗塞的風險。從支架上遷移的細胞傾向于單獨遷移,因此不太可能在肺中聚集。
然而,局部給藥也存在風險,例如高密度給藥時細胞會誘導細胞凋亡。許多局部細胞遞送途徑都存在“沖刷”效應,尤其是心肌內注射。在侵入性手術中,針頭或導管會對心臟組織造成機械損傷,打開血管并在心肌中留下針孔,從而形成一個空間,懸浮細胞可以通過該空間。
下文將詳細討論局部給藥的其他特性。
02間充質干細胞局部給藥后的作用機制
由于MSC在治療組織損傷方面具有重要的臨床意義,因此迫切需要更好地描述MSC局部注射后的作用機制。人們提出了MSC發揮其有益作用的幾種可能機制。
盡管早期有證據表明MSC直接分化和細胞替換,但最近的研究強烈表明,它們最重要的作用機制可歸因于它們能夠分泌旁分泌因子,包括細胞外囊泡 (EV) 和細胞因子,將線粒體轉移到附近的細胞 (圖2)、遷移并改變免疫反應(免疫調節)。
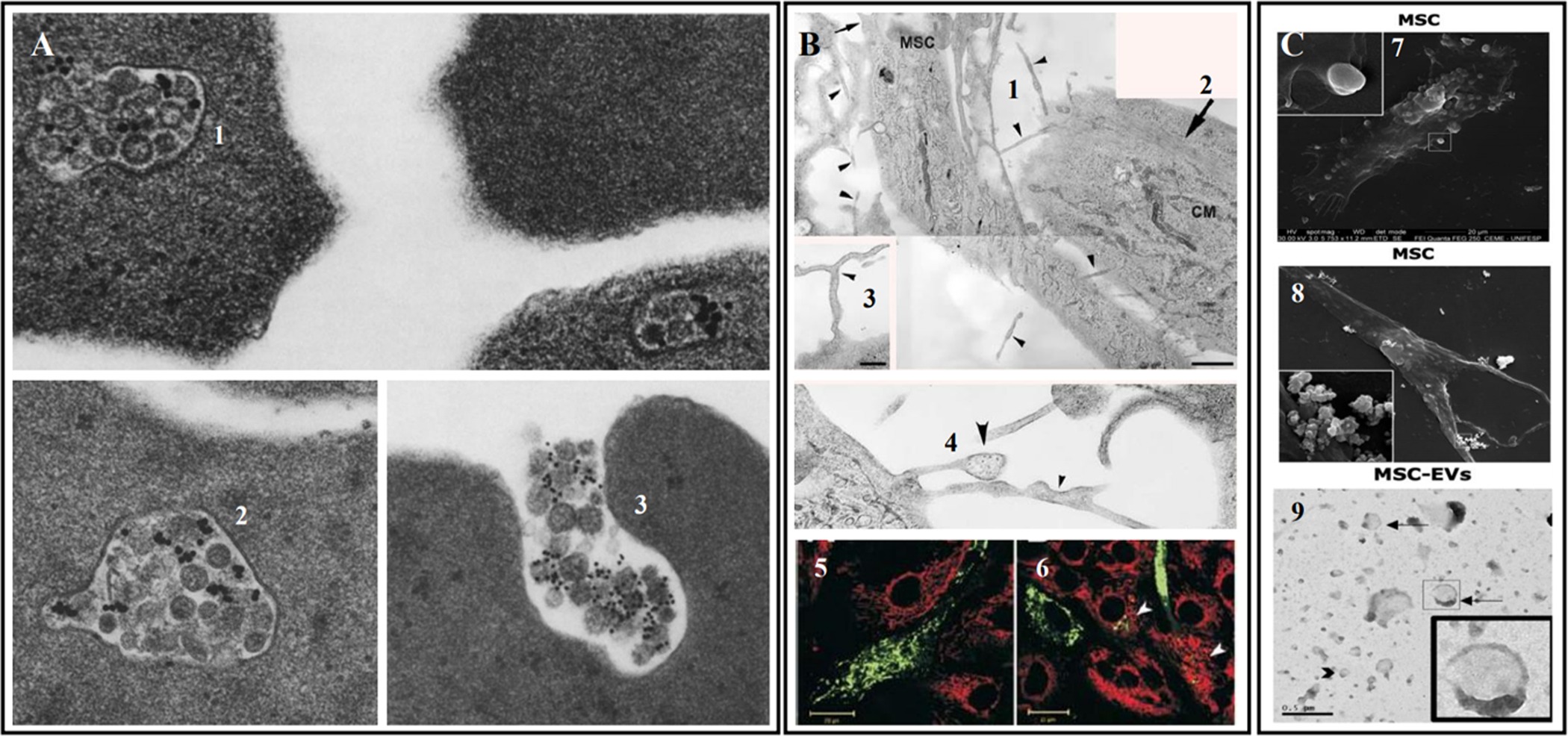
間充質干細胞的旁分泌因素
間充質干細胞會釋放大量生物活性因子(如細胞因子、趨化因子、激素、生長因子和miRNA),對局部細胞動態產生深遠影響。這些旁分泌因子構成了一個復雜網絡的一部分,可保護損傷組織,促進內源性修復/再生機制和免疫介導的吞噬作用 ,從而產生長期的有益影響。
間充質干細胞的細胞間接觸
間充質干細胞(MSCs)的細胞間接觸在它們的免疫調節作用和組織修復中扮演著重要角色。以下是一些關鍵點,概述了MSCs細胞間接觸的機制和作用:
- 免疫調節:MSCs能夠通過細胞間接觸抑制自然殺傷細胞(NK細胞)的增殖、細胞毒性和細胞因子產生。研究表明,MSCs可以抑制IL-2誘導的NK細胞增殖。此外,MSCs與NK細胞之間的相互作用能夠導致NK細胞激活受體表面表達的下調,從而抑制NK細胞的細胞毒性。
- 促進腫瘤發展:MSCs與腫瘤細胞之間的復雜相互作用促進腫瘤進展,通過創造有利于腫瘤細胞增殖、血管生成、運動、侵襲和轉移的環境。MSCs可以通過細胞接觸、釋放旁分泌因子和通過細胞外囊泡(EVs)轉移生物物質來調節腫瘤生長。
- 與內皮細胞的相互作用:MSCs與血管內皮細胞之間的直接細胞接觸可以誘導MSCs表現出類似周細胞的表型,這在血管新生和組織再生中可能起到關鍵作用。此外,MSCs通過細胞間接觸能夠調節內皮細胞的增殖和血管生成,部分是通過VE-Cadherin/β-catenin信號通路的調節。
- 旁分泌因子的增強:研究表明,促進細胞間接觸的生物材料可以增強MSCs的旁分泌功能。在三維培養中,與水凝膠中包埋的MSCs相比,種植在支架上的MSCs顯示出增強的分泌譜,并對外胚層細胞如肌細胞前體產生有益的旁分泌效應,這部分可以歸因于N-cadherin介導的細胞間相互作用。
- 抗衰老作用:MSCs的抗衰老作用部分是通過旁分泌方式和直接的細胞間接觸實現的。它們分泌的可溶性旁分泌因子包括IL-10(一種抗炎和免疫調節細胞因子)、與組織修復潛力相關的IL-6和IL-8,以及能夠促進CD8+T細胞和Treg細胞發育同時抑制Th1的TGF-β。此外,MSCs還表達FasL和PD-L1以進行接觸依賴性抑制以誘導T細胞凋亡。
綜上所述,MSCs的細胞間接觸在它們的免疫調節、促進腫瘤發展、與內皮細胞相互作用、旁分泌功能增強以及抗衰老作用中起著至關重要的作用。通過這些機制,MSCs能夠在多種生物學過程中發揮關鍵作用,包括組織修復、免疫調節和腫瘤微環境的塑造。
間充質干細胞的免疫調節
MSC具有廣泛的免疫調節能力,能夠影響適應性和先天性免疫反應。目前的證據表明,MSC對同一類型的免疫細胞發揮不同的免疫調節作用,具體取決于局部微環境或疾病狀態。
以下是間充質干細胞在免疫調節方面的幾個關鍵點:
- 對單核細胞/巨噬細胞的影響:MSCs能夠削弱單核細胞/巨噬細胞的吞噬和抗原呈遞能力,并促進這些細胞表達免疫抑制分子,如白介素(IL)-10和程序性細胞死亡蛋白1配體1(PD-L1)。
- 對樹突狀細胞的影響:MSCs能有效抑制樹突狀細胞的成熟,降低它們產生促炎細胞因子的能力,并減少對T細胞的激活。
- 對T細胞的影響:MSCs抑制CD4+T輔助細胞(Th1和Th17)的生成和促炎特性,同時促進調節性T細胞(Tregs)的增殖和抑制能力。此外,MSCs還能削弱促炎CD8+ T細胞的擴增、細胞因子分泌和細胞毒性活動。
- 對B細胞的影響:MSCs抑制B細胞的分化、增殖和抗體分泌,并促進產生IL-10的調節性B細胞(Bregs)。
- 旁分泌機制:MSCs通過旁分泌機制,涉及TGF-β、HGF、PGE2、HLAG-5、IL-6、CCL-2、CCL-5等因子,加強其在局部淋巴細胞中的作用。
- 免疫逃逸機制:MSCs通過產生免疫調節分子(如IFN-γ、COX2、PGE2和IDO)的細胞-細胞相互作用從免疫系統中逸出。
- 臨床應用:由于MSCs的免疫抑制特性,它們已成為治療炎癥性疾病(如急性移植物抗宿主病、器官/細胞移植中的移植物排斥反應和自身免疫疾病)的有前景的工具。
- 雙向免疫調節作用:MSCs是免疫環境的“調和劑”,具有雙向免疫調節作用,根據局部微環境的不同,可以表現出截然相反的免疫調節能力。
- 免疫調節特性的差異性:MSCs的免疫調節特性隨細胞來源和細胞質量等因素的不同而不同。
- 與B細胞的聯系:人源性MSCs通過接觸依賴機制改善靜止B細胞的存活,并抑制依賴T細胞的B細胞分化。
這些特性顯示了MSCs在調節免疫反應和治療免疫相關疾病方面的潛力。
間充質干細胞的遷移(歸巢)的機制
間充質干細胞(MSCs)的歸巢是指這些細胞能夠定向遷移到特定的組織部位,特別是在機體受到損傷、缺血或缺氧時,MSCs能夠被吸引到這些損傷部位進行修復和再生。以下是關于MSCs歸巢機制的一些關鍵點:
- 歸巢的定義:2009年,Karp等建議將“MSCs歸巢”定義為MSCs在目標組織的脈管系統里被捕獲,隨后跨越血管內皮細胞遷移至目標組織的過程。
- 歸巢的發現過程:1983年,Gallatin首次提出“歸巢”概念,原本指淋巴細胞的歸巢。后來這一概念被引申到干細胞,包括MSCs。
- 歸巢機制:MSCs的歸巢效應涉及多種因素,包括趨化因子及其受體。MSCs表面廣泛表達不同趨化因子、生長因子等受體,這些受體與相應配體結合,驅動MSCs歸巢。損傷部位的信號分子和MSCs表面受體相一致,使得機體內或外源移植的干細胞順利歸巢至微環境。
- 趨化因子的作用:一些趨化因子如CXCL12(SDF-1α)、CXCL16、CCL19、TGF-β1、表皮細胞生長因子、血小板源生長因子BB等與MSCs上的相應受體相互作用,是引起MSC靶向遷移的重要因素。特別是CXCL12及其受體CXCR4被認為是吸引MSC遷移的一對非常重要的細胞因子及其受體。
- 歸巢的步驟:MSC歸巢可以分為非系統歸巢和系統歸巢。系統歸巢由受損或發炎組織釋放的歸巢促進因子引導,分為五個連續步驟:滾動、激活、牢固的粘附、爬行和跨內皮遷移。
- 歸巢的重要性:歸巢能力是MSCs安全有效應用于臨床的關鍵。微環境的改變是MSCs歸巢的始動因素,組織損傷局部表達多種趨化因子、黏附因子、生長因子等各種信號分子,吸引MSCs定向到達該組織。
- 歸巢的靶向性:MSCs能夠選擇性歸巢于多種組織的損傷部位。不同的微環境分泌不同的信號分子,吸引MSCs定向到達該組織。干細胞歸巢可以歸到各個臟器、炎癥及創傷部位,甚至腫瘤部位。
這些機制共同作用,使得MSCs能夠像內置了一部“智能GPS”導航系統一樣,尋找并定居于損傷部位,發揮其治療作用。
03局部注射間充質干細胞治療特定疾病的有效性和安全性
截至2024年,已注冊的臨床試驗中,間充質干細胞的給藥幾乎在全身給藥和局部給藥之間平分秋色,大多數晚期臨床試驗采用局部給藥,例如通過鞘內注射、鞘內注射和心內膜途徑,分別用于治療背痛、肛周瘺和慢性心力衰竭。
間充質干細胞的直接原位給藥是一種可控性更強的給藥方法,可直接作用于局部損傷,通常能產生更好的治療效果。例如,對缺血性中風模型中臨床前間充質干細胞研究的薈萃分析表明,與動脈內或血管內注射間充質干細胞相比,在受損部位注射間充質干細胞能更有效地改善神經系統嚴重程度評分,盡管動脈內和靜脈內直接注射間充質干細胞也能顯著改善預后。
局部注射間充質干細胞在心血管中的作用
將MSCs局部注射到心血管系統會產生積極的結果。通常,冠狀動脈內和心肌內(心外膜和經心內膜)注射是心血管疾病中兩種最廣泛使用的細胞療法。
冠狀動脈內注射將細胞輸送到一條主要冠狀動脈(左前降支、左回旋支或右冠狀動脈)。這種給藥途徑比心肌內注射侵入性更小,心肌內注射通常需要手術干預或心內膜通路,一些研究報告稱冠狀動脈內和心肌內注射同樣有效。
2016年,循環雜志一項研究對急性心肌梗死的MSC治療臨床前和臨床研究的薈萃分析得出結論,經心內膜干細胞注射 (TESI) 表現出最大的梗死面積減少和左心室射血分數 (LVEF) 增加。相比之下,冠狀動脈內輸送沒有顯示任何改善。

在心臟中,TESI似乎是局部施用MSCs的首選方法,它是一種微創、基于導管的輸送途徑,將細胞通過心內膜直接注射到心肌中。使用TESI 作為輸送途徑的豬研究表明,梗塞疤痕減少,LVEF改善。TESI還在急性心肌梗死 (AMI) 臨床試驗中改善了LVEF。
局部注射間充質干細胞在神經系統中療效的作用
MSCs因其治療神經系統疾病的潛力而備受關注。在神經元損傷的情況下,在大鼠中風模型中,向病變部位局部注射MSCs可改善協調功能,抑制疤痕組織形成和細胞凋亡,并刺激血管生成。
神經修復和神經保護作用是MSCs的一種組織修復特性,主要表現為兩種作用機制:
(1) 神經源性分化和細胞替換,
(2) 神經營養因子的分泌。
MSCs可顯著緩解缺血性損傷,而這種挽救作用源于移植細胞分化為神經元和星形膠質細胞。相反,MSCs對神經再生的旁分泌作用是通過神經營養因子的分泌發生的。
用 (外源性) MSC衍生的外泌體接種皮質神經元可增強其生長促進和靶標激活作用,而MSC條件培養基通過增加神經生長因子 (NGF) 和腦源性神經營養因子 (BDNF) 表達來增強施萬細胞活力和增殖。
局部注射間充質干細胞在骨科中的作用
近年來,關節腔局部注射MSCs可促進軟骨組織再生修復,減輕骨關節炎(OA)引起的退變。
一項I/II期臨床試驗表明,向OA患者膝關節注射BM-MSCs與軟骨生物標志物的表達有關,可減少滑膜炎癥,減輕疼痛和癥狀,且未發生任何嚴重不良事件。
2017年,美國運動雜志的一項概念驗證I/II期臨床試驗表明,向OA膝關節內注射1.0×108AD-MSCs可改善膝關節功能、減輕膝關節疼痛,并通過再生透明樣關節軟骨減少軟骨缺損,且不會引起不良事件。
局部注射BM-或AD-MSC可顯著改善骨愈合。盡管BM-和AD-MSC之間的分子線索存在差異,但兩種細胞類型誘導的骨形成量和特性相當。直接注射到骨折部位的骨髓抽吸物成功修復了60處未愈合骨折中的53處,局部注射成骨細胞也加速了長骨骨折的骨修復。
MSC還可能通過與滑膜巨噬細胞相互作用刺激軟骨再生,從而減少促炎細胞因子(如IL1β)。事實上,注射到OA膝關節中的MSC會接觸滑膜巨噬細胞,并能夠誘導向M2細胞的極化,從而促進組織修復。
MSCs不僅可以分化為肌腱細胞(腱細胞),還可以調節炎癥和組織愈合。
目前正在進行多項研究MSCs在肌腱愈合中的應用的臨床試驗(NCT03688308、NCT01788683、NCT02484950、NCT03449082、NCT03279796、NCT03752827、NCT03454737)。
局部注射間充質干細胞在皮膚病學中的作用
在皮膚病學中,局部應用MSCs可改善燒傷、糖尿病和其他慢性疾病的治療效果、傷口愈合和皮膚移植成活率。臨床前數據表明,將BM-MSCs局部注射到切口全層傷口中可顯著縮短愈合時間,同時刺激血管生成、上皮再生和肉芽形成。
局部注射間充質干細胞在胃腸病學中的作用
MSC療法最近已獲得歐洲藥品管理局 (EMA) 的批準,用于治療肛周瘺管性克羅恩病。Darvadstrocel由MSC組成,當細胞被注射到內口和外口以及瘺管內時,可安全有效地誘導瘺管愈合。

04總結
隨著MSC臨床試驗的發展,至關重要的是要記住歷史安全問題,認識到現代臨床風險,并使用與預期作用機制一致的方法和給藥方式,以產生最有效、最安全、最經濟可行和最符合道德的治療方法。
在理解MSC療效的潛在機制方面仍然存在知識空白,這些機制可能在不同的組織中是獨一無二的。我們必須確定來自不同組織的MSC是否對不同的疾病更有治療作用,或者同種異體MSC是否在所有或僅特定疾病中比自體MSC更有治療作用。鑒于MSC的可塑性和旁分泌介導的免疫調節活性,它們在各種臨床環境中的有效性研究越來越多,并呈現出令人鼓舞的結果。
綜上所述,干細胞的給藥途徑直接影響細胞的分布、歸巢、存活、治療效果以及安全性,是影響細胞改善疾病的關鍵因素。
因此,根據具體的疾病和治療目標選擇合適的給藥途徑對于提高干細胞治療的療效至關重要。隨著研究的深入,我們有望進一步優化MSCs的臨床應用,為患者提供更有效、更安全的治療方法。
參考資料:[1]:Bagno LL, Salerno AG, Balkan W, Hare JM. Mechanism of Action of Mesenchymal Stem Cells (MSCs): impact of delivery method. Expert Opinion on Biological Therapy. 2022 Apr;22(4):449-463. DOI: 10.1080/14712598.2022.2016695. PMID: 34882517; PMCID: PMC8934282.
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。




 掃碼添加微信
掃碼添加微信