漸凍癥,學(xué)名肌萎縮側(cè)索硬化(ALS),是一種罕見(jiàn)且致命的神經(jīng)系統(tǒng)疾病。它如同一場(chǎng)無(wú)聲的風(fēng)暴,悄然侵襲患者的運(yùn)動(dòng)神經(jīng)元,導(dǎo)致肌肉逐漸萎縮、無(wú)力,最終剝奪患者的肢體功能,甚至危及生命。面對(duì)這一殘酷的疾病,傳統(tǒng)醫(yī)學(xué)手段往往力不從心,患者和家屬只能在絕望中等待。然而,隨著干細(xì)胞技術(shù)的興起,一束新的希望之光正在穿透漸凍癥的黑暗,為肢體能力的恢復(fù)帶來(lái)了前所未有的可能。
近年來(lái),科學(xué)家們將目光投向了干細(xì)胞治療漸凍癥的潛力,試圖通過(guò)移植干細(xì)胞來(lái)修復(fù)受損的神經(jīng)細(xì)胞,重建神經(jīng)連接,從而恢復(fù)患者的肢體功能。從實(shí)驗(yàn)室的初步探索到臨床試驗(yàn)的逐步推進(jìn),干細(xì)胞治療漸凍癥的研究正在不斷取得突破,一個(gè)個(gè)令人振奮的案例也逐漸浮出水面。這些案例不僅為患者帶來(lái)了身體上的改善,更為無(wú)數(shù)家庭點(diǎn)燃了希望的火種。

本文將通過(guò)臨床案例來(lái)證明干細(xì)胞治療漸凍癥,如何修復(fù)受損的肢體功能。
漸凍癥的突破:干細(xì)胞治療如何幫助患者修復(fù)受損的肢體功能?
首先干細(xì)胞治療修復(fù)受損肢體功能要通過(guò)機(jī)制的幫助,機(jī)制涉及多個(gè)層面,以下為詳細(xì)分析
細(xì)胞替代:干細(xì)胞具有分化為多種細(xì)胞類型的能力,包括神經(jīng)元、星形膠質(zhì)細(xì)胞和少突膠質(zhì)細(xì)胞。在漸凍癥中,運(yùn)動(dòng)神經(jīng)元的退化和死亡是疾病進(jìn)展的關(guān)鍵因素。通過(guò)移植干細(xì)胞,可以補(bǔ)充丟失或功能受損的運(yùn)動(dòng)神經(jīng)元,恢復(fù)神經(jīng)回路的功能。
神經(jīng)營(yíng)養(yǎng)因子分泌:干細(xì)胞能夠分泌多種神經(jīng)營(yíng)養(yǎng)因子,如腦源性神經(jīng)營(yíng)養(yǎng)因子(BDNF)、神經(jīng)生長(zhǎng)因子(NGF)、神經(jīng)營(yíng)養(yǎng)因子-3(NT-3)和膠質(zhì)細(xì)胞源性神經(jīng)營(yíng)養(yǎng)因子(GDNF)等。
免疫調(diào)節(jié):漸凍癥的發(fā)病機(jī)制中存在顯著的炎癥反應(yīng),免疫系統(tǒng)對(duì)神經(jīng)組織的攻擊加劇了疾病進(jìn)展。間充質(zhì)干細(xì)胞(MSC)具有強(qiáng)大的免疫調(diào)節(jié)能力,能夠減少促炎細(xì)胞因子的產(chǎn)生,抑制T細(xì)胞的活化,并增加抗炎細(xì)胞因子的水平。
詳情信息請(qǐng)點(diǎn)擊此處(干細(xì)胞治療漸凍癥的機(jī)制是什么?)
接下來(lái)我們通過(guò)臨床案例來(lái)分析,干細(xì)胞治療漸凍癥是如何改善患者的肢體功能的
臨床案例:間充質(zhì)干細(xì)胞治療后,ALS-FRS-R 評(píng)分和 FVC 的每月下降率有更顯著改善
ALS功能評(píng)分量表(ALS-FRS)主要由四個(gè)球部-呼吸功能、兩個(gè)上肢功能(用餐具和穿衣)、兩個(gè)下肢功能(走路和爬樓梯)及兩個(gè)其他功能(穿衣及洗漱、床上翻身)組成。ALSFRS-R 可以評(píng)估呼吸道癥狀和患者執(zhí)行獨(dú)立日常活動(dòng)能力的受損程度。
2016年3月,以色列耶路撒冷哈達(dá)薩-希伯來(lái)大學(xué)在國(guó)際期刊《JAMA Neurology》上發(fā)布了一篇《間充質(zhì)干細(xì)胞移植治療肌萎縮側(cè)索硬化癥的安全性及臨床效果1/2 期和 2a 期臨床試驗(yàn)結(jié)果》,研究的主要終點(diǎn)是該細(xì)胞療法的安全性和耐受性。次要終點(diǎn)包括治療對(duì)各種臨床參數(shù)的影響,例如 ALS 功能評(píng)定量表修訂評(píng)分和呼吸功能。
進(jìn)行了一項(xiàng) 1/2 期研究,研究單次肌肉內(nèi) (IM) 或鞘內(nèi) (IT) 注射自體 MSC-NTF 細(xì)胞。在完成 24 名目標(biāo)患者中的 12 名后進(jìn)行了積極的中期安全性分析,之后該試驗(yàn)轉(zhuǎn)變?yōu)?2a 期劑量遞增研究,通過(guò)肌肉內(nèi)和鞘內(nèi)聯(lián)合注射 MSC-NTF 細(xì)胞。
臨床結(jié)果表示:
將 MSC-NTF 細(xì)胞移植后 6 個(gè)月內(nèi) ALS-FRS-R 評(píng)分和 FVC(預(yù)測(cè)百分比)的變化率與 3 個(gè)月導(dǎo)入期的變化率進(jìn)行了比較。在研究的 1/2 期部分,IT 隊(duì)列的 ALS-FRS-R 評(píng)分和 FVC 的平均每月進(jìn)展率有所改善,但 IM 治療組沒(méi)有改善(圖1A 和圖2A)。
圖1:

在試驗(yàn)的 2a 期階段,MSC-NTF 細(xì)胞移植后觀察到 ALS-FRS-R 評(píng)分和 FVC 的每月下降率有更顯著改善(圖1B 和圖2B)。未檢測(cè)到明顯的劑量效應(yīng)。
圖2:
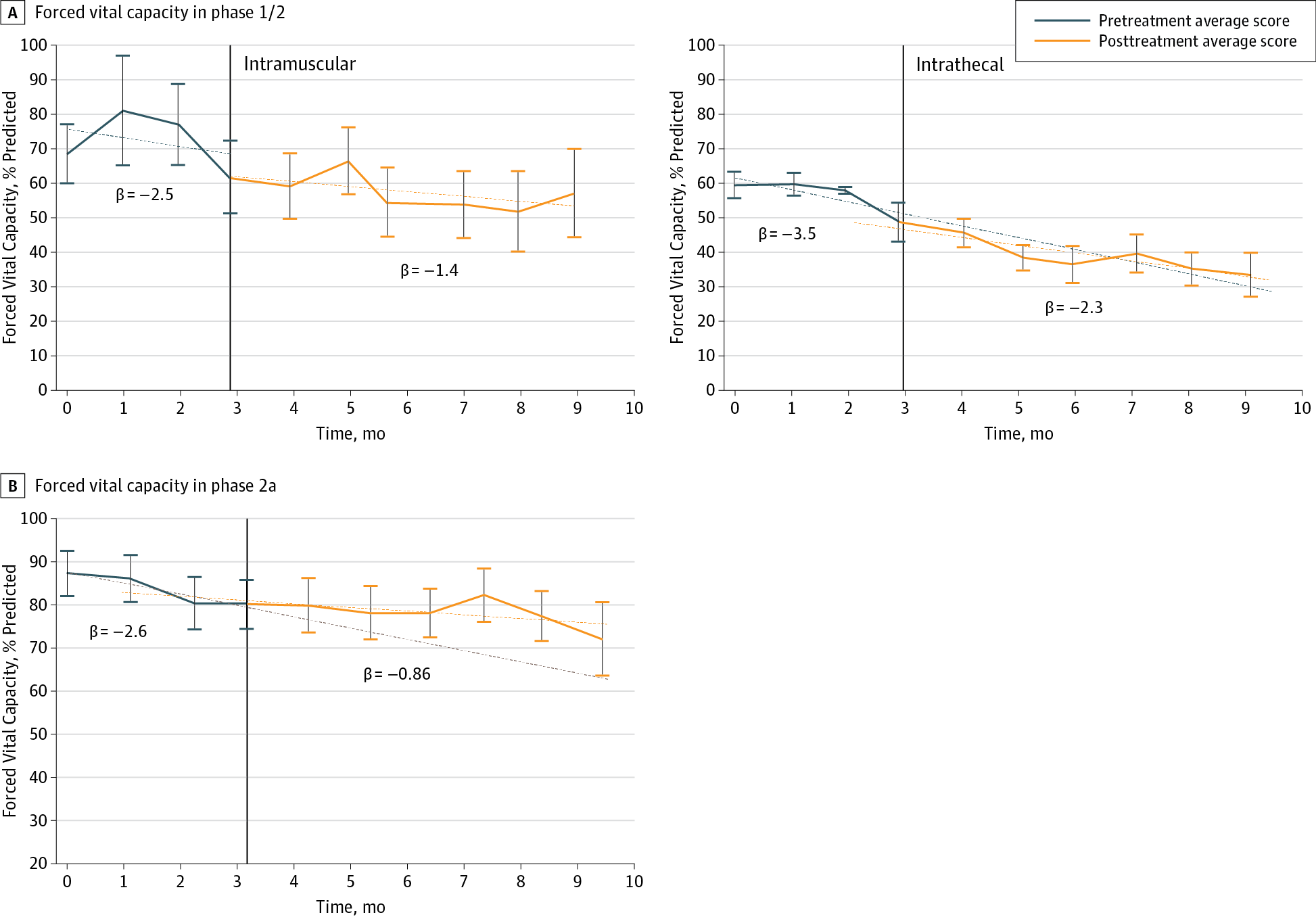
由于兩項(xiàng)研究中只有接受 IT 治療的患者似乎獲得了全身益處,因此對(duì)兩項(xiàng)研究中接受 IT 或 IT+IM 治療的患者在治療前和治療后期間的 ALS-FRS-R 評(píng)分和 FVC 進(jìn)展率進(jìn)行了事后比較,并進(jìn)行了 6 個(gè)月的隨訪,使用具有患者隨機(jī)效應(yīng)的分段線性回歸分析。
該分析顯示,FVC 進(jìn)展率有統(tǒng)計(jì)學(xué)顯著改善,并且 ALS-FRS-R 評(píng)分進(jìn)展率有改善趨勢(shì)(非常接近統(tǒng)計(jì)學(xué)顯著性)對(duì)于接受完整隨訪的患者。
臨床案例:骨髓間充質(zhì)干細(xì)胞移植治療后,可以減緩疾病的進(jìn)展,ALSFRS-R 改善
2021年12月,馬什哈德醫(yī)科大學(xué)免疫學(xué)研究中心在國(guó)際期刊《Regenerative Therapy》上發(fā)布了一篇《骨髓間充質(zhì)干細(xì)胞移植治療肌萎縮側(cè)索硬化癥的安全性和有效性》的研究結(jié)果,本研究的主要目的是確定自體骨髓間充質(zhì)干細(xì)胞(BM-MSCs)同時(shí)通過(guò) IT 和 IV 應(yīng)用對(duì) ALS 患者進(jìn)行的安全性和有效性。

臨床結(jié)果表示:
在應(yīng)用骨髓間充質(zhì)干細(xì)胞后,各個(gè)患者的 ALSFRS-R 值 3 個(gè)月內(nèi)保持穩(wěn)定(圖1B)。對(duì)所有患者的 ALSFRS-R 評(píng)分進(jìn)行回歸分析表明,與植入前評(píng)分相比,BM-MSC 移植 1 個(gè)月和 3 個(gè)月后 ALSFRS-R 斜率沒(méi)有顯著降低(圖1A -B)。
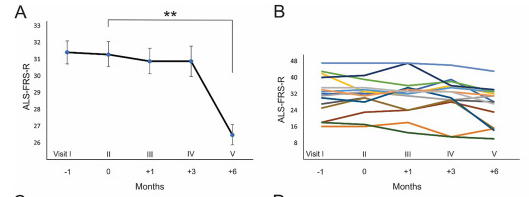
患者在接受細(xì)胞治療的3個(gè)月內(nèi),F(xiàn)VC 的平均值保持穩(wěn)定(圖1C-D)
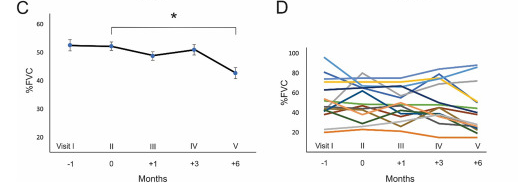
本研究表明,對(duì) ALS 患者同時(shí)進(jìn)行骨髓間充質(zhì)干細(xì)胞的 IT 和 IV 注射是一種安全的方法,沒(méi)有重大不良事件,并表明有潛在的臨床益處。在3 個(gè)月的隨訪中,ALSFRS-R 和 FVC 值在細(xì)胞治療后保持穩(wěn)定。
總結(jié)
綜上所述,干細(xì)胞治療漸凍癥可以改善患者的肢體功能,并且呼吸道癥狀也得到了改善。干細(xì)胞治療漸凍癥所展現(xiàn)出的潛力,讓我們對(duì)未來(lái)充滿了期待。相信在不久的將來(lái),隨著科學(xué)技術(shù)的不斷進(jìn)步和研究的深入,干細(xì)胞治療將成為漸凍癥的有效治療手段,幫助更多的患者恢復(fù)肢體能力,重新?lián)肀篮玫纳睢T卺t(yī)學(xué)科研人員的不懈努力下,漸凍癥患者終有一天能夠擺脫疾病的束縛,重獲行動(dòng)自由,綻放生命的光彩。
若想了解更多關(guān)于漸凍癥和干細(xì)胞治療漸凍癥的內(nèi)容請(qǐng)點(diǎn)擊此處!
免責(zé)說(shuō)明:本文僅用于傳播科普知識(shí),分享行業(yè)觀點(diǎn),不構(gòu)成任何臨床診斷建議!杭吉干細(xì)胞所發(fā)布的信息不能替代醫(yī)生或藥劑師的專業(yè)建議。
版權(quán)說(shuō)明:本文來(lái)自杭吉干細(xì)胞科技內(nèi)容團(tuán)隊(duì),歡迎個(gè)人轉(zhuǎn)發(fā)至朋友圈,謝絕媒體或機(jī)構(gòu)未經(jīng)授權(quán)以任何形式轉(zhuǎn)載至其他平臺(tái),轉(zhuǎn)載授權(quán)請(qǐng)?jiān)诰W(wǎng)站后臺(tái)下方留言獲取。




 掃碼添加微信
掃碼添加微信