間充質干細胞 (MSC) 因其免疫調節特性以及減輕自身免疫性疾病(例如多發性硬化癥 (MS))炎癥的潛力,在臨床研究中引起了廣泛關注。
間充質干細胞治療多發性硬化癥安全可行,一期臨床數據揭示神經保護與抗炎協同效應
2025年5月8號,期刊雜志“Nature”發表了一篇“Cell therapy with placenta-derived mesenchymal stem cells for secondary progressive multiple sclerosis patients in a phase 1 clinical trial”(胎盤間充質干細胞治療繼發性進行性多發性硬化癥患者的一期臨床試驗)的研究文章[1]。

本研究評估了胎盤來源的MSC (PLMSC) 在五名患有繼發性進展型多發性硬化癥 (SPMS) 的患者中應用的安全性和可行性。
結果表明,臨床結果持續改善,表現為六個月內EDSS評分、認知和心理評估以及DTI指標中的徑向擴散 (RD) 指數顯著降低。此外,fMRI分析顯示大腦連接和認知功能顯著增強。免疫學方面,治療三個月后,CD20/CD19 B細胞標志物顯著降低,抗炎細胞因子IL-10增加,而促炎細胞因子TNFα、IL-6和IL-17減少。這些發現表明PLMSC移植對SPMS患者是安全可行的。
胎盤間充質干細胞(PLMSCs)在多發性硬化癥中的免疫調節與髓鞘再生協同治療:一項I期臨床安全性與機制探索
多發性硬化癥 (MS) 是中樞神經系統最常見的免疫介導和炎癥性疾病,會攻擊髓鞘(大腦和脊髓細胞的絕緣層)。

當前的研究和治療策略越來越強調一種更整體的方法,旨在平衡多發性硬化癥中髓鞘再生和炎癥之間的相互作用,促進再生,同時維持最佳炎癥水平。間充質干細胞 (MSC)包括胎兒來源的MSC,已顯示出通過發揮抗炎、免疫調節和神經保護作用以及增強髓鞘再生來滿足這些需求的潛力。
特別是,胎盤源性間充質干細胞(PLMSCs)表達較多的CD106標記,可增強間充質干細胞的免疫調節功能,同時還表達程序性死亡配體1/2(PD-L1/2),可介導T細胞周期抑制和增殖。PLMSCs可從廢棄的妊娠組織中輕松、無創地分離出來,數量豐富,不存在倫理問題,并可分化成各種神經細胞系。此外,研究表明PLMSCs比成人間充質干細胞具有更強的免疫抑制作用。此外,體外研究也證實,與其他胎兒間充質干細胞相比,PLMSCs具有更強的免疫調節功能。
盡管這些研究結果令人鼓舞,但間充質干細胞對多發性硬化癥各方面的影響仍不明確。 因此,我們設計了一項I期臨床試驗,以評估對常規療法無反應的SPMS患者靜脈注射PLMSCs的安全性和耐受性。
胎盤間充質干細胞(PLMSCs)在治療多發性硬化癥1期臨床試驗的方法
研究設計:此項開放標簽I期研究在德黑蘭省Sina and Shariati醫院的多發性硬化癥門診進行。該試驗已在ClinicalTrials.gov(NCT06360861)和伊朗臨床試驗注冊中心(IRCT20210614051576N1)注冊。首次試驗注冊于2021年7月25日。
多發性硬化癥患者根據 “麥克唐納標準和伊朗診斷與治療方案 “進行診斷和管理。根據表1所列的納入和排除標準,西納醫院多發性硬化癥門診收治的患者被認為有資格接受細胞療法。五名SPMS患者接受了PLMSCs細胞治療。

在注射MSCs之前,已獲得所有患者的知情書面同意。
本研究項目(包括胎盤捐贈和PLMSCs制備過程)已獲得“德黑蘭醫科大學”教育、文化和研究倫理委員會的批準。圖1展示了臨床試驗的設計和患者流程。
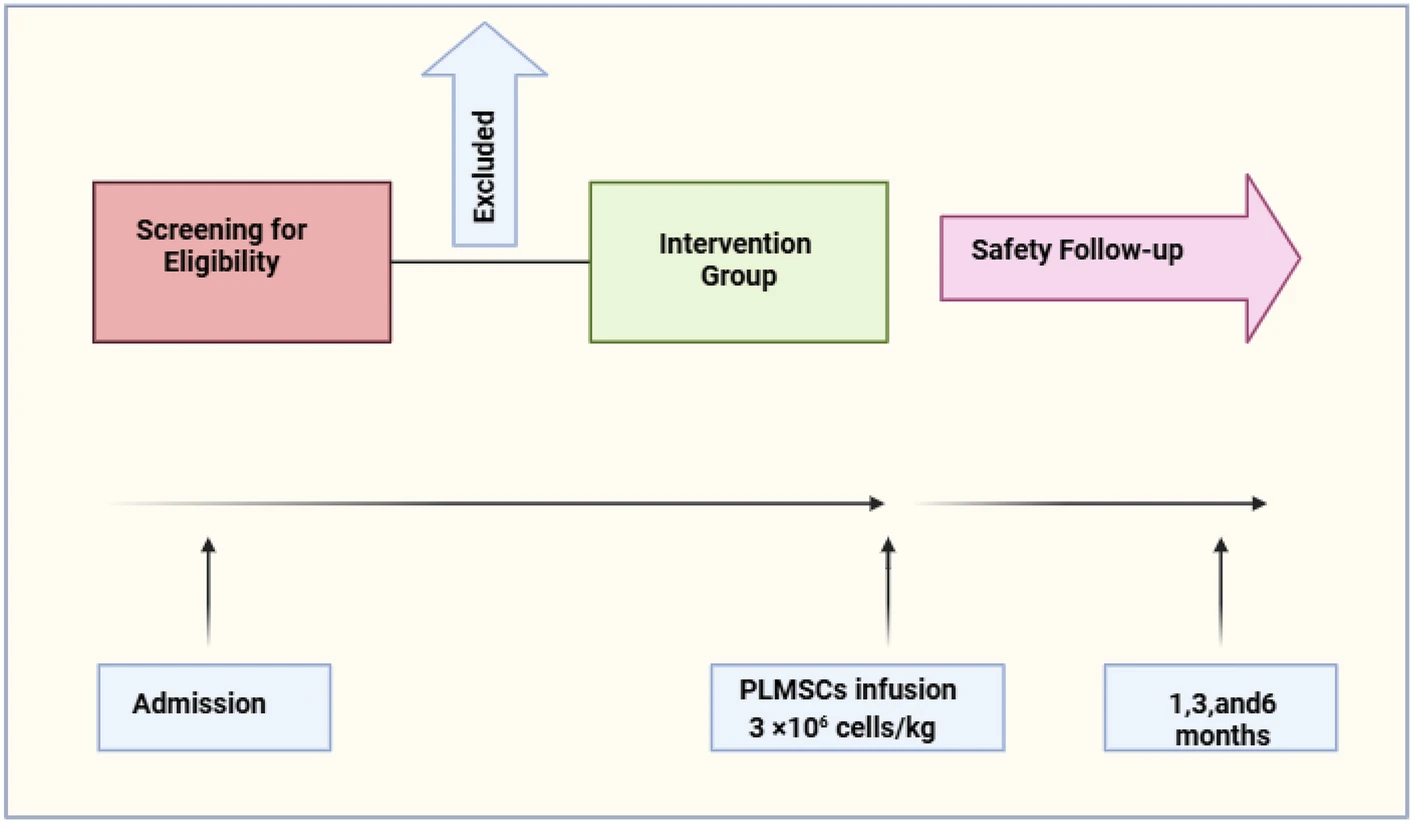
安全性(主要)及療效性結果(次要)評估
主要結果:在本I期臨床試驗中,主要目的是評估對常規療法無效的SPMS患者進行靜脈PLMSCs移植的安全性和耐受性。
- 給藥方案:患者經頭靜脈/貴要靜脈單次輸注PLMSC(劑量3×10?細胞/kg),輸注時長15分鐘;
- 安全監測:輸注前預防性使用氫化可的松(100mg)降低過敏風險,輸注期間持續監測生命體征(血壓、體溫、心率),輸注后24小時內密切追蹤早期不良反應(包括疲勞、頭痛、皮疹、寒戰、惡心、血壓波動、心肌梗死、呼吸異常、發熱及過敏性休克);
- 長期隨訪:整個研究周期(至治療后6個月)持續評估安全性與耐受性。
次要結果:次要結果側重于臨床癥狀、認知和心理問題的改善,以及全身炎癥和B細胞CD20/CD19標記物的減少。所有患者均通過臨床訪視進行監測,并由神經科醫生使用EDSS評估其臨床狀況,并在注射后0、1、3和6個月記錄測量值。
此外,在第0、3和6個月進行了DTI(用于追蹤白質完整性)、fMRI(用于研究大腦連接模式)以及認知和心理評估(MACFIMS、FSS和SL-90)以及血液測試(用于細胞因子和B細胞標志物評估)。
胎盤源性間充質干細胞治療復發緩解型多發性硬化癥的I期臨床試驗結果
臨床安全性結果(主要結果):
本研究通過初步篩選,確定了12名合格受試者,并從中選取5例納入研究。本研究中,未觀察到與PLMSC相關的嚴重并發癥。注射后,僅兩名患者(n#1和n#5)出現輕微頭痛,且為暫時性癥狀,服用一片對乙酰氨基酚片1小時后緩解。一名未告知所有癥狀緩解情況的醫生記錄了這些初始事件,在6個月的隨訪期內以及一年后未收到其他嚴重不良事件的報告。
EDSS在細胞注射后第一個月下降,兩名患者在第三個月呈下降趨勢,其余患者則保持不變(圖2)。表S1描述了注射前三年和注射MSCs后一年的EDSS變化。
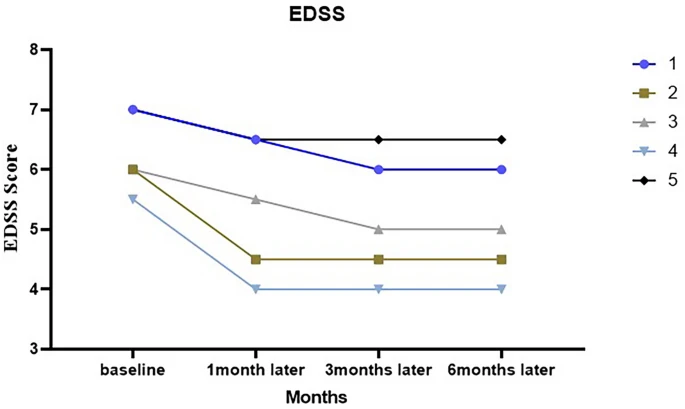
臨床療效改善結果(次要結果):
認知功能評估:本研究通過MACFIMS量表子測試發現,干預后6個月內多項認知功能指標呈現顯著改善趨勢。
BVMT-R視覺記憶測試、DKEFS分類與描述任務、CVLT-II語言學習測試在基線、3個月及6個月三個時間點均存在統計學差異。事后分析顯示,PASAT信息處理速度、BVMT-R以及DKEFS兩個子測試從基線至6個月持續顯著提升,如圖3所示。其中分類與描述任務在3-6個月間加速改善(P=0.03-0.04)。所有認知測試數據均以中位數呈現,采用弗里德曼檢驗進行統計分析。
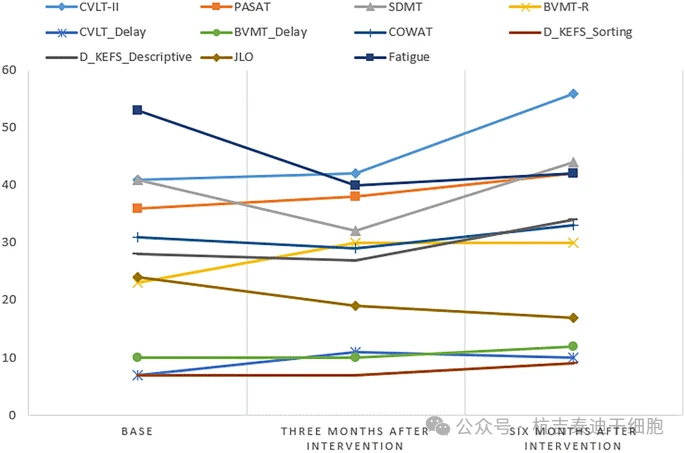
心理狀態評估:心理評估結果顯示,研究期間敵對情緒和疲勞感評分呈現顯著變化。疲勞評分在基線至3個月及6個月均顯著下降,軀體化癥狀與偏執觀念從基線到6個月也呈現持續減輕趨勢。但SCL-90總體嚴重程度量表未見顯著改變。
所有心理指標同樣以中位數為數據呈現方式,統計檢驗方法與認知評估一致,敵對情緒的下降趨勢具有統計學顯著性,如圖3和圖4所示,SCL-90整體嚴重程度量表無顯著差異。
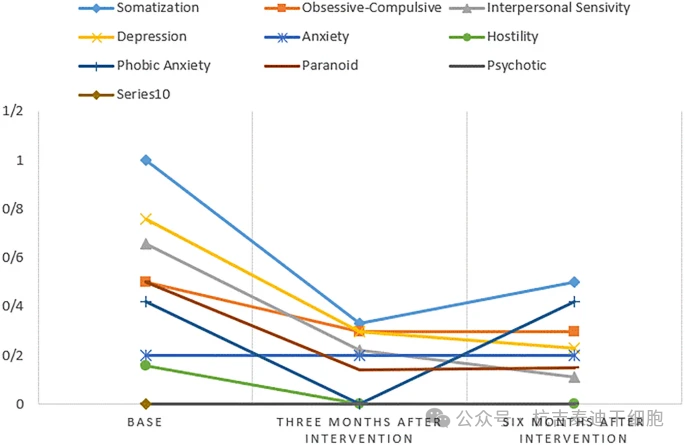
腦結構與功能變化:
- 腦容量變化:基線至隨訪期間,基底節、正常表現白質(NAWM)及異常白質的體積在3個月、6個月及基線對比中均無顯著差異,全腦總體積及白質(WM)亦未明顯減少。皮質灰質體積的下降雖存在趨勢,但無統計學意義。
- 病變特征變化:基線至6個月隨訪時,腦室周圍、皮質旁、深部白質及幕下區域的T2病灶數量、體積及負荷均無顯著變化。
彌散張量成像指標變化:
- 追蹤分析:皮質脊髓束(CST)、視輻射(OR)及胼胝體(CC)的彌散性指標在6個月內未見顯著差異。
- ROI分析:左側半球NAWM的徑向彌散度(RD)在基線至6個月及3-6個月間顯著降低(P=0.0186),而平均彌散度(MD)、軸向彌散度(AD)及分數各向異性(FA)雖呈正向趨勢,但未達統計學差異。
功能磁共振成像結果:治療后6個月,多發性硬化(MS)患者全腦網絡分析顯示,功能連接顯著增強,形成包含113個腦區及143條連接的子網絡(圖5)。
關鍵節點集中于左側默認模式網絡、左側頂葉及右側海馬旁回(節點連接度=9/8),這些區域與記憶、空間處理及靜息態活動等MS常見認知功能障礙相關。三維腦圖顯示,連接增強主要分布于顳葉、額葉、視覺區及皮層下結構,且雙側半球連接度普遍提升(節點大小與顏色分別表示連接度及權重)。
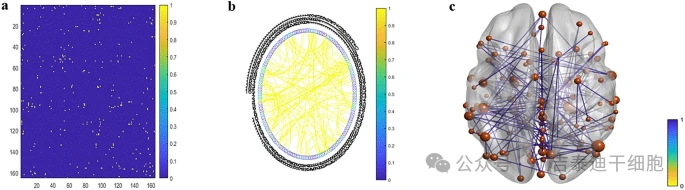
兩圖中的彩色邊和圓形網絡中的節點反映了它們的權重和節點度。 (c) 參與者在治療6個月后的功能連接變化。
實驗室檢測結果:
免疫指標變化:流式細胞術分析顯示,PLMSC療法(胎盤間充質干細胞治療)后,患者B淋巴細胞群的CD20/CD19標記表達水平降低(圖6),提示治療可能誘導B細胞數量減少,或與其聯合標準治療協同抑制B細胞活性。

細胞因子動態:治療前(基線)、治療后1個月及3個月的細胞因子檢測(圖7)表明:
- 抗炎因子IL-10:治療后3個月水平顯著升高;
- 促炎因子(IL-17、IL-6、TNFα):治療后整體顯著下降,但1例患者IL-6異常升高,可能與同期COVID-19感染相關。
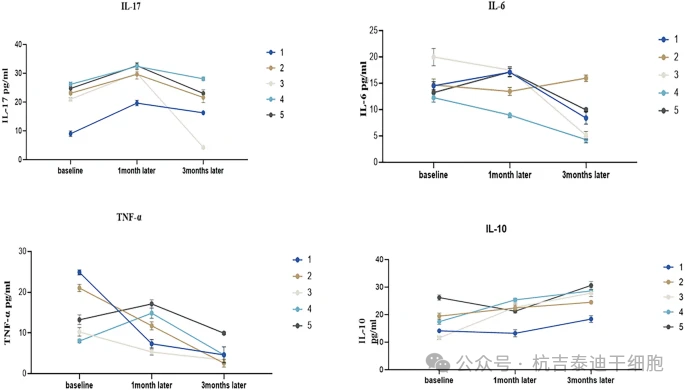
分析了注射干細胞前和注射后3個月的生物標志物,結果顯示大多數患者的TNF-α、IL-6和IL-17顯著降低。所有患者的IL-10水平均升高(P??< 0.0001)。參與者在6個月的治療期間未出現疾病活動。
數據提示胎盤間充質干細胞療法可能通過上調抗炎因子、抑制促炎因子,發揮免疫調節作用。
胎盤源性間充質干細胞治療復發緩解型多發性硬化癥的I期臨床試驗的結果討論
1、安全性及臨床改善
本研究證實胎盤間充質干細胞(PLMSC)靜脈注射對繼發進展型多發性硬化(SPMS)患者具有良好安全性與耐受性,隨訪期間及治療后一年均未報告嚴重不良事件。臨床指標顯示,EDSS評分穩定、功能障礙減輕、癥狀緩解及系統性炎癥下降,提示PLMSC可能通過免疫調節發揮神經修復潛能。但需注意,此為I期研究,樣本量小且未設對照組,結論需謹慎解讀。
2、神經影像學證據
白質完整性:左側正常表現白質(NAWM)的DTI分析顯示徑向彌散度(RD)顯著降低,可能與炎癥消退或修復機制相關。同類研究如Amanat等報道臍帶MSC改善腦癱患者白質完整性。
腦功能連接:fMRI顯示治療后記憶網絡、默認模式網絡(DMN)及空間處理網絡連接增強,與認知評估改善一致,提示PLMSC或促進神經可塑性。DMN異常是MS認知障礙的重要機制,其功能恢復可能反映治療對靜息態腦活動的調節。
3、免疫與炎癥調控
細胞因子動態:治療后抗炎因子IL-10顯著升高,促炎因子(IL-17、IL-6、TNFα)下降,支持MSCs的全身抗炎作用。IL-17水平降低尤其關鍵,因其與MS活動性病變及認知障礙惡化相關。
B細胞抑制:CD20/CD19標記的B細胞減少可能與聯合用藥利妥昔單抗(RTX)的長效B細胞清除效應相關。MSCs本身亦可能抑制B細胞活化并促進調節性B細胞(Bregs)。
4、作用機制與臨床啟示
MSCs可能通過以下途徑發揮作用:
- 免疫調節:分泌抗炎因子(如IL-10)、抑制促炎細胞因子(如IL-17)及調節B細胞功能;
- 神經修復:促進白質完整性恢復及腦網絡功能重組,改善認知與運動功能;
- 間接效應:通過旁分泌因子調控組織穩態,而非長期存活于體內。PLMSC為SPMS患者(尤其是高發認知心理障礙群體)提供了潛在新療法,但需進一步驗證其針對認知心理癥狀的特異性療效。
綜上所述,我們的研究結果表明PLMSC給藥可能具有神經保護作用。我們承認,由于隊列規模有限、隨訪時間短以及缺乏對照組,因此在解讀這些結果時務必謹慎。為了全面評估MSC移植后的神經炎癥和神經元再生,我們需要開展更大規模、重復細胞注射、更長隨訪期、對照組和客觀生物標志物的研究。
結論和未來見解
本試驗表明,在SPMS患者中注射PLMSCs后,其在短期內可能具有潛在的臨床效果和神經保護作用。然而,仍需開展更大規模的進一步研究來驗證這些發現。
我們的觀點是,對于多發性硬化癥 (MS) 患者,皮下注射的時機至關重要。PLMSCs作為多發性硬化癥 (MS) 患者的一種新療法,可以通過在炎癥初期進行多次高劑量注射來提高療效。
主要參考資料:[1]Shokati, A., Nikbakht, M., Sahraian, M.A. et al. Cell therapy with placenta-derived mesenchymal stem cells for secondary progressive multiple sclerosis patients in a phase 1 clinical trial. Sci Rep 15, 16005 (2025). https://doi.org/10.1038/s41598-025-00590-6
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。




 掃碼添加微信
掃碼添加微信