阿爾茨海默病(AD)是一種與年齡相關的神經退行性疾病,也是癡呆癥的最常見原因。由于AD具有多種病理機制,因此有學者提出多靶點治療可能比單靶點治療更有效地改變疾病的臨床病程。

臨床前研究表明,將人臍帶來源的間充質干細胞(UC-MSCs)注射到AD小鼠模型的大腦中時,MSCs會分泌多種細胞因子,幫助解決了AD的多種病理機制。
UC-MSCs分泌的可溶性細胞內粘附分子-1(sICAM-1)和AgRP可降低β淀粉樣蛋白(Aβ)水平,還通過分泌GDF-15和激活素A增強內源性成體神經發生和突觸活性,hUCB-MSC來源的半乳糖凝集素-3可以防止Aβ神經毒性。

基于這些基礎研究,Hee Jin Kim等人完成了一項關于AD的I 期臨床試驗(NCT02054208),他們將UC-MSCs立體定向注射到9名AD癡呆患者的海馬和楔前葉中,通過研究確認了MSCs治療AD的安全性和耐受性,研究結果已在《Alzheimer’s Research & Therapy》期刊發表。
該研究是一項開放標簽、單中心I期臨床試驗,主要目的是評估腦室內重復注射UC-MSCs治療AD的安全性和劑量限制毒性。共納入了9名患者,年齡50~85歲,精神狀態檢查(MMSE) 分數為18~26分。
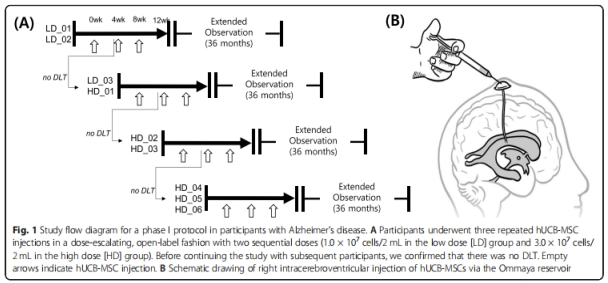
方 法:獲得當地相關機構批準以及患者的書面知情同意書后,研究人員在局部麻醉下將Ommaya儲庫植入參與者右側腦室,4周后,參與者接受第一次UC-MSCs注射,間隔4周,再重復2次UC-MSCs注射(圖 1A、B)。分為低劑量(1*107/2 mL)組和高劑量(3*107/2 mL)組。
結 果:①安全性:常見的不良事件有發燒、頭痛、惡心和嘔吐,根據 CTCAE判斷,不良事件的程度為1級,這些不良事件均在36小時內自然消退。此外,有5名參與者完成了36個月的延長觀察研究,沒有觀察到進一步的嚴重不良事件。
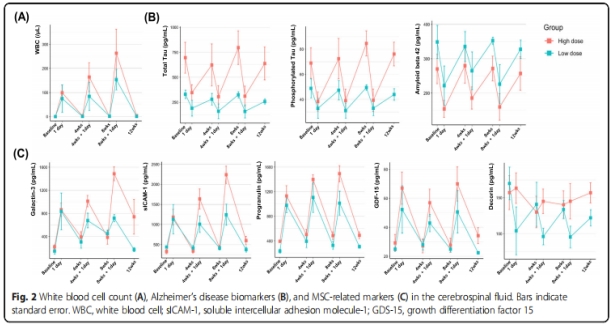
②生物標志物檢測:每次UC-MSCs注射后1天,腦脊液白細胞計數增加,4周后恢復正常(圖2A);每次UC-MSCs注射后1天,AD生物標志物下降,4周后增加到基線水平(圖2B);UC-MSCs相關標志物(Galactin-3、sICAM-1、progranulin和GDF-15)在每次注射后1天增加,4周后降至基線水平,但在腦脊液其它標志物中沒有觀察到這種情況(圖2C)。
③患者實質Aβ沉積變化:通過淀粉樣蛋白-PET測量的Aβ負荷顯示,在低劑量組的2名參與者中,PiB標準化攝取值(SUVR)從基線時的2.57 ± 0.40下降到治療后的1.92 ± 0.03;在低劑量組的另1名參與者中,florbetaben PET的SUVR從基線時的1.70下降到治療后的1.60;高劑量組中,florbetaben SUVR從基線時的1.79 ±0.07下降到治療后的1.71 ± 0.06。
總 結:在這項 I 期臨床試驗中,我們將UC-MSCs重復注射到9名輕中度AD癡呆患者的右側腦室中,僅有部分患者產生了一些輕微不良反應,表明UC-MSCs似乎是一種可行、安全且耐受性的治療方法。
該研究的局限性在于試驗中使用的UC-MSCs注射劑量是基于小鼠與人腦脊液體積比計算的,未來還需要進一步開展詳細研究來評估AD患者的最佳細胞劑量。
參考資料:
Hee Jin Kim, Kyung Rae Cho, Hyemin Jang, Na Kyung Lee, Young Hee Jung, Jun Pyo Kim,Jung Il Lee, Jong Wook Chang, Seongbeom Park, Sung Tae Kim, Seung Whan Moon,Sang Won Seo, Soo Jin Choi and Duk L. Na. Intracerebroventricular injection of human umbilical cord blood mesenchymal stem cells in patients with Alzheimer’s disease dementia: a phase I clinical trial. https://doi.org/10.1186/s13195-021-00897-2.




 掃碼添加官方微信
掃碼添加官方微信