目前制造用于治療的新β細胞的方法:
- 實驗室中源自人類多能干 細胞的成熟β細胞被移植到糖尿病患者體內。
- 在實驗室將成熟的人類多能干 細胞轉化為胰腺祖細胞,這些細胞被移植到糖尿病患者體內,在那里它們將成熟為功能性β細胞。
- 實驗室中來自其他類型細胞的成熟β細胞,例如移植到糖尿病患者體內的肝細胞。
- 使用藥物觸發糖尿病患者自身胰腺中的細胞產生新的β細胞。
- 由源自人類多能干細胞的α和β細胞組成的胰島樣簇。
而且,對于所有這些方法,正在進行的研究正在探索:
糖尿病作為一種全球性的慢性代謝性疾病,嚴重威脅著人類的健康。近年來,隨著醫學科學的飛速發展,糖尿病的治療手段不斷推陳出新。本文系統綜述了目前糖尿病治療在藥物治療、胰島移植、基因治療、干細胞治療以及生活方式干預等方面的研究進展,分析各治療方法的優勢與挑戰,展望未來糖尿病治療的發展方向,旨在為該領域的進一步研究提供參考。
目前研究用于治療糖尿病的研究進展
移植后如何保護細胞免受免疫系統的攻擊?
從多能干細胞中制造β細胞
多能細胞(胚胎干細胞或誘導性多能干細胞)可以在體內制造任何細胞類型,研究人員正在探索如何引導這些細胞制造功能齊全的β細胞。這樣的細胞可以替代朗格漢斯供體胰島的稀缺來源。迄今為止,研究人員已經成功地從人類多能干細胞中制造出細胞,這些干細胞對葡萄糖的反應方式與實驗室和小鼠中的正常β細胞相似。此外,當移植到糖尿病小鼠體內時,葡萄糖水平會變得正常。這些β細胞很快將在第一階段臨床試驗中進行安全性測試。?
從其他細胞制造β細胞
一些研究人員認為,有可能鼓勵已經存在于患者胰腺中的細胞產生新的β細胞——這一過程通常被稱為再生。尚不清楚胰腺中是否存在干細胞,但已在小鼠體內發現了β細胞前體。一些研究人員希望,如果這些前體存在于人類胰腺中,他們或許能夠找到將它們轉化為患者體內新β細胞的藥物。
顯然,即使這是可能的,也必須防止新生β細胞的自身免疫破壞。這些努力在本質上仍處于實驗階段,尚未達到臨床試驗結束的地步。
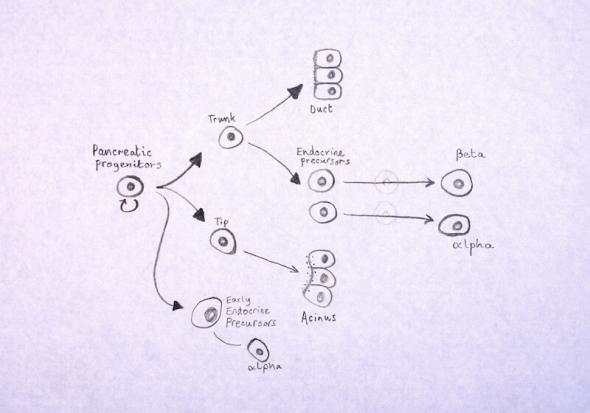
用多能干細胞制造胰島樣簇
人類胰島移植研究表明,與僅由 β 細胞組成的簇相比,由 α 細胞和 β 細胞組成的人類胰島具有更好的葡萄糖刺激胰島素分泌和代謝功能。當葡萄糖水平過高時,β 細胞會分泌胰島素以響應葡萄糖。相反,當葡萄糖水平過低時,α 細胞會分泌胰高血糖素,以引導葡萄糖從肝臟釋放到血液中。當這兩種細胞類型在治療中協同工作時,它們將對血液中的葡萄糖水平產生更精細的調節反應。
因此,由 β 細胞和 α 細胞混合組成的胰島樣簇可能優于僅將 β 細胞移植到患者體內。正如本文前面提到的,β 細胞可以從人類多能干細胞中產生。同樣,使用類似的分化方案,可以從多能干細胞中生成 α 細胞。
保護細胞免受免疫系統侵害

目前正在努力尋找封裝移植細胞以保護它們免受免疫攻擊的最有效方法。目前,一些研究小組和商業公司(ViaCyte 和 Beta-O 2 Technologies)參與了臨床 1 期研究,以制造一種膠囊,該膠囊允許葡萄糖和其他營養物質向內運輸和胰島素向外運輸,同時保護細胞免受免疫系統。
Viacyte 目前正在測試兩種設備:
PEC-Direct (VC-02):血管可以進入設備并使植入的細胞血管化。仍然需要免疫抑制劑。
PEC-Encap (VC-01):植入的細胞包含在設備中。氧氣、葡萄糖、胰島素和其他激素可以在植入的細胞和設備外部的血管之間傳播。在該設備中,植入的細胞受到免疫系統的保護。
Beta-O2 Technologies 基于水凝膠,水凝膠充當封裝細胞的支架。
探索降低免疫反應的藥物、疫苗或細胞的工作也在進行中。
這項工作的結果可以通過與β細胞移植相結合來創造更好的療法。
說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議,如有版權等疑問,請隨時聯系我。




 掃碼添加微信
掃碼添加微信