間充質干細胞 (MSC) 一直是無數臨床研究的主題,涉及從克羅恩病到移植物抗宿主病 (GVHD) 等各種病理學。
基于間充質干細胞的療法已經可用于治療一系列疾病或醫療狀況。從自身或捐贈者獲得的自體或同種異體間充質干細胞在醫療實踐中各有優點和缺點。
目前,人們正在研究干細胞在治療許多無法治療的疾病中的潛在廣泛用途。如今,現代治療策略愿意使用不同來源的間充質干細胞(MSC)。研究人員越來越意識到間充質干細胞的性質及其使用的新可能性。
由于其特性,特別是其自我再生、分化成多種細胞譜系和參與免疫調節的能力,間充質干細胞已成為開發現代有效的未來治療策略的有前途的工具。間充質干細胞的巨大潛力和可用性使其在治療許多疑難雜癥方面具有多種臨床應用。除了其許多優點和好處外,間充質干細胞的使用仍然存在問題。
間充質干細胞的作用機制是什么?他們如何到達目的地?間充質干細胞臨床應用安全嗎?這些是當間充質干細胞被視為治療工具時出現的主要問題。
一文梳理丨間充質干細胞-來源-安全性-優缺點
間充質干細胞的多樣性、其不同的臨床應用以及尚未徹底研究的許多特征是關于這些細胞的討論和爭議觀點的來源。在這里,我們回顧了目前關于間充質干細胞的治療潛力、臨床效果和臨床應用安全性的知識。
什么是間充質干細胞?
20世紀60年代,弗里登斯坦等人發現了一種在體外形成克隆集落的成纖維細胞(CFU-F,Colony Forming Unit-Fibroblast)。弗里登斯坦的觀察發現了一種特殊類型的細胞,目前被稱為間充質干細胞(MSCs)。間充質干細胞是原生的、非特化的、非造血的可塑性粘附細胞,具有巨大的增殖潛力和自我更新及分化能力。
2006年,國際細胞治療學會(ISCT)提出了定義人類多能間充質基質細胞的基本標準,間充質干細胞的名稱由此演變而來。
間充質干細胞在標準培養條件下具有可塑性粘附特性,并具有向成骨細胞、軟骨細胞和脂肪細胞三系分化的能力,此外,95%以上的間充質干細胞對三種特異性表面標志物–CD73(SH3/4)、CD90(Thy-1)和CD105(SH2)–呈陽性,不表達CD45、CD34、CD14、CD11b、CD79a、CD19或主要組織相容性復合體(MHC)II類。
間充質干細胞還表達其他標記物,包括 CD9、CD10、CD13、CD29、CD44、CD49、CD51、CD54(ICAM-1)、CD117(c-kit)、CD146(MCAM)、CD166(ALCAM)和 Stro-1,但這些標記物的特定組合表達似乎取決于宿主組織。盡管已經發現了多種描述間充質干細胞的陽性標記物,但還沒有一種標記物被認為是間充質干細胞的特異性標記物。
還應注意的是,不同來源的間充質干細胞在分化和增殖方面的潛力可能有很大差異。有研究認為,這些差異是間充質干細胞所處的特定微環境直接影響的結果。
盡管描述間充質干細胞的報道越來越多,但關于間充質干細胞的正確鑒定卻出現了許多爭議。ISCT提出的標準似乎并不充分,因為從不同組織中分離出來的間充質干細胞在分化、增殖能力和細胞表面表達等方面都代表了一個相對異質的細胞群體。
間充質干細胞的來源
目前,間充質干細胞可以從多種來源中分離出來 (圖1)。
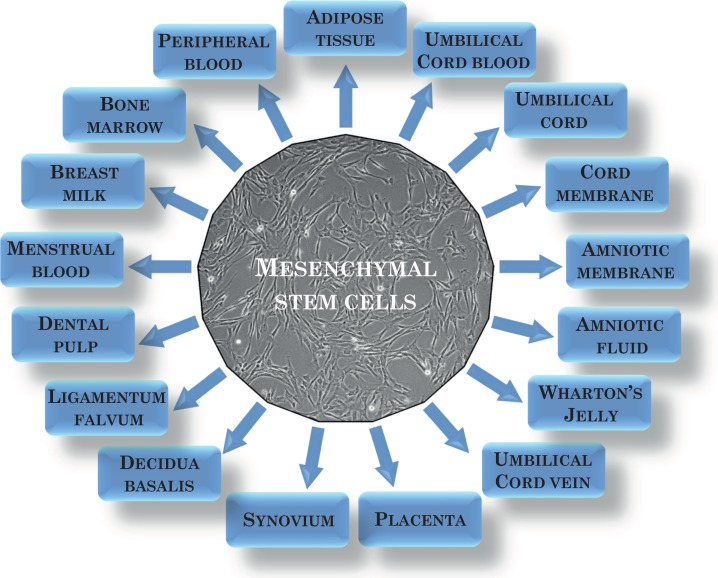
截至近日,已提出新的間充質干細胞來源。間充質干細胞存在于牙髓、牙周膜、肌腱、皮膚、肌肉和其他組織中(圖1)。然而,分離效率存在差異,這與供體組織的可用性、狀況和年齡有關。一個非常重要的問題是供體細胞的年齡。從年輕供體獲得的細胞不易受到氧化損傷和變化的影響,它們在培養物中的老化速度要慢得多,并且增殖率更高。
目前,許多研究集中在間充質干細胞在細胞治療中的應用。間充質干細胞被用作治療關節退行性變化以及重建骨骼和軟骨的工具,并用于整形外科、美容醫學、心血管疾病、內分泌和神經系統疾病、細胞移植以及受損肌肉骨骼組織的修復。由于這些細胞的特殊性質,例如快速增殖、高分化能力以及遷移到損傷部位的能力,新的臨床應用正在接受測試。
干細胞治療的新方法是使用細胞外囊泡 (EV),它可以用作MSC的替代品。EVs作為治療載體具有旁分泌作用,無需細胞直接參與。它們從干細胞中釋放出來,并向靶位點提供許多成分,例如mRNA、DNA 和蛋白質。最近的許多研究都描述了這種方法但仍然需要對干細胞外泌體的作用機制有透徹的了解。
間充質干細胞的遷移和歸巢
間充質干細胞的治療效果取決于其到達損傷部位的能力,而這種能力是由于間充質干細胞能夠遷移、粘附和移植到目標組織中。影響間充質干細胞歸巢治療效果的因素有很多。其中,培養條件、傳代次數、供體年齡、輸送方法和宿主的接受能力起著重要作用。
細胞療法的功效很大程度上取決于遞送方法。最常見的MSC給藥方法是靜脈輸注。然而,在細胞到達目標之前,大多數細胞被困在各個器官的毛細血管內,尤其是肺部。這種損耗可以用以下事實來解釋:MSC是相對較大的細胞并表達各種粘附分子。盡管間充質干細胞可能被困在肺部,但大量證據表明它們能夠歸巢于受損組織。
有趣的是,最近的數據還表明,盡管存在與靜脈輸注相關的問題,但這種途徑與其他 MSC 輸送方式具有相似的功效。在某些情況下,動脈內注射似乎是更有效的途徑。研究表明,與通過靜脈給藥相比,通過頸內動脈輸送MSC可以更有效地促進其遷移和歸巢到受傷的大腦中。與該遞送途徑相關的風險包括可能在微血管中出現的閉塞。當間充質干細胞直接輸送到心臟受損區域附近時,到達梗塞周圍區域的細胞數量要高得多。
如前所述,有效的間充質干細胞療法的必要條件是細胞能夠到達損傷部位并歸巢到受影響的組織。毫無疑問,特定的受體和粘附分子以及與內皮細胞的相互作用在這種遷移和歸巢過程中起著至關重要的作用。細胞粘附蛋白在質膜中表達,如整合素,參與細胞與細胞外基質蛋白(EMC)(如膠原蛋白、纖連蛋白和層粘連蛋白)的粘附。
體內研究表明,間充質干細胞具有趨化特性,靜脈注射后能夠附著在內皮細胞上,并在炎癥條件下上調的因子作用下在內皮細胞之間向損傷組織遷移。然而,它們的跨內皮遷移(TEM)、透射以及向損傷和炎癥部位歸巢的詳細機制尚未得到詳細解釋。據推測,這種機制可能與白細胞的機制類似(圖2),但有不同的粘附分子參與。
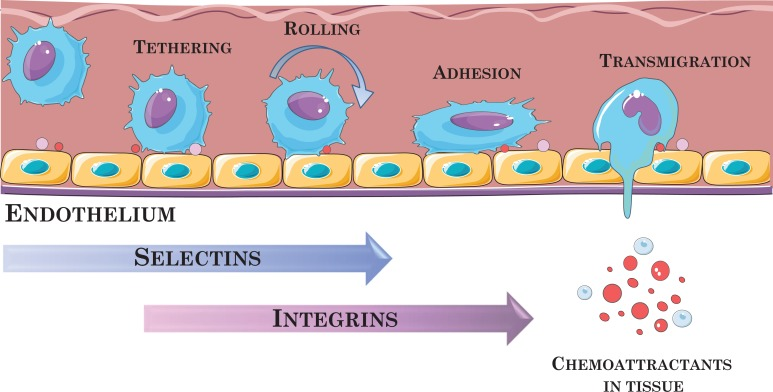
間充質干細胞的免疫學特性
一般認為,間充質干細胞不具有免疫原性,因此無需免疫抑制即可移植到異基因宿主體內。間充質干細胞的作用機制基于其免疫調節特性和免疫抑制活性。它們能夠抑制免疫系統不同細胞的增殖和活化。這些相互作用可能直接發生(即細胞-細胞相互作用),也可能間接發生(通過可溶性因子),而且這種抑制途徑與間充質干細胞和T細胞之間的MHC匹配無關。間充質干細胞的免疫調節作用體現在許多T細胞特性上,如活化和增殖,從而有效抑制免疫反應。
一般認為,間充質干細胞不具有免疫原性,因此無需免疫抑制即可移植到異基因宿主體內。間充質干細胞的作用機制基于其免疫調節特性和免疫抑制活性。它們能夠抑制免疫系統不同細胞的增殖和活化。這些相互作用可能直接發生(即細胞-細胞相互作用),也可能間接發生(通過可溶性因子),而且這種抑制途徑與間充質干細胞和T細胞之間的MHC匹配無關。間充質干細胞的免疫調節作用體現在許多T細胞特性上,如活化和增殖,從而有效抑制免疫反應。
間充質干細胞療法的安全性
迄今為止,已經進行了許多研究來調查基于MSC的療法的安全性。臨床試驗表明,體外培養的人類間充質干細胞不易受到不良變化的影響。
加拿大的一個小組分析了使用BM-MSC的臨床試驗。在對36項研究進行徹底分析后,他們發現MSC的使用與致瘤潛力之間沒有關系,并且沒有報道該療法的嚴重副作用。
Karussis等人還研究了MSC治療的安全性和影響。多發性硬化癥和肌萎縮側索硬化癥患者。在一項持續25個月的研究中,在34名接受檢查的患者中,沒有觀察到治療造成的嚴重不良反應。此外,20名患者在移植后1年接受了檢查,MRI結果沒有顯示任何令人不安的變化。然而,需要對使用間充質干細胞療法的安全性進行更長期的研究和觀察。
間充質干細胞生物學的缺點
間充質干細胞(MSCs)作為一種治療工具,雖然在許多疾病治療中展現出潛力,但也存在一些明顯的缺點和潛在風險:
- 治療效果的不確定性
- MSCs的治療效果可能因個體差異而有所不同。不同的患者在接受相同MSC治療時,可能觀察到不同的療效,這需要進一步的研究和臨床試驗來驗證。
- 高昂的治療成本
- MSCs療法的成本較高,包括干細胞的采集、分離、培養和處理等步驟,這些過程需要高技術和設備支持,導致治療費用昂貴。對于普通患者而言,經濟負擔較大。
- 潛在的副作用
- 盡管MSCs療法相對安全,但仍存在一些潛在的副作用和風險。例如,干細胞移植可能引發感染、排異反應或系統性過敏等問題。此外,干細胞在體內的行為尚未完全掌握,存在一定的未知風險。
- 技術與法規的挑戰
- MSCs療法的推廣和應用面臨技術和法規方面的挑戰。干細胞的培養和擴增技術需要不斷優化,同時,干細胞療法的安全性和有效性需要得到充分驗證。此外,相關法規和監管政策也需進一步完善,以確保干細胞療法的規范應用。
這些缺點和潛在風險提示在臨床應用中需要謹慎考慮MSCs的使用,并可能需要進一步的研究和臨床試驗來克服這些挑戰。
間充質干細胞生物學的優點
間充質干細胞(MSCs)是一種多功能干細胞,具有多種潛在的治療應用,以下是間充質干細胞的一些主要優點:
- 免疫調節能力:MSCs能夠調節免疫系統,降低移植排斥反應的風險,這使得它們在同種異體移植中特別有用。
- 組織修復和再生:MSCs能夠遷移到損傷部位,并分化成多種類型的細胞,有助于組織和器官的再生。這種能力使得MSCs在治療關節退行性疾病、骨折愈合和心肌修復等方面具有潛力。
- 易于獲取和培養:MSCs可以從多種組織中分離出來,如骨髓、脂肪組織、臍帶等,且這些細胞在體外培養中相對容易維持。
- 低免疫原性:與其他類型的干細胞相比,MSCs的免疫原性較低,這意味著它們在治療過程中不太可能引起強烈的免疫反應。
- 廣泛的應用范圍:MSCs在臨床試驗中已被用于治療多種疾病,包括心血管疾病、神經系統疾病、糖尿病等,顯示出了良好的安全性和療效。
- 倫理優勢:與胚胎干細胞相比,MSCs的獲取不需要涉及胚胎,因此在倫理上更為可接受。
這些優點使得MSCs成為再生醫學和細胞治療領域的重要研究方向。
結束語
干細胞無疑是治療多種疾病的巨大希望。由于它們存在于許多成體組織中并且不會引起倫理問題,因此它們比胚胎干細胞具有巨大的優勢。由于其獨特的功能,例如易于分離和培養、在許多組織中的可用性、免疫調節特性以及其使用不存在倫理問題,我們相信它們可用于自體和同種異體移植。
根據我們的數據,間充質干細胞的同種異體臨床應用似乎是再生醫學中有前途的工具。
參考資料:Musia?-Wysocka A, Kot M, Majka M. The Pros and Cons of Mesenchymal Stem Cell-Based Therapies. Cell Transplant. 2019 Jul;28(7):801-812. doi: 10.1177/0963689719837897. Epub 2019 Apr 24. PMID: 31018669; PMCID: PMC6719501.
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請及時跟本公眾號聯系,我們將在第一時間處理。



 掃碼添加微信
掃碼添加微信