近年來,急性和慢性肺部疾病的發病率和死亡率持續攀升,已成為全球性公共衛生負擔。然而,現代醫學對炎癥相關肺部疾病的治療方法仍存在局限,緩解病情并實現肺組織再生修復成為亟待解決的關鍵科學問題。
間充質干細胞(MSCs)憑借其抗炎、抗凋亡及促進組織再生的能力,已被廣泛應用于多種炎癥性疾病的治療研究。基于MSC的療法在再生醫學領域日益受到重視,顯示出作為肺部疾病理想治療策略的潛力。在肺損傷動物模型中,MSCs表現出顯著的組織修復效果,其機制涵蓋減輕肺泡上皮與內皮細胞炎癥、降低通透性、增強肺泡液體清除能力以及抑制氧化應激等多個方面。
MSCs被廣泛研究的一個重要原因在于其強大的免疫調節功能,能夠通過調控先天性與適應性免疫反應中多種免疫細胞的行為發揮作用。越來越多的證據表明,MSCs可通過調節中性粒細胞、巨噬細胞、T細胞和B細胞等免疫細胞,顯著緩解多種肺部疾病的病理進程。
近日,浙江中醫藥大學附屬第一醫院(浙江省中醫院多個科室在《Nature》上發表題為“Mesenchymal stem cells for lung diseases: focus on immunomodulatory action”的綜述文章,系統回顧了間充質干細胞通過免疫細胞調控緩解肺部疾病的證據[1]。

該文從MSCs的免疫調節特性出發,總結了其在先天性與適應性免疫中的具體作用機制,并探討了MSCs在三大肺部疾病治療中的臨床研究進展。
間充質干細胞對肺部疾病期間先天免疫反應的影響
中性粒細胞
中性粒細胞的激活與募集在急性肺損傷(ALI)的病理機制中起到關鍵作用。在急性炎癥過程中,中性粒細胞通過多步驟募集級聯迅速從血液遷移至炎癥部位,是最早到達損傷區域的免疫細胞。盡管中性粒細胞在宿主防御和清除細胞碎片中具有重要作用,其過度活化卻會釋放大量毒性物質,包括活性氧(ROS)、促炎細胞因子(如NF-κB、IL-1β、IL-17)及蛋白酶,進一步放大炎癥反應并導致組織損傷。因此,靶向中性粒細胞已成為ALI治療的新策略。
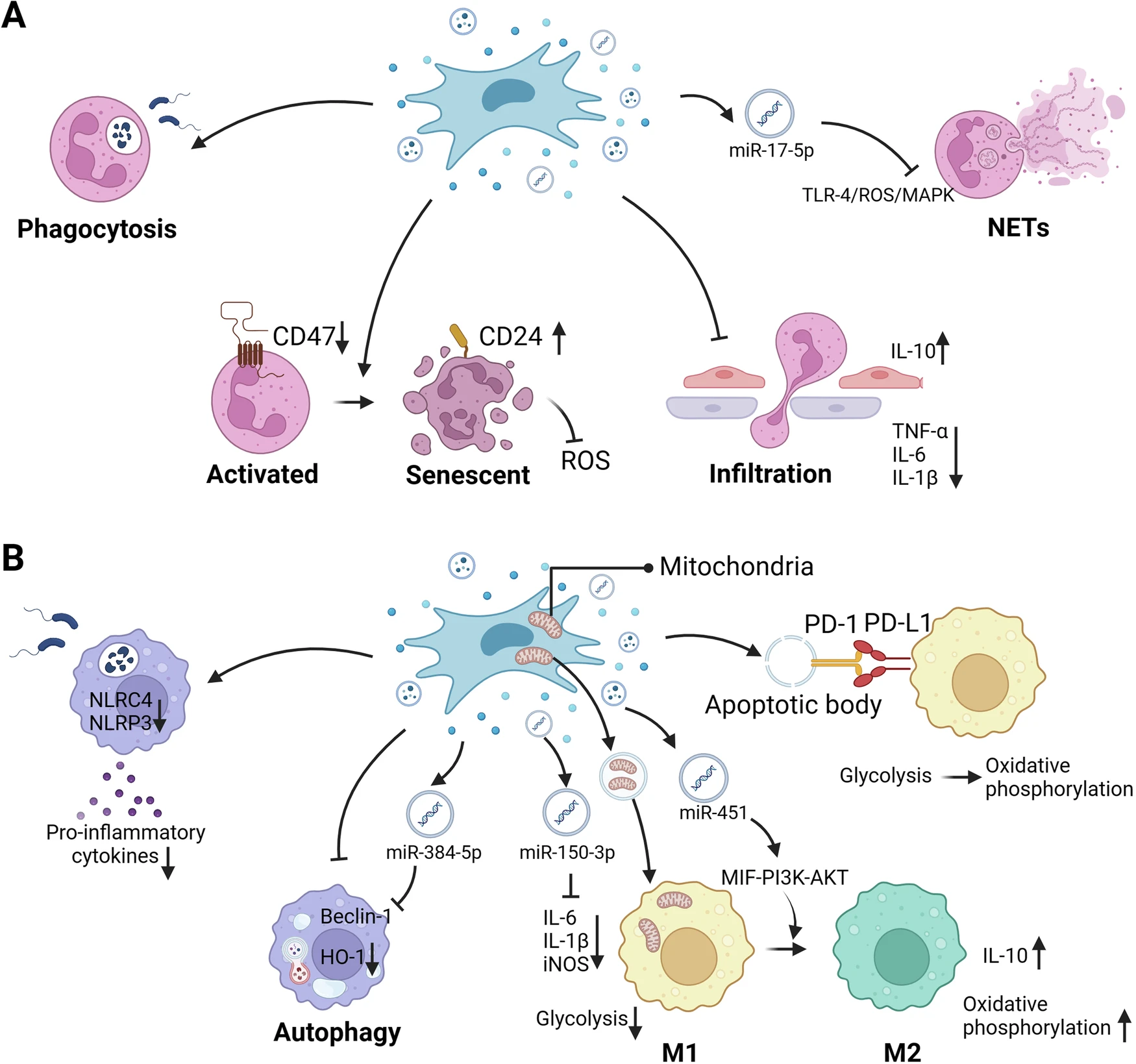
多項研究表明,MSCs能夠多方面調控中性粒細胞反應:抑制其遷移與浸潤,降低ROS及炎癥因子的釋放,并通過上調CD24表達促使活化的中性粒細胞向衰老類型轉化,從而緩解氧化應激與組織損傷。此外,MSCs及其外泌體還可通過抑制中性粒細胞胞外陷阱(NET)的形成,阻斷TLR-4/ROS/MAPK信號通路,避免炎癥反應的進一步加劇。
巨噬細胞
肺組織中的巨噬細胞在炎癥反應中起著核心作用。多項臨床前研究表明,MSCs及其分泌因子可以通過靶向巨噬細胞來修復肺組織損傷(表1、圖1B)。MSCs及其胞外囊泡可以減少巨噬細胞的浸潤,降低巨噬細胞中促炎細胞因子的水平,提高抗炎因子的水平,并提高其吞噬功能,最終改善肺組織損傷。
嗜酸性粒細胞
哮喘是一種慢性炎癥性氣道疾病,嗜酸性粒細胞在其中發揮著重要作用。嗜酸性粒細胞是參與過敏性疾病的末端效應細胞。在接收到刺激信號后,嗜酸性粒細胞通過釋放各種免疫調節因子(如細胞因子、趨化因子、生長因子和細胞毒性蛋白)發揮免疫調節和促炎功能。
多項研究表明,MSCs同樣展現出免疫調節作用。它們不僅能降低氣道內嗜酸性粒細胞數量,緩解過敏性炎癥和氣道重塑,還可通過外泌體遞送miR-146a-5p抑制ILC2活化,減少嗜酸性粒細胞持續性增多。
綜上,MSCs通過多靶點、多機制干預先天免疫細胞功能,有效緩解肺部疾病的炎癥反應和組織損傷。
MSCs對肺部疾病期間適應性免疫反應的影響
T細胞
CD4?T細胞是適應性免疫反應中的主要細胞,在機體發育與穩態維持中發揮重要作用。
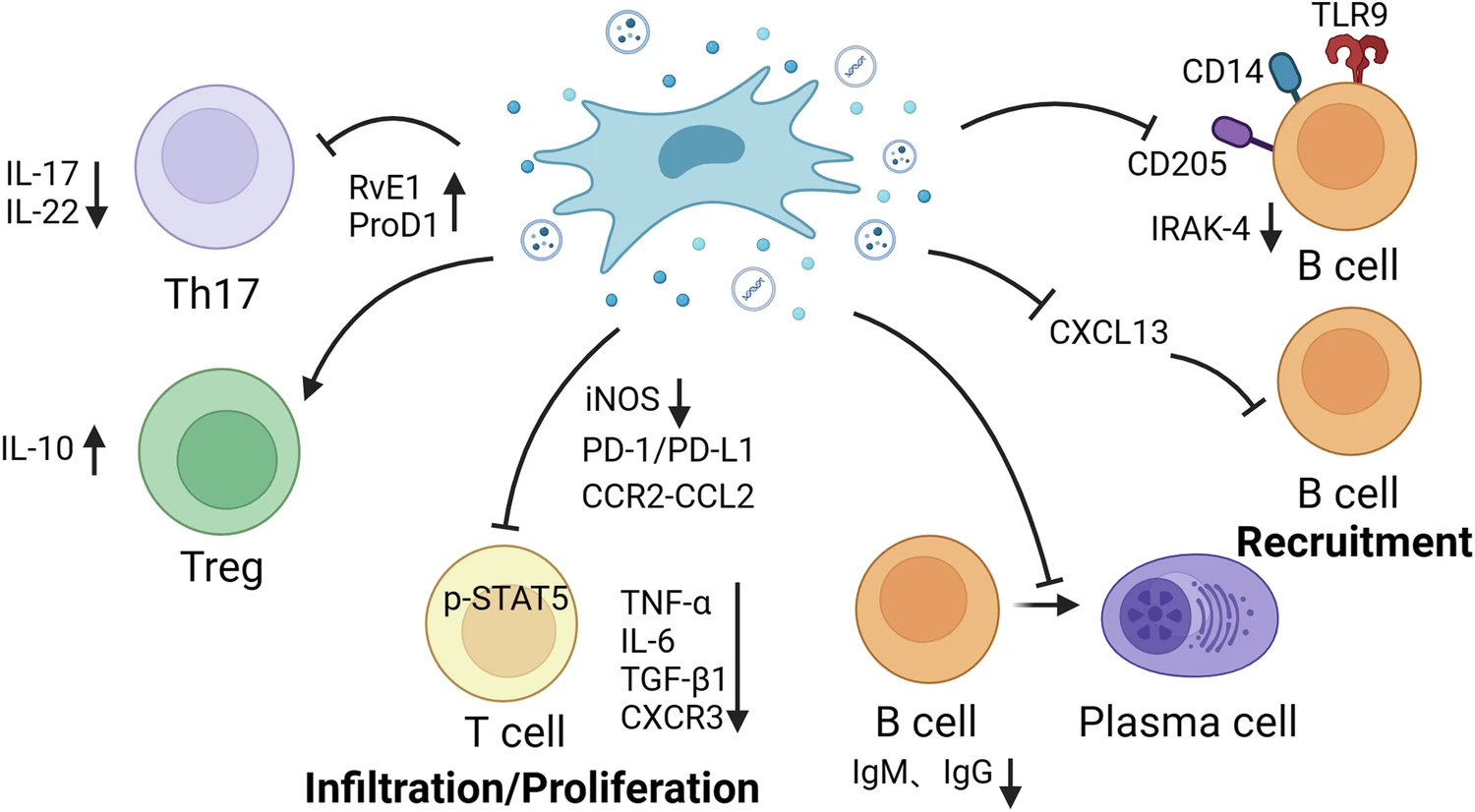
在肺部疾病中,MSCs通過調控CD4?T細胞亞群平衡 來緩解炎癥和組織損傷。Tregs具有抗炎和促進修復的作用,而Th17細胞則通過分泌IL-17加劇炎癥和組織損害。MSCs能抑制初始CD4?T細胞向Th17分化,減少IL-17、IL-22的產生,同時誘導Tregs增加,提升IL-10、Foxp3表達,從而恢復Th17/Treg平衡,促進肺泡上皮修復并減輕肺損傷。
此外,MSCs還能作用于CD8?T細胞和CD3?T細胞,通過PD-1/PD-L1通路抑制其浸潤和促炎因子釋放,從而減輕纖維化并改善肺功能。同時,MSC治療降低CXCR3表達,減少CD8?T細胞趨化和中性粒細胞浸潤,進而緩解炎癥反應。研究顯示,MSCs移植不僅能改善急性肺損傷,還能減輕博來霉素或百草枯誘導的肺纖維化,體現出其在調控適應性免疫反應中的多重保護作用(表2、圖2)。
B細胞
B細胞在適應性免疫反應中既能作為抗原提呈細胞,又能分泌多種細胞因子,并分化為抗體分泌的漿細胞。其在呼吸系統疾病中的浸潤和IgM、IgG、IgE等免疫球蛋白的產生與疾病嚴重程度密切相關。研究表明,MSCs能抑制B細胞的增殖與漿細胞分化,減少免疫球蛋白的生成,并下調相關基因(如Iglc2、Iglc3、Ighd)的表達,從而減輕炎癥和肺損傷。
此外,MSCs還能通過調控B細胞相關趨化因子的表達影響免疫反應。例如,MSCs可抑制ALI小鼠中B細胞分泌CCL4,減少中性粒細胞的募集;胎膜來源MSCs(HAMSCs)則通過抑制CXCL13干預肺纖維化中B細胞的募集與歸巢。
同時,MSCs還能降低CpG誘導的B細胞傳感器(CD205、TLR9、CD14)的表達,抑制下游炎癥信號通路,進一步發揮免疫調節和抗炎作用。
干細胞治療3大肺部疾病的臨床試驗
01、干細胞治療慢阻肺疾病的臨床研究
2024年,吉美瑞生超級器官研發中心首席科學家、同濟大學醫學院/附屬東方醫院左為教授與廣州醫科大學附屬第一醫院鐘南山院士、李時悅教授團隊及陸軍軍醫大學附屬西南醫院戴曉天教授合作在《Science》子刊《Science Translational Medicine》期刊發表了題為“Autologous transplantation of P63+ lung progenitor cells for chronic obstructive pulmonary disease therapy”(移植自體P63陽性肺前體細胞用于慢性阻塞性肺病的治療)的研究論文[2]。

研究表明,經氣道基底層干細胞治療后,超過70%的慢阻肺病患者的肺換氣功能顯著改善、運動能力提升。此外,長期隨訪顯示,慢阻肺病患者生存期在治療后明顯延長,最早的患者目前已隨訪到治療后第9年。該論文是第一個正式發表的基于肺臟再生機理的細胞治療臨床試驗,證實了氣道基底層干細胞移植能夠顯著提升患者的肺換氣功能,實現肺功能的逆轉與再生修復。
2025年3月24日,首例慢阻肺病患者在上海交通大學醫學院附屬瑞金醫院海南醫院順利完成了干細胞治療,由周敏教授完成支氣管鏡給藥操作[3]。
該患者因慢性阻塞性肺疾病長期活動受限,經推薦接受自體氣道基底層干細胞移植治療。該療法由左為教授團隊基于R-Clone專利技術自主研發,治療過程包括:從患者氣道健康區域提取成體干細胞,體外擴增約1個月后,通過支氣管鏡精準回輸至肺部受損區域。該技術安全、簡便,僅需一次治療,便能帶來長期療效。
02、干細胞治療哮喘的臨床研究
2025年6月,《Medicine》報道一例54歲女性患者,在接受Regentime干細胞療法后,不僅踝關節骨關節炎癥狀改善,哮喘也獲臨床緩解。該患者通過吸入途徑接受干細胞治療,喘息與呼吸困難癥狀在治療后一個月消失,并維持緩解超過24個月[4]。

03、干細胞治療肺纖維化的臨床研究
2025年1月,由上海交通大學醫學院附屬第六人民醫院、浙江大學醫學院附屬第一醫院、蘇州大學生物與基礎醫學學院等多個單位聯合完成的研究,首次在臨床上應用小氣道自體干細胞移植治療難治性IPF,取得了顯著突破,并在國際頂級醫學期刊《柳葉刀》子刊《eBioMedicine》上發表[5]。

自體基底細胞移植顯著改善肺功能:這項研究以三名晚期特發性肺纖維化(IPF)患者為對象,利用支氣管鏡獲取其小氣道基底細胞(BC),在體外擴增后再回輸至患者體內。
結果顯示,所有患者在治療后肺功能均有顯著改善,特別是在肺活量(FVC)和小氣道功能方面表現突出。治療24周后,三位患者的FVC分別由42.2%、53.3%和42.5%提升至50.5%、70%和52.7%。值得注意的是,彌散能力(DLCO)在回輸24小時后即明顯上升,并能長期維持。
在小氣道功能方面,患者的50%呼氣流量(FEF50)和最大呼氣流量(PEF)等指標均有明顯提升。CT影像學結果進一步證實了療效:肺容量增加、肺密度降低,炎癥反應及過度沉積的細胞外基質被吸收,間質纖維化明顯緩解。整體來看,基底細胞移植有效改善了肺通氣和彌散功能,為晚期IPF的治療提供了新的思路。
這項研究的意義:研究提出了一種用于IPF管理的新型細胞治療方法,強調了進一步研究近端和遠端BC在IPF進展中的具體特征的必要性。從近端氣道分離的功能性BC能夠增強IPF患者的肺功能,這表明它們有可能成為一種有效的治療選擇,并可能引發IPF治療的范式轉變。這項研究提供了基礎數據,支持未來開展更大規模臨床試驗的需求。
結論
肺部疾病目前仍缺乏有效的治療方法,研究人員正在努力尋找新的有效藥物。
MSC及其衍生的分泌蛋白組對肺部疾病具有保護作用,提示可能是一種潛在的治療方法。免疫細胞在肺部疾病的進展中起著至關重要的作用。MSC具有免疫調節特性,可以作用于中性粒細胞、巨噬細胞、T細胞和B細胞,并在肺部疾病期間的先天性和適應性免疫反應中發揮作用。
然而,MSC及其分泌蛋白組在臨床應用中面臨諸多挑戰,例如異質性、體內轉化不安全、存活率低以及缺乏標準化的胞外囊泡分離、提取和儲存方法。未來需要開展更全面的基礎研究和更大規模的臨床試驗來解決這些問題。
參考資料:
[1]:Feng, Y., Lu, J., Jiang, J. et al. Mesenchymal stem cells for lung diseases: focus on immunomodulatory action. Cell Death Discov. 11, 52 (2025). https://doi.org/10.1038/s41420-025-02303-4
[2]:https://www.science.org/doi/10.1126/scitranslmed.adi3360
[3]:肺干細胞治療前沿技術落地!上海交大瑞金醫院(海南醫院)正式啟用氣道基底層干細胞治療慢阻肺病新技術
[4]:Boulos RT, Najjoum CF, Mansour VJ, El Asmar EA, Abi Chahine NH. The Regentime stem cell procedure efficacy in asthma treatment: A case report. Medicine (Baltimore). 2025 Jun 13;104(24):e42887. doi: 10.1097/MD.0000000000042887. PMID: 40527844; PMCID: PMC12173279.
[5]:https://www.thelancet.com/journals/ebiom/article/PIIS2352-3964(24)00574-7/fulltext
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加微信
掃碼添加微信