最近的研究表明,間充質干細胞 (MSC) 因其免疫調節和再生特性以及實驗動物模型中有限的副作用,對于患病或受傷肺部的細胞治療非常重要。臨床前研究表明,MSC還通過調節其活性、增殖和功能對免疫細胞產生顯著影響,而免疫細胞在多種肺部疾病的發病機制中起著重要作用。
間充質干細胞在治療肺部疾病中進展;從研究到臨床
近日,浙江大學聯合悉尼大學生物醫學工程學院、德克薩斯A&M大學在《Am J Stem Cells》期刊雜志發表了一篇“基于間充質基質細胞的肺部疾病療法;從研究到臨床”的文獻綜述。綜述討論了近期臨床和臨床前研究中關于間充質干細胞在治療一些常見且研究較為深入的肺部疾病方面的作用的關鍵研究成果。

成果表明干細胞技術不僅在治療肺部疾病方面展現了巨大的潛力,同時它也正在成為治療各種疑難性/難治性疾病的新方式。
介紹
間充質基質細胞 (MSC) 是一種分布廣泛、具有自我更新能力的多能細胞群,常用于各種臨床試驗(表格1) 因其再生能力而被用于細胞療法。此外,間充質干細胞的治療潛力源于其能夠分化成許多不同類型的細胞、在體外能夠快速增殖、免疫原性降低以及能夠分泌多種可用于組織修復和再生的生物元素。盡管MSC在體外共培養體系中的免疫原性較低,但它們仍然可以引發免疫反應。
此外,MSC可對氧濃度、pH值的變化和微環境中的其他變化作出反應,產生多種營養和免疫調節因子,這些因子在組織修復和再生中起重要作用。間充質干細胞可以從多種來源分離并用于臨床前和臨床應用。
| ClinicalTrials.gov 標識符 | 病癥或疾病 | 干預/治療 | 實際入組人數 | 主要終點 | 主要結果測量 |
|---|---|---|---|---|---|
| NCT03137199 | 哮喘 | 同種異體人類間充質基質細胞 (hMSCs) | 3名參與者 | 輸注后第4周 | 治療期間出現嚴重不良事件的參與者人數 |
| NCT02192736 | 哮喘 | 臍帶間充質基質細胞的營養因子 | 20名參與者 | 1個月 | 發生不良事件的患者人數 |
| NCT01902082 | 急性呼吸窘迫綜合征(ARDS) | 同種異體脂肪來源的 MSCs | 20名參與者 | 從治療開始第 0天至第28天 | 比較間充質基質細胞治療組和安慰劑組的不良事件 |
| NCT01385644 | 特發性肺纖維化 (IPF) | 胎盤間充質基質細胞 (MSC) | 8名患者 | MSC輸注后6 個月 | 與基線相比,用力肺活量 (FVC) 評估的肺功能百分比變化 |
| NCT02013700 | 特發性肺纖維化 (IPF) | 同種異體成人人類間充質基質細胞 (hMSC) | 9名參與者 | 輸液后一個月 | 任何治療引起的嚴重不良事件 (TE-SAE) 的發生率 |
| NCT01919827 | 特發性肺纖維化 (IPF) | 源自骨髓的自體間充質基質細胞 | 17名患者 | 最長12個月 | 出現不良副作用的參與者人數 |
多種組織、器官和液體(如骨髓、羊水、脂肪組織、胎盤、臍帶血、皮膚和肺)均可用于分離MSC。這些特性使MSC成為修復和再生病變肺部的主要細胞類型。培養的MSC可以抑制免疫反應,并分化為II型肺泡上皮細胞(AT2)。此外,MSC既能介導組織再生,又能抑制炎癥,這是其用于治療多種主要呼吸系統疾病的基礎,例如特發性肺纖維化 (IPF)、哮喘、慢性阻塞性肺病 (COPD) 和急性呼吸窘迫綜合征 (ARDS)?。
由于MSC具有強大的抗炎和免疫抑制作用,它在肺部疾病方面具有明顯的臨床意義。許多最近的臨床和研究表明,MSC是治療多種常見肺部疾病的有前途的方法。
間充質干細胞在治療肺部疾病中進展:從研究到臨床
因此,本文的目的是回顧和討論最近臨床和臨床前研究中關于間充質干細胞在治療常見肺部疾病方面的作用的關鍵研究成果。
- 我們在本文中擴展了討論范圍,包括基于間充質干細胞的治療已深入研究的肺部疾病的潛在機制。
- 此外,我們回顧了間充質干細胞在減輕肺損傷/炎癥和促進損傷后肺泡細胞再生方面的近期應用。
- 我們還描述了基于間充質干細胞的療法在治療肺炎、ARDS、COPD、哮喘和纖維化等主要肺部疾病中的作用。
間充質干細胞治療肺部疾病的機制
01、間充質干細胞具有強大的旁分泌和免疫調節作用,通過旁分泌作用分泌多種蛋白、小肽、核酸等來介導對炎癥反應的抑制作用。
在治療感染性肺部疾病的過程中,通過免疫調節作用,間充質干細胞可發揮抗炎、抗凋亡以及抗微生物作用,能有效的保護肺內皮和肺泡上皮細胞,增強肺泡液清除,抑制肺纖維化。
自新冠疫情暴發以來,國內國外發表的多項關于間充質干細胞治療新型冠狀病毒肺炎的臨床研究也都證實了間充質干細胞具有抗炎和免疫調節功能,能抑制重癥患者體內由冠狀病毒引發的細胞因子風暴,改善患者肺部纖維化,促進肺組織損傷修復,顯著降低新冠肺炎的死亡率,利用間充質干細胞治療新型冠狀肺炎重癥患者效果顯著。
多項臨床研究均顯示,間充質干細胞治療在抑制炎癥風暴,改善和修復肺部損傷情況有明顯的積極作用,同時安全性和有效性都得到了初步驗證。
02、間充質干細胞可以通過分泌受體拮抗因子IL-1來改善肺部纖維化,并且間充質干細胞還可以分泌大量促血管生成因子和抗細胞凋亡因子包括bFGF、VEGF、PlGF、MCP-1等,表明間充質干細胞可以幫助毛細血管結構的重生成和抵抗內皮細胞的凋亡。
目前特發性肺纖維化的治療效果并不是很理想,診斷后患者的平均生存周期只有3-5年。而間充質干細胞的治療則為這些飽受疾病折磨的患者帶來了新的希望。
針對特發性肺纖維的特征,即間質炎癥和上皮細胞損傷,間充質干細胞表現出抑制連續的損傷和改善肺部功能的效果,到目前為止,來自臨床前動物實驗的數據給人極大的鼓舞和希望,并且臨床試驗中未報告嚴重不良事件,再次表明間充質干細胞移植治療特發性肺纖維化的安全性和可行性。
03、干細胞,是人體自然的“治愈細胞”,它們能減少人體內的炎癥反應。而炎癥是造成很多疾病的根源,所以,通過利用自己的細胞減少炎癥非常可行,且安全無副作用。
干細胞通過靜脈輸注等方式補充進患者身體后,會在體內循環到心臟,然后從心臟再到肺部。
這些進入到肺部的干細胞就會自主趨向炎癥反應高發的地方,發揮修復和控制炎癥的功效。干細胞可以釋放各種因子,來抵抗和抑制炎癥反應,并能再生新的細胞、組織,來有效修復肺部損傷,恢復肺部功能。
間充質干細胞在治療呼吸系統疾病方面的治療潛力
由于肺泡上皮屏障和肺泡 II 型 (AT2) 的破壞是肺部疾病患者的主要特征,因此 MSCs 在治療呼吸系統疾病中的應用是一個熱門且有趣的研究課題。本綜述的以下部分將描述基于 MSCs 的治療幾種主要肺部疾病的潛力。
間充質干細胞治療哮喘的臨床應用
哮喘是一種主要的慢性炎癥性肺部疾病,其特征是氣道慢性炎癥、支氣管黏膜腫脹和黏液分泌增加。為了應對氣道炎癥,活性肥大細胞和嗜堿性粒細胞會分泌多種趨化因子和炎癥細胞因子,包括IL-6、IL-1β、TNF-α和IL-4,以促進多種細胞類型在肺中的積聚,例如循環嗜酸性粒細胞、中性粒細胞和CD4+ Th2細胞。
活性中性粒細胞和嗜酸性粒細胞可釋放多種基質降解酶和細胞因子,通過促進支氣管收縮、細胞外基質沉積和上皮層降解來誘導支氣管高反應性和氣道重塑。此外,CD4+Th2細胞可以IL-5依賴的方式增強嗜酸性粒細胞的活化,并以IL-3依賴的方式促進氣道的高反應性以及杯狀細胞的化生(圖1)。
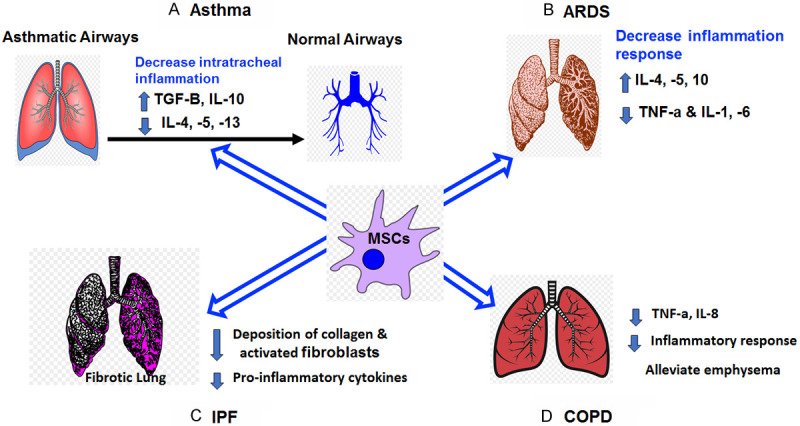
A. MSCs治療哮喘可以增加TGF-beta和IL-10,但減少細胞因子IL-4、IL-5和IL-13。
B. 使用MSCs治療ARDS可導致IL-4、IL-5和IL-10增加,但減少TNF-alpha、IL-1和IL-6。
C. MSCs治療IPF可減少膠原蛋白、活化成纖維細胞和促炎細胞因子的沉積。
D. 使用MSCs治療COPD可減少TNF-alpha、IL-8和炎癥反應,并減輕肺氣腫。
多項臨床研究已測試了MSC療法對哮喘患者的安全性和有效性。
一項臨床試驗NCT03137199測試了同種異體BM-MSC治療哮喘的安全性。該試驗涉及向兩組接受不同劑量的哮喘患者(共6名患者)靜脈注射BM-MSC。每4周評估和測試一次肺容量和功能、外周嗜酸性粒細胞增多和呼吸困難以及生活質量。
1期臨床試驗NCT03137199于2020年終止。有趣的是,NCT02192736臨床研究也在20名哮喘成人患者中測試了同種異體hUC-MSC衍生營養因子 (MTF) 等MSC衍生因子的安全性和有效性。1期臨床試驗NCT02192736也于2020年完成。
間充質干細胞治療的肺炎和急性呼吸窘迫綜合征緩解
ARDS(急性呼吸窘迫綜合征)是一種嚴重的肺部損傷,由于肺泡上皮屏障被破壞,液體積聚在肺內。ARDS的進展通常與其他生理變化有關,例如炎癥細胞浸潤和間質水腫,并可導致急性呼吸衰竭。這種呼吸衰竭的特征是基質沉積增強以及II型肺泡細胞、成纖維細胞和肌成纖維細胞增殖增加。
如果不進行藥物治療,ADRS可能危及生命,死亡率很高(34-44%)。值得注意的是,自2019年以來,SARS-CoV-2病毒感染一直是ADRS的主要原因。這種感染可破壞肺泡上皮細胞并誘導促炎細胞因子的分泌。
在一些臨床前研究中,MSC和MSC衍生的分泌蛋白組均已用于治療ARDS。由于革蘭氏陰性菌感染通常會導致ARDS發展,MSC可用于以旁分泌方式改善由LPS誘發的ARDS小鼠模型中肺泡的炎癥,而無需直接細胞接觸。
- 從機制上講,MSC可以通過IL-10依賴的方式介導炎性TNF-α表達水平的降低和中性粒細胞流入肺組織。此外,在ARDS損傷的肺中,MSCs可以通過分泌某些類型的生長因子和其他分子,如角質形成細胞生長因子 (KGF)、HGF、血管內皮生長因子 (VEGF)、血管生成素-1、白細胞介素 1 (IL-1) 受體拮抗劑 (IL-1RN)、前列腺素 E2 (PGE2),以及清除氧化物和自由基,促進AT2細胞再生和肺泡上皮屏障的修復(圖1)。
間充質干細胞治療急性呼吸窘迫綜合征的效力取決于某些免疫調節因素,這些因素可以降低MSCs向AT2樣細胞的分化。例如,研究表明,microRNA-615-3p和microRNA-155-5p可以調節免疫細胞的活性和細胞因子的產生,而過表達的microRNA-615-3p或microRNA-155-5p能夠通過Wnt/β-catenin通路減弱MSCs向AT2細胞的分化。
此外,間充質干細胞的治療潛力已在多項臨床試驗中得到評估(表格1) 通過測量ARDS的生物標志物(例如 IL-6、IL-8和SP-D)來治療ARDS。
其中一項臨床試驗由Fizsimmons等人進行,表明單獨靜脈輸注同種異體骨髓間充質干細胞 (BM-MSC) 可使9名ARDS患者耐受,且未出現劑量限制性毒性或臨床不穩定性,并顯著減少肺損傷。
臨床研究表明,輸注最多300萬個細胞/千克MSC不會升高促炎性細胞因子水平,同時會暫時抑制促炎性細胞因子,這表明與先天免疫相關的機制。I期和II期臨床研究也評估了間充質干細胞移植治療中度至重度ARDS的安全性和有效性。
基于間充質干細胞治療特發性肺纖維化 (IPF) 的方法
與其他器官相比,肺臟的再生能力有限,這是眾所周知的特征之一。目前的藥物對肺纖維化無效。因此,FDA批準的幾種治療藥物(如尼達尼布和吡非尼酮)只能減緩特發性肺纖維化患者肺功能的衰退。
IPF的發病機制與肺上皮細胞穩態失衡有關。多項研究表明,肺泡上皮異常損傷可激活肺泡上皮細胞 (AEC) 分泌凝血、促纖維化和炎性細胞因子,這些細胞因子激活成纖維細胞增殖并分化為肌成纖維細胞,從而分泌形成細胞外基質 (ECM) 的蛋白質。成纖維細胞增生、反復性肺損傷、AT2細胞凋亡增加、細胞外基質沉積增強以及上皮-間質細胞相互作用異常均已被多項臨床研究確認為IPF病理改變。上皮-間質轉化可破壞肺結構,導致纖維化進展和肺功能衰竭。然而,引發IPF的因素仍然未知,目前正在研究中,包括可引起AT2細胞功能障礙、從而導致纖維化的環境和遺傳因素。
MSCs被廣泛認為是特發性肺纖維化 (IPF) 的潛在治療方法,因為它們可以促進AT2細胞的生成,減少降解酶的分泌,并抑制肺部浸潤的免疫細胞產生促纖維化因子。有趣的是,MSCs的給藥可以通過抑制膠原積累、炎性細胞因子產生和成纖維細胞增殖來預防放射引起的肺纖維化。
間充質干細胞治療肺纖維化的臨床試驗
MSCs用于各種臨床試驗(表格1) 因其在治療肺纖維化方面的安全性和有效性而受到高度重視。
例如,一項著名的臨床試驗 ( NCT01385644 ) 在其I期研究中重點研究了來自胎盤的間充質基質細胞 (PL-MSC) 在治療特發性肺纖維化 (IPF) 中的治療和治愈潛力。在這項研究中,8名患者每公斤體重靜脈注射100萬或200萬個PL-MSC。參與研究的患者對兩種劑量(100萬或200萬個PL-MSC)的耐受性良好。
另一方面,PL-MSC注射對這些患者的IPF沒有影響。在另一項I期臨床研究 (NCT02013700) 中,9名IPF患者靜脈注射了2000萬、1億或2億個同種異體MSC,并觀察了近14個月。不幸的是,本研究中接受治療的患者中有2人死于IPF,另外5人報告了各種副作用。相比之下,支氣管內注射來自脂肪組織的同種異體AT-MSC是一種安全的治療方法,可以改善IPF患者的健康和生活參數,并且在接受MSCs治療的兩年內沒有引起這些患者嚴重的副作用。
2021年,一項針對輕度至中度IPF患者的I期多中心臨床試驗 ( NCT01919827 ) 評估了通過支氣管內注入自體BM-MSC的可行性、有效性和安全性。該臨床試驗的結果表明,盡管通過支氣管內注入的BM-MSC細胞不能立即在IPF患者中引起顯著的不利影響,但相當多的患者在功能和臨床方面均經歷了改善。
基于間充質干細胞治療慢性阻塞性肺病
COPD(一種慢性阻塞性肺病)是一種慢性炎癥性疾病,可導致肺部氣流阻塞。COPD的定義是肺實質惡化導致肺氣腫,終末支氣管惡化導致肺部阻塞性支氣管炎,以及由于有害氣體或顆粒物導致氣流受限。導致 COPD發展的其他變化包括氧化應激的幾種改變、浸潤肺部的免疫細胞以及活性蛋白酶與其抑制劑之間的平衡。吸煙史、氣道高反應性和父母哮喘史都是COPD發展的主要危險因素。體外研究表明,吸煙也會影響吸煙者COPD的免疫調節能力。
間充質干細胞治療慢阻肺病的作用機制
由于MSC具有抑制有害免疫反應、維持氧化穩態和控制降解基質的酶活性的獨特能力,因此在多項實驗和臨床研究中已顯示出治療COPD的潛力。在通過彈性蛋白酶滴注或香煙煙霧暴露誘發的COPD動物模型中,輸注脂肪組織-MSC和BM-MSC顯示出對COPD治療安全且有希望的結果。基于MSC的治療還可以減少支氣管周圍、肺泡隔和血管周圍間質中的炎癥細胞數量。
間充質干細胞治療慢性阻塞性肺病的臨床試驗
對62名COPD患者進行同種異體人類間充質干細胞治療可以抑制炎癥,因為這些患者的血清C反應蛋白水平降低 。然而,與未接受治療的COPD患者相比,這些治療并沒有顯著改變肺功能或生活質量指標。
值得注意的是,另一項臨床研究 (ISRCTN70443938) 表明,系統性給予hUC-MSC可以改善COPD患者的生活質量。
此外,Hoang等人最近進行的一項研究為COPD患者建立了同種異體hUC-MSCs(I/II 期)匹配病例對照試驗。
間充質干細胞在治療肺病中的應用最新進展
近三年來,間充質干細胞在肺部疾病和研究中的應用進展迅速。此外,外泌體和細胞外囊泡在呼吸系統疾病中的應用也受到了越來越多的關注。例如,來自MSC的外泌體miR-7704被用于調節實驗性急性肺損傷。這一發現有助于更好地了解外泌體miRNA在肺部炎癥性疾病中的治療潛力。
值得注意的是,基于間充質干細胞的療法有望通過膽堿能抗炎途徑緩解衰老和急性呼吸窘迫綜合征。此外,MSC衍生的細胞外囊泡可以重新編程ARDS疾病模型中的巨噬細胞,并在調節COVID-19誘發的缺血事件后的炎癥反應、治療急性肺損傷和急性呼吸窘迫綜合征以及治療COVID-19疾病方面具有潛在益處。
最近的臨床試驗(表格1) 評估了脂肪來源的間充質干細胞治療嚴重細菌性肺炎的有效性和安全性。 他們發現這些干細胞在這種嚴重肺炎中耐受性良好。 同樣,MSCs在其他呼吸系統疾病患者(如COPD、ARDS和COVID-19患者)中的治療選擇也有充分的報道。
有趣的是,最近的一項I期研究評估了同種異體MSC輸注在囊性纖維化患者中的耐受性和安全性,發現同種異體MSC靜脈輸注耐受性良好且安全。此外,華通氏膠衍生的MSCs是肺纖維化患者的潛在療法。值得注意的是,用MSC或MSC衍生的細胞外囊泡治療新生兒可改善肺結構、減少肺部炎癥、減輕肺纖維化、提高存活率,并治療支氣管肺發育不良。
最終結論和未來方向
MSCs具有免疫調節和再生特性,并且在實驗動物模型中副作用有限,因此是疾病和/或受損肺部的細胞療法所必需的。免疫細胞在多種肺部疾病的發病機制中起著關鍵作用。MSCs通過調節這些免疫細胞的活性、增殖和功能對其產生顯著影響。MSCs可以抑制肺部浸潤的免疫細胞和有害的免疫反應。
總之,基于干細胞的肺部疾病治療方法正在持續進步,而且發展速度很快,包括特發性肺纖維化、哮喘、慢性阻塞性肺病和其他疾病。事實上,臨床前研究積累的數據和結果表明 MSC 在這些疾病中具有治療潛力。一些早期臨床試驗表明MSC給藥是安全的,這些試驗中幾乎沒有報告不良反應。
這項研究將對MSC應用產生重大影響,因為迄今為止,人們對移植MSC的命運知之甚少,而且很少有臨床試驗顯示患者的臨床改善時間超過12個月。還需要對移植MSC在較長時間后的生物分布進行更多研究,以進一步解釋MSC的長期臨床影響。
參考資料:Yuan D, Bao Y, El-Hashash A. Mesenchymal stromal cell-based therapy in lung diseases; from research to clinic. Am J Stem Cells. 2024 Apr 25;13(2):37-58. doi: 10.62347/JAWM2040. PMID: 38765802; PMCID: PMC11101986.
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加微信
掃碼添加微信