腦癱(Cerebral Palsy, CP)是一種由胎兒或嬰幼兒期腦損傷或發育異常引起的運動和姿勢障礙疾病,目前尚無根治方法。近年來,干細胞治療因其潛在的神經修復和再生能力,成為腦癱治療領域的研究熱點。然而,不同年齡段的腦癱兒童接受干細胞治療的療效也存在差異顯著,這與大腦發育階段的可塑性、干細胞類型、治療時機及技術手段密切相關。
本文結合最新臨床研究數據,探討干細胞治療在不同年齡段腦癱兒童中的療效差異及影響因素。

腦癱兒童的黃金治療期:為何干細胞療法越早治療效果越好?
一、年齡相關的療效差異機制
1.神經可塑性窗口:嬰幼兒(0-3歲)大腦處于高速發育期,神經可塑性極強,干細胞更易整合到新生神經網絡中,促進運動及認知功能重建。研究表明,3歲以下患兒治療后神經突觸密度可增加20%-30%,而青少年(>10歲)僅增加5%-10%。
2.干細胞歸巢效率:嬰幼兒血管通透性高,干細胞更易穿過血腦屏障,歸巢效率較青少年高3倍。例如,臍帶血干細胞在嬰幼兒腦損傷區域的滯留率可達60%,而青少年僅20%。
3.炎癥微環境差異:嬰幼兒腦組織炎癥反應較輕,干細胞分泌的抗炎因子(如IL-10)能更有效抑制神經損傷后的慢性炎癥,而青少年因長期繼發性損傷,微環境中促炎因子(如TNF-α)水平較高,削弱干細胞修復效果。
二、不同年齡段的臨床療效數據對比
2024年中旬,土耳其干細胞研究中心在國際知名期刊《世界臨床病例雜志》發表了一項臨床研究成果,題為《同種異體間充質干細胞可能是治療腦癱的一種可行方法》。
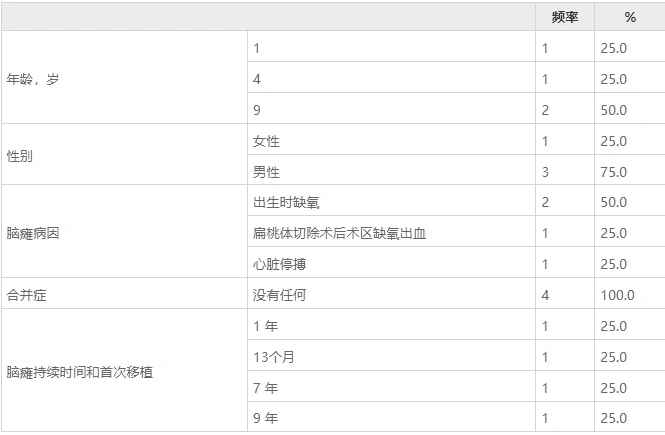
該研究旨在探討年齡對干細胞療法治療腦癱療效的影響,納入了四名腦癱患兒,年齡分別為1歲、4歲及兩名9歲兒童。所有受試者均接受了臍帶來源的同種異體間充質干細胞治療,并在治療后1周、1個月、2個月、4個月及12個月的時間點進行多時點療效評估。

方法:我們的樣本包括四名腦癱患者,他們在沒有外部支撐的情況下無法站立或行走。所有這些病例均接受了六次同種異體MSCT,使用臍帶源性MSC(UC-MSC)進行鞘內、靜脈內和肌內注射,劑量為1×106/kg。我們使用Wee功能獨立測量 (WeeFIM)、粗大運動功能分類系統 (GMFCS) 和手動能力分類量表 (MACS) 儀器對患者治療前和治療后進行監測和評估。我們使用改良阿什沃斯量表 (MAS) 來測量痙攣狀態。(見表1)
病例1:嬰幼兒期
患者是一名1歲女童因出生時缺氧被診斷為腦性癱瘓。治療前評估顯示:WeeFIM評分為18(反映日常生活能力嚴重受限),MAS評分為14(雙側肌張力顯著增高),GMFCS和MACS均為5級(提示嚴重運動功能障礙)。該患者使用UC-MSCs接受了六次同種異體MSCT,分別為1×106/kg IT、IV和IM。
治療四個月后,她的WeeFIM認知評分增加了1,MAS評分(兩側)下降了1。此外,她的GMFCS和MACS分數下降至3。在第二次和第三次應用后,患者沒有表現出任何副作用,除了持續約12小時的低熱,并在冷敷后消退。
病例2:兒童期
第二例患者是一名4歲男性因1年前扁桃體切除術期間出血導致缺氧,被診斷為腦性癱瘓(CP),伴有嚴重痙攣。治療前評估顯示:WeeFIM評分為18(日常生活能力重度受限),MAS評分為21(雙側肌張力極度增高),GMFCS和MACS均為5級(提示極重度運動功能障礙)。患者接受6次異基因臍帶間充質干細胞(UC-MSCs)治療,劑量為1×10?/kg,通過鞘內(IT)、靜脈(IV)和肌肉(IM)聯合給藥。
干預后他的WeeFIM評分沒有變化,但他的MAS評分從術后第一周開始下降,最終達到兩側18。他的GMFCS和MACS分數下降至3。該患者在整個隨訪期間沒有表現出任何副作用。
病例3:青少年期
患者是一名9歲男性,出生11個月后因不明原因心臟驟停被診斷為癱。治療前,該病例的WeeFIM評分為18分(日常生活能力重度受限),MAS評分為28分(提示雙側肌張力極度增高),GMFCS評分為5分(極重度運動功能障礙),MACS評分為5分(極重度運動功能障礙)。除了肢體痙攣外,患者還表現出明顯的軀干痙攣并呈伸肌姿勢。他使用UC-MSC接受了六次同種異體MSCT,分別為1×106/kgIT、IV和 IM。
干預后他的WeeFIM分數沒有變化,但他的MAS分數在四個月時下降了3分(雙方)。患者的GMFCS和MACS評分沒有改善。同樣,該病例在使用3次后沒有出現任何副作用,除了低熱,冷敷后約12小時內退燒。
病例4:青少年期
最后一個病例是一名9歲男性,被診斷患有CP,因出生時缺氧而發生。治療前,他的WeeFIM評分為48分(提示中度日常生活能力受限),MAS 評分為17分(肌張力顯著增高),GMFCS評分為4分(提示中重度運動功能障礙),MACS評分為4分(提示中重度運動功能障礙)。他使用UC-MSC接受了6次同種異體MSCT,劑量為1×106/kgIT、IV和IM。
從第二個月開始,該患者的WeeFIM運動評分顯著增加了32分,MAS評分(兩側)下降了2分。此外,干預后他的GMFCS和MACS分數下降至兩分。至于副作用,患者在注射后僅感到注射部位暫時疼痛。
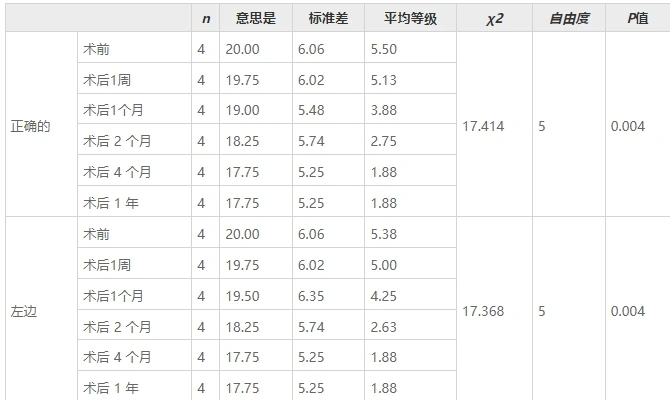
綜上所述,年齡是決定療效的關鍵因素。
嬰幼兒期(0-3歲)患兒(病例1)展現出最顯著的改善:運動功能(GMFCS/MACS等級從5級降至3級)、肌張力(MAS評分下降1分)及認知功能(WeeFIM認知評分提升)均明顯提升,這與嬰幼兒大腦高度可塑性密切相關,干細胞可能通過促進神經修復和再生實現功能重建。
相比之下,兒童期(4歲,病例2)和青少年期(9歲,病例3、4)患兒療效差異顯著:兒童期MAS評分下降3分但運動功能改善有限,而青少年期患者中,病情較輕者(病例4)運動功能(WeeFIM運動評分激增32分)和功能分級(GMFCS/MACS降至2級)改善明顯,但病情極重度者(病例3)僅實現MAS評分小幅下降,運動功能無改善。這表明,青少年期患者對治療的響應高度依賴初始病情嚴重程度,輕癥患者仍可獲益,而重癥患者療效受限。
疾病嚴重程度與治療時機的協同作用同樣顯著。病例1和病例2初始評分均極低(WeeFIM均為18分),但嬰幼兒期患兒因年齡優勢獲得更顯著的功能恢復,而病例4初始病情較輕(WeeFIM 48分),盡管處于青少年期,仍實現運動功能的大幅提升。這一現象提示,早期干預(嬰幼兒期)和輕癥階段是提高療效的核心策略:
- 嬰幼兒期(0-3歲)是干細胞治療的最佳窗口期,此時神經可塑性最強,功能恢復潛力最大;
- 輕癥患者(如病例4)即使年齡較大,仍可通過干細胞治療獲得顯著改善,而重癥患者(如病例3)因病程進展及神經損傷不可逆性,療效受限;
- 對于年齡較大的患者,需優先篩選病情較輕者(如WeeFIM評分較高、GMFCS/MACS分級較低)以最大化治療獲益。
三、響療效的關鍵因素:年齡之外的變量
1. 干細胞類型與來源:精準選擇決定修復潛力
臍帶/臍血間充質干細胞(UC-MSCs/UCB):因其免疫原性低、易于獲取及多向分化潛能,成為嬰幼兒期腦癱患兒的首選。UC-MSCs可通過分泌神經營養因子(如BDNF、NGF)和抗炎因子(如IL-10)抑制腦損傷后的炎癥反應,促進神經保護與血管新生。
神經干細胞(NSCs):相較于UC-MSCs,NSCs具有更直接的神經再生能力,定向分化為運動神經元或基底節神經元,修復斷裂的神經環路,同時分泌GDNF等因子促進突觸連接與髓鞘修復,對神經元缺失主導的損傷(如缺氧缺血性腦病)更具潛力。
自體vs同種異體:嬰幼兒因免疫系統未成熟,對同種異體干細胞耐受性良好,可避免免疫排斥;而成人患者則需自體NSCs或誘導多能干細胞(iPSCs)以降低風險。
2.給藥途徑與劑量:靶向性與滲透性的平衡
靜脈注射(IV):是嬰幼兒期的首選途徑,因其操作簡便且安全性高。但干細胞通過血腦屏障的比例較低,需通過多次給藥。
鞘內注射/腦內移植:對青少年和成人更有效,尤其是NSCs的移植。鞘內注射可使細胞直接進入腦脊液循環,而立體定向腦內注射則能精準修復特定區域損傷。盡管創傷較大,但療效顯著。
鼻內注射NSCs::作為新興非侵入性途徑,鼻內給藥通過嗅神經通路直接將NSCs遞送至大腦,繞過血腦屏障,顯著提高靶向效率和細胞存活率。研究表明,鼻內注射NSCs后,細胞可遷移至損傷區域(如基底核或小腦),促進神經突觸修復和膠質瘢痕減少。此方法尤其適合嬰幼兒期和兒童期患者,因其創傷小、可重復給藥,且操作便捷。
劑量差異:劑量與療效呈正相關,但需權衡安全性。例如,UC-MSCs劑量達5×10?/kg時,神經修復效果最佳,但可能引發短暫發熱;而NSCs的劑量需根據損傷體積精確計算。
3.聯合治療與康復訓練:協同作用提升功能重塑
干細胞+康復訓練:神經可塑性是功能恢復的核心機制,干細胞與康復訓練的協同效應尤為關鍵。例如,UC-MSCs移植后配合重復經顱磁刺激(rTMS)或機器人輔助運動訓練,可顯著增強突觸可塑性和神經網絡重組。
早期干預:嬰幼兒期大腦可塑性最強,干細胞治療與康復的“黃金窗口”效應顯著。
多模式聯合療法:如NSC移植與基因治療的結合(如AAV介導的神經生長因子過表達),或干細胞與外泌體的聯合應用,可進一步放大修復效果。
結論:抓住黃金窗口,推動精準治療
干細胞治療為腦癱患兒提供了新的希望,但其療效與年齡密切相關:嬰幼兒期(0-3歲)是最佳治療窗口,青少年期需針對特定類型選擇方案。未來需通過技術優化、聯合康復治療及標準化評估體系,進一步提升療效并擴大適用人群。隨著中國在干細胞領域的加速布局(如臍帶血庫建設、臨床試驗推進),這一技術有望成為腦癱治療的“中國方案”,為全球患兒帶來福音。
相關閱讀:干細胞療法能否為腦癱帶來長期改善?205例患者揭示真相
參考資料:
Boyal? O, Kabatas S, Civelek E, Ozdemir O, Bahar-Ozdemir Y, Kaplan N, Savrunlu EC, Kara?z E. Allogeneic mesenchymal stem cells may be a viable treatment modality in cerebral palsy. World J Clin Cases. 2024 Mar 26;12(9):1585-1596. doi: 10.12998/wjcc.v12.i9.1585. PMID: 38576742; PMCID: PMC10989435.
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加微信
掃碼添加微信