背景:慢性腎臟病 (CKD) 是一個日益嚴重的公共衛(wèi)生問題,現(xiàn)有的治療方法不足以限制疾病進展。新的策略,包括基于再生細胞的療法,已經(jīng)成為治療的替代品。包括我們自己在內(nèi)的幾個小組的結(jié)果報告了間充質(zhì)基質(zhì)細胞 (MSC) 在CKD小鼠模型的功能恢復(fù)和組織損傷預(yù)防中的支持作用。在這些數(shù)據(jù)的推動下,開展了一項開放性試點研究,以評估單次注射自體脂肪組織來源的 MSCs (AT-MSCs) 治療CKD的安全性和有效性。

介紹
慢性腎臟病 (CKD) 的特征是腎功能進行性和永久性喪失。由于慢性腎臟病的發(fā)病率和患病率不斷增加、腎臟替代療法的高成本以及發(fā)病率和死亡率的顯著增加,慢性腎臟病代表了一個主要的公共衛(wèi)生問題。可用的藥物不能阻止疾病進展并具有重大風險,因此促使人們尋找新的治療策略。
間充質(zhì)基質(zhì)細胞 (MSC) 是多能基質(zhì)細胞,存在于血管化器官的血管網(wǎng)絡(luò)內(nèi),在全身具有廣泛的組織支持作用。在糖尿病腎病、部分腎切除術(shù)和同種異體移植物腎病的嚙齒動物模型中,已經(jīng)證實了間充質(zhì)干細胞在實驗性急性腎損傷以及慢性腎病中保護腎臟結(jié)構(gòu)和功能的能力。
間充質(zhì)干細胞的有益作用包括限制炎癥反應(yīng)、減少蛋白尿以及保護腎小管和間質(zhì)結(jié)構(gòu)。值得注意的是,全骨髓 (BM) 移植似乎沒有發(fā)揮類似的有益效果。CKD與干細胞數(shù)量和功能的喪失有關(guān),尤其是當患者進展到疾病末期時。證據(jù)還表明,與CKD和尿毒癥毒素(例如同型半胱氨酸或?qū)追樱┫嚓P(guān)的促炎狀態(tài)可以加速干細胞衰老和細胞凋亡。
最近的一項薈萃??分析表明,間充質(zhì)干細胞的療法在慢性腎病的臨床前模型中是有效的,并且全身施用間充質(zhì)干細胞被認為可以安全地治療人類的腎臟和心血管疾病。然而,間充質(zhì)干細胞療法在治療慢性腎病的臨床轉(zhuǎn)化仍處于早期階段,最佳細胞來源、給藥方式和預(yù)期臨床效果仍未得到很好的表征。
因此,我們開展了一項開放性試點研究,以評估單次注射自體脂肪組織來源的MSCs (AT-MSCs) 治療慢性腎病的安全性和有效性。
方法
自體脂肪間充質(zhì)干細胞以100萬個細胞/kg的劑量靜脈輸注到6名慢性腎病患者體內(nèi)。在間充質(zhì)干細胞輸注前和輸注后一年,患者病情穩(wěn)定并隨訪一年。
主要結(jié)果
慢性腎病功能參數(shù)的變化,包括間充質(zhì)干細胞輸注后12個月內(nèi)的GFR和定量24小時尿蛋白排泄率。由于這項研究的試點性質(zhì)和沒有對照組的小樣本量,變量在治療前12個月(控制期)進行測量,并與MSC給藥后12個月(干預(yù)期)的測量值進行比較。
次要結(jié)果
提示與治療相關(guān)的不良事件或警告的臨床或生化變化如下所述。
結(jié)果
輸液安全和患者隨訪
所有輸注均具有良好的耐受性,并且沒有報告與治療相關(guān)的不良事件。為評估疾病進展,患者在進入研究前12個月通過優(yōu)化和穩(wěn)定治療穩(wěn)定病情,然后隨訪一年。表1總結(jié)了所有數(shù)據(jù)。

蛋白尿測量
在治療前的12個月內(nèi),6名患者中有4名表現(xiàn)出蛋白質(zhì)排泄增加(增加20%至205%)。相反,在輸注MSC 后的12個月內(nèi),除4號腎發(fā)育不良患者外,所有病例的蛋白尿均從基線中位數(shù)0.75g/天(范圍0.15–9.57)下降至0.54(范圍,0.01-2.66克/天)輸注后第12個月(P=0.046)(圖2和補充表 1)。一名患者在輸注后表現(xiàn)出10%的下降,一名患者表現(xiàn)出60%的下降。值得注意的是,盡管MSC治療后患者4的蛋白質(zhì)排泄絕對水平?jīng)]有下降,但在MSC輸注后12個月內(nèi)觀察到的蛋白尿增加百分比僅為12%,而在輸注前12個月內(nèi)為205%,建議改進。
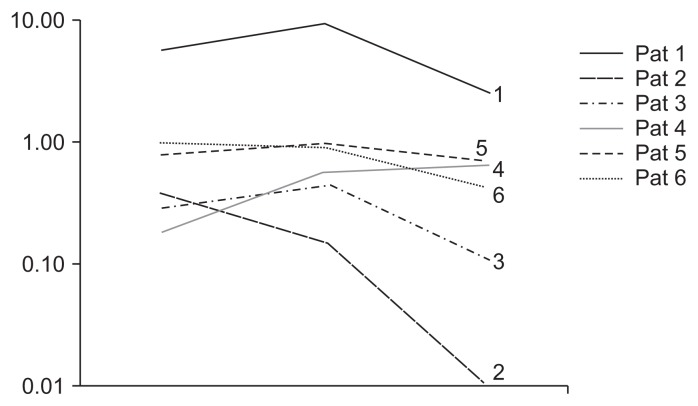
為了評估疾病進展的變化,患者 (Pat) 在進入方案之前通過優(yōu)化和穩(wěn)定治療穩(wěn)定了12個月,并在AT-MSC給藥后隨訪了一年。除患者4外,所有病例的蛋白尿均有所減少,從基線時的中位數(shù)0.75克/天(范圍0.15-9.57)到一個月時的中位數(shù)0.54(范圍0.01-2.66克/天)輸注后12 ( P=0.046)。為了簡化曲線,僅描繪了主要的三個時間點(治療前12個月、輸注時間、治療后12個月)。
肌酐和MDRD eGFR
總體而言,通過血漿肌酐水平和MDRD eGFR評估的腎功能在MSC輸注后12個月時有所下降,盡管這種下降沒有統(tǒng)計學(xué)意義 ( P=0.065)。除患者4外,所有病例的eGFR均略有下降,范圍為7.5%至49.0%。
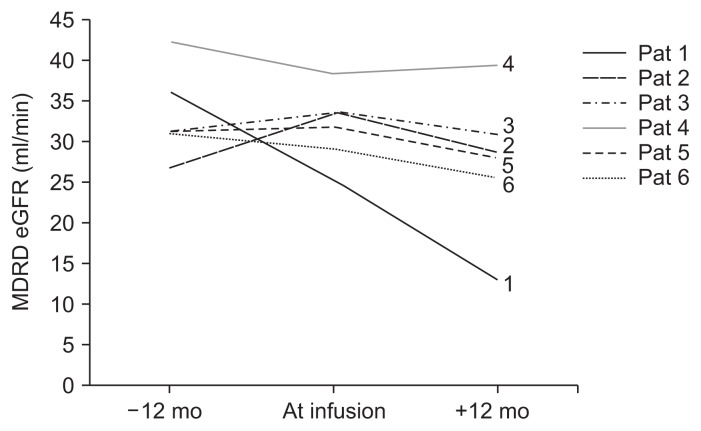
注射AT-MSC前后12個月時,通過血漿肌酐和MDRD估計的腎小球濾過率 (eGFR) 估計的腎功能。除患者4外,所有個案均顯示MDRD eGFR 略有下降,范圍從7.5%到 49%。每個患者治療前和治療后的回歸分析的eGFR斜率沒有顯著差異。為了簡化曲線,僅描繪了主要的三個時間點(治療前12個月、輸注時間、治療后12個月)。
討論
雖然并非所有6名患者的反應(yīng)都相同,但這些結(jié)果表明,自體AT-MSC輸注減少了6名患者的24小時蛋白尿,而沒有明顯的不良反應(yīng)。
關(guān)于干細胞治療慢性腎病的可能機制的證據(jù)越來越多。MSCs能夠自我更新、增殖和遷移到受損區(qū)域,在那里它們可以分化成成熟的功能細胞。由于在ivMSC輸注后可能會出現(xiàn)低水平的持續(xù)組織植入,因此人們認為治療益處主要由營養(yǎng)和/或免疫介導(dǎo)的作用來解釋。MSC的免疫活性由分泌分子和細胞間接觸介導(dǎo),并且可能涉及樹突狀細胞、B細胞、自然殺傷細胞和多種 T 輔助細胞。顯著的旁分泌和營養(yǎng)作用是由血管生成和抗細胞凋亡因子(如血管內(nèi)皮生長因子、胰島素生長因子和肝細胞生長因子)的分泌介導(dǎo)的。MSC產(chǎn)生的廣泛的分泌和免疫調(diào)節(jié)因子庫有可能促進腎臟再生,因為MSC條件培養(yǎng)基可以提供與直接細胞相當?shù)哪I臟保護作用。
結(jié)論
總之,我們報告了一項初步試驗研究,提供證據(jù)表明可以為慢性腎病患者的細胞治療生成自體脂肪間充質(zhì)干細胞,并且輸注治療不會在治療后的一年內(nèi)引起不良事件。
自體脂肪間充質(zhì)干細胞顯示出改變慢性腎病進展的潛力,因為治療減少了尿蛋白排泄,尿蛋白排泄是腎臟疾病進展的眾所周知的替代標志物。這種有希望的初步結(jié)果證明設(shè)計和進行未來的臨床試驗是合理的,這些試驗進一步評估自體脂肪間充質(zhì)干細胞治療慢性腎病的臨床反應(yīng)和分子機制,并評估反應(yīng)患者的特征以告知未來最好的治療候選人。



 掃碼添加微信
掃碼添加微信