帕金森病 (PD) 是最常見的神經退行性疾病之一,影響基底核,導致運動和認知功能受損。多巴胺能 (DAergic) 神經元的喪失或其變性以及路易體的聚集是這種疾病的標志。用于治療帕金森病的藥物可以緩解癥狀并維持生活質量,但目前尚無治愈方法。需要開發能夠有效阻止或逆轉神經變性的療法。
隨著細胞替代療法技術的快速進步,醫療專業人員正在努力尋找可以恢復多巴胺神經遞質的治療方法。由于間充質干細胞在體內含量豐富、具有增殖能力和免疫調節能力,研究人員已開始關注使用間充質干細胞 (MSC) 的細胞療法。在這里,我們回顧了基于間充質干細胞治療帕金森病的方法及其修復帕金森病患者多巴胺神經元的各種機制。

干細胞作為治療帕金森病的候選者
神經系統中神經元的進行性死亡稱為神經變性。最近的研究表明,神經元甚至在死亡之前就失去了其正常的結構和功能,這意味著簡單地阻止這些神經元死亡不太可能是一種成功的治療技術。因此,干細胞療法似乎是最成功的治療選擇。
1979年,將產前大鼠DAergic神經元移植到具有良好移植物存活和軸突生長的大鼠PD模型中,以改善運動障礙。這項研究證明,細胞療法可以恢復由輕微腦組織損傷引起的缺陷——一種將骨髓源性間充質干細胞(BM-MSCs)轉化為神經營養因子分泌細胞(NTFSCs)的程序,該細胞可釋放腦源性神經營養因子( BNDF)和膠質細胞源性神經營養因子(GDNF)已經建立。在PD細胞模型中,NTF-SC條件培養基提供了顯著的保護,并且在損傷后將NTF-SC移植到大鼠模型中導致移植細胞重新定位到受影響的部位并恢復受損的DAergic神經末梢系統在紋狀體中。
干細胞的類型
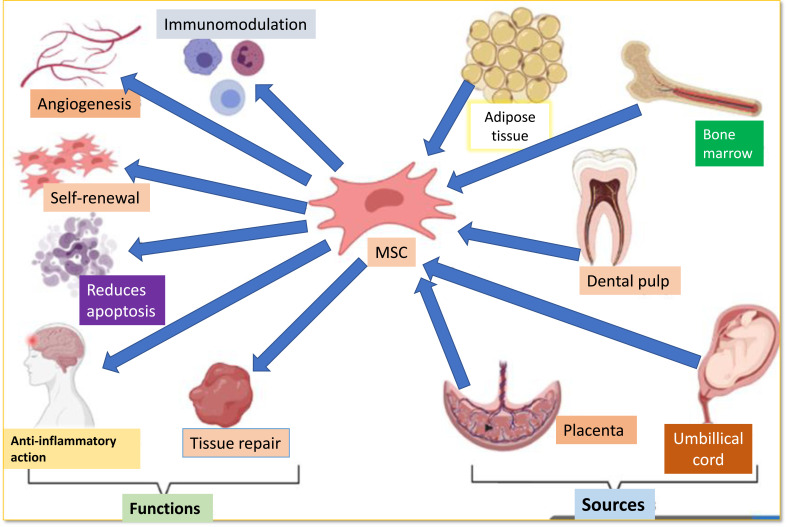
干細胞根據其分化和起源的分類如圖所示(11)。

不同類型的間充質干細胞比較
不同來源的間充質干細胞被發現具有一定的相似性,例如相同的表面標記和一些差異。因此,整理這些相似點和差異以確定哪一種最適合細胞治療至關重要。此外,對于干性相關基因,BM-MSC和脂肪組織源性MSC (AD-MSC) 具有非常相似的轉錄譜。臍帶源性干細胞(UC-MSCs)、BM-MSCs和AD-MSCs的表面抗原表達、分化能力和免疫抑制活性相同,但UC-MSCs表現出比其他細胞更高的增殖率和最低的表達量衰老標志物。另一方面,AD-MSCs的培養時間最短,增殖率最低。其他研究發現ADMSCs比BM-MSCs具有更大的增殖潛力,并且分化的AD-MSCs中神經標志物的表達更高。BM-MSCs中血管內皮生長因子 (VEGF)、轉化生長因子-β1 (TGFβ1) 等某些因子的分泌水平明顯高于AD-MSCs。
此外,UCMSCs比牙髓源性MSC(DP-MSCs)具有更高的增殖率,而DP-MSCs的細胞凋亡和衰老發生率較低,并且在傳代培養后其細胞形狀保持不變。此外,與BM-MSC相比,DP-MSC和源自人脫落乳牙(SHED)的干細胞表現出更好的神經發生分化能力。人子宮內膜干細胞(hEDSC)是PD治療中細胞療法的新來源。它們似乎可以通過簡單、安全、無痛的方法(如子宮頸抹片檢查)廣泛獲得和收集。
表格1:MSC的不同來源及其應用。
| 來源 | 差異勢 | 臨床應用 | 參考 |
|---|---|---|---|
| 骨髓 | [1] 脂肪細胞 [2] 胚胎組織 [3] 星形膠質細胞[4] 心肌細胞 [5] 成骨細胞 [6] 軟骨細胞 [7] 肝細胞 [8] 基質細胞 [9] 肌細胞 [10] 神經細胞 [ 11]系膜細胞 | ?通過多機制作用對抗PD病理生理學的治療潛力。 慢性缺血性中風 脊髓損傷 1 型糖尿病 大鼠肝硬化 放射胃腸道綜合征的治療 血液惡性腫瘤 器官修復 組織工程膀胱再生及纖維化預防 子宮內膜粘連的治療一只老鼠 | [ 41 – 49 ] |
| 脂肪組織 | ? 脂肪細胞 ? 骨細胞 ? 軟骨細胞 ? 肌肉細胞 | 心臟病發作后 心肌重建心肌修復骨 再生 神經系統重建 皮膚重建軟骨 修復 肝臟 重建 增強肝細胞癌的放療效果。 ? 骨關節炎 ? 促進傷口愈合 ? 中風 | [ 50 – 56 ] |
| 牙髓 | 成牙本質細胞 成骨細胞 脂肪細胞 軟骨細胞 神經源性細胞 肌源性細胞 | 不可逆性牙髓炎 治療人類牙槽骨缺損 牙周組織和骨損傷 的再生 肌源性血管的形成 遺傳性疾病 牙髓再生 | [ 57 – 62 ] |
| 羊水和胎盤 | AF-MSCs:神經干細胞脂肪細胞 成骨細胞 軟骨細胞 肝細胞 P-MSCs: 胰腺細胞 | AF-MSCs: 脊髓損傷和脫髓鞘疾病 神經元 再生治療 癌癥治療 通過抵抗DNA損傷改善卵巢功能 高氧肺損傷 缺血性 心臟損傷 腎管 壞死和急性膀胱損傷 P-MSCs 心臟疾病、潰瘍、骨修復 ? 自身免疫性疾病 ? 支氣管肺發育不良 | [ 63 – 69 ] |
| 出生源組織 | UC-MSCs: ? 脂肪細胞 ? 軟骨細胞 WJ-MSCs: ? DAergic 神經元 ? 軟骨細胞 | UC-MSCs: 肌肉骨骼疾病 脊髓損傷 APP 和早老素(PS1)雙轉基因小鼠 提高抗癌作用 軟骨再生 WJ-MSCs 腎損傷、肺損傷、骨科損傷、癌癥治療 傷口愈合和頭發生長 | [ 44 , 56 , 70 – 74 ] |
間充質干細胞治療帕金森病的作用機制
間充質干細胞是多能祖細胞,間充質干細胞可以分化為多巴胺神經元,這將有助于帕金森病患者丟失的神經元的功能恢復。一旦MSC被動員到受損部位,就會通過激活各種機制來參與組織修復和再生。在多項研究中,MSC的多效作用已被揭示,為它們提供了相當大的治療潛力。
- 由于間充質干細胞在體內的廣泛利用性、增殖能力和免疫調節特性,引起了對帕金森病感興趣的研究人員的極大關注。間充質干細胞具有多種發揮治療潛力的途徑。保護性神經營養因子、生長因子如血管內皮生長因子(VEGF)、胰島素樣生長因子1(IGF-1)、肝細胞生長因子(HGF)、腦源性神經營養因子(BNDF)、轉化生長因子-β(損傷部位的MSC會分泌TGF-β)、β-神經生長因子(β-NGF)、膠質細胞源性神經營養因子和成纖維細胞生長因子2(FGF-2)、抗凋亡因子和細胞因子。MSC可以通過產生白介素 (IL)-10和TGF-β39等抗炎細胞因子,以及抑制腫瘤壞死因子-α、干擾素-γ (IFN-γ) 等促炎細胞因子,從而以這種方式幫助修復PD患者的大腦。
- 通過旁分泌信號傳導和多能性,間充質干細胞還可以調節造血作用并促進組織再生。
- MSC可以分化成神經譜系,其中包括DAergic神經元前體。
- 由于受損的線粒體在DAergic神經元的神經變性中發揮著至關重要的作用,最近的研究表明MSC可以將線粒體轉運至受損部位,這表明了另一種可能在PD治療中發揮優勢的潛在機制。
- MSC治療不存在腫瘤轉化的風險,而且是安全的。
- 由于自噬溶酶體生成不足而導致的自噬功能障礙可能與神經毒素治療的PD模型中的DAergic細胞死亡有關。然而,MSC治療增強了自噬溶酶體的產生并抑制了α-syn的表達,可能增加了DAergic神經元對環境神經毒素的存活率。
研究表明,免疫系統可以識別并破壞PD患者大腦中異常積累的α-突觸核蛋白作為抗原。患者體內多種炎癥細胞因子增加。間充質干細胞在細胞遷移和免疫調節中的作用對于治療各種疾病將變得非常重要。在一定的培養條件下,MSC還可以發育成神經元樣細胞。研究結果顯示,運動功能得到極大改善。如圖(3) 顯示了MSC在PD中的機制。
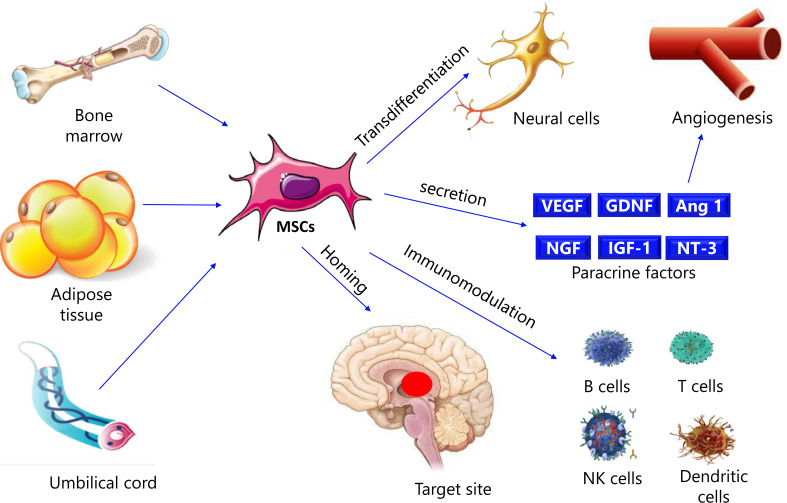
間充質干細胞誘發的多巴胺修復神經元的可能機制
成功的MSC治療涉及多種機制。外源性和內源性因素以多種方式共同作用,以協助恢復。外部因素對于干細胞(SC)至關重要,注射的細胞通過外部因素改變潛在的微環境,甚至整合到宿主神經元網絡中。內源性因素與宿主對SC引入的反應及其對SC行為和生存的影響有關。
MSC有兩個主要作用:由MSC分泌的多種營養因子和細胞因子介導的營養作用,以及分化形成多種細胞以恢復丟失的細胞。它們可以抑制免疫系統細胞的生長和激活。這些相互作用可以直接發生(即細胞與細胞相互作用)或間接發生(通過可溶性因子)。MSC可以通過被抗原呈遞細胞吞噬來調節免疫系統。根據最近的一項研究,抗原呈遞細胞(APC)隨后展示間充質干細胞抗原,導致一系列抗炎作用,從而增強治療過程的結果。
轉分化和融合:間充質干細胞與神經膠質細胞、神經元細胞、神經元干細胞以及星形膠質細胞或神經元條件培養基共培養,可以提高MSC分化為神經元的能力。Noggin、腦源性神經營養因子 (BDNF) 和Notch細胞內結構域 (NICD) 等基因的過度表達對神經發育和功能至關重要,也可以加速MSC神經轉分化。同樣,基于化學誘導、基因轉染、共培養和條件培養基的多種技術可用于將MSC轉化為DAergic神經元。
旁分泌因子的分泌:MSC被發現能分泌多種生長因子和細胞因子,對DAergic神經元具有神經營養和神經保護作用。因此,移植的MSC和激活的宿主細胞釋放的生長因子可能與MSC在許多動物PD模型中的治療作用有關。
與宿主細胞的相互作用:移植的MSC已被證明可以通過釋放旁分泌因子影響內源性神經干細胞 (NSC)、神經膠質細胞和血管,除了對宿主DAergic神經元有影響外,還有助于神經元組織修復和功能恢復。
間充質干細胞的免疫調節和抗炎作用:炎癥在PD病因學中的作用表明,MSC的免疫調節和抗炎作用可能有助于其在PD動物模型中移植后的治療效果。
干細胞治療帕金森病的臨床試驗
多巴胺替代藥物(L-DOPA 或左旋多巴)是人類PD的主要治療方法;然而,它具有副作用和缺點,即它無法阻止黑質中DAergic神經元損失的進展。在尋找DAergic神經元再生的方法時,用MSC治療人類實驗性PD模型所取得的積極成果凸顯了采用這種策略的潛力。
由于其免疫原性低、無畸胎瘤風險和倫理問題以及移植到人體后致瘤性低的可能性,使用間充質干細胞作為治療劑的臨床試驗正在進行中。如表2所示。
| 標題 | 研究類型 | 學習規劃 | 參加人數 | 給藥途徑 | 結果衡量 | 臨床試驗.gov ID |
|---|---|---|---|---|---|---|
| 研究骨髓間充質干細胞移植治療帕金森病的安全性和有效性 | 介入治療 | 單組作業 | 5 | 大腦的 | 使用 UPDRS(統一帕金森病評分量表)和時間測試評估患者臨床狀況的改善。 | NCT00976430 |
| 對PD患者進行自體骨髓來源的MSC的 I/II期試驗。 | 介入治療 | 單組作業 | 20 | 靜脈 | 經歷不良影響的參與者人數 | NCT01446614 |
| 自體間充質干細胞治療進行性核上性麻痹:一項隨機、雙盲、對照臨床試驗 | 介入治療 | 隨機化 | 25 | 動脈 | 不良反應的發生率 | NCT01824121 |
| 同種異體骨髓間充質干細胞治療特發性帕金森病的 I 期試驗研究 | 介入治療 | 非隨機 | 20 | 靜脈 | iPD 患者中同種異體 MSC 治療的安全性,由已確認與治療相關的不良事件的存在表明 | NCT02611167 |
| 臍帶間充質干細胞移植治療帕金森病患者的安全性和有效性研究 | 介入治療 | 單組作業 | 20 | 靜脈 | 統一帕金森病評定量表(UPDRS)的變化 | NCT03550183 |
| 間充質干細胞(MSC) 分化為神經干細胞(NSC) 對帕金森病 (PD)患者運動和非運動癥狀影響的安全性和有效性研究。 | 介入治療 | 隨機化 | 10 | 鞘內和靜脈內 | 注射引起的治療緊急不良事件 (TAEA) 的發生率 | NCT03684122 |
| 同種異體骨髓間充質干細胞作為特發性PD的疾病緩解療法:IIa 期雙盲隨機安慰劑對照試驗 | 介入治療 | 隨機化 | 45 | 沒有定義的 | 根據運動障礙協會統一帕金森病評定量表 (MDS-UPDRS) 第 III 部分測量的 MSC 的最安全有效劑量數 | NCT04506073 |
結論和未來展望
帕金森病是一種使人衰弱的退行性疾病,目前尚無法治愈。黑質致密部,其病理特征為DAergic神經元持續變性。
帕金森病可以通過多種方式治療,包括藥物治療和手術。然而,目前帕金森病還沒有有效的治療方法。通過多機制技術,當前的研究強調了間充質干細胞改善帕金森病發病機制的能力(免疫調節、抗炎和抗凋亡作用以及神經營養和神經源性潛力)。這些令人鼓舞的發現為間充質干細胞治療神經退行性疾病(尤其是PD)的臨床試驗鋪平了道路。
參考資料:Unnisa A, Dua K, Kamal MA. Mechanism of Mesenchymal Stem Cells as a Multitarget Disease- Modifying Therapy for Parkinson’s Disease. Curr Neuropharmacol. 2023;21(4):988-1000. doi: 10.2174/1570159X20666220327212414. PMID: 35339180; PMCID: PMC10227913.
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。




 掃碼添加微信
掃碼添加微信