持續的神經炎癥可能導致至少一部分受影響個體出現自閉癥譜系障礙 (ASD) 癥狀。間充質基質細胞 (MSC) 已證明具有調節神經炎癥的能力,但間充質干細胞治療自閉癥兒童的安全性和可行性尚未得到充分證實。
干細胞治療12名自閉癥患者,隨訪一年,50%患者癥狀有改善的跡象
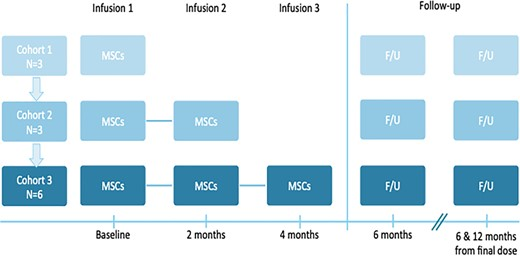
在這項開放標簽I期研究中,12名4至9歲之間的ASD兒童接受了人臍帶組織間充質基質細胞 (hCT-MSC) 靜脈 (IV) 輸注治療,這是一種由無關供體臍帶組織制成的第三方MSC產品。兒童每2個月接受一次、兩次或三次劑量的2×106個細胞/公斤。臨床和實驗室評估在基線和6個月時親自進行,并在最后一次輸注后12個月進行遠程評估。
除了一些參與者在靜脈注射和輸注過程中出現躁動之外,hCT-MSC耐受性良好。五名參與者產生了新的I類抗人類白細胞抗原 (HLA) 抗體,這些抗體與特定批次的hCT-MSC或供體和受體之間的部分HLA匹配有關。這些抗體在臨床上沒有表現,并且迄今為止與任何臨床表現無關。12名參與者中有6名在至少兩項ASD特異性指標上表現出改善。人臍帶間充質干細胞的輸注似乎對患有自閉癥的幼兒來說是安全可行的。將在隨后的II期隨機安慰劑對照臨床試驗中評估療效[1]。
什么是自閉癥譜系障礙 (ASD)
自閉癥譜系障礙 (ASD) 是一種異質性神經發育障礙,在兒童早期出現,自閉癥的癥狀包括重復行為、活動范圍受限和社交溝通障礙。ASD的治療包括強化行為、職業和言語治療以及教育支持和精神藥物治療。
值得注意的是,美國食品藥品監督管理局 (FDA) 批準的ASD藥物并不能解決核心癥狀。此外,盡管有可用的治療方法,ASD往往會導致嚴重的功能障礙,需要終生支持、依賴看護者和住宿。

自閉癥的病因涉及多種遺傳和環境風險因素之間的復雜相互作用。鑒于神經系統和免疫系統之間的密切相互作用,特別是在早期發育過程中,神經炎癥、小膠質細胞活化和/或免疫失調在相當一部分ASD患者中起著致病作用。因此,目前正在研究免疫調節療法在治療特定ASD兒童群體中的應用。
干細胞治療12名自閉癥患者,隨訪一年,50%患者癥狀有改善的跡象
間充質基質細胞 (MSC) 是一組異質性未分化的多能細胞,可從體內的幾種不同組織中分離出來。它們不表達MHCII類或其他共刺激分子,因此免疫原性較低,無需對供體和受體進行HLA匹配。MSC不會植入受體體內,而是通過旁分泌和營養信號發揮作用。它們可以改變多種細胞活動,包括血管生成、(抗)凋亡、化學吸引、祖細胞的生長和分化以及免疫功能,因此,它們正在被研究用于治療多種疾病。MSC還被證明可以調節神經炎癥、提供神經保護并增強突觸功能,使其成為治療某些神經系統疾病(包括ASD)的有吸引力的候選藥物。
人臍帶組織MSC (hCT-MSC) 是一種第三方同種異體人MSC產品,由供體臍帶組織制成,經消化和培養擴增、收獲、冷凍保存,并儲存在液氮的氣相中直至使用。在體外臨床前模型中,hCT-MSC抑制T細胞反應并降低小膠質細胞活化。我們假設hCT-MSC可能通過這些機制改善患兒的ASD核心癥狀,并進行了一項I期研究,測試在患有ASD的兒童中靜脈輸注一劑、兩劑或三劑hCT-MSC。
方法:本研究是一項I期開放標簽劑量遞增試驗,研究對象為患有ASD的幼兒,靜脈輸注一次、兩次或三次hCT-MSC(圖1)。該研究經杜克大學機構審查委員會批準(Pro00079421),根據FDA的IND17313進行,并在Clinicaltrials.gov上注冊(NCT03099239)。
結果
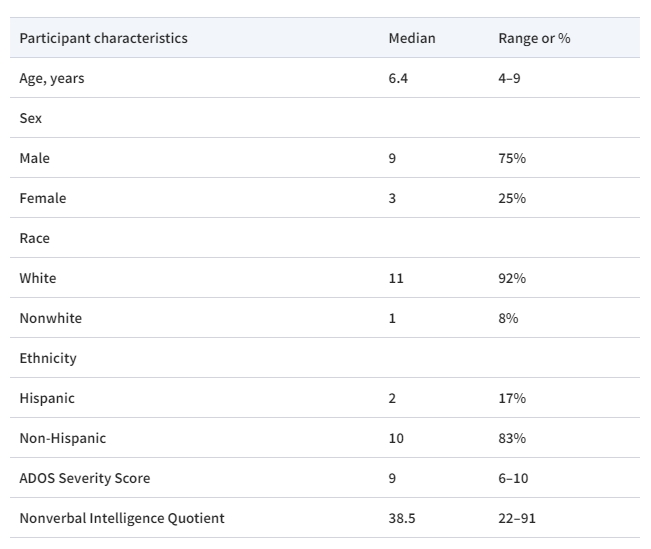
參與者特征:有12名患有ASD的兒童(9名男孩、3名女孩)入選,平均年齡為6.4 歲(范圍為4-9歲)(表1)。11名參與者為白人,1名為亞裔;2名為西班牙裔或拉丁裔。基線時非語言智商中位數為38.5(范圍為22-91),ADOS-2比較分數中位數為9(范圍為6-10,分數越高表示癥狀越多)。一名參與者沒有關于基線PDDBI的完整數據;所有其他評估均按計劃完成。在整個研究期間,參與者未接觸任何其他細胞產品。
人臍帶間充質干細胞輸注的安全性
所有參與者均按計劃接受了劑量注射。兩名參與者在hCT-MSC輸注期間或之后立即出現產品相關不良事件。第2組中的一名參與者在第二次輸注期間出現超敏反應和輕度低血壓,原因是父母要求在輸注前用藥計劃中做出改變(不使用苯海拉明)。癥狀出現后立即停止輸注,隨后進行靜脈輸液和額外劑量的甲基強的松龍注射,參與者完全康復。在隨后注射最初省略的苯海拉明后,剩余的hCT-MSC輸注得以成功完成。第3組中的一名參與者在完成第三次輸注后出現中度低血壓(分別為78/30、年齡的第10百分位數和第4百分位數),通過額外靜脈輸液得到緩解。
在12名入選參與者中,有11人報告了總共66起非嚴重不良事件,這些事件并非明確歸因于研究產品(圖2)。所有這些報告的事件都是輕微的。最常見的事件是輸液過程中的躁動,這與放置和維持靜脈注射以及在醫院病房輸液的要求有關,所有這些事件都在同一天得到解決。

A:按參與者劃分的AE頻率。B:按AE類型劃分的AE頻率
在整個研究過程中,血細胞計數、化學反應、基本炎癥標志物(CRP、ESR)或體液和細胞免疫特征均未發生令人擔憂的變化,也沒有任何參與者出現移植物抗宿主病的證據。所有參與者均保持Coombs陰性。
值得注意的是,所有12名參與者在基線和6個月時都收集了抗HLA抗體數據,11/12名參與者在最后一次hCT-MSC劑量后≥12個月也收集了數據。三名參與者在接受hCT-MSC治療前基線時已檢測到抗HLAI類抗體。在治療前未檢測到抗HLA抗體的9名參與者中,有5名參與者在首次hCT-MSC劑量6個月后出現低滴度抗HLAI類抗體,并且持續≥12個月(圖3)。
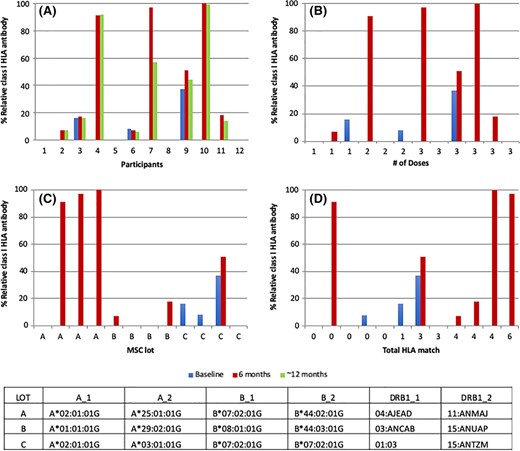
A:參與者在基線、6個月和>12個月時存在I類HLA抗體。
B:I類HLA抗體和基線和6個月的hCT-MSC劑量數。
C:基線和6個月的I類HLA抗體,按hCT-MSC批次計算。
D:hCT-MSC供體和受體之間的HLA匹配(在HLA-A、B、C、DRB1)的I類HLA抗體。
HLA,人類白細胞抗原;MSC,間充質基質細胞
抗HLA抗體針對的是MSC上表達的HLA等位基因/抗原,而不是參與者自身表達的HLA等位基因/抗原。一名捐贈者似乎比其他兩名捐贈者更容易引發抗HLA抗體的形成。
臨床結果評估
臨床心理結果評估結果如表2所示。報告的指標包括社交溝通技巧評估(VABS-3社交分量表分數),增加3分及以上表示改善,自閉癥癥狀嚴重程度評估(PDDBI自閉癥綜合評分),減少至少5分表示改善,以及專家臨床判斷(CGI-I),范圍從無改善到有很大改善。
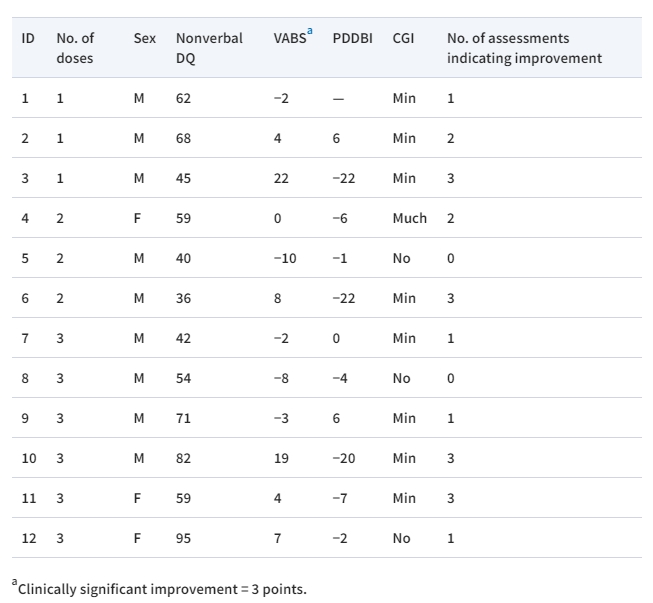
縮寫:CGI,臨床總體印象改進量表;DQ,發育商;F,女性;M,男性;Max,最大值;Min;最小值;PDDBI,廣泛性發育障礙行為清單自閉癥綜合量表;VABS,Vineland 適應性行為量表,第三版,社會化分量表標準分數。
50% (6/12) 的參與者在≥2/3的指標上表現出改善;4/12在三項指標上表現出改善,2/12在兩項指標上表現出改善。在6名在≥2/3的結果指標上有所改善的兒童中,兩名兒童接受了一劑hCT-MSC,兩名兒童接受了兩劑,兩名兒童接受了三劑。
討論
在本報告中,我們描述了一項開放標簽、安全性和可行性的I期劑量遞增試驗的結果,該試驗測試了在12名患有ASD的兒童中靜脈注射hCT-MSC(一種來自捐贈的同種異體第三方臍帶組織的MSC產品)。總體而言,輸注是安全的,耐受性良好。50%的參與者描述了ASD核心癥狀有所改善的跡象,證據是三項臨床結果測量中的兩項有所改善。
行為障礙和合并精神癥狀在患有ASD的兒童中很常見,因此,在為期12個月的研究期間,預計有七名參與者報告了至少一次行為或精神方面的AE。在這些參與者中,大多數人的AE都是自限性的,并已得到解決。在研究的12名兒童中,有10名兒童(包括3名其照顧者報告了多次精神/行為AE的參與者)在所進行的三項ASD癥狀測量中至少有一項得到了改善。這凸顯了描述和報告ASD癥狀隨時間推移而發生的變化所固有的挑戰。
在醫學文獻中,只有另外兩份臨床報告測試了同種異體hCT-MSC對患有ASD的兒童的作用。
2013年,山東省交通醫院進行了一項人類臍帶血單核細胞和臍帶間充質干細胞移植治療自閉癥的研究[2]。

15名兒童接受了四劑臍帶血單核細胞 (CBMNC) 治療,這些細胞通過靜脈和鞘內注射(n=14)、CBMNC+鞘內臍帶組織MSC(n=9)或標準療法(n=14)。治療相關的唯一副作用是五名參與者出現短暫性發燒。治療六個月后,兩個治療組的ASD指標改善均大于安慰劑組。
2019年,國際期刊雜志《干細胞轉化醫學》發表的研究報告了20名兒童臍帶組織MSC治療的結果,這些兒童以開放標簽方式接受治療,在九個月的時間內每12周分四天接受靜脈注射約3600萬個細胞。細胞在含有胎牛血清的培養基中制造,并在冷凍保存前擴增至第5代。輸注前未使用藥物,治療期間未評估細胞解凍后的特性,兒童在一段時間內接觸了多位捐獻者。安全性進行了臨床評估[3]。

據報道,在20%的劑量給藥后會出現輕度至中度不良反應。并非所有參與者都進行了隨訪,但自閉癥治療評估清單 (ATEC) 有所改善。
結論
我們報告了一項臍帶間充質干細胞治療自閉癥兒童的小型I期試驗的良好安全結果。需要進行更多試驗才能充分評估這種方法的安全性和有效性。
因此,我們的中心最近啟動了一項II期隨機雙盲研究,以評估hCT-MSC在改善患有自閉癥的幼兒社交溝通能力方面的安全性和有效性 (NCT04089579)。
參考資料:
[1]:Jessica M. Sun, Geraldine Dawson, Lauren Franz, Jill Howard, Colleen McLaughlin, Bethany Kistler, Barbara Waters-Pick, Norin Meadows, Jesse Troy, Joanne Kurtzberg, Infusion of human umbilical cord tissue mesenchymal stromal cells in children with autism spectrum disorder, Stem Cells Translational Medicine, Volume 9, Issue 10, October 2020, Pages 1137–1146, https://doi.org/10.1002/sctm.19-0434
[2]:Lv, YT., Zhang, Y., Liu, M. et al. Transplantation of human cord blood mononuclear cells and umbilical cord-derived mesenchymal stem cells in autism. J Transl Med 11, 196 (2013). https://doi.org/10.1186/1479-5876-11-196
[3]:Neil H. Riordan, Maria Luisa Hincapié, Isabela Morales, Giselle Fernández, Nicole Allen, Cindy Leu, Marialaura Madrigal, Jorge Paz Rodríguez, Nelson Novarro, Allogeneic Human Umbilical Cord Mesenchymal Stem Cells for the Treatment of Autism Spectrum Disorder in Children: Safety Profile and Effect on Cytokine Levels, Stem Cells Translational Medicine, Volume 8, Issue 10, October 2019, Pages 1008–1016, https://doi.org/10.1002/sctm.19-0010
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請及時跟本公眾號聯系,我們將在第一時間處理。




 掃碼添加微信
掃碼添加微信