概述:年齡相關性黃斑變性 (AMD) 是一種常見的眼病,它會模糊您進行閱讀和駕駛等活動所需的清晰的中心視力。顧名思義,AMD在60歲以上的人群中最為常見,并且隨著人口老齡化,越來越多的人患有 AMD。
在這個部分:
- 什么是年齡相關性黃斑變性?
- 如何治療年齡相關性黃斑變性?
- 我們如何使用干細胞來了解年齡相關性黃斑變性?
- 干細胞治療年齡相關性黃斑變性的潛力有多大?
- 干細胞治療年齡相關性黃斑變性的臨床現狀如何?
什么是年齡相關性黃斑變性?
年齡相關性黃斑變性 (AMD) 是一種進行性眼病,會導致黃斑受損,黃斑是負責中央視力的一小塊視網膜區域。隨著時間的推移,您的視力中心可能會變得模糊或起伏不定,從而難以進行需要敏銳視力的事情,例如閱讀、駕駛和識別面孔。
黃斑是一小塊神經組織,直徑約5.5毫米,位于負責中央視覺的視網膜后部。它密集地充滿了稱為視桿細胞和視錐細胞的感光細胞,它們通過電神經沖動將光線從視網膜傳輸到視神經并進入大腦。這些光感受器由稱為視網膜色素上皮(RPE) 的相鄰細胞層支持,后者通過從血液中輸送營養物質并清除視桿細胞和視錐細胞產生的廢物來支持視桿細胞和視錐細胞。AMD由RPE的損傷和逐漸喪失發展而來。有兩種類型的AMD,干型和濕型。
在AMD中,RPE細胞停止執行其支持功能,視桿細胞和視錐細胞死亡,導致中心視力喪失。干性AMD通常會發展數年。在不太常見的濕性AMD中,中心視力可能會在幾周或幾天內喪失。
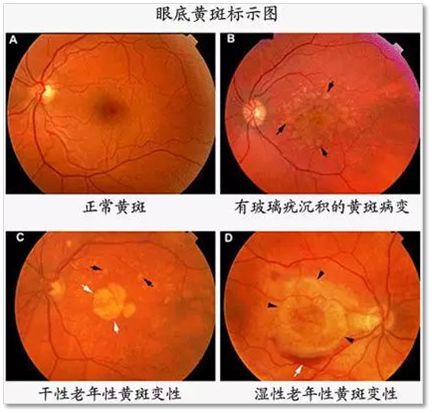
干性AMD:在干性AMD(也稱為地圖樣萎縮)中,稱為玻璃膜疣的小沉積物會在視網膜下積聚。隨著時間的推移,黃斑附近的RPE細胞層受損,進而導致視桿細胞和視錐細胞逐漸分解。這些變化導致中心視力喪失。
濕性AMD:在濕性AMD(也稱為新生血管性AMD)中,異常血管在視網膜和黃斑下方生長。這個過程稱為脈絡膜新生血管 (CNV)。這些新血管很脆弱,經常將液體和血液泄漏到視網膜層中。這會導致腫脹或疤痕形成,并阻止RPE細胞發揮作用。損害可能迅速而嚴重。
如何治療年齡相關性黃斑變性?
干性AMD:目前尚無針對干性AMD的良好治療方法。鼓勵患者通過富含綠葉蔬菜、堅果和魚的飲食來支持一般的眼睛健康,并且隨著病情的發展,用關鍵的維生素和礦物質補充他們的飲食。請參閱美國眼科學會的相關建議。
濕性AMD:對于濕性AMD,醫生使用藥物治療和手術技術來幫助保持現有視力。目前的一線治療是向患眼注射藥物以抑制新血管的形成。這些藥物會阻止血管內皮生長因子或VEGF的產生,VEGF會向身體發出信號以制造新血管。對于許多人來說,需要每四到六周重復注射一次。
對于某些類型的濕性AMD,還可以使用各種激光手術來移除或減少血管數量或密封它們并減緩它們的滲漏。不幸的是,即使是最成功的治療也不一定能阻止新血管的形成或修復后的血管再次滲漏。此外,手術會造成疤痕或進一步損害附近的RPE細胞。
我們如何使用干細胞來了解相關性黃斑變性?
科學家們正在利用干細胞研究來更好地了解眼睛中的細胞以及它們如何患病,制造可以替代眼睛中受損細胞的細胞,并確定可以治療AMD的新藥。
眼睛的特殊屬性:眼睛是干細胞治療的良好目標。它相對獨立,有許多障礙阻止細胞遷移到身體的其他部位。評估眼睛治療的有效性很容易,因為研究人員擁有觀察眼睛內部和測量其視覺功能的工具。他們還能夠比較同一患者接受治療的眼睛和未經治療的眼睛的結果。
了解眼睛中的細胞以及它們如何患病
科學家在實驗室研究干細胞,以幫助他們了解視網膜中不同細胞類型如何共同發育和發揮作用,這導致了更復雜的方法來模擬正常眼睛發育實驗室并了解健康的眼組織如何患病。
制造可以替代眼睛中受損細胞的細胞
科學家們正在探索使用干細胞替代 AMD 中丟失的細胞的方法。在濕性和干性 AMD 中,支持桿狀和錐狀感光器功能的 RPE 層受損。干細胞研究人員正在研究如何用實驗室制造的 RPE 細胞替換受損的 RPE 層,他們相信這將阻止甚至逆轉與 AMD 相關的視力喪失。科學家們也在努力更換感光細胞(視桿細胞和視錐細胞)本身。
更換視桿細胞和視錐細胞具有挑戰性,因為這些細胞必須與神經纖維建立聯系,神經纖維將信號饋送到視神經,視神經將這些信號發送到大腦進行解釋。研究人員正在積極研究這種方法,但要確保新的視桿細胞和視錐細胞在移植后與患者現有的視桿細胞和視錐細胞一起與現有神經纖維正確整合是非常復雜的。
相比之下,RPE 細胞不需要與神經纖維連接,因此讓它們與現有的視網膜細胞整合可能更容易。新的 RPE 細胞可以替代患病的 RPE 細胞并承擔它們的一些支持功能。如果在視桿細胞和視錐細胞丟失之前進行移植,新的 RPE 細胞可能能夠防止它們死亡,從而改善中心視力,或者至少阻止疾病的進展。
確定可以治療AMD的新藥
此外,干細胞還被用于確定新的藥物治療方法。健康的干細胞來源的 RPE 細胞可能會受到壓力,從而產生顯示 AMD 特征的異常細胞。這些細胞可以在實驗室中培養和研究,以更好地了解 AMD 的進展情況,這可能會導致更早的檢測和更好的預后。這些細胞還可用于篩選潛在藥物的安全性和有效性。
干細胞也被用于藥物發現?,即發現新療法的過程。健康的 RPE 細胞可能會受到壓力,從而產生顯示 AMD 特征的異常細胞。這些細胞可以在實驗室中培養和研究,以更好地了解 AMD 的進展情況,這可能會導致更早的檢測和更好的診斷。這些細胞還可用于篩選潛在藥物的安全性和有效性。
干細胞治療年齡相關性黃斑變性的潛力有多大?
研究人員正在采取多種方法來制造用于移植的RPE細胞。他們正在嘗試不同的細胞來源和不同的方法將細胞輸送到眼睛。
從長遠來看,隨著對眼睛中不同細胞類型如何發育以及產生視桿細胞和視錐細胞的技術得到改進的了解越來越多,研究人員希望與 RPE 細胞一起替代視桿細胞和視錐細胞。
制造替代RPE細胞:一些研究人員正在使用誘導多能干 (iPS) 細胞來培養RPE細胞。iPS細胞由皮膚或血細胞制成,這些細胞在實驗室中被操縱成為可以形成體內任何細胞的干細胞。iPS細胞甚至可以由患者自身制成,以減少移植后免疫系統排斥的機會。為了加快這一過程,研究人員正在研究獲取患者皮膚或血細胞并將其直接轉化為RPE細胞的方法。
其他小組正在使用其他類型的干細胞,例如人類胚胎干細胞,或來自RPE的干細胞。這些RPE特異性干細胞可以從成人RPE中培養,例如,從捐贈給眼庫的眼睛中培養。
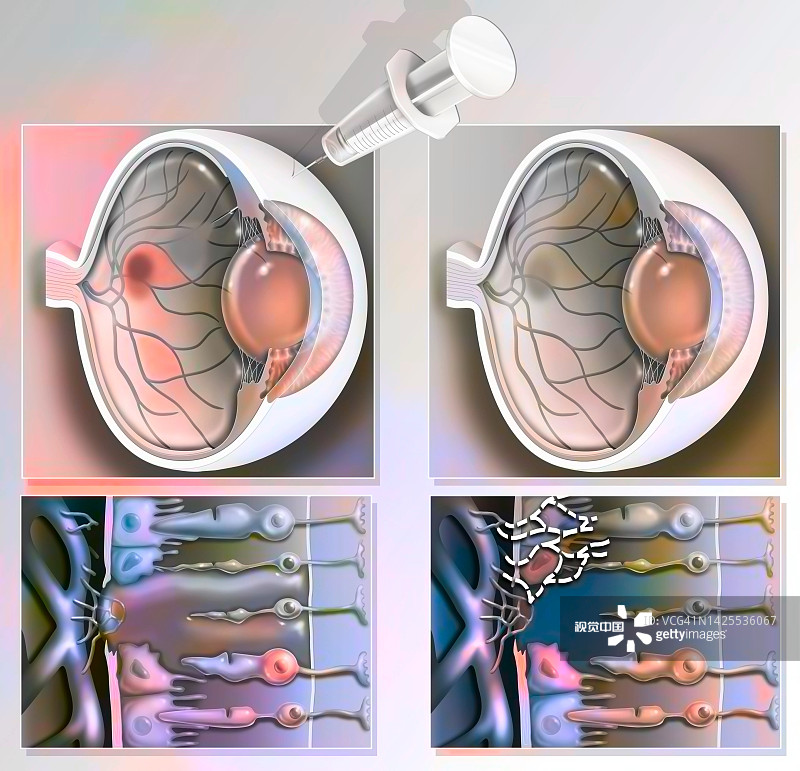
輸送到眼睛:研究人員正在探索將替代RPE細胞輸送到眼睛的不同方法,包括在實驗室中創建RPE細胞斑塊。在一種方法中,將源自iPS細胞、人類胚胎干細胞或成人RPE干細胞的單細胞厚RPE細胞層植入眼睛。在動物試驗中,這些“補丁”顯示出了希望;RPE細胞似乎很穩定,不會遷移到眼睛的其他區域。
輸送細胞的另一種方式是將細胞懸浮液注射到視網膜下的眼睛中。來自 iPS 細胞、人類胚胎干細胞或 RPE 干細胞的細胞在實驗室中生長并分化為 RPE,然后置于液體中并注射。這種方法可能侵入性較小。
對于這兩種方法,一個關鍵問題是這些細胞是否會與患者自身的 RPE 細胞很好地整合,并長期發揮它們滋養視桿細胞和視錐細胞的作用。
干細胞治療年齡相關性黃斑變性的臨床現狀如何?
截止2022年11,在美國國立衛生研究院的最大臨床試驗注冊庫clinicaltrials.gov網站上注冊的有關干細胞治療年齡相關性黃斑變性的臨床研究項目有34項。
現在計劃或正在進行多項早期試驗,以測試生成實驗室制造的RPE細胞并將其輸送至視網膜以治療AMD的不同方法。其中一些試驗針對干性AMD患者,另一些針對濕性AMD患者。
對于每種策略,初始試驗主要是測試不同的方法是否可行以及是否可以安全地進行。迄今為止,這些研究僅包括極少數人。其中一些試驗的第一份報告令人鼓舞——細胞耐受性良好,參與者的視力沒有惡化,在某些情況下,至少在短期內有所改善。
隨著時間的推移,醫師科學家繼續跟蹤進展,并更好地了解新的 RPE 細胞如何與干性和濕性 AMD 中的現有組織相互作用。他們正在擴大試驗以包括更多人,并確定 RPE 細胞治療的益處。
2015年,第一篇關于干細胞治療黃斑變性的多中心臨床試驗文章“Human embryonic stem cell-derived retinal pigment epithelium in patients with age-related macular degeneration and Stargardt’s macular dystrophy: follow-up of two open-label phase 1/2 studies”發表在柳葉刀上,試驗納入了18名病人,將人胚胎干細胞分化的色素上皮細胞( hESC-derived RPE )懸液注射于受試者的視網膜下,平均隨訪約22個月,移植細胞的存活和患者視力的提高是不穩定的,有些患者視力提高了,有些完全沒有、甚至下降。
2017年,另一篇采用誘導多能干細胞(iPSC)分化的RPE治療晚期AMD的病例“Autologous Induced Stem-Cell–Derived Retinal Cells for Macular Degeneration”發表在了新英格蘭雜志上。作者將iPSC分化的RPE(iPSC–derived RPE)于體外種在一塊補片上,再將補片植于視網膜下方,隨訪了1年,移植的RPE是存活的,但患者的視力并無提高。
科技帶給我們的改變是我們難以想象的,干細胞治療為視網膜變性患者重見光明開辟了新的治療途徑,將是未來一段時間眼科領域研究重點。期待干細胞療法早日點亮黑暗中的人們,為他們重啟心靈的窗戶!
版權聲明:本文來自互聯網,目的在于介紹生物醫療領域前沿資訊、科學普及細胞領域的相關知識,僅用于分享、交流和學習,供訪問者參考。版權屬于原作者所有,如有侵權,請聯系我們及時刪除。




 掃碼添加微信
掃碼添加微信