膝骨關節(jié)炎 (OA) 是一種退行性關節(jié)疾病,非手術治療選擇有限。脂肪間充質干細胞 (AD-MSC) 療法已成為一種頗具前景的再生療法;然而,自體和同種異體AD-MSC的療效和安全性尚不明確。
為此,近日,知名醫(yī)學期刊雜志“Cureus”發(fā)表了一篇“自體與同種異體脂肪間充質干細胞治療膝骨關節(jié)炎:隨機對照試驗的系統(tǒng)評價、成對和網絡薈萃分析”的臨床研究綜述。

該系統(tǒng)綜述和網狀薈萃分析 (NMA) 評估了關節(jié)內 AD-MSC 治療 Kellgren-Lawrence II-IV 級膝骨關節(jié)炎成人患者的有效性和安全性。
結果表明:高劑量自體AD-MSCs在12個月內持續(xù)緩解疼痛,而高劑量同種異體AD-MSCs表現(xiàn)出卓越的長期功能改善。這些發(fā)現(xiàn)支持雙階段治療模式,其中自體AD-MSCs提供早期和長期癥狀緩解,同種異體AD-MSCs有助于長期關節(jié)恢復。總體而言,AD-MSC療法耐受性良好,可能代表一種可行、個性化、非手術的膝關節(jié)OA管理策略。
膝骨關節(jié)炎的簡介與背景
膝骨關節(jié)炎 (OA) 是全球范圍內導致疼痛和致殘的主要原因,其特征是進行性軟骨退化、慢性滑膜炎癥和結構性關節(jié)退化。目前的非手術治療,包括非甾體類抗炎藥 (NSAID)、關節(jié)內皮質類固醇和透明質酸注射,可以緩解癥狀,但無法阻止病情進展。由于除手術干預外,其他治療選擇有限,間充質干細胞 (MSC) 療法已成為一種頗具前景的再生療法。MSC 通過分泌IL-10和TGF-β發(fā)揮抗炎作用,調節(jié)炎癥,促進組織修復,并改善關節(jié)功能。
在眾多MSC來源中,脂肪間充質干細胞(AD-MSC)因其產量高、易于提取和強大的增殖潛力而備受關注。與骨髓間充質干細胞(BM-MSC)相比,AD-MSC可通過微創(chuàng)吸脂術獲取,并具有強大的旁分泌活性,有助于軟骨修復和免疫調節(jié)。然而,盡管臨床研究不斷增加,但仍存在一些關鍵的不確定性,包括自體與同種異體AD-MSC的療效比較、最佳給藥策略以及長期安全性考慮。

自體與同種異體AD-MSC治療:機制和臨床潛力
AD-MSC主要通過旁分泌信號傳導、分泌細胞因子、生長因子和細胞外囊泡來發(fā)揮治療作用,從而調節(jié)免疫反應、減輕炎癥并促進細胞外基質重塑。這些特性對骨關節(jié)炎 (OA) 尤為有益,因為慢性炎癥會加速軟骨退化。
AD-MSC 可以是自體的(來自患者自身組織),也可以是同種異體的(來自供體)。自體 AD-MSC 因其免疫相容性、較低的排斥風險以及在關節(jié)環(huán)境中可能持續(xù)更長時間而被認為具有優(yōu)勢。相反,同種異體 AD-MSC 是一種現(xiàn)成的治療選擇,可能具有更強的免疫調節(jié)作用,但可能存在免疫識別和清除的風險。
一些研究表明,自體 AD-MSC 可以更快地緩解疼痛,而同種異體 AD-MSC 則有助于持續(xù)的再生作用。新興證據(jù)還表明,治療效果可能與劑量有關,細胞劑量越高,效果可能越強、持續(xù)時間越長。然而,最佳給藥閾值仍不清楚,而且很少在不同研究中進行比較。
需要進行全面的比較分析
盡管評估AD-MSC療法的隨機對照試驗 (RCT) 越來越多,但研究設計、治療方案、隨訪時間和結果測量的多樣性導致了相互矛盾的結論。雖然之前的薈萃分析已經評估了MSC治療OA的效果,但沒有一項分析能夠完全解決不同劑量自體和同種異體AD-MSC的比較效果。
我們的研究使用貝葉斯網絡薈萃分析 (NMA) 解決了這一空白,它通過整合直接和間接證據(jù)提供了強大的解決方案,可以在統(tǒng)一的分析框架內比較多種AD-MSC治療方案,從而對治療策略進行排名。通過評估多個時間點的結果,我們旨在明確最有效和最安全的膝關節(jié)OA管理AD-MSC方案,并為臨床決策和試驗設計提供參考。
盤點干細胞治療骨關節(jié)炎:自體效果好還是異體好?高劑量安全還是低劑量?
研究目標:本系統(tǒng)綜述采用成對和網狀薈萃分析,旨在全面評估低劑量同種異體、高劑量同種異體和高劑量自體AD-MSC療法治療膝關節(jié)OA的療效和安全性。主要療效指標包括疼痛緩解(以視覺模擬量表 (VAS) 測量)和功能改善(以西安大略大學和麥克馬斯特大學骨關節(jié)炎指數(shù) (WOMAC) 評估)(3、6 和12個月)。此外,本研究還考察了不同AD-MSC方案的不良反應 (AE) 情況,以根據(jù)累積排序下表面概率 (SUCRA) 確定最有效的干預措施。為確保研究結果的可靠性,我們進行了一致性檢驗,以評估NMA框架內直接和間接比較的有效性。
假設與研究意義:本研究假設,高劑量自體AD-MSC因其更強的早期抗炎作用,將能夠快速緩解疼痛。相比之下,高劑量同種異體AD-MSC因其持久的免疫調節(jié)和再生活性,將表現(xiàn)出更優(yōu)異的長期功能改善。
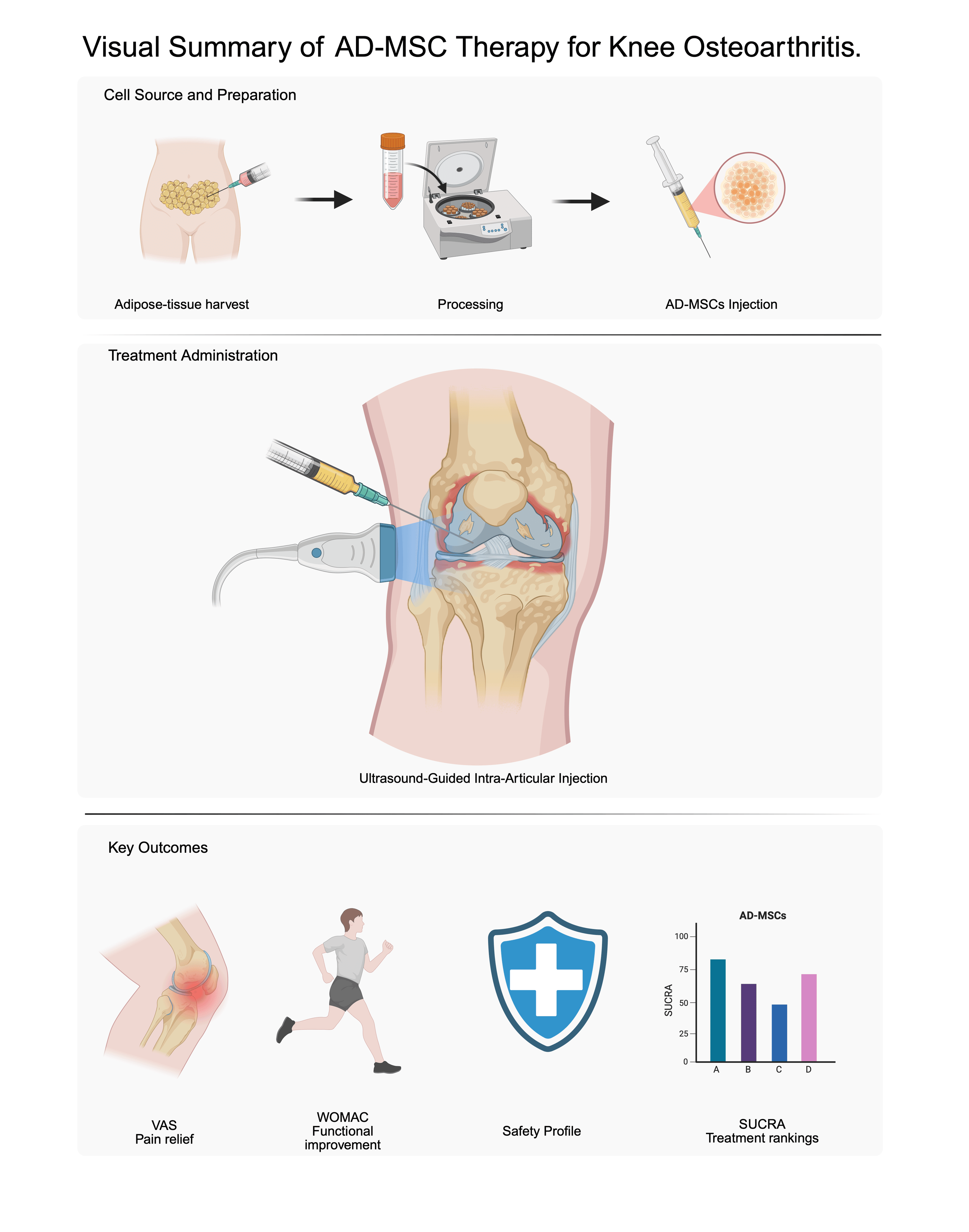
本研究旨在整合多項 RCT 的直接和間接證據(jù),以數(shù)據(jù)驅動的方式,為膝關節(jié)骨關節(jié)炎 (OA) 的最佳 AD-MSC 治療策略提供洞察。本研究旨在支持再生醫(yī)學標準化方案的制定。本薈萃分析的結果也可能為未來的臨床試驗提供參考,并有助于完善患者選擇標準,最終提升脂肪間充質干細胞療法在膝關節(jié)骨關節(jié)炎管理中的治療潛力。圖1
展示了AD-MSC治療過程和臨床終點的概覽。
研究方法:在 PubMed/MEDLINE、Cochrane CENTRAL、Embase、 ClinicalTrials.gov 、Web of Science 和世界衛(wèi)生組織國際臨床試驗注冊平臺 (ICTRP)上進行系統(tǒng)性檢索,共發(fā)現(xiàn) 994 條記錄。刪除 477 條重復記錄后,剩余 517 條記錄用于標題和摘要篩選,其中 461 條因不相關而被排除。剩余 56 份全文報告用于資格評估;然而,其中 23 份報告無法檢索,因此需要進行全面審查的研究總數(shù)減少到 33 份。
經過全文評估,25項研究被排除,主要原因是使用了非脂肪來源的干細胞、缺乏對照組或與其他干預措施聯(lián)合使用。最終,8項RCT符合納入標準,并被納入傳統(tǒng)的成對和網絡薈萃分析(圖2)。

研究特征:本研究納入了8項RCT,評估了不同劑量的同種異體和自體AD-MSCs與透明質酸、生理鹽水或標準治療的療效。表1總結了主要療效指標,包括WOMAC、VAS、膝關節(jié)損傷和骨關節(jié)炎療效評分 (KOOS) 以及隨訪1至24個月期間評估的不良事件。
| 作者(年份) | 研究設計 | MSC 劑量(細胞數(shù)) | 平均年齡(標準差) | 體重指數(shù)(平均值±標準差) | 性別分布 | KL等級(范圍) | 干細胞來源 | 比較器 | 結果測量 | 隨訪(月) | ||
| 治療 | 控制 | 治療:男/女 | 控制:M/F | |||||||||
| Chen 等人(2021) | 隨機對照試驗 | 一次注射-16M | 67.7(6.84) | 70.5(8.37) | 27.65(3.026) | 17(3/14) | 8(3/5) | 二至三期 | 同種異體 | 透明質酸 | WOMAC、VAS、KSCRS、AE、SAE | 1、3、6、9、12、18、24 |
| 一次注射-32M | 68.6(6.45) | 26.72(4.192) | 17(2/15) | |||||||||
| 一次注射-64M | 64.9(4.91) | 25.66(3.782) | 15(3/12) | |||||||||
| 安慰劑(透明質酸) | 70.5(8.37) | 25.47(3.494) | 8(3/5) | |||||||||
| Freitag等人(2019) | 隨機對照試驗 | 一次注射-100M | 54.6(6.3) | 51.5(6.1) | 31.6(5.9) | 10(4/6) | 10(5/5) | 二至三期 | 自體 | 標準護理 | NPRS、WOMAC、KOOS、AE、MOAKs | 1、3、6、12 |
| 二次注塑-100M | 54.7(10.2) | 30.4(5.6) | 10(7/3) | |||||||||
| 安慰劑(保守) | 51.5(6.1) | 25.2(3.4) | 10(5/5) | |||||||||
| Freitag等人(2024) | 隨機對照試驗 | 一次注射-10M | 57.0(6.7) | 39.1(10.8) | 26.30(3.81) | 8(5/3) | 8(7/1) | 二至三期 | 同種異體 | 等離子萊特 | NRPS、KOOS、AE | 1、3、6、9、12 |
| 一次注射-20M | 45.5(12.0) | 26.76(4.66) | 8(6/2) | |||||||||
| 一次注射-50M | 49.0(9.6) | 26.47(3.12) | 8(5/3) | |||||||||
| 一次注射-100M | 47.6(5.9) | 27.59(4.28) | 8(5/3) | |||||||||
| 安慰劑(Plasma-lyte) | 39.1(10.8) | 27.81(3.86) | 8(7/1) | |||||||||
| Kim 等人(2023 年) | 隨機對照試驗 | 一次注射-100M | 63.7(7.1) | 63.8(7.1) | 26.3(3.2) | 125(39/86) | 127(26/101) | 三 | 自體 | 鹽水 | WOMAC、VAS、KOOS、SF-36 | 1、3、6 |
| 安慰劑(鹽水) | 63.8(7.1) | 25.9(3.1) | 127(26/101) | |||||||||
| Kuah等人(2018) | 隨機對照試驗 | 一次注射-3.9M | 50.8(7.3) | 55.0(10.42) | 27.7(2.05) | 8(6/2) | 4(1/3) | 一至三 | 同種異體 | 冷凍保存劑 | WOMAC、VAS、AE | 1、3、6、9、12 |
| 一次注射-6.7M | 55.0(5.15) | 26.8(2.98) | 8(5/3) | |||||||||
| 安慰劑 | 55.0(10.42) | 25.5(2.84) | 4(1/3) | |||||||||
| Lee等人(2019) | 隨機對照試驗 | 一次注射-100M | 62.2(6.5) | 63.2(4.2) | 25.3(4.9) | 12(3/9) | 12(3/9) | 二至四 | 自體 | 鹽水 | WOMAC、VAS、KOOS、SF-36、AE | 1、3、6 |
| 安慰劑(鹽水) | 63.2(4.2) | 25.4(3.0) | 12(3/9) | |||||||||
| Lu 等人(2019) | 隨機對照試驗 | 二次注塑-50M | 55.03(9.19) | 59.64(5.97) | 24.27(3.04) | 26(3/23) | 26(3/23) | 一至三 | 自體 | 透明質酸 | WOMAC、VAS、SF36 | 1、6、12 |
| 安慰劑(透明質酸) | 59.64(5.97) | 24.26(2.59) | 26(3/23) | |||||||||
| Sadri等人(2023) | 隨機對照試驗 | 一次注射-100M | 52.85(7.25) | 56.1(7.21) | 28.37(3.26) | 20(2/18) | 20(2/18) | 二至三期 | 同種異體 | 鹽水 | WOMAC、VAS、KOOS、SF-36 | 1、3、6、12 |
| 安慰劑(鹽水) | 56.1(7.21) | 29.12(4.0) | 20(2/18) | |||||||||
表2詳細列出了研究方法,包括隨機化、盲法、倫理審批、組織采集地點、治療流程和資金來源。大多數(shù)試驗采用雙盲法,并由企業(yè)資助,AD-MSC主要從腹部組織采集。
| 作者(年份) | 隨機化方法 | 致盲 | 倫理批準/試驗注冊 | 組織采集地點 | 治療過程 | 資金來源 |
| Chen 等人(2021) | 置換塊隨機化 | 單盲 | 已批準,NCT02784964 | 未說明 | 3毫升 | 工業(yè)界和政府資助(UnicoCell BioMed Co. Ltd.、中華民國經濟部 A+ 工業(yè)創(chuàng)新研發(fā)計劃)。 |
| Freitag等人(2019) | 隨機數(shù)生成器 | 雙盲 | 已批準,ACTRN12614000814673 | 腹部 | 3毫升 | 由行業(yè)和機構資助(麥哲倫干細胞、墨爾本干細胞中心)。 |
| Freitag等人(2024) | 計算機生成的塊 | 雙盲 | 已批準,ACTRN12617001095358 | 未說明 | 5毫升 | 行業(yè)資助(Magellan Biologicals Pty Ltd.)。 |
| Kim 等人(2023年) | 置換塊隨機化 | 雙盲 | 已批準,NCT03990805 | 腹部 | 3毫升 | 行業(yè)資助(R-Bio 有限公司)。 |
| Kuah等人(2018) | 隨機化區(qū)組安排表 | 雙盲 | 已批準,ACTRN12615000439549 | 未說明 | 2毫升 | 行業(yè)資助(Regeneus Ltd.)。 |
| Lee等人(2019) | 隨機化區(qū)組安排表 | 雙盲 | 已批準,NCT02658344 | 腹部 | 3毫升 | 行業(yè)資助(R-Bio 有限公司)。 |
| Lu 等人(2019) | 計算機生成的隨機化 | 雙盲 | 已批準,NCT02162693 | 腹部 | 2.5毫升 | 由行業(yè)和政府資助(細胞生物醫(yī)藥組、中國國家重點研發(fā)計劃)。 |
| Sadri等人(2023) | 置換塊隨機化 | 三盲 | 已批準,IRCT20080728001031N23 | 未說明 | 5毫升 | 政府和學術機構資助(伊朗衛(wèi)生和醫(yī)學教育部、魯瓦揚干細胞生物學和技術研究所)。 |
網絡結構:網絡薈萃分析納入了8項隨機對照試驗,共11對比較,涵蓋四個治療組:高劑量自體AD-MSCs、高劑量異體AD-MSCs、低劑量異體AD-MSCs和對照組。部分試驗包含多個治療組,構成一個連接良好的網絡。該網絡結構構成一個緊密結合的子網絡,確保在無法進行直接頭對頭試驗的情況下進行間接比較。例如,由于高劑量自體和高劑量異體均與對照組進行了比較,而未相互比較,因此仍可通過以標準對照組為參考的間接比較來估計它們的相對療效。通過整合這些比較,該分析對AD-MSCs療法治療膝骨關節(jié)炎的療效和安全性進行了全面評估。
盤點干細胞治療骨關節(jié)炎:自體效果好還是異體好?高劑量安全還是低劑量?結果介紹
本節(jié)介紹傳統(tǒng)的成對薈萃分析和網狀薈萃分析的結果,評估不同干預措施在緩解疼痛和改善功能方面的有效性,這些有效性以VAS和WOMAC評分為衡量標準。分析在三個時間點(3個月、6個月和12個月)進行,以評估短期和長期治療效果。此外,還檢查了所有時間點的不良反應,以評估每種干預措施的安全性。
治療排名總結:為了確定最佳治療方案,我們計算了所有時間點的VAS和WOMAC評分的SUCRA值。SUCRA條形圖概述了哪些治療方案在3個月、6個月和12個月內最有效。這些排名可以直接比較干預措施,從而促進基于證據(jù)的決策,確定最佳疼痛管理策略。
VAS評分變化(三個月)
一、傳統(tǒng)薈萃分析:高劑量自體 AD-MSCs 早期鎮(zhèn)痛效果領先,異質性特征顯著
納入8項研究共270名參與者的固定效應薈萃分析顯示,3個月時高劑量自體AD-MSCs的VAS評分改善最顯著,其次為高劑量異基因 AD-MSCs,低劑量異基因 AD-MSCs 效果較弱但仍顯著。異質性分析表明,低劑量異基因組異質性較低(I2=12%),而高劑量異基因(I2=68%)和自體組(I2=72%)存在較高異質性,提示不同研究間治療效果存在差異。漏斗圖顯示整體對稱,僅高劑量異基因組存在輕微不對稱,可能與小規(guī)模研究效應相關,但無明確出版偏倚。
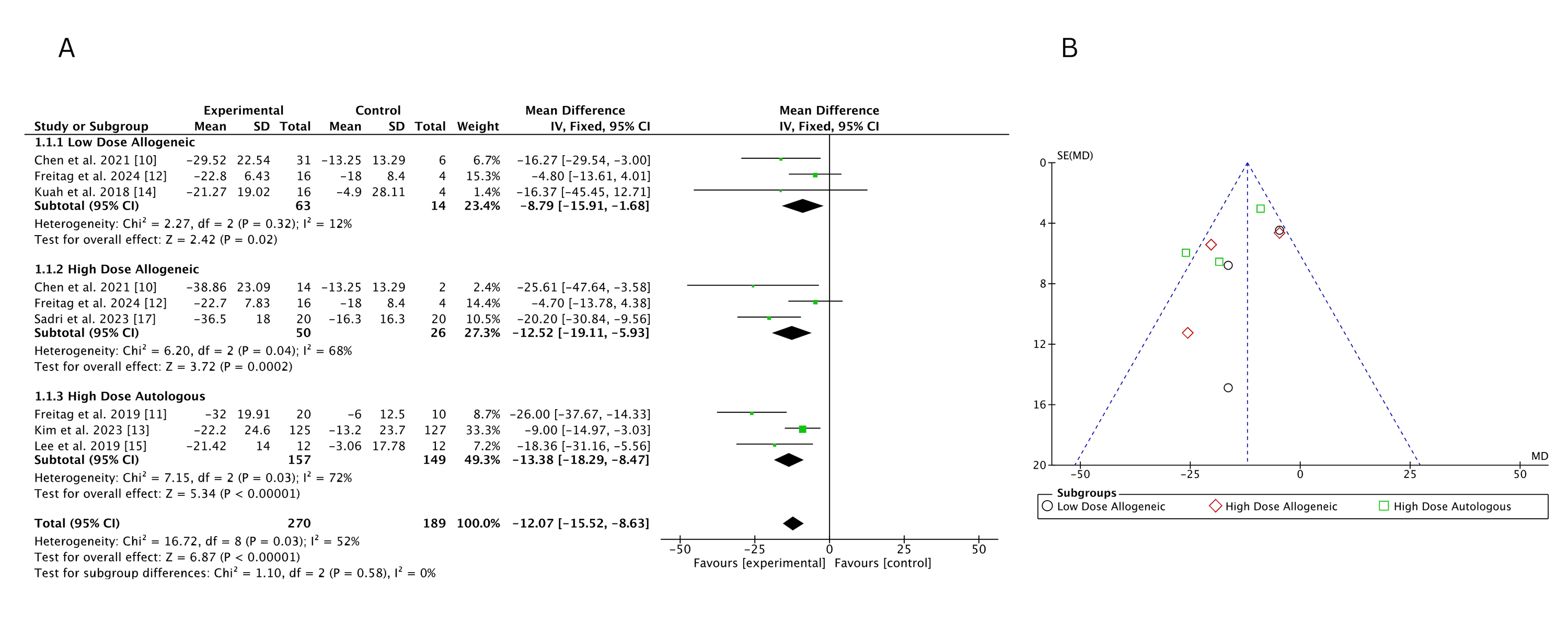
二、頻率學派網絡薈萃分析:高劑量組療效明確,低劑量組效果波動
低劑量異基因 AD-MSCs 在 Chen 等(2021 年)研究中表現(xiàn)出顯著鎮(zhèn)痛效果,但 Freitag 等(2024年)和 Kuah 等(2018 年)研究因置信區(qū)間寬泛,效果不確定性突出。高劑量異基因 AD-MSCs 在 Chen 等(2021年)研究中效果最強,但部分研究反應差異較大。高劑量自體 AD-MSCs 在 Freitag 等(2019 年)研究中 VAS 評分降幅最大,Kim等(2023 年)和 Lee等(2019年)研究也觀察到類似趨勢,整體表現(xiàn)出穩(wěn)定且強效的早期鎮(zhèn)痛效果。高劑量與低劑量異基因組的直接比較未顯示顯著差異。
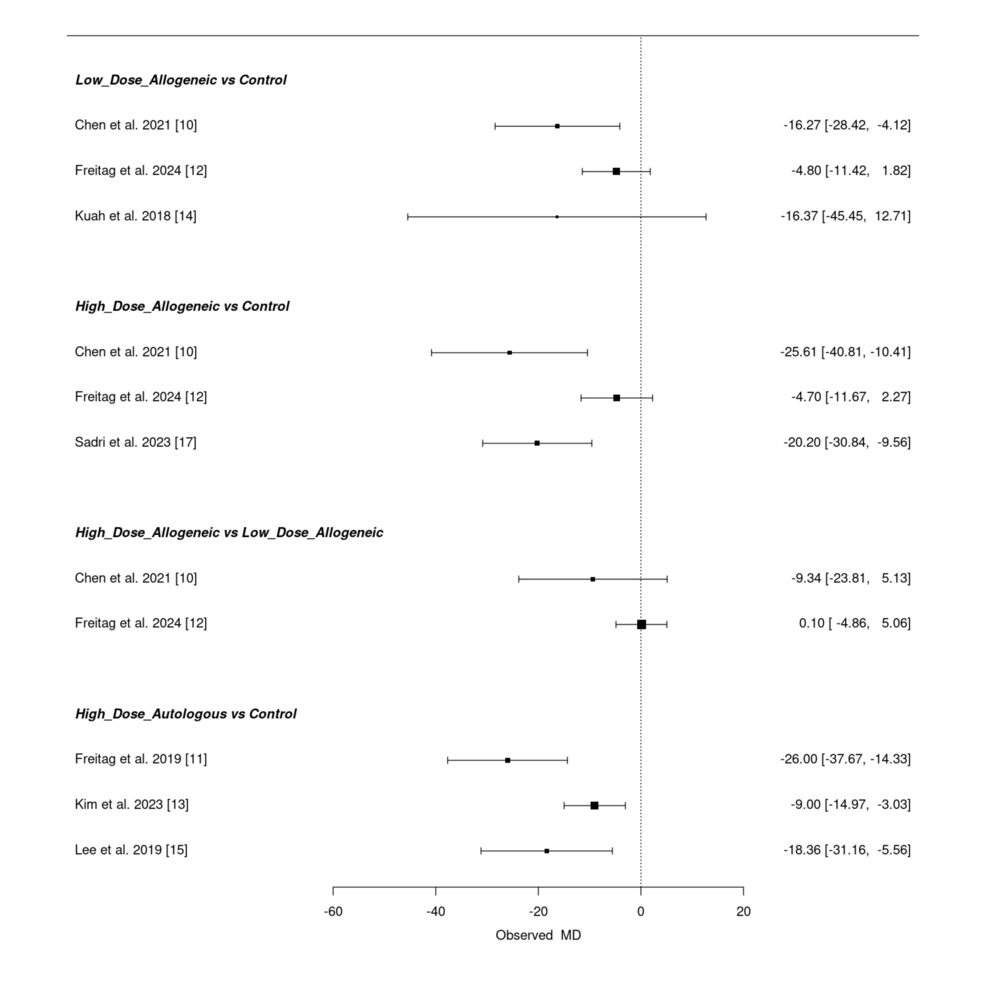
三、SUCRA 排名:高劑量自體 AD-MSCs 短期鎮(zhèn)痛優(yōu)勢顯著,異基因組緊隨其后
通過SUCRA分析,高劑量自體AD-MSCs以75.99%的概率位列3個月VAS評分降低的首位,高劑量異基因 AD-MSCs 以 71.39% 緊隨其后,兩者顯著優(yōu)于低劑量異基因AD-MSCs(50.53%)和對照組(2.08%)。徑向秩圖和 Litmus Rank-O-Gram 均證實,高劑量自體組成為最優(yōu)治療的概率最高,早期鎮(zhèn)痛效果兼具高效性與穩(wěn)定性;高劑量異基因組雖稍遜,但仍顯著優(yōu)于低劑量和對照。低劑量異基因方案因效果波動且優(yōu)勢有限,臨床應用中更傾向選擇高劑量 AD-MSCs 以實現(xiàn)早期疼痛緩解的最大化效益。
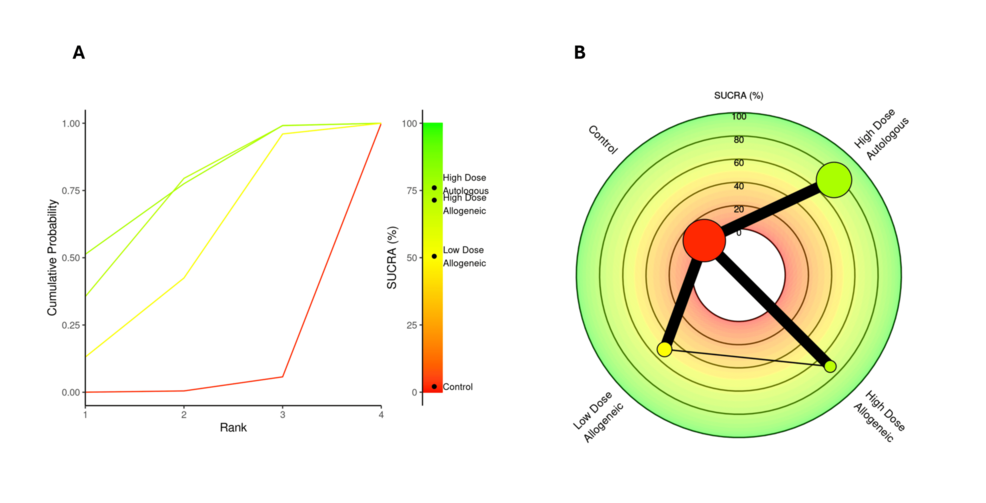
WOMAC分數(shù)變化(三個月)
一、傳統(tǒng)薈萃分析:高劑量異基因 AD-MSCs 早期功能改善領先,低劑量組效果不顯著
納入270名參與者的固定效應配對薈萃分析顯示,3 個月時高劑量異基因 AD-MSCs 的 WOMAC 評分改善最顯著,其次為高劑量自體AD-MSCs;低劑量異基因AD-MSCs效果最弱,與對照組相比無顯著差異(p=0.12)。異質性分析表明,低劑量異基因組無異質性(I2=0%),而高劑量異基因(I2=74%)和自體組(I2=69%)存在中至高度異質性,提示不同研究間干預措施的差異影響結果。漏斗圖顯示高劑量異基因組可能存在小規(guī)模研究效應,但無顯著出版偏倚。
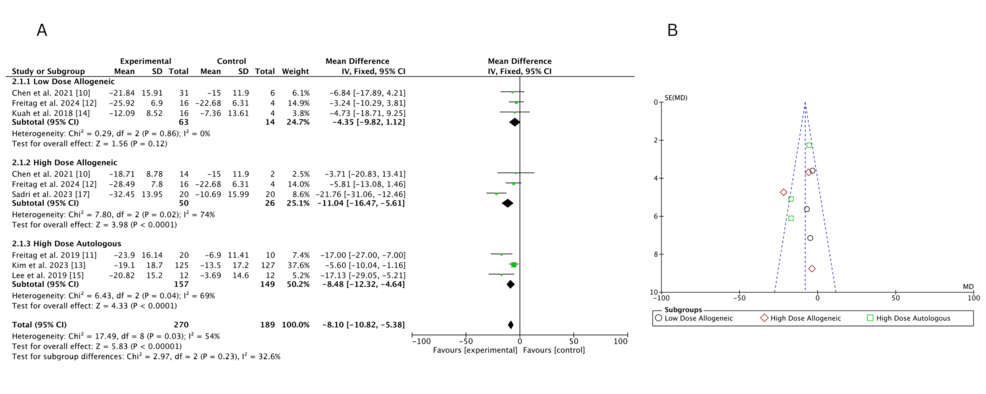
二、頻率學派網絡薈萃分析:高劑量組療效明確,低劑量組效果波動且有限
低劑量異基因AD-MSCs在Chen等(2021年)和Freitag 等(2024年)研究中僅表現(xiàn)出小幅改善(MD 分別為 – 6.46 和 – 3.24),Kuah 等(2018 年)因置信區(qū)間寬泛,療效不確定性突出。高劑量異基因 AD-MSCs 在 Sadri 等(2023 年)研究中實現(xiàn)強效改善,F(xiàn)reitag 等(2024 年)也觀察到顯著但較溫和的效果(MD=-5.81),但 Chen 等(2021 年)因置信區(qū)間較寬,效果存疑。高劑量自體 AD-MSCs 在 Freitag(2019 年,MD=-17.00)和 Lee(2019 年,MD=-17.13)等研究中均顯示顯著改善,即使 Kim 等(2023 年)的中等效果(MD=-5.60)仍優(yōu)于低劑量組。高劑量與低劑量異基因組的直接比較因置信區(qū)間重疊,未顯示明確劑量優(yōu)勢。

三、SUCRA 排名:高劑量自體 AD-MSCs 早期功能改善居首,異基因組緊隨其后
通過SUCRA分析,高劑量自體AD-MSCs以79.75%的概率位列3個月WOMAC評分改善第一,顯著優(yōu)于高劑量異基因 AD-MSCs(67.72%),低劑量異基因組排名最低(48.06%),對照組療效最差(4.46%)。徑向秩圖和 Litmus Rank-O-Gram 均證實,高劑量自體組憑借更穩(wěn)定的早期療效占據(jù)優(yōu)勢,而高劑量異基因組雖稍遜,但仍顯著優(yōu)于低劑量和對照。這一結果表明,早期關節(jié)功能改善中,高劑量AD-MSCs(尤其是自體來源)可作為優(yōu)先選擇,低劑量異基因方案因效果微弱且不穩(wěn)定,臨床價值有限。
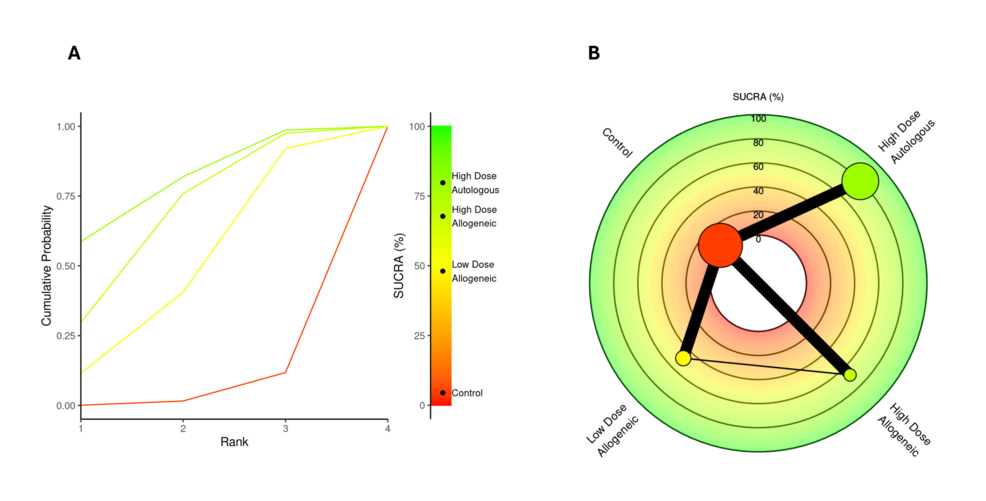
VAS評分變化(六個月)
一、傳統(tǒng)薈萃分析:高劑量自體 AD-MSCs 顯著緩解疼痛,低劑量異基因無明顯獲益
納入300名受試者的固定效應配對薈萃分析顯示,6個月時高劑量自體AD-MSCs的VAS評分改善最顯著,其次為高劑量異基因AD-MSCs;低劑量異基因AD-MSCs效果最差,結果與零效應線重疊,提示與對照組相比無顯著疼痛緩解。異質性分析表明,高劑量異基因(I2=90%)和自體組(I2=68%)存在較高異質性,低劑量異基因組中等異質性(I2=49%)。漏斗圖顯示高劑量異基因組可能存在小樣本研究效應,但整體分布平衡,出版偏倚風險較低。
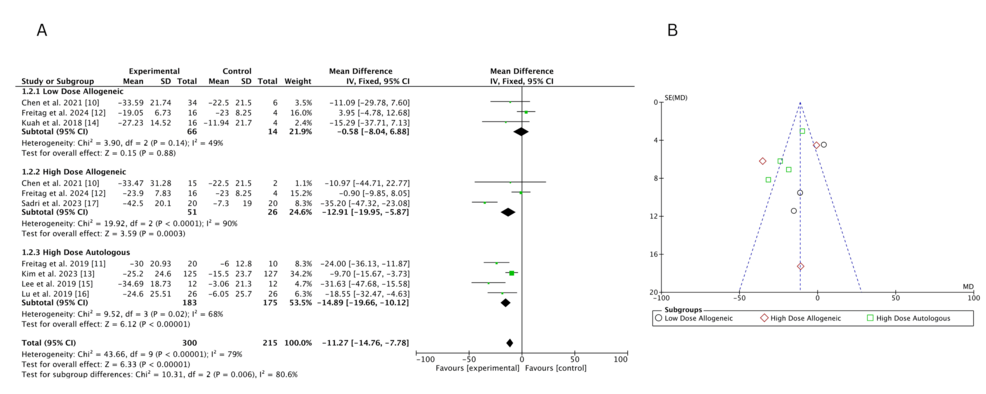
二、頻率學派網絡薈萃分析:高劑量組療效領先,低劑量組效果差異顯著
低劑量異基因 AD-MSCs 在不同研究中效果不一致:Chen 等(2021年)報告中度疼痛緩解,F(xiàn)reitag 等(2024年)卻顯示輕微正值,Kuah 等(2018年)因置信區(qū)間寬泛,療效不確定性突出。高劑量異基因 AD-MSCs 在 Sadri 等(2023 年)研究中表現(xiàn)優(yōu)異,但其他研究效應較弱且置信區(qū)間重疊,一致性不足。高劑量自體 AD-MSCs 在 Freitag(2019 年,MD=-24.00)和 Lee(2019年,MD=-31.63)等研究中均顯示強效鎮(zhèn)痛,盡管部分研究(如 Kim 等 2023 年)效果較溫和,但整體仍為疼痛緩解的最優(yōu)方案。
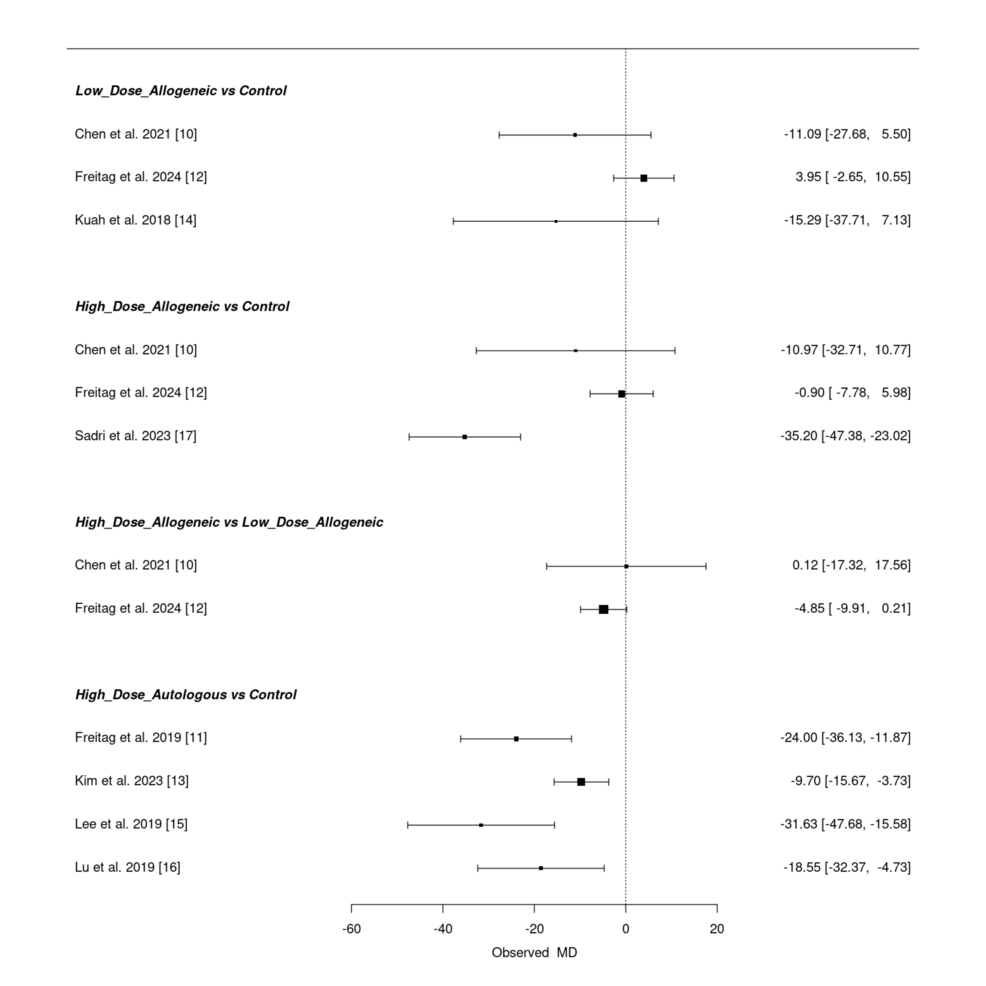
三、核心趨勢與關鍵差異
6 個月時,高劑量自體 AD-MSCs 在疼痛緩解(VAS 評分)中保持領先地位,療效穩(wěn)定且顯著優(yōu)于低劑量異基因 AD-MSCs;高劑量異基因 AD-MSCs 雖在部分研究中表現(xiàn)突出,但受異質性影響,整體療效略遜于自體組。低劑量異基因 AD-MSCs 因效果微弱、置信區(qū)間寬泛,臨床獲益不明確。兩類高劑量方案的異質性提示不同研究間的干預差異(如細胞制備、注射技術)可能影響結果,而低劑量方案的無效性進一步支持臨床實踐中優(yōu)先選擇高劑量 AD-MSCs 以實現(xiàn)疼痛管理的最大化效益。
WOMAC分數(shù)變化(六個月)
傳統(tǒng)薈萃分析:高劑量異基因AD-MSCs顯著改善WOMAC評分,低劑量組效果不明確
納入 300 名參與者的固定效應配對薈萃分析顯示,6個月時高劑量異基因AD-MSCs的WOMAC評分改善最顯著,其次為高劑量自體AD-MSCs;低劑量異基因AD-MSCs與對照組相比無顯著差異。異質性分析表明,高劑量異基因組存在高度異質性(I2=88%),自體組中等異質性(I2=74%),低劑量異基因組無異質性(I2=0%)。漏斗圖提示高劑量異基因組可能存在小規(guī)模研究效應,但無顯著出版偏倚。
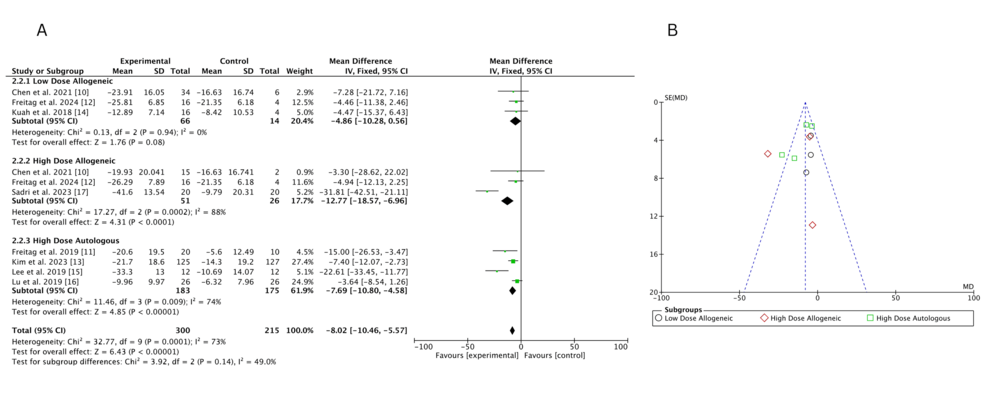
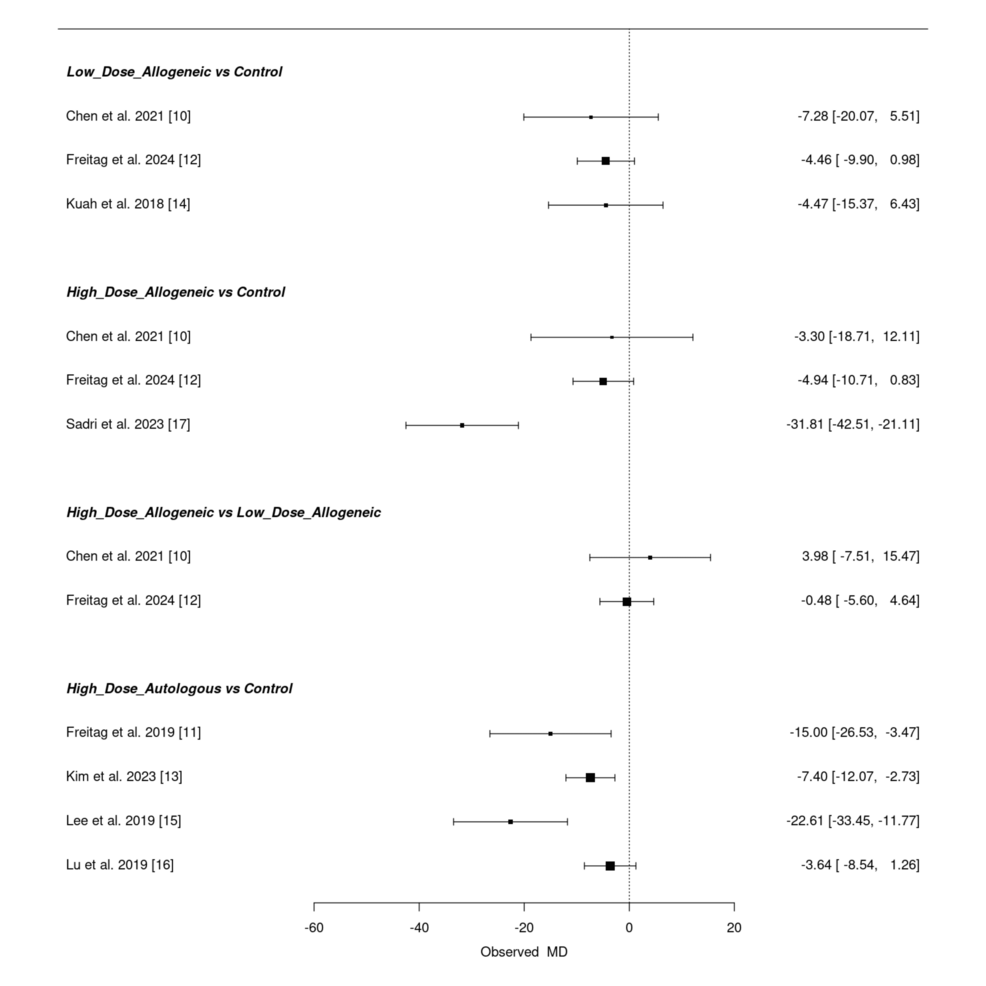
頻率學派網絡薈萃分析:高劑量組療效領先,低劑量組效果多變且不確定
低劑量異基因AD-MSCs在不同研究中效果不一,部分研究置信區(qū)間寬泛,顯示治療反應差異;高劑量異基因 AD-MSCs 在 Sadri 等(2023年)研究中表現(xiàn)突出,但其他研究效應較小且置信區(qū)間重疊。高劑量自體 AD-MSCs 在 Lee 等(2019 年)和 Freitag 等(2019年)研究中顯示顯著改善,但Lu等(2019年)研究因置信區(qū)間跨過零,提示療效變異性。高劑量與低劑量異基因組的直接比較未顯示明確優(yōu)勢(置信區(qū)間重疊)。
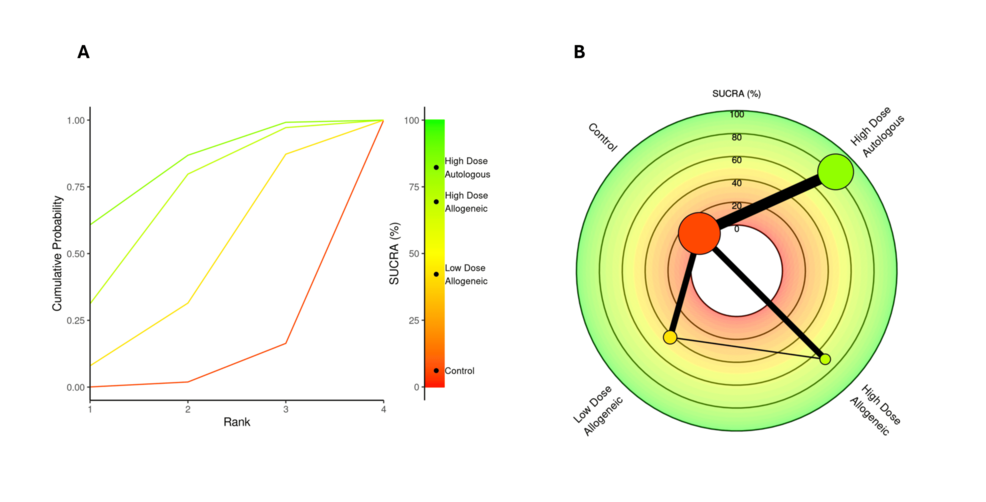
三、SUCRA 排名:高劑量異基因AD-MSCs中期功能改善領先,自體組稍居次位
通過 SUCRA 分析,高劑量異基因 AD-MSCs 以74.59%的概率位列6個月WOMAC評分改善第一,超越高劑量自體 AD-MSCs(67.62%),低劑量異基因組排名中等(52.11%),對照組療效最差(5.67%)。徑向秩圖和 Litmus Rank-O-Gram 均顯示,高劑量異基因組隨時間推移有效性提升,成為中期關節(jié)功能改善的最優(yōu)方案,而自體組因部分研究效果差異稍居次位,低劑量組因效果不穩(wěn)定仍缺乏明確臨床優(yōu)勢。
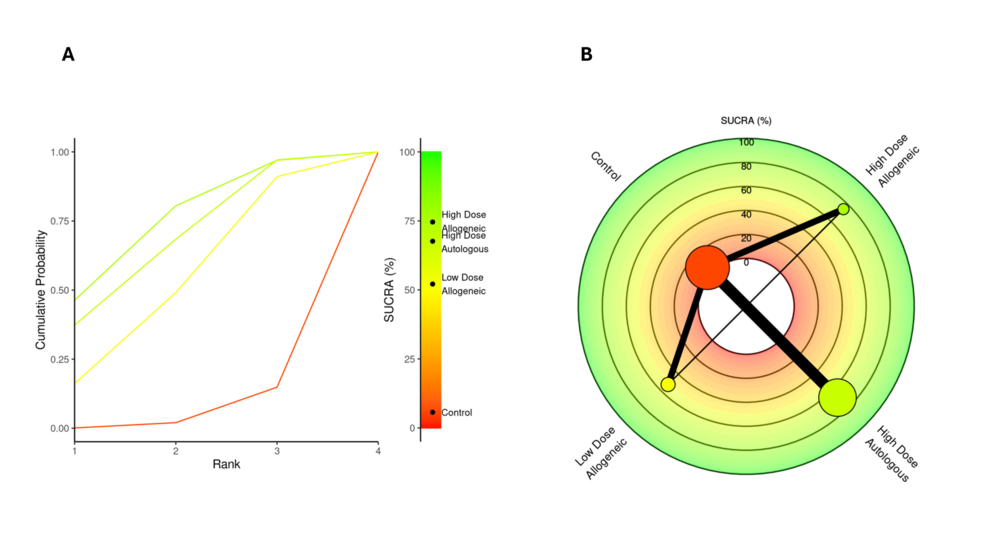
VAS評分變化(12個月)
傳統(tǒng)薈萃分析:高劑量自體AD-MSCs鎮(zhèn)痛效果最優(yōu),異質性特征差異顯著
研究納入163名受試者,通過固定效應配對薈萃分析比較不同劑量及來源的脂肪間充質干細胞(AD-MSCs)對 12 個月時 VAS 評分的影響。結果顯示,高劑量自體AD-MSCs療效最顯著,其次為高劑量異基因AD-MSCs,低劑量異基因 AD-MSCs 效果較弱但仍顯著。異質性分析顯示,低劑量異基因組無異質性(I2=0%),而高劑量自體組(I2=63%)和高劑量異基因組(I2=82%)存在中至高度異質性,提示不同研究間存在差異;漏斗圖顯示高劑量異基因組可能存在小規(guī)模研究效應。

頻率學派網絡薈萃分析:高劑量自體AD-MSCs鎮(zhèn)痛優(yōu)勢穩(wěn)定,低劑量異基因療效差異較大
通過直接與間接比較評估三種治療方案,高劑量自體 AD-MSCs 在多項研究中均表現(xiàn)出 VAS 評分最大降幅,療效明確且顯著。高劑量異基因 AD-MSCs 在部分研究中效果突出,但部分研究置信區(qū)間較寬,提示療效異質性。低劑量異基因 AD-MSCs 效果不一,部分研究顯示顯著鎮(zhèn)痛,另一些研究因置信區(qū)間寬泛而存在不確定性。高劑量與低劑量異基因組的直接比較未顯示明顯優(yōu)勢(置信區(qū)間重疊)。
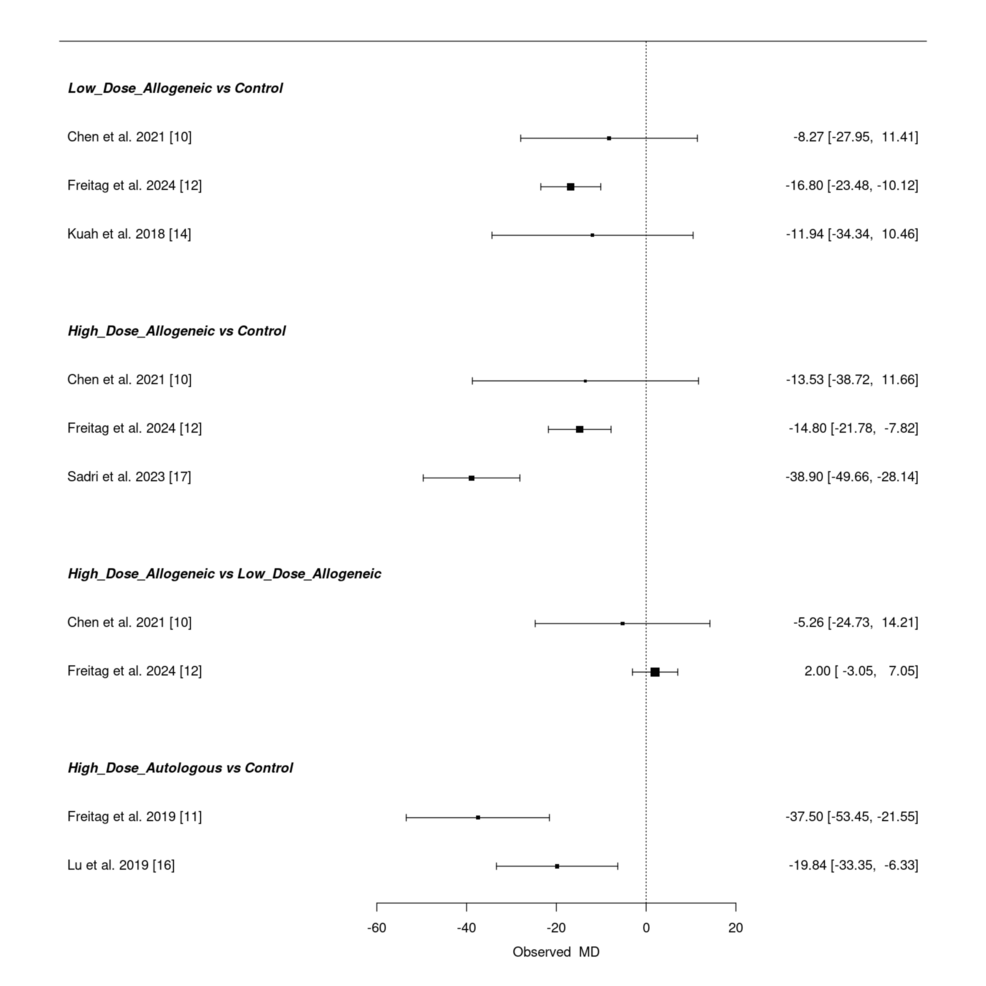
SUCRA排名:高劑量自體AD-MSCs持續(xù)領先,療效排序明確
通過 SUCRA 分析對有效性排名,高劑量自體 AD-MSCs 以 81.65% 的概率位列第一,為12 個月時降低 VAS 評分的最優(yōu)方案;高劑量異基因 AD-MSCs 排名第二(SUCRA=69.32%),低劑量異基因AD-MSCs排名第三(SUCRA=46.48%),對照組療效最差(SUCRA=2.55%)。徑向秩圖和Litmus Rank-O-Gram均證實,高劑量自體AD-MSCs在鎮(zhèn)痛效果上具有持續(xù)且顯著的優(yōu)勢,而低劑量異基因組因研究間結果差異,有效性概率較低。

WOMAC分數(shù)變化(12個月)
傳統(tǒng)薈萃分析:高劑量異基因AD-MSCs顯著改善WOMAC評分,異質性特征差異顯著
研究納入 163 名受試者,通過固定效應配對薈萃分析比較不同劑量及來源的脂肪間充質干細胞(AD-MSCs)對 12 個月時 WOMAC 評分的影響。結果顯示,高劑量異基因 AD-MSCs 治療后評分改善最顯著,其次為高劑量自體 AD-MSCs,低劑量異基因 AD-MSCs 表現(xiàn)出中等程度改善。

異質性分析表明,高劑量異基因組(I2=89%)和高劑量自體組(I2=94%)存在高度異質性,低劑量異基因組異質性中等(I2=49%)。漏斗圖顯示高劑量異基因組存在不對稱性,提示可能存在小樣本研究效應,但尚未明確為發(fā)表偏倚。
頻率學派網絡薈萃分析:高劑量異基因與自體 AD-MSCs 療效領先,低劑量異基因效果多變
通過直接與間接比較評估三種治療方案,高劑量異基因 AD-MSCs 在 Sadri 等(2023 年)研究中表現(xiàn)出最強改善,F(xiàn)reitag 等(2024 年)研究也證實其顯著效果,但 Chen 等(2021 年)研究因置信區(qū)間較寬(MD=-6.12, 95% CI: -20.12~7.88)存在效果不確定性。高劑量自體 AD-MSCs 在 Freitag 等(2019 年)研究中 WOMAC 評分降幅顯著,但 Lu 等(2019 年)研究顯示效果較弱且不確定。低劑量異基因 AD-MSCs 效果差異較大,F(xiàn)reitag 等(2024 年)研究顯示中等改善,而 Kuah 等(2018 年)研究未觀察到顯著效果。高劑量與低劑量異基因組的直接比較因置信區(qū)間重疊,未顯示明確優(yōu)勢。
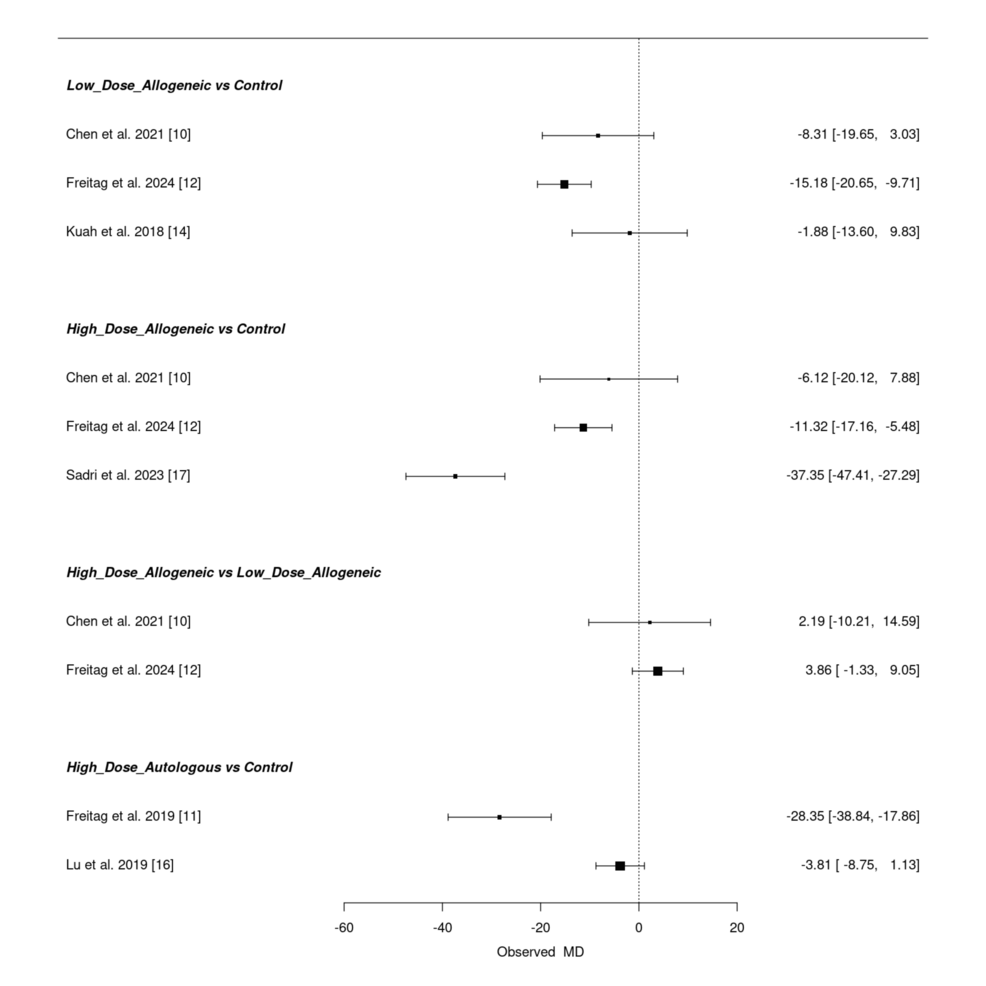
SUCRA 排名:高劑量異基因AD-MSCs略優(yōu),自體組緊隨其后
通過SUCRA分析對改善WOMAC評分的有效性排序,高劑量異基因AD-MSCs以71.71%的概率位列第一,稍高于高劑量自體AD-MSCs(64.63%),表明兩者在長期癥狀改善中持續(xù)領先;低劑量異基因AD-MSCs排名第三(SUCRA=54.66%),對照組療效最差(SUCRA=8.99%)。徑向秩圖和 Litmus Rank-O-Gram 均顯示,高劑量干預方案(異基因與自體)顯著優(yōu)于低劑量及對照,其中高劑量異基因組憑借更穩(wěn)定的綜合效應在排名中略占優(yōu)勢,而高劑量自體組因部分研究效果差異稍居次位。
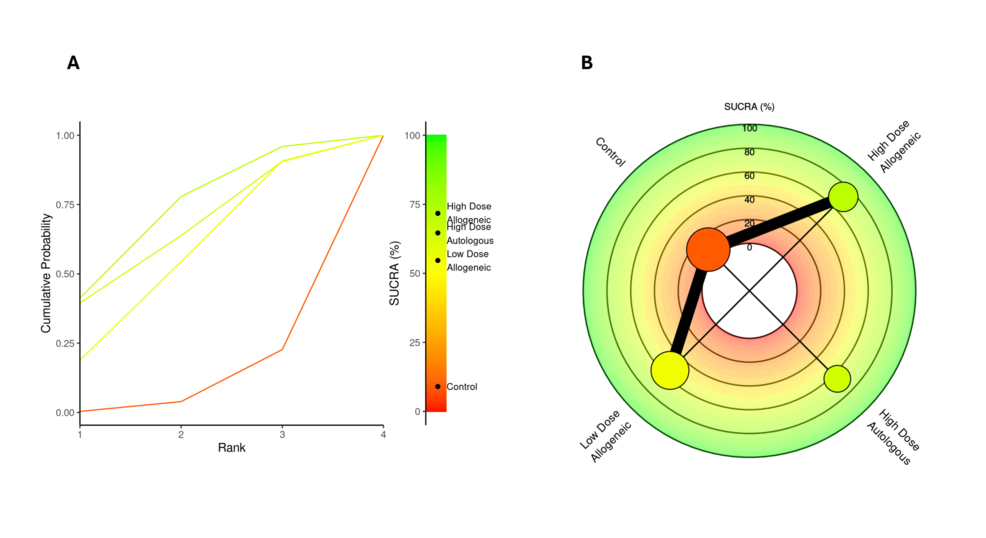
SUCRA總體排名
圖22總結了所有時間點的疼痛緩解和功能改善的總體SUCRA排名。
不良反應(總體,所有時間點)
圖23總結了不良影響結果。它同時呈現(xiàn)了傳統(tǒng)薈萃分析森林圖、頻率學派 NMA 森林圖和 SUCRA 排名。

討論:干細胞治療骨關節(jié)炎的療效概述和治療模式
主要發(fā)現(xiàn)總結:本研究利用傳統(tǒng)的成對薈萃分析和網狀薈萃分析,對3個月、6個月和12個月時間點的AD-MSC療法治療膝關節(jié)OA的療效和安全性進行了全面評估。研究結果突出了疼痛減輕(VAS評分)、功能改善(WOMAC評分)和不良反應的不同模式,從而可以對治療方案進行比較評估。
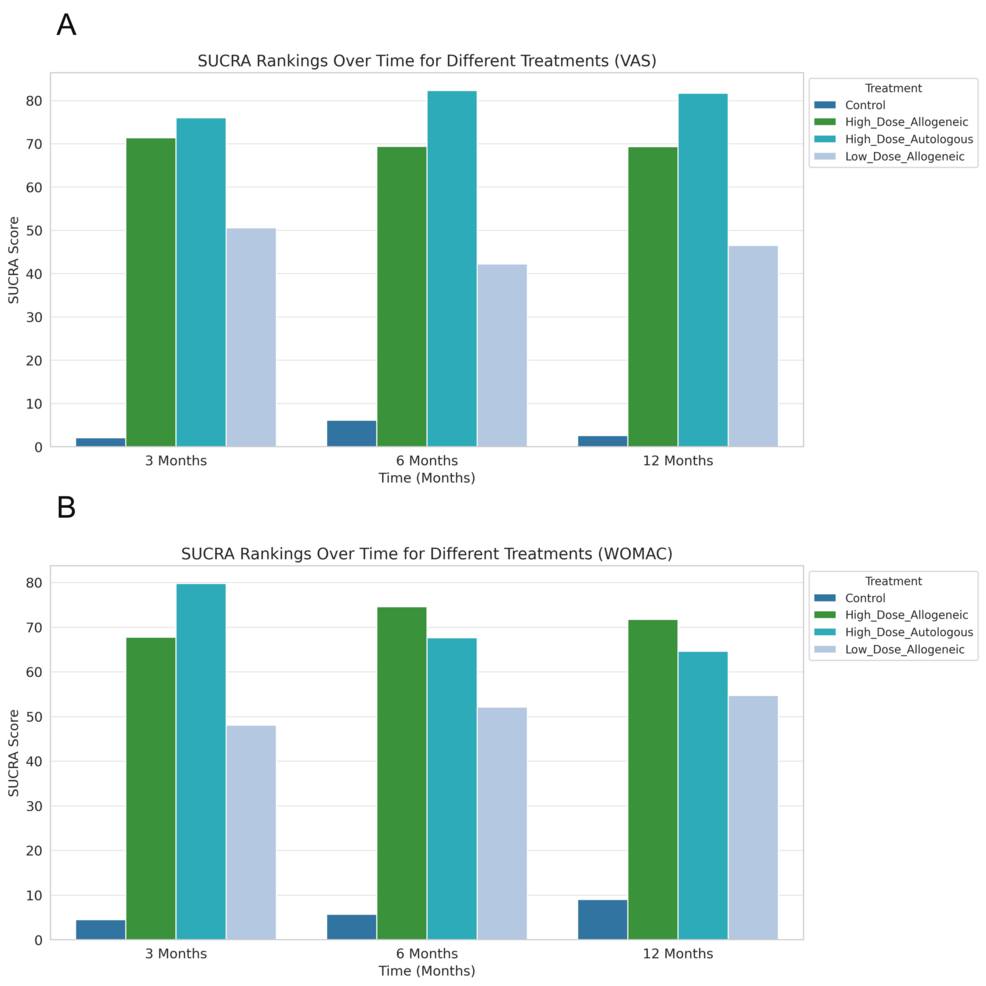
MSC 療法的長期有效性:三個月后,高劑量自體 AD-MSC 療法在緩解疼痛方面排名最高(VAS SUCRA:75.99%),其次是高劑量異體 AD-MSC 療法(SUCRA:71.39%),而低劑量異體 AD-MSC 療法的排名明顯較低(SUCRA:50.53%)。在功能改善方面也觀察到了類似的趨勢,高劑量自體 AD-MSC 療法(WOMAC SUCRA:79.75%)和高劑量異體 AD-MSC 療法(SUCRA:67.72%)均優(yōu)于低劑量 AD-MSC 療法(SUCRA:48.06%)。
六個月后,高劑量自體AD-MSCs仍是緩解疼痛最有效的方法(VAS SUCRA:82.27%),但自體和異體高劑量AD-MSCs之間的差距縮小。值得注意的是,功能改善排名發(fā)生了變化,高劑量異體MSCs在WOMAC改善方面超過了自體AD-MSCs(SUCRA:74.59% vs. 67.62%)。
12個月時,高劑量自體AD-MSCs繼續(xù)提供最高的疼痛緩解(VAS SUCRA:81.65%),而高劑量異基因AD-MSCs在功能改善方面排名最高(WOMAC SUCRA:71.71%)。在所有時間點,對照組的排名始終最低,這證實了其在控制OA癥狀方面的療效與基于AD-MSCs的療法相比有限。
VAS 與 WOMAC 趨勢(一致與分歧):疼痛緩解(VAS)和功能改善(WOMAC)的治療排名隨時間推移既一致又分歧。三個月時,高劑量自體 AD-MSC 在兩種結果中均排名最高,表明其在癥狀緩解和關節(jié)功能方面均具有顯著的早期療效。然而,隨著時間的推移,排名開始出現(xiàn)分歧。六個月時,高劑量自體 AD-MSC 仍然是緩解疼痛最有效的治療方案(VAS SUCRA:82.27%),而高劑量異基因 AD-MSC 則成為功能改善方面排名最高的治療方案(WOMAC SUCRA:74.59%)。這種分歧在 12 個月時仍然存在,高劑量自體 AD-MSC 在緩解疼痛方面保持領先地位(VAS SUCRA:81.65%),而高劑量同種異體 AD-MSC 在功能恢復方面繼續(xù)排名最高(WOMAC SUCRA:71.71%)。
這些趨勢表明,短期疼痛緩解與長期關節(jié)功能改善可能存在不同的生物學機制。自體AD-MSC可能通過快速免疫調節(jié)、高細胞因子分泌和快速抑制炎癥發(fā)揮其早期鎮(zhèn)痛作用。相比之下,同種異體AD-MSC可能通過促進持續(xù)的組織重塑和關節(jié)結構與功能的逐漸改善,提供延遲但持久的益處。
療效分歧機制與劑量依賴性效應
疼痛緩解與功能改善的排名分歧反映了不同作用機制:自體AD-MSCs可能通過快速免疫調節(jié)和抗炎反應實現(xiàn)早期及持續(xù)鎮(zhèn)痛,而異體 AD-MSCs 則通過促進長期組織重塑和軟骨修復,在中晚期展現(xiàn)更優(yōu)的關節(jié)功能改善。劑量依賴性顯著,高劑量組在所有時間點均優(yōu)于低劑量組,提示細胞濃度對療效的關鍵影響。研究支持 “雙階段模型”:自體療法以強效抗炎主導短期至長期的疼痛控制,異體療法通過延遲但持久的組織修復實現(xiàn)功能優(yōu)化,為骨關節(jié)炎(OA)的精準治療提供了基于細胞來源和劑量的差異化策略。
自體和異體間充質干細胞治療骨關節(jié)炎的效果為什么會產生差異?
自體和異體AD-MSC隨時間推移產生的不同療效模式可能歸因于細胞存活率、免疫原性和作用機制的差異。高劑量自體AD-MSC在3個月、6個月和12個月時持續(xù)提供最佳的疼痛緩解效果,這可能是由于快速的細胞整合、強大的早期旁分泌信號以及強效的抗炎細胞因子釋放,尤其是IL-10和TGF-β。自體干細胞來源于患者,因此不太可能被免疫系統(tǒng)清除,從而能夠產生更強勁的早期旁分泌信號并快速緩解癥狀。
相比之下,同種異體AD-MSC雖然并非自體來源,但它們具有免疫特權特性,能夠調節(jié)宿主的免疫力。這些效應,包括抑制T細胞增殖和促進M2巨噬細胞極化,可能營造持續(xù)的抗炎和促再生關節(jié)環(huán)境。這種免疫重塑可以減輕排斥反應,并促進更長期的持續(xù)存在和整合,從而支持軟骨修復并隨著時間的推移改善功能。
總體而言,觀察到的臨床趨勢可能通過AD-MSC療法的三種主要機制相互作用來解釋:(1) 旁分泌信號傳導,通過抗炎細胞因子介導早期癥狀緩解;(2) 免疫調節(jié),改變慢性炎癥途徑并促進免疫耐受;以及 (3) 組織再生,實現(xiàn)關節(jié)組織的長期結構修復。這些效應隨時間動態(tài)演變,并受AD-MSC來源、劑量和生物學行為的影響。這或許有助于解釋為何自體細胞能夠快速緩解疼痛,而同種異體細胞則更有利于長期功能恢復。
自體與異體間充質干細胞在治療骨關節(jié)炎上,有什么區(qū)別?
AD-MSC療法在緩解疼痛(VAS)和改善功能(WOMAC)方面的排名在不同時間點呈現(xiàn)出顯著變化,反映了作用機制、劑量依賴性反應和治療持久性的差異。高劑量自體 AD-MSC 可隨時間持續(xù)提供鎮(zhèn)痛效果,在 3 個月、6 個月和 12 個月時疼痛緩解排名最高。值得注意的是,高劑量同種異體 AD-MSC 在 6 個月和 12 個月時功能改善排名最高,表明其對關節(jié)功能的再生作用更為漸進和持久。
間充質干細胞治療骨關節(jié)炎的安全性怎么樣?
不良反應和安全性:安全性分析強調了療效與不良反應之間的重要權衡。在AD-MSC治療中,低劑量同種異體AD-MSC的不良反應風險最高(SUCRA:22.24%),其次是高劑量同種異體AD-MSC(SUCRA:26.52%)。高劑量自體AD-MSC雖然安全性低于對照組,但在AD-MSC治療中仍然是最安全的(SUCRA:54.08%)。對照組被認為是最安全的選擇(SUCRA:97.16%)。
嚴重不良事件(AD-MSCs 療法有風險嗎?):在納入的研究中,嚴重不良事件 (SAE) 罕見,對照組的發(fā)生率與 AD-MSC 治療組相似或更高。沒有 SAE 直接歸因于 AD-MSC 療法。
臨床相關性(不良事件是否值得獲益?):雖然高劑量 AD-MSC 偶爾會導致注射部位短暫性關節(jié)疼痛或腫脹,但這些影響較輕且無需干預即可緩解。
療效-安全性平衡與個體化治療策略如何選擇?
高劑量AD-MSC(尤其是自體來源)在疼痛緩解和功能改善中優(yōu)勢顯著,且未伴隨劑量依賴性風險增加,打破 “低劑量更安全” 的傳統(tǒng)認知。臨床決策應結合患者病情(如骨關節(jié)炎嚴重程度)和耐受性,對中重度患者而言,高劑量自體AD-MSC 可實現(xiàn)安全性與療效的最佳平衡;而異基因制劑的選擇需警惕低劑量方案的風險 – 獲益比。研究強調,細胞來源(自體 vs. 異基因)和劑量是影響AD-MSC療法安全性與有效性的核心因素。
脂肪間充質干細胞在膝關節(jié)骨關節(jié)炎 (OA) 中的治療作用是什么?
本網狀薈萃分析的結果為 AD-MSCs 療法在膝關節(jié)骨關節(jié)炎的臨床應用提供了寶貴的見解。高劑量 AD-MSCs,尤其是自體 AD-MSCs,在緩解疼痛方面表現(xiàn)出更佳的效果(VAS),而高劑量同種異體AD-MSCs在長期關節(jié)功能方面則表現(xiàn)出更顯著的改善(WOMAC)。這些結果表明,AD-MSC 療法可能是一種比皮質類固醇或透明質酸等傳統(tǒng)關節(jié)內注射療法更有效的替代方案,尤其適用于對傳統(tǒng)藥物或注射療法無效的患者。
臨床醫(yī)生應該選擇自體還是異體間充質干細胞 (MSC)?
自體和異體間充質干細胞 (AD-MSC) 之間的選擇應以治療目標和臨床情況為指導。高劑量自體AD-MSC在所有時間點均表現(xiàn)出更強效、更持續(xù)的疼痛緩解效果,使其成為尋求快速控制癥狀的患者的理想選擇。相比之下,高劑量異體AD-MSC在6個月和12個月時的功能改善排名更高,表明其具有更佳的長期再生效果。實際因素也會影響臨床決策。自體 AD-MSC需要從患者體內采集和處理,這可能會增加手術負擔、成本和治療延遲。同時,異體AD-MSC具有現(xiàn)成的便利性,更容易獲取,并可能具有更廣泛的可擴展性。
結論
這項網絡薈萃分析表明,與傳統(tǒng)的膝關節(jié)骨關節(jié)炎關節(jié)內注射治療相比,高劑量AD-MSC療法在緩解疼痛和改善功能方面效果更佳。研究觀察到明顯的劑量依賴性反應,高劑量在癥狀緩解和功能恢復方面始終優(yōu)于低劑量。高劑量自體AD-MSC在快速和持續(xù)緩解疼痛方面效果最佳,而高劑量異基因AD-MSC在6個月和12個月的長期功能恢復方面效果最佳,表明兩種療法的療效特征各異。雖然高劑量組患者出現(xiàn)短暫性關節(jié)疼痛和腫脹等輕度至中度不良反應的幾率更高,但嚴重不良事件罕見,且發(fā)生率與對照組相似,這支持了AD-MSC療法的總體安全性。
臨床上,對于尋求立即緩解癥狀的患者,高劑量自體AD-MSC可能更佳,而高劑量異體AD-MSC可能更有利于長期關節(jié)功能。鑒于其良好的安全性和相對有效性,AD-MSC療法對于對皮質類固醇或透明質酸等常規(guī)治療無效的患者而言,是一種頗具前景的替代方案。
未來的研究應優(yōu)先考慮超過12個月的長期隨訪、自體和異體AD-MSC的直接頭對頭比較、基于生物標志物的患者選擇以及給藥方案的優(yōu)化。本研究提供了一個框架,用于指導在膝骨關節(jié)炎治療中根據(jù)劑量和來源選擇AD-MSC療法。
參考資料:Kasagga A, Verma A, Saraya E, et al. (April 21, 2025) Autologous Versus Allogeneic Adipose-Derived Mesenchymal Stem Cell Therapy for Knee Osteoarthritis: A Systematic Review, Pairwise and Network Meta-Analysis of Randomized Controlled Trials. Cureus 17(4): e82713. doi:10.7759/cureus.82713
免責說明:本文僅用于傳播科普知識,分享行業(yè)觀點,不構成任何臨床診斷建議!杭吉干細胞所發(fā)布的信息不能替代醫(yī)生或藥劑師的專業(yè)建議。如有版權等疑問,請隨時聯(lián)系我。




 掃碼添加微信
掃碼添加微信