自閉癥譜系障礙(ASD)作為一類高度異質性的神經發育性疾病,全球發病率已攀升至1:54(美國CDC 2020年數據),其核心癥狀——社交溝通障礙、重復刻板行為及感知覺異常——嚴重制約患者終身發展。盡管行為干預與藥物對癥治療可部分緩解癥狀,但約60%的ASD患者仍存在難治性功能缺陷,亟需靶向病理生理機制的創新療法。
近年來,免疫-神經軸異常在ASD發病中的作用逐漸明晰:小膠質細胞活化、促炎細胞因子失衡及母胎界面免疫耐受缺陷等證據,提示免疫調節可能成為突破性治療靶點。間充質干細胞(MSCs)憑借其多重修復潛能——包括抑制神經炎癥、促進突觸可塑性及通過外泌體介導的旁分泌效應——已在ASD動物模型中展現神經行為改善作用,但臨床轉化仍面臨療程設計、劑量優化及應答異質性等挑戰。
自閉癥兒童從5到9歲持續干細胞治療,深度重塑神經發育軌跡,同時消除癲癇!
2025年5月4號,國際著名期刊雜志“Cureus”發表了一篇“間充質基質細胞治療緩解自閉癥譜系障礙癥狀:病例報告”的文章[1]。

該報告介紹了一名患有嚴重自閉癥譜系障礙 (ASD)、癲癇和病理性腦電圖 (EEG) 的男孩的病例,該男孩在5.75歲至9歲之間接受了五次干細胞治療,治療采用來自非親屬供體的同種異體胎盤和臍帶組織的間充質干細胞。
每個療程后均觀察到顯著的臨床反應,包括癲癇發作消失、首次療程后腦電圖恢復正常以及自閉癥癥狀、社交技能和情緒表達持續改善。同種異體間充質干細胞可能為部分自閉癥譜系障礙兒童提供一種頗具吸引力的創新治療模式,并可能成為治療癲癇癥兒童的一種有前景的療法。
此外,該研究還提出了臨床研究方向,以開發這些創新療法并規劃未來的研究。
自閉癥的免疫病因學與間充質干細胞免疫調節特性的關聯
每60到150名兒童中就有1名患有自閉癥譜系障礙 (ASD),其中一些兒童的日常生活功能受到嚴重限制,包括溝通、社交互動和感官知覺方面的缺陷,以及重復性和限制性行為。癲癇發作會影響約20%的ASD兒童。

鑒于其癥狀多樣,治療方案多種多樣,以癥狀為導向,必須個體化定制。這些方案包括減輕癥狀的藥物治療,以及高度結構化和密集的行為、心理和/或教育治療,以培養生活技能并最大限度地減少挑戰性行為。然而,許多患者無法實現獨立,需要終生支持。
流行病學、血清學、免疫遺傳學和放射學證據越來越多地表明,相當一部分自閉癥譜系障礙 (ASD) 兒童存在免疫和炎癥病因。研究已將自閉癥譜系障礙 (ASD) 的標志性特征與以下因素聯系起來:先天性和適應性免疫反應功能障礙、母體血清中識別胎兒腦抗原的抗體、腦脊液和血漿中促炎細胞因子水平升高,以及自閉癥譜系障礙兒童腦內小膠質細胞的大小、密度和活性異常。
雖然尚無靶向生物療法,但基于間充質基質細胞 (MSC) 的療法 (MSCT) 因其跨人類白細胞抗原 (HLA) 屏障的強大免疫調節作用而被提出。這種獨特的非造血多能細胞群具有顯著的免疫調節、歸巢和分泌能力,已安全地整合到廣泛的臨床應用中,包括治療難治性移植物抗宿主病、慢性炎癥性疾病、心臟病和一系列自身免疫性疾病。
我們介紹了一名患有嚴重ASD和癲癇的兒童在接受五次間充質干細胞移植后病情的顯著改善。從這種創新治療方法中獲得的見解將被提出用于未來的研究。
自閉癥患者的介紹及家族史
病例介紹:一名32個月大男孩被診斷為自閉癥譜系障礙(ADOS評分23),臨床表現為協調性差、運動不耐受(行走約50米即疲倦)、震顫、環境感知及交流能力嚴重低下。18個月起出現不明原因發育倒退,逐漸喪失所有言語及溝通技能。醫生建議立即啟動職業治療與溝通治療。患兒自出生起受嚴重胃食管反流困擾,每日嘔吐、胃灼熱致體重增長緩慢,且對蚊蟲叮咬過敏。
診斷1個月后,患兒出現強直陣攣性癲癇發作,腦電圖顯示左半球高頻中央顳區棘波(無全身癥狀)(圖1A)。初始使用丙戊酸治療,因控制不佳,先后加用卡馬西平、左乙拉西坦、大麻二酚油及氯硝西泮(搶救用藥),但1年內仍因8次失控性癲癇發作住院。長期頻繁發作及進食不足導致體重驟降,并發危及生命的嚴重呼吸暫停。母親孕期曾患甲狀腺功能減退癥,經Eltroxin治療,無其他妊娠并發癥,患兒足月出生。
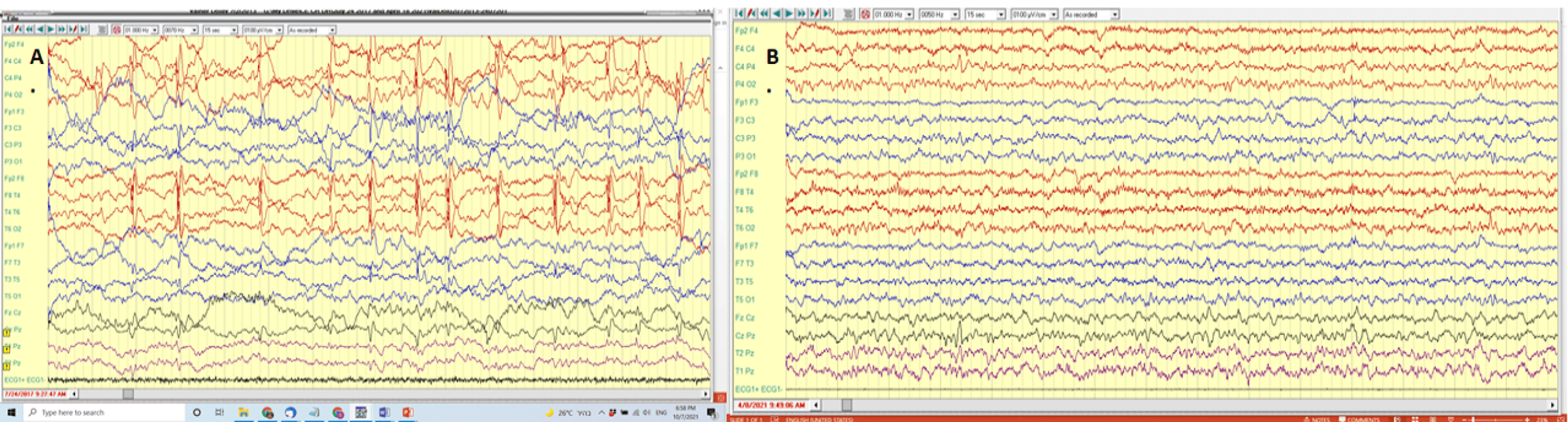
A)治療前睡眠腦電圖顯示癲癇樣放電,左半球出現多個棘波,并伴有繼發性全身性放電(2017年7月24日)。B)治療后腦電圖顯示睡眠記錄正常,無癲癇樣放電(2021年8月)。
家族史:孩子有一個11個月大的哥哥,患有癲癇和典型的自閉癥早期癥狀,還有一個7歲的妹妹,發育正常。父母都患有哮喘、注意力缺陷/多動障礙(ADHD)和學習困難,父親患有甲狀腺功能減退癥。作為父母,他們的工作和職業都很正常。 這位母親的家族中有很多學習困難和多動癥患者,其中一位叔叔患有輕度自閉癥,他的女兒被診斷患有自閉癥。另一位叔叔患有克羅恩病,他的一個女兒患有ASD,另一個患有躁郁癥。父親的家族病史包括甲狀腺功能減退癥,一個兄弟患有ASD和嚴重的社交焦慮癥。
異體間充質基質細胞療法治療自閉癥的過程
家長在知情同意的情況下同意讓患兒接受非親緣母嬰的靜脈注射異體間充質基質細胞移植(alloMSCT)(表1;附錄A、B)。在整個治療期間,患兒繼續接受相同的職業和交流治療。所有評估均由神經病學和/或兒童發展專業的獨立兒科醫生在兒童發展研究所(隸屬于國家規定的健康基金)進行并記錄在案。
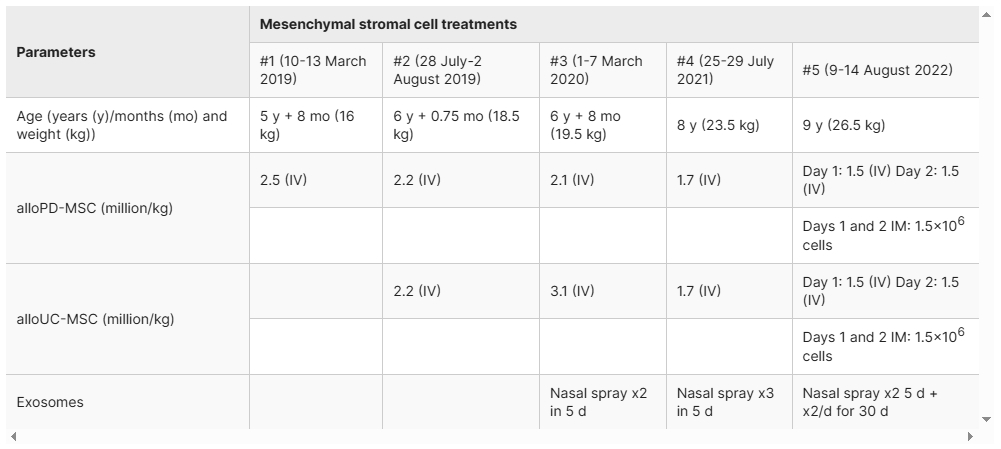
5歲8個月時,孩子接受了一劑2.5×10^6胎盤來源間充質干細胞(PD-MSC)/千克(MSCT;2019年3月)。 兩天后,孩子變得更加放松,開始與兄弟姐妹玩耍。 治療18周后,沒有出現癲癇發作,腦電圖評估結果正常(圖1B)。 與此同時,患兒開始用較長的句子和較好的發音與人交流,主動與人交談,并表現出社交興趣和互動。他已經斷奶,不再使用奶瓶和尿布,這反映出他的發育已經成熟。此外,他的嘔吐頻率和胃灼熱程度也有所改善,因此食欲和體重都有所提高。
間充質干細胞移植治療自閉癥的初期癥狀改善情況(四個月后):四個月后,患兒接受第二次MSCT(2.2×10?PD-MSC/kg),兩日后續注2.2×10?UCD-MSC/kg,感覺運動能力顯著提升,可獨立行走15-20分鐘無疲倦,協調能力改善至能自主擺動。抗驚厥藥物及大麻類藥物逐步停用。12周停藥期結束(2019年12月),患兒首次握筆繪制簡筆畫及字母,此前因震顫和運動障礙無法完成;言語與社交互動能力增強,表現為環境感知提升、詞匯量增加及自發造句(句子簡短但有條理,2020年1月)。
間充質干細胞移植治療自閉癥及長期隨訪(八個月后至七歲):八個月后(2020年3月)行第三例MSCT,靜脈輸注2.1×10?PD-MSC/kg,兩日后續注3.1×10?alloUCD-MSC/kg,治療當天經鼻給予同供體MSC來源外泌體(3×10?MSC/kg)。患兒出現短暫發熱、寒戰,撲熱息痛治療后緩解。七歲隨訪顯示,情緒發育突破性進展:首次主動表達感受、描述不適,主動與陌生人交流、打招呼,能用英語朗讀整本書、希伯來語溝通,并自創規則游戲。
七歲半癥狀管理與檢查:患兒7.5歲時評估燒心、嘔吐癥狀,確診嗜酸細胞性食管炎,采用耐信凝膠聯合外用布地奈德(0.5mg,每日兩次)治療。
第四至五次MSCT治療及持續改善:因新冠疫情,第四次MSCT推遲至第三次治療18個月后,劑量調整為靜脈輸注1.7×10?PD-MSC/kg及UC-MSC/kg,同步連續三日經鼻給予外泌體。
治療4-6周后,焦慮與多動減輕,言語能力進一步提升(詞匯量、句子長度及發音改善),社交互動顯著增強:主動聯系朋友、減少攻擊性、關注他人需求,非語言交流(面部表情等)及日常活動獨立性(洗澡、作業)提升,可理解復雜指令并自主執行計劃,學業表現(注意力、閱讀寫作、學術興趣)及社交適應性均獲進步。11個月后(2022年8月)行MSCT,采用靜脈、肌肉注射聯合經鼻外泌體給藥(持續30天)。
后續六個月,認知能力顯著提升:思維速度與清晰度、決策成熟度、情感及生理需求表達能力增強,出現社交互動渴望并主動參與家務。自閉癥治療評估清單(ATEC)及社會反應量表-2(SRS第二版)所有子領域分數恢復正常范圍,歷次治療前血液檢查均顯示各項指標正常。
從五大要點討論干細胞治療自閉癥的前景
討論:該患兒患有重度自閉癥譜系障礙(ASD)、難治性癲癇發作和胃腸道癥狀,在接受五次異基因MSCT治療后,持續表現出積極的臨床反應(表2)。改善包括自閉癥行為的典型特征減少、癲癇發作和胃腸道癥狀消退、社交技能和情緒表達能力改善,以及病理性腦電圖恢復正常。
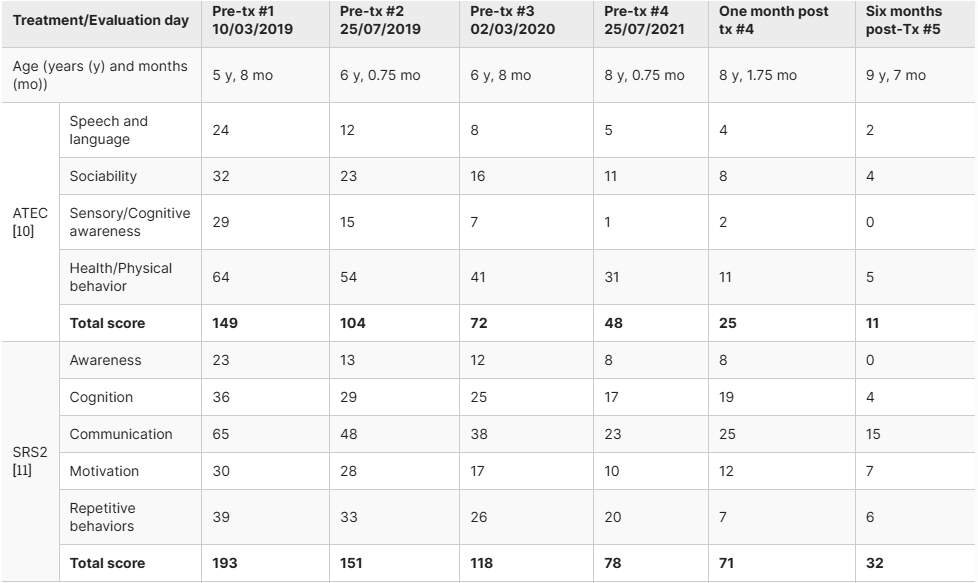

自閉癥治療評估清單(ATEC)由四個分量表組成:I.言語/語言交流(14項),II.社交能力(20項),III.感覺/認知意識(18項),以及IV.健康/身體/行為(25項)。分數越低,自閉癥表現越輕;社會反應量表第二版(SRS2)是一個65項的量表,由以下分量表組成:I.社會意識(8項),II.社會認知(12項),III.社交交流(22項),IV.社會動機(11項),以及V.興趣狹窄和重復行為(12項)。每個項目均采用四點李克特量表進行評分。
1、家族病史揭示ASD免疫學基礎
患兒家族中自身免疫性疾病、自閉癥譜系障礙(ASD)及其他神經精神疾病高發,這與ASD和免疫系統存在關聯的研究結論相契合。這一發現暗示ASD亞組可能存在免疫學發病基礎,未來研究可探索通過自閉癥特異性生物標志物實現疾病診斷與治療反應監測。
2、癲癇與ASD的關聯及間充質干細胞移植治療的價值
患兒在接受治療后,嚴重癲癇發作迅速消失,腦電圖持久恢復正常,且停用所有抗驚厥藥物,同時ASD癥狀得到臨床改善,有力證實了癲癇與ASD之間的內在聯系。盡管部分研究將伴有癲癇的ASD患者排除在MSCT治療之外,但該案例顯示MSCT對癲癇的治療效果顯著,表明癲癇發作不應成為MSCT治療的禁忌。此外,癲癇腦電圖結果可作為評估MSCT治療效果的客觀指標。
3、干細胞在自閉癥治療中的應用潛力
干細胞生物學在神經系統、神經退行性及免疫系統疾病等領域應用前景廣闊。因自體臍帶血冷凍保存后MSC含量與活性受限,來自健康捐贈者的胎盤來源間充質干細胞(PD-MSC)和臍帶來源間充質干細胞(UCD-MSC)更具應用價值。多項研究表明,無論是無關捐贈者的UCD-MSC,還是自體UCD-MSC,均能改善ASD患者癥狀,且大腦網絡變化與行為、溝通改善存在關聯。基于胎盤與臍帶衍生細胞的特性差異,聯合治療方案值得進一步探索。
4、間充質干細胞移植治療自閉癥方案的優化方向
MSCT治療ASD的最佳年齡與方案尚未明確。早期治療因大腦可塑性高可能更有效,但ASD診斷年齡限制了低齡兒童治療。研發適用于三歲以下兒童的客觀診斷工具,與優化治療方案同樣關鍵。此外,給藥間隔、治療次數及MSCs劑量的有效范圍均需校準,臨床實踐中應根據耐受性調整劑量以提升療效。
5、細胞療法分子機制與外泌體應用探索
細胞療法對ASD癥狀的改善已得到證實,但其分子機制仍不明確。MSC分泌的外泌體具備免疫調節與修復功能,在無細胞療法或輔助治療中極具潛力。本病例中,外泌體在治療中的臨床價值尚不明確,未來需結合多組學分析揭示治療響應機制,同時擴大臨床樣本驗證不同細胞來源、劑量及聯合療法的長期效益與風險。
結論:本病例展現了一位患有嚴重自閉癥和難治性癲癇的兒童在接受五次異基因干細胞移植治療后,其社交、語言和認知能力顯著改善,癲癇發作和胃腸道癥狀也完全緩解。該病例印證了人們對干細胞治療自閉癥兒童日益增長的興趣,并值得進一步評估其作為一種治療方式的潛力。
主要參考資料:
[1]Gesundheit B, Hochbaum L, Fetyukhina A, et al. (May 04, 2025) Mesenchymal Stromal Cell Treatment Alleviates Autism Spectrum Disorder Symptoms: A Case Report. Cureus 17(5): e83440. doi:10.7759/cureus.83440
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。




 掃碼添加微信
掃碼添加微信