
在再生醫學領域,間充質干細胞(MSCs)被譽為“種子細胞”,它們具備修復受損組織、調節免疫系統、減輕炎癥反應等多項潛能,廣泛應用于疾病治療與研究。但你可曾想過,像胎盤、臍帶這類傳統意義上的“醫療廢棄物”,是如何一步步走進實驗室,最終成為符合臨床使用標準的干細胞藥品?這篇文章將帶你全程解析干細胞新藥的制備過程,并揭示高標準實驗室的三大核心要素。

一、臍帶:間充質干細胞的“天然寶庫”
臍帶在過去常被視為廢棄物處理,而現代科學研究表明,其中富含間充質干細胞,具備以下優勢:
- 采集便捷:源自足月分娩,無需額外手術干預;
- 倫理可接受:不涉及胚胎,規避倫理爭議;
- 細胞特性優良:增殖能力強、免疫原性低,更易實現標準化擴增與臨床應用。
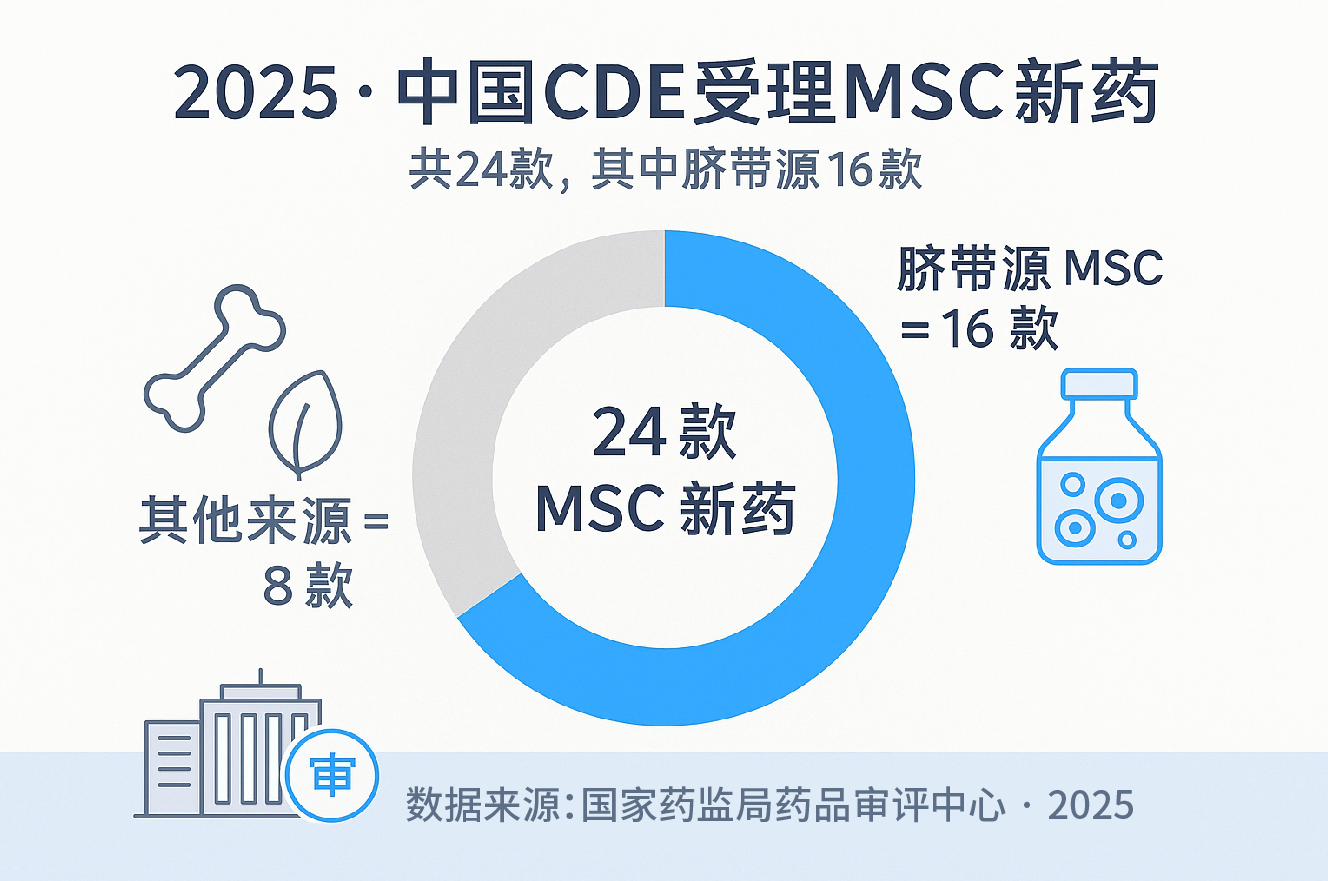
正因如此,臍帶已成為全球干細胞藥物研發的重要來源。
二、生產核心:GMP級實驗室三大要素
干細胞被視作“活的藥物”,其制備環境必須滿足極其嚴格的標準。一個符合藥品生產質量管理規范(GMP)的實驗室,須統籌以下三大要素:

1、環境控制
潔凈度須達到B+A級別,實現幾乎無塵無菌的空氣環境;溫濕度、壓差與設備表面狀態均需實時監測。所有操作均按標準化流程執行,最大限度杜絕微生物污染。可以說,實驗室環境如同一個“無菌艙”,為細胞制備全程保駕護航。

2、人員專業素養
關鍵崗位操作人員須具備生物醫藥相關專業背景,經系統培訓且考核合格后方可上崗。從供體篩查到細胞凍存,全程實施責任到人制度和溯源機制,確保每一環節可控、可查。

3、質量體系認證
優秀的干細胞實驗室通常通過CNAS、ISCT、ISO9001、AABB等國內外權威認證,并取得政府核發的相關資質。嚴格執行標準操作規程(SOP)和批次記錄制度,并引入第三方檢測,從系統層面保障每一批次細胞產品的質量穩定與安全可靠。質量體系如同最后的“守門員”,確保藥品合格。

三、從組織到藥品:干細胞制備全流程解析
一份胎盤或臍帶是如何轉變成符合臨床使用標準的干細胞藥品?主要包括以下關鍵環節:
1、供體篩選與組織采集
干細胞原料并非隨意獲取,必須來自健康的足月產婦。母體血液及組織需經過嚴格的病毒學檢測(包括HIV、乙肝、丙肝、梅毒、支原體等),排除感染風險。采集后8小時內,組織需在低溫條件下快速轉運至實驗室——正如生鮮冷鏈,時限與溫度直接決定細胞的“鮮活”程度。

2、樣本運送與預處理
樣本送入實驗室前須經歷多輪清洗與消毒。操作人員使用含肝素鈉的生理鹽水反復沖洗組織,徹底清除血液殘留,為后續細胞培養打下潔凈基礎。
3、細胞分離與釋放
真正的細胞“釋放”步驟開始:將組織切碎后置于酶消化液中,在37℃水浴搖床中溫和振蕩。消化時間須嚴格控制在1–1.5小時,時間過短則細胞產出不足,過長則可能導致細胞損傷——如同把握烹飪火候,精準控制至關重要。

4、培養與擴增
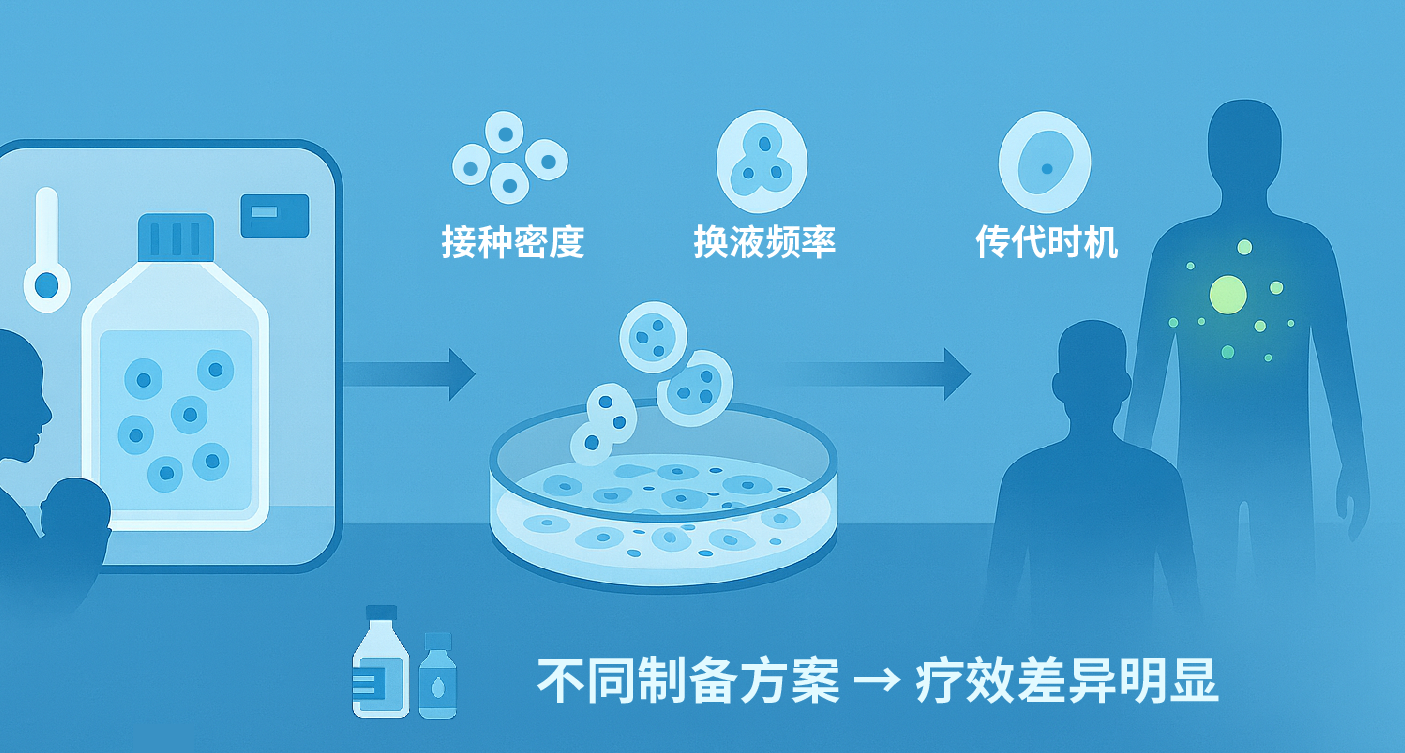
分離得到的間充質干細胞接種于特定培養基中,在適宜的溫濕度、二氧化碳濃度等條件下貼壁生長。接種密度、換液頻率與傳代時機等因素均直接影響細胞狀態與功能,不同實驗室工藝參數的差異也是導致臨床療效不一致的重要原因。
5、凍存與保存
擴增后的細胞需通過程序降溫設備,以約每分鐘-1℃的速率緩慢冷凍,最終儲存于-196℃液氮環境中。緩慢降溫可有效防止冰晶形成,維護細胞結構與功能完整性。

6、檢驗與放行
細胞產品必須經過嚴格質檢,包括:
- 細胞身份鑒定(CD73+/CD90+/CD105+,CD34-/CD45-);
- 存活率檢測(通常要求≥95%);
- 安全性檢測(無菌、無內毒素、無支原體);
- 功能驗證(成骨、成脂分化能力或免疫調節功能)。
全部合格后方可作為“干細胞藥品”用于臨床。

四、為何如此嚴格?
與化學藥物不同,干細胞是“活的藥物”,其安全性與有效性高度依賴:
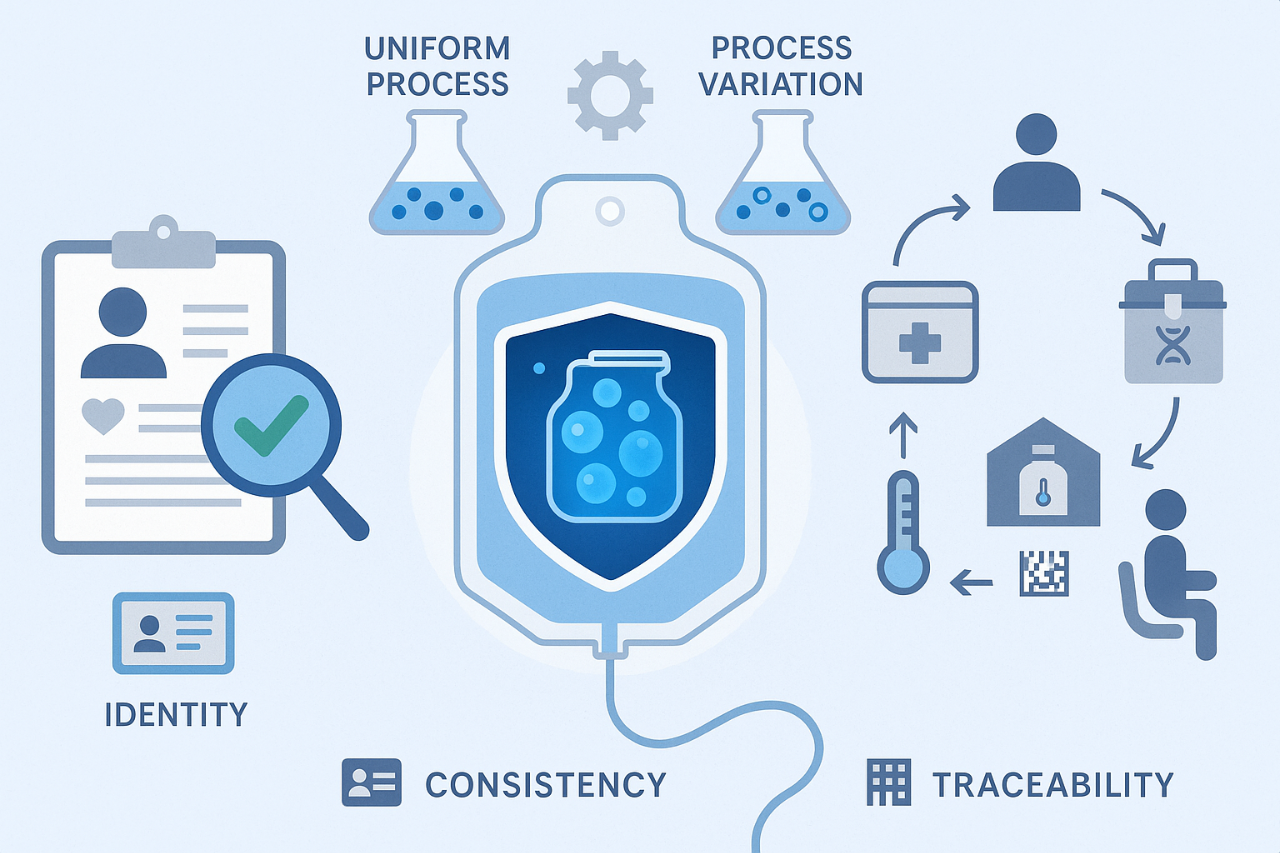
- 明確的供體來源與完備篩查;
- 工藝一致性:培養條件的細微差異可能導致細胞特性顯著不同;
- 全流程可追溯:從供體到受者,每一環節均需記錄可查。
只有實現標準化、可重復、全鏈條質控,才能真正保障干細胞藥品的安全與有效。
五、結語
從“廢棄組織”到“干細胞藥品”,臍帶與胎盤完成了一場華麗的轉身。這一切的背后,依托的是嚴苛的GMP環境、專業的技術團隊、標準化制備工藝與全程質量管理體系。隨著制備工藝和監管政策的持續完善,未來我們將有望見證更多來源于新生兒附屬物的干細胞產品走向臨床,為更多患者帶來希望。
參考資料:
1、Fernández-Santos ME, Garcia-Arranz M, Andreu EJ, et al. Optimization of Mesenchymal Stromal Cell (MSC) Manufacturing Processes for a Better Therapeutic Outcome. Frontiers in Immunology
2、Mebarki M, Abadie C, Larghero J, Cras A. Human umbilical cord-derived mesenchymal stem/stromal cells: a promising candidate for the development of advanced therapy medicinal products. Stem Cell Research & Therapy
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。




 掃碼添加微信
掃碼添加微信