靶向修復大腦:移植人類干細胞衍生的A10神經元,為治療抑郁癥提供新策略
2025年8月11日,中國科學院神經科學研究所聯合優力生物等研究機構在頂級期刊《細胞·干細胞》(Cell Stem Cell)上發表了一項里程碑“人類干細胞來源的A10多巴胺能神經元特異性整合到小鼠神經回路中并改善抑郁樣行為”的研究,并被選為封面文章[1]。

該研究首次證明,移植干細胞來源的特定亞型神經元能夠精準修復大腦受損的神經環路,從而有效改善抑郁樣行為,為精神疾病的細胞治療帶來了革命性的突破。
一、抑郁癥的治療困境與A10神經元的希望
抑郁癥是21世紀最常見的精神障礙之一,預計到2030年將成為全球疾病負擔的三大原因之一。盡管現有抗抑郁藥物在臨床上得到廣泛應用,但仍約有三分之一的患者屬于難治性抑郁癥(TRD),對所有藥物治療反應不佳。
患者表現出的核心癥狀,如快感缺乏、動機不足和焦慮,與大腦中一類特定的多巴胺能神經元——A10亞型神經元——的功能紊亂密切相關。這些神經元主要位于腹側被蓋區(VTA),負責調控大腦的獎賞、動機和情緒回路。
然而,長期以來,領域內面臨兩大挑戰:第一,如何從人類多能干細胞(hPSC)中高效、特異地規模化生產A10神經元?第二,移植后的神經元能否在復雜的大腦中找到正確的“位置”并成功“上崗”,實現功能整合?本研究正是對這兩個關鍵問題的有力回答。
二、方法突破:高效生成A10神經元的“GAD”配方
研究團隊的首要任務是建立一種高效、穩定的分化方案,以獲得高純度的A10樣多巴胺能神經元。
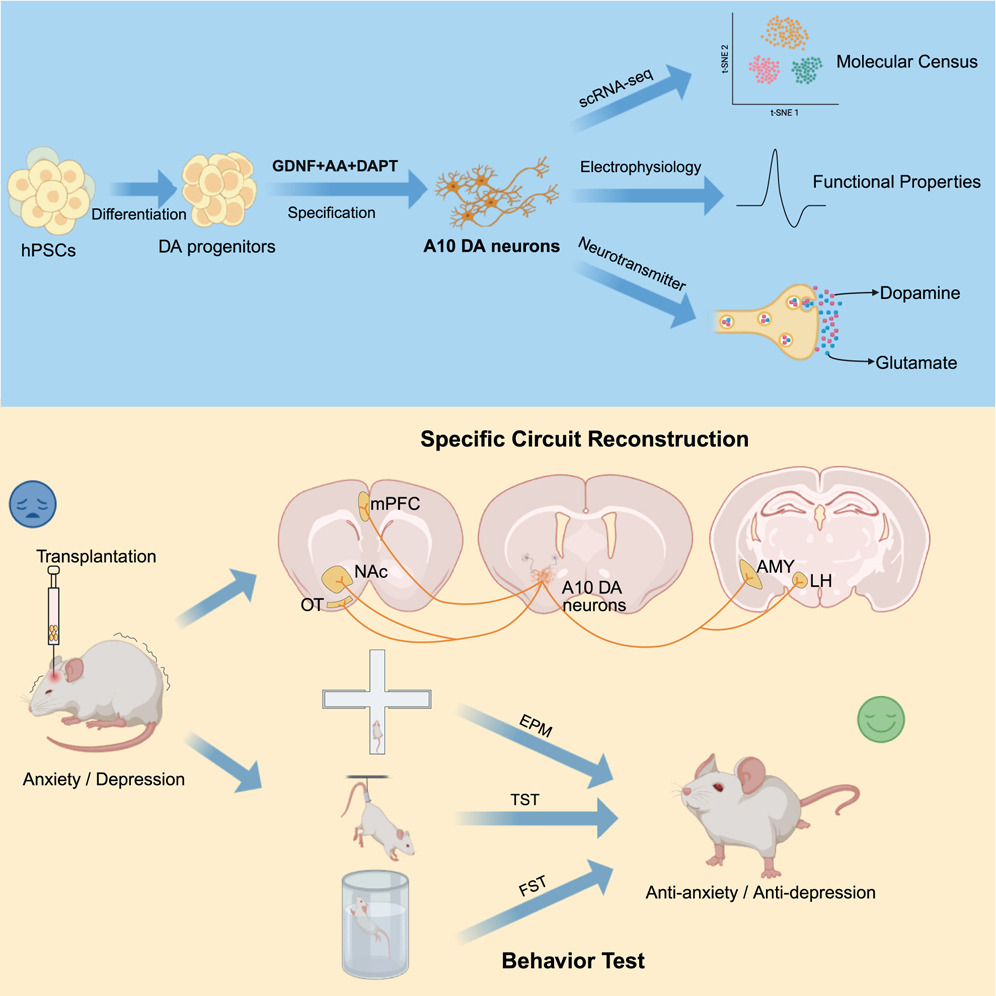
該過程的核心是一個多階段分化方案,并在一個特定的時間窗口使用關鍵的因子組合進行干預。其巧妙的策略在于:A9和A10亞型神經元擁有共同的早期發育路徑,因此研究保留了產生mDA祖細胞的既定早期方案(圖1A)。

關鍵的區別在于分化中后期。研究發現,在特定的“第V階段” ,使用由膠質細胞源性神經營養因子(GDNF)、抗壞血酸(AA)和γ-分泌酶抑制劑DAPT組成的“GAD” 混合物進行處理一周,是誘導A10亞型特化的最優窗口,能最高效地產生共表達酪氨酸羥化酶(TH)和鈣結合蛋白(CALB1)的A10樣神經元。
實驗證實,這種“GAD”組合對于生成A10樣神經元是必要且充分的。去除其中任何一種因子都會顯著損害A10神經元的產生,而必須三者同時使用才有效。最終生成的細胞絕大多數表達中腦多巴胺能神經元的標志性轉錄因子(如OTX2, EN1, FOXA2),并表現出正確的電生理特性,證明了其真實的細胞身份。
三、 核心發現:A10神經元內在的“GPS”導航能力
在成功獲得高純度的A10樣神經元后,下一個關鍵問題是:這些在體外制造的細胞,移植后能否在體內找到正確的“工作崗位”?
為了驗證這一點,研究團隊進行了精妙的移植實驗。他們發現,無論將hPSC衍生的A10多巴胺能神經元移植到小鼠腹側被蓋區(VTA,原位移植)還是伏隔核(NAc,異位移植),這些細胞都展現出了一種驚人的內在本能:它們能夠精準地投射至內源性A10神經元的所有天然靶腦區,并特異性地整合到宿主的神經環路中,與宿主神經元形成功能連接(圖2A)。
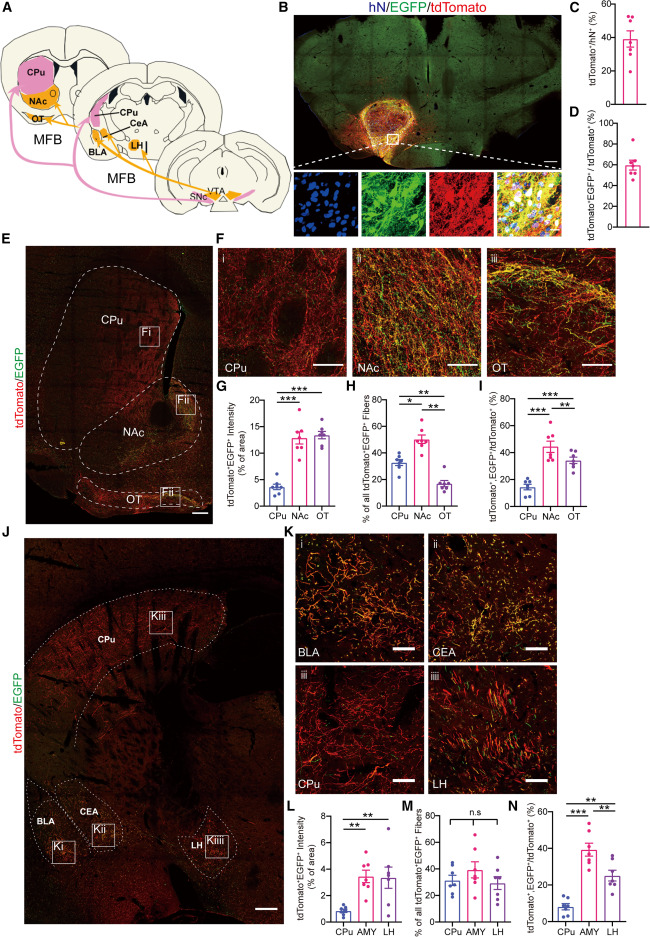
該結果表明,A10多巴胺能神經元具有顯著的亞型特異性和與生俱來的精準環路整合能力,就像腦中自帶了一套精密的“GPS導航系統”,確保它們能夠重建功能失調的中腦邊緣多巴胺通路。
四、功能驗證:精準激活移植神經元,逆轉抑郁行為
細胞成功整合后,最令人振奮的問題是:它們是否能功能性地改善疾病行為?為了回答這個問題,研究團隊運用了先進的化學遺傳學技術。
他們通過CRISPR/Cas9技術構建了一種特殊的干細胞系,能夠選擇性地在移植的A10神經元中表達一種可被藥物CNO激活的受體(hM3Dq)。這使得研究人員可以在特定時間,精準地“開啟”這些移植神經元的活動(圖3A)。

在行為學層面,結果非常顯著:
- 在高架十字迷宮實驗中,激活移植到伏隔核的A10神經元,小鼠立刻表現出明顯的抗焦慮樣行為。
- 在慢性應激誘導的抑郁模型中,激活這些神經元能顯著改善抑郁樣行為:恢復蔗糖偏好(逆轉快感缺乏) 并大幅減少在強迫游泳和懸尾實驗中的不動時間(減輕行為絕望)。
機制探究揭示了行為改善背后的原因:通過體內微透析技術,研究人員證實,激活移植的神經元能顯著提升伏隔核區域的多巴胺水平。這直接證明了移植的神經元不僅結構上整合了,更能功能性地釋放神經遞質,從而調控行為。多巴胺水平的恢復,正是其發揮治療作用的關鍵分子機制。
五、 總結與展望:邁向精神疾病的精準細胞治療
本研究首次證明,移植hPSC衍生的特定神經元亞型(A10) 可以精準重建該神經環路,并有效改善模型小鼠的行為異常。
這項工作的意義遠不止于抑郁癥。它提供了一個強大的“概念驗證”:即通過細胞移植來專門重建某一條功能失調的神經回路,從而實現對復雜精神疾病的精準治療。
這為未來干細胞治療抑郁癥、成癮、雙相情感障礙等與多巴胺系統相關的疾病,開辟了一種全新的、充滿希望的細胞治療思路。
參考資料:
[1]:https://www.cell.com/cell-stem-cell/fulltext/S1934-5909(25)00264-4
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。




 掃碼添加微信
掃碼添加微信