腦卒中是全球死亡和殘疾的主要原因,缺血性中風占中風的80%以上。在美國,估計約有700萬成年人有中風病史,約占人口的 2.5%。目前有效的治療方法包括再灌注療法,例如重組組織纖溶酶原激活劑;但這必須在有限的時間窗口內進行(中風發作后4.5小時內);因此,只有2-4%的患者從中受益。中風后殘疾帶來嚴重的社會和經濟負擔;很少有人自發康復,很多人永久殘疾。傳統的康復治療往往收效甚微。
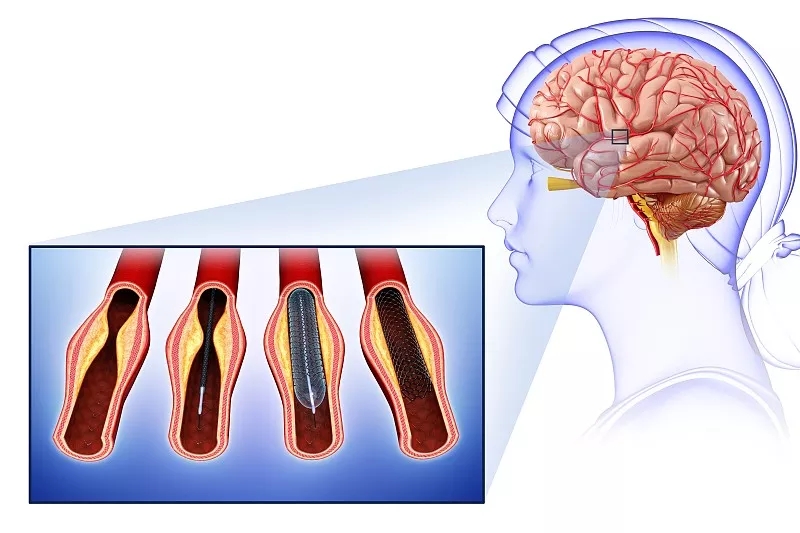
受損的中樞神經系統 (CNS) 自我修復的能力是有限的,因此尋找促進恢復的替代方法將徹底改變中風治療。干細胞療法是一種新型療法,有望替代急性期溶栓和慢性期康復。神經干細胞 (NSC) 和神經干/祖細胞 (NSPC) 被認為是建立干細胞庫的理想候選者,干細胞庫可以為修復神經網絡和血管重塑提供持續供應的神經元、星形膠質細胞和少突膠質細胞。
使用神經干細胞進行移植治療腦卒中具有四個被廣泛接受的優點:
(1)比胚胎干細胞(ESCs)具有更高的腦樣相似性;神經干細胞可以分裂和分化成與其周圍微環境中的細胞相對應的細胞類型,并且它們的形態和功能與附近的宿主細胞非常相似。
(2) 比間充質干細胞更容易遞送;中樞神經系統具有特殊的結構,即血腦屏障 (BBB),使外源性“種子細胞”難以進入,而常規移植到室管膜下區或齒狀回的神經干細胞具有“占位符”效應。
(3) 比神經元類似物更低的排斥反應;即使對于移植的個體間或物種神經干細胞,免疫排斥也極為罕見。
(4) 較強的趨化性和遷移能力;神經干細胞具有遷移到受損部位的能力。
本綜述總結了近期發表的研究成果,重點關注神經干細胞來源、和機制以及臨床試驗,旨在為治療干預提供決策依據,并為未來神經干細胞移植治療腦卒中推向臨床應用的研究方向提供建議。
神經干細胞的類型和來源
胚胎干細胞衍生的神經干細胞系(胚胎供體):這些細胞系是源自早期胚胎或胚胎神經組織的NSC。早期ESC是受精后5-7天、植入子宮之前胚泡中的未分化細胞。它們是全能干細胞,具有發育成任何細胞類型的能力。部分外胚層會分化成神經系統的細胞。
成人腦神經干細胞系(成人供體):人腦中有兩個主要的神經源性生態位,即腦室下區 (SVZ) 和亞顆粒區,可以從中獲得成人NSC。
誘導多能干細胞衍生的神經干細胞:高橋等人成功將人類細胞重編程為誘導多能干細胞(iPSC),這些細胞已成為理想的自體移植細胞資源。移植的iPSC-NSCs在中風治療中的優勢很多,例如增強運動感覺功能、減少梗死面積、促進軸突發育、促進血管生成和調節炎癥因子。
目前神經干細胞移植治療腦卒中的臨床級產品有哪些
已在臨床試驗中探索了轉基因干細胞系。修飾的細胞系可以在體外以穩定的速率無性繁殖,形成永生化細胞系。永生化細胞系具有增殖能力強、對環境適應性好、細胞身份易控制和同化入人體組織等優點。
CTX0E03:CTX0E03是一種人類神經干細胞系,已使用與突變雌激素受體融合的條件永生化c-MYC基因進行基因修飾。無血清生產的CTX0E03被認為是最有希望的治療級人類神經干細胞系。
Sinden等人的評論詳細介紹了CTX細胞治療從實驗室起源到臨床進展的全過程。人類神經干細胞 (CTX0E03) 的移植促進了中風患者的顯著行為恢復。恢復程度與細胞劑量和旁分泌機制呈正相關(表格1)。
| 代號 | 初始來源 | 處理方法 | 細胞來源 | 臨床前研究證據 | 臨床試驗 | 疾病 | 限制 | 參考 |
|---|---|---|---|---|---|---|---|---|
| CTX0E3 | 同種異體 | 用c-mycER轉染 | 永生化人類神經干細胞系 | 神經發生和血管發生(外泌體) | NCT01151124 | 慢性缺血性中風 | 入學后長期恢復 | Stroemer等人2009年; Kalladka等人2016年 |
| NT2N | 同種異體 | 視黃酸處理后的體外神經元表型 | 克隆人畸胎癌細胞系 | 多巴胺能表型 | 納爾遜等人。(2002) | PD、HD、外傷 | 腫瘤形成經歷;凋亡樣細胞死亡;對中風的治療影響可忽略不計 | Borlongan等人1998年; 赫爾伯特等人1999年; 貝克等人2000年;尼爾森等人2002年 |
| SB623 | 同種異體 | 含有Notch-1胞內結構域的轉染表達載體 | 骨髓間充質干細胞 | 神經營養、血管生成和神經保護作用 | NCT01287936 | 慢性穩定性中風和外傷 | 更少的研究和試驗;非隨機設計 | Dezawa等人2004年; 斯坦伯格等人2016年 |
| NSI-566 | 同種異體 | 未經基因改造的單個胎兒脊髓 | 原代貼壁人神經干細胞系 | 與宿主組織整合;免疫抑制作用 | NCT03296618 | 肌萎縮側索硬化癥、脊髓損傷 | 較少的臨床試驗 | Glud等人2016年; 柯蒂斯等人2018年; 張等人2019a |
NT2N:NT2N (hNT) 細胞是源自克隆人畸胎癌細胞系的神經元,在體外視黃酸處理后獲得永久性的有絲分裂后神經元表型,并已顯示在體內形成操作性突觸和分泌神經遞質。
SB623:SB623細胞是通過用編碼人NOTCH1細胞內結構域的表達載體瞬時轉染間充質干細胞而開發的,并且已顯示在實驗性局灶性缺血后遞送至嚙齒動物大腦后可減少病變體積并促進功能恢復。
NSI-566:NSI-566是一種來自單個胎兒脊髓的穩定的初級貼壁人-NSC 系,未經基因改造,已獲得美國食品和藥物管理局的臨床試驗授權。它在完成的II期肌萎縮側索硬化癥和I期脊髓損傷試驗中顯示出良好的安全性和耐受性。
神經干細胞移植治療腦卒中的作用機制
歸巢和細胞更換:歸巢是神經祖細胞 (NPC)/NSC 利用趨化性移動到損傷部位的過程。
旁分泌作用:隨著研究的進展,用干細胞替代丟失的神經元被證明不是主要的神經重塑機制,因為干細胞替代不能完全解釋在體內實驗中觀察到的現象。
旁分泌證據:首先,示蹤方法表明,歸巢干細胞的數量遠小于移植的干細胞數量,通過動靜脈途徑注射的細胞仍然可以發揮作用。此外,人們認為血管通路中的干細胞很少通過BBB。其次,細胞替代機制不能解釋早期NSC移植的功效;神經細胞的分化、突觸的重建和神經網絡的重排很難在短時間內完成。
旁分泌囊泡:細胞外囊泡被認為是介導受損腦組織恢復的關鍵。外泌體和microRNA (miR) 的發現為大腦重塑過程和細胞修復機制提供了基礎。
炎癥效應:繼發性炎癥加劇中風后少突膠質細胞死亡,和含有內源性T調節細胞的干細胞可以調節成纖維細胞生長因子和白細胞介素6的水平并抑制白質損傷。調節炎癥反應的關鍵步驟是抑制小膠質細胞的活化。
神經干細胞移植治療腦卒中的臨床試驗概述
臨床試驗比動物模型實驗更難推進。自2020年4月20日以來,已有88項中風臨床試驗在ClinicalTrials.gov注冊。在涉及神經干細胞的六項研究中,三項已公布了結果。還有兩項針對兒童缺氧缺血性腦病和缺血相關性腦癱的神經干細胞移植的臨床試驗。表2)。
使用神經干細胞治療中風的臨床試驗(主動和募集)
| NCT number | Tittle | Status | Interventions | Study type | Outcome measure | Population | Sponsor | Process observed |
| NCT03296618 | Intracerebral transplantation of neural stem cells for the treatment of ischemic stroke | Active (completed) | NSI-566: A group: 1.2 × 107; B group: 2.4 × 107; C group: 7.2 × 107 | Interventional (one-time intra-cerebral injections) | AE & NIHSS & mRS, MMSE, FMMS | Enrollment: 9; age: 33–65 yr (150–743 d post-stroke) | Suzhou Neuralstem Biopharmaceuticals Neuralstem Inc. | NP; NG; MR; VR |
| NCT03725865 | A clinical study of iNSC intervent cerebral hemorrhagic stroke | Not yet recruiting | iNSCs | Interventional | Emergent AE | Enrollment:12; age: 30–65 yr; sex: both | Allife Medical Science and Technology Co. Ltd. | NP; NG; MR; VR |
| NCT01151124 | Pilot investigation of stem cells in stroke | Active (completed) | CTX0E03 (NSCs), single doses of 2 million, 5 million, 10 million, or 20 million cells | Intervention (stereotactic ipsilateral putamen injection) | AE&BI& MMSE, mRS, EQ-5D | Enrollment: 12; age: 60–85 yr (29 mon post-stroke); sex: male | ReNeuron Limited (Division of Clinical Neurosciences, Glasgow) | NP; NG; MR; VR |
| NCT03629275 | Investigation of neural stem cells in ischemic stroke | Recruiting | Combination product: CTX0E03 drug product and delivery device; Drug: placebo | Intervention | mRS at 6 mon BI; basic mobility changing and TUG, CAHAI & SDMT & COWAT & MNT & MCA | Enrollment: 110; Age: 35–75 yr (adult, older adult); aex: both | ReNeuron Limited (University of California, Irvine, CA, USA) | NP; NG; MR; BN; VR |
| NCT02854579 | Neural progenitor cell and paracrine factors to treat hypoxic ischemic encephalopathy | Active (completed) | Biological: NPC; Biological: paracrine factors; Biological: progenitor cell and paracrine factors | Interventional; intra-cerebral injections | Neonatal behavioral assessment; adverse events; Bayley score; Peabody development measure scale; MRI or CT | Enrollment:120; age: up to 14 d (child); sex: both | Navy General Hospital, Beijing, China | NP; NG; MR; BN; VR |
| NCT02117635 | Pilot investigation of stem cells in stroke phase II efficacy | Complete | Biological: CTX DP | Interventional | ARAT and after CTX; NIHSS; RFA & BI after CTX; Safety/ Tolerability; FMMS after CTX | Enrollment: 23; age: 40 yr older (adult, older adult); sex: both | ReNeuron Limited (Queen Elizabeth Hospital, Birmingham, UK) | NP; NG; MR; VR; |
| NCT04047563 | Efficacy of sovateltide (PMZ-1620) in patients of acute ischemic stroke | Recruiting | Drug: PMZ-1620 (sovateltide) along with standard treatment | Interventional, phase 3 | NIHSS/mRS; change in quality-of-life; change in Stroke-Specific Quality of Life | Enrollment: 110; age: 18–78 yr (adult, older adult); sex: both | Pharmazz, Inc. | NP; NG; MR; VR |
| NCT03005249 | Neural stem cells therapy for cerebral palsy | Recruiting | Biological: NSC | Interventional, intranasal administration | GMFM-88 score; Fine Motor Function Measure score; modified Ashworth Scale score; AEEG/ MRI/EMG | Enrollment: 20; age: 1–12 yr (child); cerebral palsy | The First Affiliated Hospital of Dalian Medical University, Dalian, China | NP; NG; MR; VR |
AE:不良事件;AEEG:振幅綜合腦電圖;ARAT:行動研究手臂測試;BI:巴塞爾指數;BN:大腦網絡;CAHAI:Chedoke 手臂和手部活動量表;COWAT:受控的口語聯想任務(語言技能);CTX:CTX0E03,人類NSC系;DP:藥品;肌電圖:肌電圖;EQ-5D:EuroQol-5D;FMMS:Fugl-Meyer 運動評分;GMFM-88:粗大運動功能測量儀-88;iNSC:誘導的 NSC;MCA:蒙特利爾認知評估(語言技能);MMSE:簡易精神狀態檢查;MNT:多語言命名測試(語言技能);MR:髓鞘修復;mRS:改良Rankin量表;NG:神經突生長;NIHSS:美國國立衛生研究院卒中量表;NP:神經元極性;NPC:神經祖細胞;NSCs:神經干細胞;射頻識別:Rankin 重點評估;SDMT:符號數字模式測試(語言技能);TUG:定時啟動測試;VR:血管再生。
NCT01151124是近年來干細胞治療腦卒中最有影響的臨床研究之一。CTX0E03細胞的良好功效和安全性為人類神經干細胞移植項目的開展提供了足夠的信心。由ReNeuron (PISCES-III) 公司主持的NCT03629275研究將包括比NCT01151124試驗(12個中心,預計110名患者)更多的參與者,以進一步證明CTX0E03細胞的臨床效果。
需要注意的是,ReNeuron還為中風患者使用了人胎神經干細胞移植,并且在I期和II期研究中未發現細胞相關或免疫學不良事件(分別為11和42名患者)。然而,從Steinberg等人的SB623移植試驗的積極結果來看。招募了18名穩定的慢性卒中患者,還應該認識到,盡管具有長期療效,但移植的安全性不容忽視。
使用NSI-566細胞進行的NCT03296618研究最近發表了令人鼓舞的結論,這些細胞以前曾在脊髓損傷方面進行過臨床試驗(Curtis 等人,2018年)。三個隊列被一次性腦內注射1.2×107、2.4× 107或7.2 ×107的NSI-566細胞移植,用于治療慢性運動性卒中導致的偏癱,以確定未來試驗的最大耐受劑量。用他克莫司進行免疫抑制治療28天。12個月后,9名參與者的平均Fugl-Meyer運動評分顯示改善16點(P=0.0078),平均改良Rankin量表顯示改善0.8點,平均美國國立衛生研究院卒中量表顯示改善3.1個點。在24個月的隨訪中,這些變化保持穩定。
神經干細胞移植治療腦卒中目前面臨的問題
細胞來源:盡管取得了積極的成果,但神經干細胞的臨床應用卻很困難。神經干細胞臨床試驗中遇到的問題之一是細胞來源。自體細胞的排斥相對不常見,但與胎兒神經干細胞相比,成人神經干細胞的數據非常有限,缺乏系統表征和提取部位的差異。
時間:移植時間是否應選擇在卒中急性期(24-72小時內)尚有爭議。在此期間接收者的狀態很難估計。在卒中恢復期和慢性卒中期(卒中后90天)可提倡神經干細胞治療。總之,神經干細胞移植時間最有可能在受傷后一百天左右最有益。目前進行的所有I期臨床試驗都假設治療期越長,細胞對人身安全構成的風險就越小。
評估移植途徑和細胞劑量:不同給藥途徑的有效劑量顯著不同:靜脈內>動脈內>鞘內>腦內。
對于中風,NSPCs主要使用腦內途徑進行研究。腦內注射的神經元可以重建宿主大腦中受損的長軸突投射和突觸連接。與康復對照組相比,接受治療的慢性中風患者的運動功能也得到了顯著改善。
腦內和鞘內給藥快速而直接,但兩者都是具有高風險的侵入性治療,如繼發性腦水腫和顱內高壓。基礎研究表明,細胞替代不是干細胞的主要治療機制,干細胞具有遷移能力;因此,需要重新評估以這種方式將細胞運送到現場的風險。
與手術植入相比,動脈內和血管內注射侵入性更小,更容易進行,但可能會發生嚴重后果,例如血管閉塞和肺栓塞。血管輸送可能對細胞存活產生重大影響,并且很難確保有效數量的細胞通過BBB。所以,沒有足夠的證據表明NSC遞送的血管途徑具有治療潛力。
值得注意的是,正在評估一些更無創且可接受的遞送途徑。例如,在鼻內給藥后,干細胞和神經營養因子可以通過喙狀板遷移到中樞神經系統中。這NCT03005249試驗已注冊用于神經干細胞鼻內給藥。
結論
神經干細胞移植有利于損傷后大腦結構和功能的修復,并在臨床前和臨床研究中得到充分驗證。預計神經干細胞移植將在腦卒中的治療中取得顯著成果。然而,神經干細胞的臨床應用仍有幾個緊迫的問題需要解決。
- 1、對網絡微環境的功能恢復過程和結構修復機制進行了深入細致的解釋;
- 2、深入研究神經干細胞移植的治療機制;
- 3、選擇最合理的給藥途徑、劑量和時機;
- 4、完善評價體系和倫理標準。我們的綜述初步總結了目前神經干細胞神經再生和腦卒中損傷后功能恢復的機制。圖2。
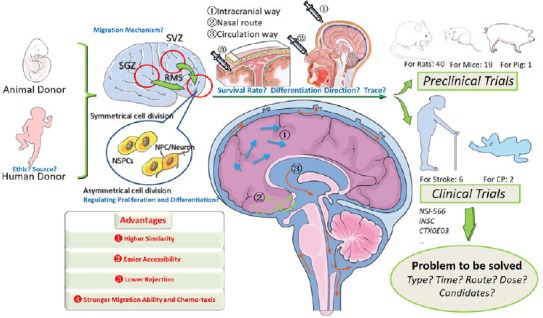
NSCs具有獨特的細胞替代、旁分泌作用、炎癥調節和神經保護機制。NSC治療的基礎和臨床研究有望實現中風后的功能恢復。CP:腦癱;NPC:神經祖細胞;NSC:神經干細胞;NSPC:神經干/祖細胞;RMS:喙洄游流;SGZ:亞粒區;SVZ:腦室下區。
神經干細胞移植治療腦部疾病的相關科研及臨床研究正在多方位展開,得到了快速的發展,取得了可喜的成績。相信隨著科學研究與醫療技術的不斷進步,神經干細胞移植療法可以將腦部疾病的治療窗口延長,為腦部疾病的治療提供新型的解決方案。
參考資料:Jiao Y, Liu YW, Chen WG, Liu J. Neuroregeneration and functional recovery after stroke: advancing neural stem cell therapy toward clinical application. Neural Regen Res. 2021 Jan;16(1):80-92. doi: 10.4103/1673-5374.286955. PMID: 32788451; PMCID: PMC7818886.
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加微信
掃碼添加微信