導語:類風濕關節炎是一種自身免疫性疾病,當您的免疫系統錯誤地攻擊自己身體的組織時,就會發生類風濕關節炎。隨著再生醫學的發展,利用干細胞的自我更新和分化潛能,為類風濕關節炎患者提供新的修復策略。再生醫學和臍帶間充質干細胞(UC-MSC)療法的使用最近成為潛在的選擇。
什么是類風濕關節炎
類風濕關節炎(RA)是一種慢性全身性自身免疫性疾病,主要影響關節,但也可能累及其他器官。其病因尚不完全明確,但與遺傳、環境和感染等因素密切相關。該病的發病高峰年齡在30-50歲之間,女性發病率高于男性。
隨著再生醫學的發展,利用干細胞的自我更新和分化潛能,為類風濕關節炎患者提供新的修復策略。間充質干細胞療法的使用最近成為潛在的選擇。
本文主要盤點干細胞治療類風濕關節炎患者的臨床試驗的結果,從而評估干細胞移植作為類風濕關節炎患者的潛在治療方法的安全性和有效性。

四項研究677例患者證實:干細胞治療類風濕關節炎安全有效!
臨床研究一:《臍帶血間充質干細胞靜脈輸注治療類風濕關節炎:Ia 期臨床試驗 》
2018年8月首爾大學醫院的研究人員在國際期刊《Stem Cell Translational Medicine》上發布了一篇關于《臍帶血間充質干細胞靜脈輸注治療類風濕關節炎:Ia 期臨床試驗?》的研究結果。

有效性評估
在11名接受篩選的類風濕關節炎患者中,有9人入選。參與者主要是女性 (78%),平均年齡為 57.4 歲。針對已確診類風濕關節炎患者進行的 Ia 期 臍帶血間充質干細胞輸注試驗未發現短期安全問題。
在輸注臍帶血間充質干細胞長達4周,所有群集中均未出現不祥的安全信號。
在輸注臍帶血間充質干細胞期間生命體征穩定,未觀察到有臨床意義的心電圖變化。5 × 10 7個細胞組中僅有一名患者在輸注后60分鐘出現關節疼痛,但確定這與輸注臍帶血間充質干細胞無關。
血液學特征中未發現重大異常,肝腎功能等血清化學特征未觀察到異常。4 周時血清尿酸水平略有升高,但變化較小,未發生相關不良事件。未報告嚴重不良事件或劑量限制性毒性 (DLT)。
安全性性評估
這項 Ia 期研究表明,單次靜脈輸注臍帶血間充質干細胞治療類風濕關節炎受試者具有良好的安全性。在后續的隨訪中未出現任何不良反應。
臨床案例二:《臍帶間充質干細胞治療類風濕關節炎患者的療效和安全性:一項前瞻性 I/II 期研究》
2019年,中國人民解放軍空軍第986醫院在國際期刊《Drug development treatment》上發布了一篇《臍帶間充質干細胞治療類風濕關節炎患者的療效和安全性:一項前瞻性 I/II 期研究》的研究結果。

研究招募64名年齡為18~64歲的類風濕關節炎患者,通過血清學標志物檢測評估安全性,通過28關節疾病活動評分(DAS28)和健康評估問卷(HAQ)評估療效。
有效性評估
圖1:圖中患者,68歲,男性,1998年確診為類風濕性關節炎,2010年首次入院。
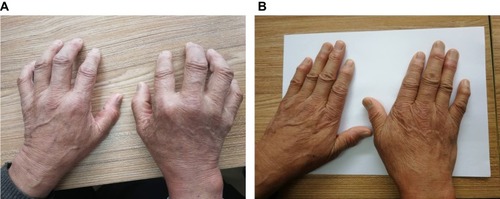
(圖1A)表現為雙手不能伸直。
(圖1B)治療3年后,停用抗風濕藥物5年,雙手伸展自如,關節周圍風濕結節逐漸變軟、消退。
圖2:圖中患者,33歲,女性,病程4年
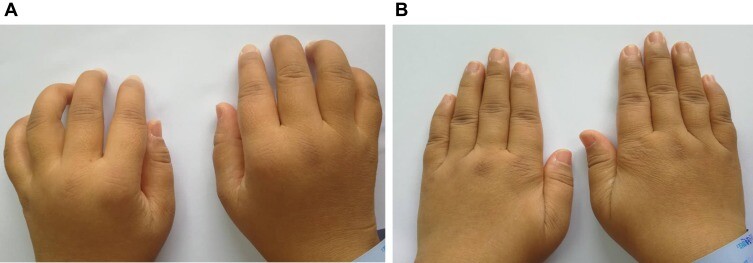
( 圖2A )咬牙困難,腫脹疼痛,晨僵;
( 圖2B )經臍帶間充質干細胞細胞治療1周后,癥狀明顯改善。
安全性評估
我們觀察了類風濕關節炎患者接受期待間充質干細胞治療后長達8個月的情況,發現在臍帶間充質干細胞輸注期間或之后均未出現任何急性嚴重副作用,只有少數患者(4%)在輸注過程中出現輕微不良反應,如流感等癥狀,這些癥狀在數小時內消失,無需任何治療。
在后續的隨訪中未出現任何不良反應。
臨床案例三:《基于間充質干細胞的類風濕關節炎治療》
2021年10月,納扎爾巴耶夫大學在國際期刊《International Journal of Molecular Sciences》上發布了一篇《基于間充質干細胞的類風濕關節炎治療》的研究結果。

招募了276名類風濕關節炎患者,以評估不同劑量同種異體間充質干細胞的療效。
有效性評估
使用間充質干細胞治療類風濕關節炎的臨床試驗
| 臨床試驗標識符 | 研究設計 | 細胞來源 | 患者人數 | 給藥途徑和劑量 | 隨訪時間(月) | 治療前或對照組的臨床狀況 | 治療后臨床狀況 |
|---|---|---|---|---|---|---|---|
| NCT01663116 | 隨機、多中心、雙盲、安慰劑對照、劑量遞增 Ib/IIa 期 | 同種異體 AT MSCs | 53 | 1、2或 4 × 10 6細胞/kg 體重,每周三次靜脈注射 | 6 | 1 個月后DAS28-ESR ↑、CRP ↑、 ACR20 反應(29%)和 3 個月后(0%) | DAS28-ESR ↓、CRP ↓、 1 個月后 ACR20 反應(20–45%)和 3 個月后 ACR20 反應(15–25%) |
| NCT03333681 | 第一階段 | 自體骨髓間充質干細胞 | 9 | 1至2×106細胞/kg體重,單次靜脈注射 | 12 | DAS28-ESR ↑、VAS ↑、ESR ↑、CRP ↑、RF ↑、抗-CCP↑ | DAS28-ESR↓、VAS↓、ESR↓、CRP↓(NS)、RF↓、抗 CCP↓ (NS) |
| NCT01873625 | 隨機、三盲、單中心、安慰劑對照 I/II 期 | 自體骨髓間充質干細胞 | 30 | 4.2 × 10 7個細胞/患者,單次 IA 注射 | 12 | DAS28 ↑、VAS ↑、WOMAC ↑、ESR ↑、CRP ↑、疼痛 FWD ↓、WD ↓、凝固時間↓、站立時間↓ | DAS28 ↓(NS)、VAS ↓、WOMAC ↓、ESR ↓(NS)、CRP ↓(NS)、疼痛 FWD ↑、WD ↑、凝固時間 ↑、站立時間 ↑ |
| NCT01547091 | 前瞻性 I/II 期 | 同種異體 UC MSCs | 172 | 4 × 10 7個細胞/患者,單次靜脈注射 | 36 | DAS28 ↑、HAQ ↑、CRP ↑、ESR ↑、RF ↑、抗CCP ↑、TNF-α ↑、IL-6 ↑ | DAS28↓、HAQ↓、CRP↓、ESR↓、RF↓、抗 CCP↑、TNF-α↓、IL-6↓ |
| NCT02221258 | Ia 期,開放標簽,劑量遞增 | 同種異體臍帶血干細胞 | 9 | 2.5 × 10 7、5 × 10 7或 1 × 10 8細胞/患者,單次靜脈注射 | 1 | DAS28 ↑、VAS ↑、HAQ↑、CRP↑、IL-1β↑、IL-6↑、IL-8↑、TNF-α↑ | DAS28↓、VAS↓、HAQ↓、CRP↓、IL-1β↓、IL-6↓、IL-8↓、TNF-α↓ |
研究顯示,與安慰劑組患者相比,根據韓國西安大學和麥克馬斯特大學關節炎指數 (WOMAC)、視覺模擬量表 (VAS)、凝固時間和長達 12 個月的無痛步行距離,接受膝關節內注射骨髓間充質干細胞的患者表現出更優的臨床效果。
基于這些數據,作者提出,對于類風濕關節炎患者來說,膝關節內注射骨髓間充質干細胞通常是安全的,并且耐受性良好。
安全性評估
在接受間充質干細胞治療的類風濕關節炎患者中,15–25%的人在3個月后仍保持這種治療效果,但在安慰劑對照組中并非如此。結論是,間充質干細胞的使用耐受性良好,且未表現出劑量依賴性毒性。
在后續隨訪中未出現任何不良反應。
臨床研究四:《間充質干細胞治療類風濕關節炎疾病的安全性和有效性:臨床試驗的系統評價和薈萃分析》
2023年7月,BioXscience 先進療法和轉化醫學的研究人員在《PLOS ONE》上發布了一篇《間充質干細胞治療類風濕關節炎疾病的安全性和有效性:臨床試驗的系統評價和薈萃分析》的研究結果。

358例患者納入的研究
有效性評估
我們的系統評價和薈萃分析是第一項實質性總結全身性間充質干細胞治療類風濕性關節炎的安全性的研究,這些間充質干細胞是從臍帶 (UC)、脂肪組織 (AT) 和骨髓 (BM) 中分離出來的。
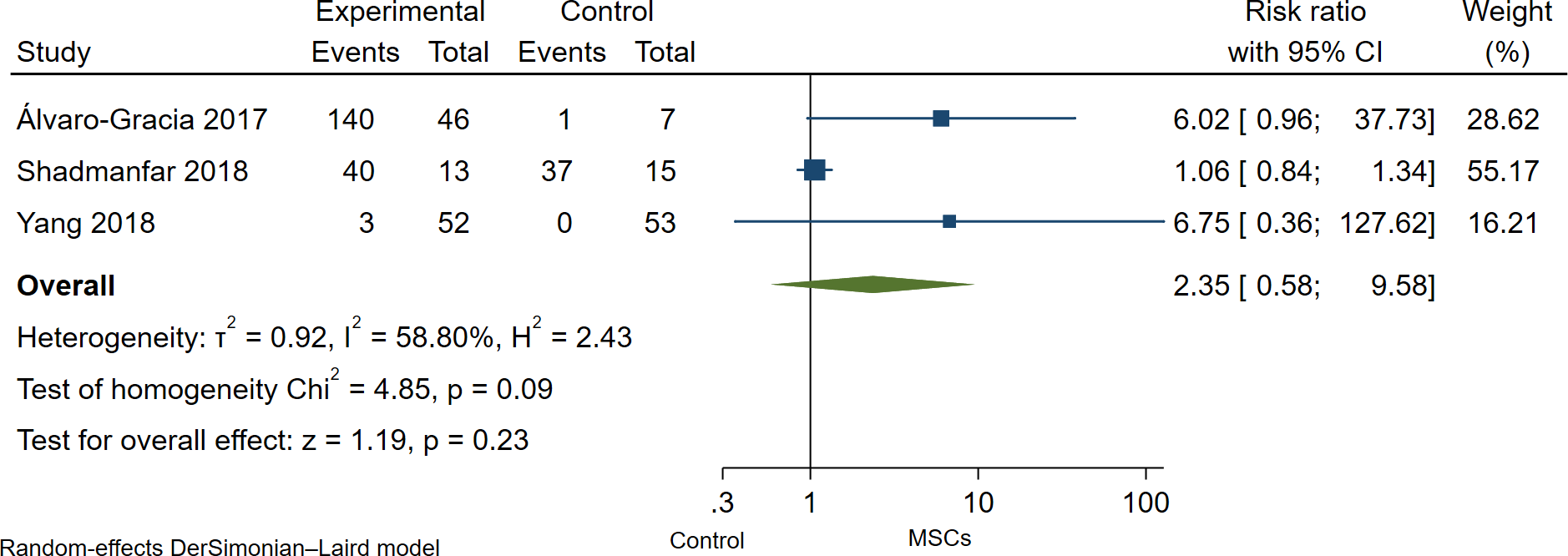
這項研究未發現每個系統器官類別在間充質干細胞給藥期間或之后出現嚴重不良事件。
álvaro-Gracia等人沒有報告實驗室值異常或相關生命體征異常、惡性腫瘤或死亡。Yang等人的研究未發現常規血液檢查、肝腎功能分析、尿液分析或心電圖有顯著異常。
安全性評估
我們的研究結果表明,當傳統的合成抗風濕藥物 (cs-DMARDs) 治療失敗且生物DMARDs不可行時,可以考慮使用間充質干細胞療法治療類風濕關節炎。總體而言,在類風濕關節炎患者中觀察到良好的安全性,并且沒有危及生命的事件。在后續的隨訪中未出現任何不良反應。
干細胞治療類風濕關節炎的臨床研究進展
截止2024年9月4日,在美國國立衛生研究院的最大臨床試驗注冊庫clinicaltrials.gov網站上注冊的有關干細胞治療類風濕關節炎臨床研究項目有19項,已完成的有11項。
結論
臨床研究結果顯示干細胞治療類風濕關節炎是有效且安全的,能夠促進受損神經細胞的保護和修復、促進內源性神經干細胞的增殖與遷移、促進突觸重塑、新血管形成,并整合到主要神經回路中,從而恢復受損的神經功能。
盡管干細胞治療總體上安全,仍存在一些潛在風險,例如,低熱和頭暈和輕微不適反應。因此,患者在接受干細胞治療前需要進行詳細的檢查和評估,并在專業醫生的指導下進行治療。
隨著研究的深入和技術的成熟,我們期待干細胞治療能夠在類風濕關節炎治療中發揮更大的作用。
參考資料:
álvaro-Gracia, J.M.; Jover, J.A.; García-Vicu?a, R.; Carre?o, L.; Alonso, A.; Marsal, S.; Blanco, F.; Martínez-Taboada, V.M.; Taylor, P.; Martín-Martín, C. Intravenous administration of expanded allogeneic adipose-derived mesenchymal stem cells in refractory rheumatoid arthritis (Cx611): Results of a multicentre, dose escalation, randomised, single-blind, placebo-controlled phase Ib/IIa clinical trial.?Ann. Rheum. Dis.?2017,?76, 196–202.?
Shadmanfar, S.; Labibzadeh, N.; Emadedin, M.; Jaroughi, N.; Azimian, V.; Mardpour, S.; Kakroodi, F.A.; Bolurieh, T.; Hosseini, S.E.; Chehrazi, M. Intra-articular knee implantation of autologous bone marrow–derived mesenchymal stromal cells in rheumatoid arthritis patients with knee involvement: Results of a randomized, triple-blind, placebo-controlled phase 1/2 clinical trial. Cytotherapy 2018, 20, 499–506.
Yang Y., He X., Zhao R., Guo W., Zhu M., Xing W., Jiang D., Liu C., and Xu X., Serum IFN-γ levels predict the therapeutic effect of mesenchymal stem cell transplantation in active rheumatoid arthritis, Journal of Translational Medicine. (2018) 16, no. 1, Erratum in: Journal of Translational Medicine 2021 Sep 23; 19(1): 402, PMID: 29903026.https://doi.org/10.1186/s12967-018-1541-4, 2-s2.0-85048612688.
Ghoryani, M.; Shariati-Sarabi, Z.; Tavakkol-Afshari, J.; Ghasemi, A.; Poursamimi, J.; Mohammadi, M. Amelioration of clinical symptoms of patients with refractory rheumatoid arthritis following treatment with autologous bone marrow-derived mesenchymal stem cells: A successful clinical trial in Iran. Biomed. Pharmacother. 2019, 109, 1834–1840.
Shadmanfar S., Labibzadeh N., Emadedin M., Jaroughi N., Azimian V., Mardpour S., Kakroodi F. A., Bolurieh T., Hosseini S. E., Chehrazi M., Niknejadi M., Baharvand H., Gharibdoost F., and Aghdami N., Intra-articular knee implantation of autologous bone marrow-derived mesenchymal stromal cells in rheumatoid arthritis patients with knee involvement: results of a randomized, triple-blind, placebo-controlled phase 1/2 clinical trial, Cytotherapy. (2018) 20, no. 4, 499–506, https://doi.org/10.1016/j.jcyt.2017.12.009, 2-s2.0-85044681809.
Wang L, Wang L, Cong X, et al. Human umbilical cord mesenchymal stem cell therapy for patients with active rheumatoid arthritis: safety and efficacy. Stem Cells Dev. 2013;22(24):3192–3202. doi:10.1089/scd.2013.002323941289
Chen FH, RS T. Mesenchymal stem cells in arthritic diseases. JAr Ther. 2008;10(5):223.
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。
版權說明:本文來自杭吉干細胞科技內容團隊,歡迎個人轉發至朋友圈,謝絕媒體或機構未經授權以任何形式轉載至其他平臺,轉載授權請在網站后臺下方留言獲取。




 掃碼添加微信
掃碼添加微信