慢性阻塞性肺病簡稱慢阻肺(COPD)作為全球第三大致死疾病,長期困擾著超1億中國患者。
現在的常規治療主要靠支氣管擴張劑(比如沙美特羅、福莫特羅)和吸入性糖皮質激素(如布地奈德)來控制癥狀,它們能緩解氣道痙攣、抑制炎癥,但修復已經受損的肺泡和逆轉氣道重塑卻無能為力。
因此,近年來再生醫學中的干細胞技術成為研究熱點——科研團隊希望通過細胞修復與免疫調節,彌補傳統藥物的不足,以期為慢阻肺患者提供新的治療選擇。
本文結合最新臨床數據與技術進展,系統梳理2025年1月到10月全球各地有關干細胞治療慢阻肺的核心突破以及臨床進展,為慢阻肺患者帶來最新的新聞資訊。

突破呼吸困境!2025年干細胞治療慢阻肺全球臨床進展匯總!(截至10月)
2025年1-10月干細胞治療慢阻肺臨床進展匯總
2025年1月干細胞治療慢阻肺最新臨床進展
1月29日,行業期刊《干細胞研究與治療》上發表了一篇關于《氣道基礎干細胞治療肺部疾病:一種新興的再生醫學策略》的研究成果,文章匯總了近年來氣道干細胞在肺病修復方面的多項進展,指出這些技術正從實驗室一步步走向臨床應用。[1]

研究表明干細胞療法在COPD治療中取得顯著突破:
臨床試驗顯示,自體SOX9+氣道基底細胞移植可修復支氣管擴張患者的肺組織,而一項I期臨床試驗證實自體P63+肺祖細胞治療使COPD患者肺一氧化碳彌散量平均提高18.2%,肺功能與生活質量顯著改善。
技術層面,CRISPR/Cas9基因編輯通過校正干細胞突變(如CFTR功能恢復至正常水平30-50%)為遺傳性肺病提供新策略;脂質納米顆粒(LNP)靜脈遞送技術在動物模型中實現肺上皮靶向效率達45-80%,且表達持續660天,優于傳統吸入法。
此外,靶向TGF-β/NOTCH通路的小分子藥物及氣道干細胞衍生的類器官模型(如解析BCL11A致癌基因作用)進一步揭示COPD病理機制并優化治療靶點。
總體來看,這些進展把干細胞療法從“緩解癥狀”拉向了“修復組織、校正病因”的方向,但要真正走上大規模臨床應用,仍需要解決長期安全性、標準化生產和法規審批等問題。換句話說,前景令人期待,但離常規化應用還有幾步路要走。
2025年2月干細胞治療慢阻肺最新臨床進展
2月27日,行業期刊《細胞免疫學》上發表了一篇關于《霧化間充質干細胞來源的外泌體減輕慢性阻塞性肺病大鼠模型中的氣道炎癥》的研究成果。[2]

首先,在療效層面,處理過的大鼠肺順應性更好,顯微鏡下肺組織的炎癥浸潤、過量黏液分泌和膠原沉積都明顯減少——換句話說,肺看起來“更健康”了。
同期測的炎癥和纖維化相關因子也降了:血清、BALF以及肺組織里的TNF-α、IL-6、IL-1β和TGF-β1都有下降,說明外泌體在抑炎和抑制纖維化上同時起作用。值得一提的是,研究里低劑量組的改善最明顯,提示以后要更精細地做劑量-效應研究。
在分子機制上,團隊用 qPCR 與免疫組化做了跟蹤,發現BMSCs-Exos能抑制 Wnt/β-catenin 通路的活性,從而阻斷氣道重塑和上皮-間質轉化(EMT)。這點很關鍵:它把外泌體的表觀療效和具體信號通路聯起來,為后續尋找干預靶點提供了方向。
總體來說,這項工作首次把“霧化給藥+BMSCs-Exos”這個方案證明能同時發揮抗炎、抗纖維化和抑制重塑的多重作用,能有效減輕慢阻肺大鼠的病理損傷。雖然目前還停留在動物實驗階段,但研究為臨床轉化提供了實質性依據——接下來需要更嚴格的劑量、安全性和長期效果評估,才能決定這條路能走多遠。
2025年3月干細胞治療慢阻肺最新臨床進展
3月,海南博鰲樂城國際醫療旅游先行區正式宣布:國內首批干細胞治療臨床研究項目完成備案并公布收費標準,其中針對慢性阻塞性肺病(COPD)的氣道基底層干細胞(ABSCs)治療技術以15萬元/次的價格正式落地。[3]
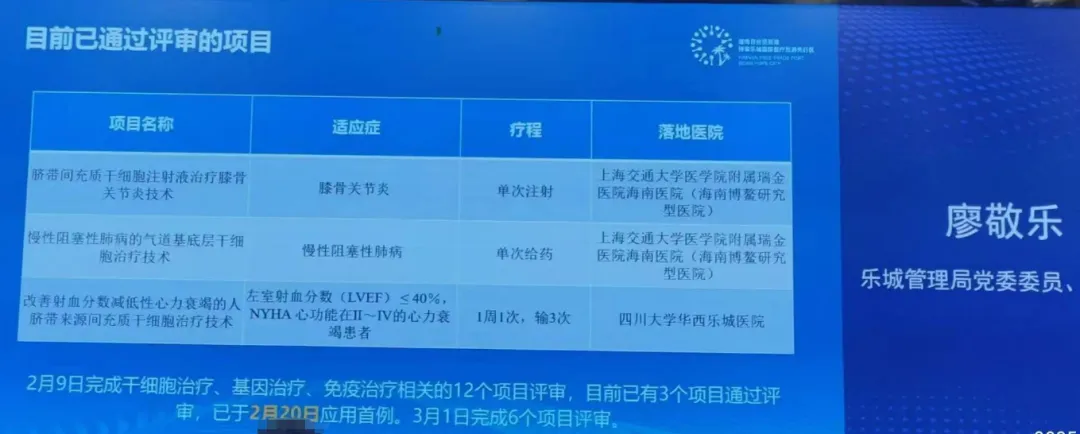
這一突破性進展標志著中國在再生醫學領域正式邁入“規范化、可支付”的新階段,為全球數億慢阻肺患者提供了顛覆性治療選擇。
根據博鰲樂城院方公開數據顯示,針對慢性阻塞性肺病(COPD)的氣道基底層干細胞(ABSCs)治療技術是從2016年起便踏上了探索肺再生醫學的征程,歷經十年磨礪,終在曙光中迎來突破。
最初三年(2016-2019年),團隊開展了包含20例COPD患者的探索性臨床試驗,運用自主研發的R-Clone專利技術,擴增患者氣道健康部位的P63/KRT5陽性成體干細胞,再通過支氣管鏡精準移植至受損肺部。
2021年6月,REGEND001獲得國家藥監局頒發的針對肺彌散功能障礙的慢性阻塞性肺病(COPD)的藥物臨床試驗批準通知書后,正式開啟了Ⅰ期臨床試驗,這一階段聚焦于安全性評估與初步療效觀察。
2022年8月1日,REGEND001在廣州醫科大學附屬第一醫院順利完成中國首例受試者給藥。
2023年3月,Ⅱ期臨床試驗多中心啟動,采用隨機盲法、安慰劑對照設計,全面評估療效與安全性;
同年9月,在2023歐洲呼吸學會國際大會(ERS Conference)以新聞發布會和口頭匯報雙重形式向全球首次公布了Ⅰ期多中心IIT臨床試驗研究成果:
所有17例受試者對細胞治療耐受良好,未報告細胞治療相關嚴重不良事件。細胞治療受試者表現出肺彌散功能(DLCO)和用力肺活量(FVC)的改善,結果具有統計學顯著意義。

在這項試驗中,35%的患者患有嚴重COPD,53%的患者患有極度嚴重的COPD。通常,如果病情惡化,許多患有這種嚴重COPD的患者會很快死亡。我們使用一個帶有刷子的微型導管從患者自己的氣道收集祖細胞。我們克隆這些細胞以產生多達10億個細胞,然后通過支氣管鏡將它們移植回患者的肺部,以修復受損的肺組織。
- 12周后,接受治療的患者的肺中位(平均)彌散能力 (DLCO)(用于測試肺部和血液之間的空氣交換情況)從治療前的30% 增加到39.7%,然后在24周時進一步增加到40.3%。
- 六分鐘步行距離測試(6MWD) 中位距離從治療前的410米增加到24周時的447米。
- 生活質量測試(圣喬治呼吸問卷或 SGRQ)中位分數降低了7分,表明有所改善。在兩名患有輕度肺氣腫(一種通常為永久性和進行性的肺損傷)的患者中,治療修復了肺損傷。
左教授表示:“我們發現,P63+祖細胞移植不僅改善了COPD患者的肺功能,還緩解了他們的呼吸困難、運動能力下降、持續咳嗽等癥狀。這意味著患者可以過上更好的生活,通常預期壽命會更長。”“如果肺氣腫惡化,死亡風險就會增加。在這次試驗中,我們發現P63+祖細胞移植可以修復輕度肺氣腫,使肺損傷消失。
2024年2月,REGEND001治療COPD的I期臨床研究成果發表在《科學-轉化醫學》(Science Translational Medicine)上。研究結果顯示,細胞治療后有超過70%的COPD患者表現為肺換氣功能的顯著改善并伴隨運動能力的提升,長期隨訪提示COPD患者的生存期得到明顯延長。[4]

研究中,28名Ⅱ~Ⅳ期COPD患者接受了P63+肺祖細胞移植治療。研究結果顯示:
- 氣體傳輸能力顯著改善:干細胞治療組的肺一氧化碳擴散能力(DLCO)在24周后增加了18.2%,而對照組則下降了17.4%。
- 肺功能明顯改善:經過6分鐘步行測試,干細胞治療組患者的步行距離增加了30米以上,表明肺功能得到了明顯改善。
- 安全性良好:治療過程中未發現嚴重不良反應,證明干細胞治療是安全的。
再將時間往后推,REGEND001預計在2025年內啟動REGEND001針對COPD的III期確證性臨床試驗。并且首例慢阻肺病患者已在3月24日完成了干細胞治療。

2025年4月干細胞治療慢阻肺最新臨床進展
4月30日,美國加利福尼亞州斯坦福市心血管研究所在期刊《臨床醫學雜志》上發表了一篇關于《慢性肺病治療學的進展:從標準療法到新興突破》的研究成果。本綜述評估了慢性肺部疾病治療干預措施的演變,從一系列成熟的吸入式聯合療法到生物制劑、基因療法,甚至基于人工智能的患者分層療法。[5]

干細胞治療慢阻肺的核心進展:
1.間充質干細胞(MSC)的抗炎與修復作用
MSC通過分泌抗炎因子(如IL-10、TGF-β)抑制肺部炎癥反應,降低促炎細胞因子(TNF-α、IL-6)水平,緩解COPD相關的慢性炎癥。
在動物模型中,MSC可修復肺泡-毛細血管屏障功能,改善氣體交換效率,為COPD急性加重期患者的肺損傷修復提供新思路。
2.臨床試驗驗證安全性與初步療效
多項臨床試驗顯示,靜脈輸注MSC可顯著降低COPD患者C反應蛋白(CRP)水平,減輕全身炎癥負擔,部分患者肺功能(如FEV1)和生活質量(SGRQ評分)有所改善。
靶向給藥策略(如支氣管內注射MSC聯合單向支氣管瓣技術)進一步提升局部療效,研究發現此類方法可使肺內皮標志物CD31表達增加3倍,提示干細胞可能促進肺組織修復。
2025年5月干細胞治療慢阻肺最新臨床進展
5月13日,我國科研人員在行業期刊《細胞療法》上發表了一篇關于《慢性阻塞性肺病的細胞療法》的研究成果。系統梳理了干細胞治療COPD的臨床試驗進展。[6]
研究指出,盡管骨髓間充質干細胞(BM-MSC)、臍帶間充質干細胞(UC-MSC)及脂肪來源干細胞(AD-MSC)等多源干細胞治療COPD的臨床試驗已逐步推進,但療效與機制仍需深入驗證。

1.早期研究與核心發現:
一是安全性可以被確認,但療效尚不穩定。比如巴西2009年的 NCT01110252(4 例 GOLD IV)證明了靜脈注射 BM-MSC 的安全性,但樣本太小,無法下結論;隨后更大的隨機對照試驗 NCT00683722 顯示同種異體BM-MSC能降低全身炎癥標志物CRP,卻并未在FEV1或SGRQ生活質量評分上看到顯著改善。
二是干細胞可能對肺內皮有修復作用:Stolk團隊在2016年(NCT01306513)結合肺減容手術發現,接受BM-MSC的患者肺內皮標志(CD31)上升了約3倍,但對FEV1的提升很有限。此外,給藥方式也是一大問題——2018 年 Armitage的研究(ACTRN12614000731695)提示,靜脈注射的BM-MSC多數滯留在肝臟,能在肺里的時間只有30分鐘到24小時不等,說明要想把效果做大,遞送策略必須優化。
2.創新療法與療效驗證:
靶向給藥突破:de Oliveira團隊(NCT01872624)采用支氣管內注射BM-MSC聯合單向支氣管瓣(EBV),結果顯示CRP水平顯著下降,患者生活質量指標(mMRC評分、SGRQ)改善。
脂肪干細胞的潛力:Comella研究(NCT02041000)通過靜脈輸注自體脂肪干細胞(SVF)觀察到SGRQ評分顯著降低(從73降至45),但缺乏肺功能數據;Le Thi Bich團隊(ISRCTN70443938)發現D期COPD患者對UC-MSC反應優于C期,而土耳其研究(樣本量5例)報道FEV1/FVC比值從66.9%提升至69.58%,提示UC-MSC可能改善肺功能,但需更大規模驗證。
總體來看,干細胞治療COPD的核心思路是精準抑炎、促進肺組織修復并改進遞送方式。接下來需要把類器官模型、多組學分析與臨床試驗結合起來,弄清楚到底哪個細胞、哪個給藥途徑在什么患者身上最有效,并探索與抗炎藥、基因修復等聯合方案。
2025年6月干細胞治療慢阻肺最新臨床進展
6月20日,吉林大學基礎醫學院重點實驗室牽頭在行業期刊《干細胞研究與治療》上發表了一篇名為《間充質干細胞衍生的外泌體——一種改善慢性阻塞性肺病神經認知障礙的有希望的治療方法》的研究成果。[7]

研究提出了間充質干細胞來源的外泌體(MSC-Exos)可能通過三種潛在機制改善慢阻肺引起引起的神經認知障礙(COPD-NCDs):
(1) 通過改善肺部功能發揮間接神經保護作用:MSC-Exos可以減少肺部炎癥,從而減少全身炎癥循環和隨后的神經炎癥,最終改善神經認知功能障礙;
(2) 直接作用于中樞神經系統:MSC-Exos可以穿過血腦屏障 (BBB) 發揮神經保護作用,具體方式包括:恢復血腦屏障的完整性、調節神經炎癥、促進神經發生、增強髓鞘形成和改善突觸可塑性;
(3) 肺腦軸調節:新興證據表明MSC-Exos可能通過特定的肺神經通路發揮作用。舉例來說,靜脈注射干細胞在小鼠實驗中被發現能通過肺迷走神經-腦軸調節中樞神經系統的血清素水平,從而產生抗抑郁作用。
因為MSC-Exos是干細胞分泌的核心活性因子,它們在肺-腦軸介導的COPD-NCD改善中的潛力值得進一步探索。未來,這種機制可能為慢阻肺伴神經認知障礙的治療提供全新的思路。
2025年7月干細胞治療慢阻肺最新臨床進展
7月2日,《BMC Pulmonary Medicine》期刊上發表了一篇名為《MSCs通過Nrf2通路調節氧化應激治療慢性阻塞性肺病》的研究成果。[8]

本次研究采用煙草煙霧暴露及細菌脂多糖滴鼻法建立小鼠COPD模型,監測MSCs移植后COPD病情進展。與對照組相比,模型小鼠肺內巨噬細胞數量增多,炎癥細胞浸潤,肺泡增大,并出現肺纖維化。
MSC移植后,氧化應激水平降低,肺部狀況改善,COPD小鼠體內4-HNE降低90pg/mg prot,IL-6降低15.55pg/ml,ROS降低1.9×107,血液中PCT降低0.51 μg/L,EOS降低29.02%,WBC降低3.41^9/L,CRP降低15.8 mg/ml。此外,我們的數據表明MSC可能通過調控Nrf2通路減輕氧化應激,從而減輕COPD引起的肺損傷。
本研究證實了移植MSCs對煙草和脂多糖誘發的COPD的治療作用,并揭示了MSCs通過調節氧化應激相關通路改善COPD。
2025年8月干細胞治療慢阻肺最新臨床進展
8月15日,上海瑞金落地的慢阻肺干細胞治療臨床實驗室吉美瑞生再生醫學集團(Regend Therapeutics)正式宣布,將在2025年9月28日于荷蘭阿姆斯特丹舉辦的歐洲呼吸學會國際大會(ERS)上,以口頭匯報形式向全球披露其自主研發的全球首創氣道基底層干細胞產品REGEND001,在治療慢性阻塞性肺疾病(COPD)臨床Ⅱ期研究中的安全性與有效性核心數據,為全球慢阻肺病治療領域帶來新的關注焦點。[9]

該試驗是針對伴有彌散功能障礙的COPD患者開展的一項多中心、隨機盲法、安慰劑對照的Ⅱ期臨床試驗研究(NCT05638776)。
REGEND001制劑是吉美瑞生研發的全球首創(First-in-class)氣道基底層干細胞新藥,采用單次肺內給藥技術,主要研究終點為治療后受試者的肺彌散功能改善情況,同時觀察受試者治療后生活質量、運動能力以及肺部CT影像的改善情況。
本臨床試驗主要研究者為中華醫學會呼吸分會副主任委員、廣州醫科大學附屬第一醫院呼吸內科主任李時悅教授,其他臨床試驗參與單位包括北京、上海和重慶等地的高水平醫療機構。
目前所有患者已完成為期52周的隨訪觀察。療效與安全性數據將在此次ERS大會上由左為教授向全球呼吸科臨床醫生、投資方和跨國藥企等發布。
2025年9月-10月干細胞治療慢阻肺最新臨床進展
9月27日至10月1日,在全球呼吸領域頂級會議——第35屆歐洲呼吸學會(European Respiratory Society,ERS)年會上,一項標志著慢性阻塞性肺疾病(COPD)治療進入再生醫學新紀元的突破性臨床研究正式公布。[10]

吉美瑞生董事長/首席科學家、同濟大學左為教授以口頭報告形式,向來自全球的呼吸領域專家學者公布了全球首創自體肺臟再生細胞藥物——REGEND001自體氣道基底層干細胞療法治療COPD的Ⅱ期臨床試驗的成果。
研究數據顯示,REGEND001能夠顯著且持久地改善COPD患者的肺彌散功能,并促進肺泡結構修復,為這一既往被認為“不可逆”的疾病提供了全新的治療范式。
Ⅱ期臨床實驗中COPD患者接受單次REGEND001肺氣道基底層干細胞治療后52周隨訪顯示:
1.肺彌散功能取得根本性改善
關鍵療效終點肺彌散換氣功能(DLCO)在細胞治療組表現出持續且顯著的提升,與對照組相比,治療組在移植后24周和第52周均顯示出統計學意義的顯著改善。DLCO相對基線水平的提升從4周即開始顯現,于24周達到峰值,并穩定持續至52周,證明了單次給藥的持久效力。
2.肺泡容積增加,結構修復顯現
與DLCO改善相呼應的,細胞治療組的肺泡容積(VA)在24周和52周時較對照組也呈現顯著增加。更令人鼓舞的是,通過CT影像三維重建分析,首次觀察到治療組患者的功能性肺容積增加,以及肺氣腫區域(尤其在下葉)得到部分修復—— 這為“結構修復引領功能改善”提供了直觀的影像學證據。
3.患者生活質量顯著提升
在患者報告結局方面,細胞治療組在COPD評估測試(CAT)評分和改良版英國醫學研究委員會(mMRC)呼吸困難評分上的改善程度均在統計學上顯著優于對照組,表明患者日常生活受疾病影響的程度在多個維度(包括咳嗽、咳痰、胸悶氣喘、運動能力、睡眠與情緒等)得到了實質性改善。其中,細胞治療24周后,CAT評估臨床穩定或改善的人數比例高達100%。
4.良好的安全性得到證實
研究期間,治療組與對照組總體不良事件發生率相當,支氣管鏡下移植治療慢性阻塞性肺疾病(COPD)具備安全性可行性。
德國波斯特研究中心、萊布尼茨肺研究中心教授、ERS會議和研討會負責人Silke Meiners教授在接受專訪時,對左為教授帶領團隊在干細胞治療COPD領域的開拓性成果給予了高度評價:“這些精彩的進展代表了COPD治療的新方法和新方向。很久以前,各位同行就有這個想法,這兩年我們終于接近了當初的夢想。肺的再生是我們的終極目標,但是如果我們能夠改變肺損傷部位的干細胞狀態,它們可能會進一步改變周圍的微環境,啟動自身的再生程序。這也是一種可行的策略,因為我們并不一定要讓整個肺再生,我們只需要通過干細胞移植或者其他方法激活損傷部位干細胞的再生能力。總之,這個方向充滿希望,有著無限可能!”
10月11日,荷蘭萊頓大學醫學中心實驗室牽頭在《Advanced Drug Delivery Reviews》上發表了一篇名為《肺部疾病的細胞療法:概述與展望》的研究成果。[11]

臨床研究顯示,間充質干細胞(MSCs)治療慢阻肺具有良好的安全性,即使用異體干細胞,也未出現嚴重不良反應或排斥反應,耐受性高,符合臨床應用的基本要求。
在療效方面,MSCs因其具備免疫調節、抗炎和組織修復能力,在部分臨床觀察中已顯示出改善患者肺部炎癥、減輕呼吸困難、提升生活質量等積極效果。尤其是在聯合外泌體或精準給藥策略中,干細胞展現出更強的修復潛力,為慢阻肺患者帶來了新的治療希望。
2025年干細胞治療慢阻肺最新臨床進展總結
綜上來看,2025年干細胞治療COPD在機制研究和技術優化方面都有不小的突破:
靶向遞送更精準:像支氣管鏡直接移植或霧化外泌體的方法,讓干細胞在肺部停留更久、效果更集中;
基因編輯與新型載體:CRISPR/Cas9 技術配合脂質納米顆粒(LNP)載體,讓干細胞的修復能力更強,也更容易“找到”受損部位;
多組學與類器官模型:把基因、蛋白質和代謝信息結合起來,用類器官模型模擬肺部環境,能更清楚地看清COPD的病理機制,也方便篩選潛在治療靶點。
總的來說干細胞治療為COPD患者帶來了突破傳統藥物依賴的創新路徑,其核心價值在于通過源頭修復肺組織和調控慢性炎癥,延緩疾病進展并改善長期預后。
隨著遞送技術、基因工程及個體化醫療的融合,干細胞療法有望成為COPD精準管理的重要組成部分,推動呼吸系統疾病治療模式從“被動控制”向“主動修復”轉變,最終惠及全球數億患者。
結語
2025年,多項研究顯示,干細胞治療慢阻肺正從探索走向臨床驗證。支氣管鏡定向植入和霧化外泌體等新型遞送方式提升了治療精準性;基因編輯與新型載體則進一步增強了細胞修復潛力。同時,多組學分析和類器官模型為揭示疾病機制提供了更直觀的工具。
展望未來,如果制備標準能逐步統一,長期安全性得到確認,再結合個體化醫療的推進,干細胞或許會真正成為慢性肺病治療的關鍵武器,給更多患者帶來更持久的康復希望。
參考資料:
[1]Liu, X., Wang, X., Wu, X. et al. Airway basal stem cell therapy for lung diseases: an emerging regenerative medicine strategy. Stem Cell Res Ther 16, 29 (2025). https://doi.org/10.1186/s13287-025-04152-5
[2]Min Wang, Yuxin Hao, Wei He, Hui Jia, Zhaoshuang Zhong, Shuyue Xia,Nebulized mesenchymal stem cell-derived exosomes attenuate airway inflammation in a rat model of chronic obstructive pulmonary disease,Cellular Immunology,Volumes 409–410,2025,104933,ISSN 0008-8749,https://doi.org/10.1016/j.cellimm.2025.104933.
[3]https://www.medvalley.cn/yiyao/77041.html
[4]Yujia Wang et al.,Autologous transplantation of P63+ lung progenitor cells for chronic obstructive pulmonary disease therapy.Sci. Transl. Med.16,eadi3360(2024).DOI:10.1126/scitranslmed.adi3360
[5]Brewer, K.D.; Santo, N.V.; Samanta, A.; Nag, R.; Trotsyuk, A.A.; Rajadas, J. Advances in Therapeutics for Chronic Lung Diseases: From Standard Therapies to Emerging Breakthroughs. J. Clin. Med. 2025, 14, 3118. https://doi.org/10.3390/jcm14093118
[6]Le, BP.T., Le, QD. (2025). Cell Therapy for Chronic Obstructive Pulmonary Disease. In: Liem, N.T., Forsyth, N.R., Heke, M. (eds) Cell Therapy. Springer, Singapore. https://doi.org/10.1007/978-981-96-1261-1_17
[7]Xiao, H., Yu, X., Liu, Y. et al. Mesenchymal stem cell-derived exosomes–a promising therapeutic approach to improve neurocognitive disorders in chronic obstructive pulmonary disease. Stem Cell Res Ther 16, 314 (2025). https://doi.org/10.1186/s13287-025-04457-5
[8]Zhou, Y., Zhou, W., Li, Y. et al. MSCs regulate oxidative stress through the Nrf2 pathway to treat chronic obstructive pulmonary disease. BMC Pulm Med 25, 304 (2025). https://doi.org/10.1186/s12890-025-03770-2
[9]http://www.regend.cn/news/show-350.html
[10]https://bydrug.pharmcube.com/news/detail/5b4479951cd87231d9888aa036b38960
[11]van der Does AM, V Schledorn L, Olmer R. Cell-based treatments of lung diseases: overview and outlook. Adv Drug Deliv Rev. 2025 Oct 11;227:115712. doi: 10.1016/j.addr.2025.115712. Epub ahead of print. PMID: 41083106.
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。




 掃碼添加微信
掃碼添加微信