慢性阻塞性肺疾病(COPD)作為高發的慢性呼吸系統疾病,長期面臨氣流受限、炎癥反復及急性加重等治療挑戰。近年來,隨著醫藥技術的快速發展,靶向藥物、無創呼吸支持技術以及再生醫學等新策略不斷突破并應用于臨床,正推動COPD治療向個體化、精準化方向發展。
本文將系統梳理截至2025年10月底慢阻肺的6種前沿治療技術進展,涵蓋:新型PDE抑制劑、生物制劑與靶向治療、吸入療法優化、臨床治療策略優化、干細胞療法以及無創呼吸支持治療這6大最新突破。為慢阻肺患者帶來最前沿的臨床資訊。

2025慢阻肺的5種最新治療方法:從PDE抑制劑到干細胞療法的最新突破
一、新型PDE抑制劑:雙靶點與單靶點協同突破
1.1 PDE3/4雙靶點抑制劑HRS-9821
2025年7月28日,恒瑞醫藥宣布與葛蘭素史克(GSK)達成協議,將潛在同類最佳(Best-in-Class)的PDE3/4雙靶點抑制劑HRS-9821項目(除中國區外)的全球獨家權利。[1]

HRS-9821作為潛在同類最佳的PDE3/4雙靶點抑制劑,其臨床價值在于雙重機制的協同效應:通過抑制PDE3擴張支氣管,同時抑制PDE4減少炎癥因子釋放,從而同步改善慢性阻塞性肺疾病(COPD)的氣流受限和氣道炎癥。
研發進展方面,截至2025年7月,該藥物的吸入混懸液已完成Ⅰ期臨床;其吸入粉霧劑則已于2025年4月10日獲批臨床試驗。兩種劑型的差異化布局,展現了恒瑞在呼吸系統藥物領域的技術積累。
1.2 恩司芬群(ensifentrine)
2025年2月7日,優銳醫藥(Nuance Pharma)宣布,恩司芬群(ensifentrine)已獲得中國澳門特別行政區藥物管理局的批準,用于成人慢性阻塞性肺病(COPD)的維持治療。
該產品可通過普通霧化器直接遞送到肺部,使用簡便,不需要復雜的手口協調操作。該療法也在2024年初被行業媒體Evaluate列為2024有望獲批的10款重磅療法之一。
2024年9月,優銳醫藥完成了恩司芬群用于COPD維持治療的中國3期臨床試驗ENHANCE-CHINA的患者招募工作。
2025年5月16日,宣布恩司芬群在慢性阻塞性肺病 (COPD) 治療的3期ENHANCE-CHINA試驗中達到主要終點。[2]

研究結果:
主要終點:第12周時,經安慰劑校正后,其0-12小時平均 FEV?曲線下面積較基線增加110 mL,在年齡、病情嚴重程度等關鍵亞組中均有顯著臨床改善。
次要終點方面:第12周峰值FEV?增加174mL,0-4小時和6-12小時平均 FEV?分別增加162mL和77mL,證實每日兩次給藥方案有效。
癥狀和生活質量上:6至24周內呼吸困難(TDI)、呼吸道癥狀(E-RS)持續改善,24周時生活質量(SGRQ)較安慰劑顯著改善-2.9個單位。24周內中度 / 重度惡化率降低28%,首次發作風險降低25%。
安全性方面:耐受性良好,治療相關不良事件發生率與安慰劑相似。
研究人員表示,ENHANCE試驗的各項數據,包括肺功能、癥狀、生活質量指標的改善以及疾病發作次數的減少,加上良好的安全性,都支持了對恩替芬堿將改變慢阻肺治療模式的信念。計劃于2025年下半年向中國國家藥品監督管理局提交新藥申請。
1.3 正大天晴TQC3721混懸液
2025年7月29日,CDE官網顯示,正大天晴吸入用TQC3721混懸液擬納入突破性治療品種,用于慢性阻塞性肺疾病(COPD)的維持治療。[3]
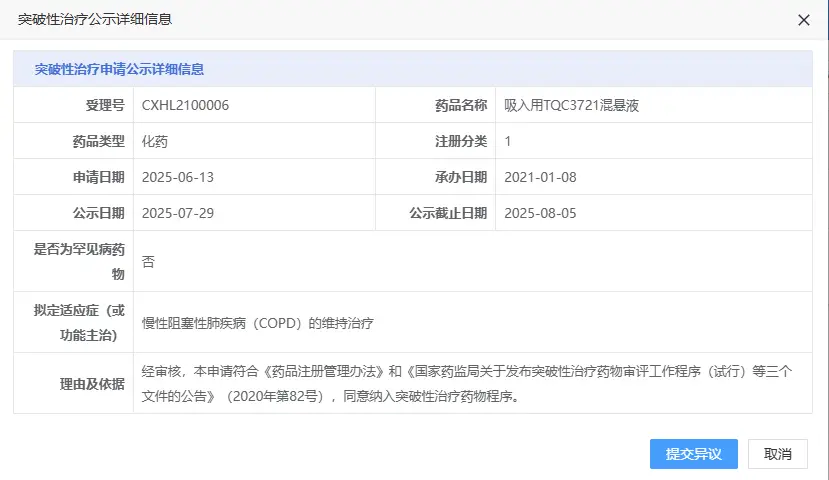
TQC3721是一款全新機制的吸入性PDE3/4抑制劑,具有擴張支氣管和抗炎的雙重作用,從而減輕患者癥狀,并抑制炎癥,控制疾病進展。
臨床研究結果顯示,TQC3721在單支擴劑和雙支擴劑背景治療的COPD患者中,肺功能和癥狀評分有顯著改善,相關數據將在近期國際學術會議上公布。
值得一提的是,吸入用TQC3721混懸液已經獲得CDE批準開展Ⅲ期注冊臨床研究,用于COPD的維持治療。相較于已上市PDE3/4產品,TQC3721的Ⅲ期臨床研究將額外納入雙支擴劑背景治療患者,覆蓋更為廣泛的COPD患者人群。
此外,除吸入用混懸液外,TQC3721吸入粉霧劑正處在臨床Ⅰ期開發階段,干粉劑型有望進一步提升患者的依從性。
二、生物制劑與靶向治療:突破難治型患者瓶頸
2.1 TSLP單抗(Tezepelumab)
2025年7月29日,哥本哈根呼吸研究中心在《JTD》期刊上發表了一篇名為《使用tezepelumab控制慢性阻塞性肺病的急性加重:來自COURSE試驗的見解》的研究成果。[4]

本次研究是一項雙盲、隨機、安慰劑對照的2a期臨床試驗,在10個國家的90個研究中心開展。共333例中度至重度慢性阻塞性肺病 (COPD)患者被隨機分配接受tezepelumab 420mg(n=165)或安慰劑(n=168)治療,每4周皮下注射一次,療程最長為52周。
在療效方面,本研究結果顯示,tezepelumab組中度或重度急性加重年發生率為1.75,安慰劑組為2.11,雖未達主要研究終點,但基線血嗜酸性粒細胞≥150個/毫升患者的發作率降低更明顯。
安全性方面,兩組副作用無差異,未出現過敏反應或治療相關死亡,tezepelumab組不良事件發生率81%、嚴重不良事件30%,安慰劑組分別為75%和30%,52周治療及12周隨訪中安全性良好。
2.2 度普利尤單抗(Dupilumab)
2024年9月27日,賽諾菲宣布,達必妥?(度普利尤單抗注射液)獲得中國國家藥品監督管理局(NMPA)批準,用于血嗜酸性粒細胞升高且控制不佳的慢性阻塞性肺疾病成人患者。[5]
達必妥?是全球首個獲批的慢阻肺病靶向治療藥物,結束慢阻肺病創新療法長達十年的沉寂期,開辟靶向治療新紀元。

此次達必妥?的獲批主要是基于兩項具有里程碑意義的 III 期臨床試驗(BOREAS和NOTUS)的臨床數據,研究分別在 40~80 歲(BOREAS)和 40~85 歲(NOTUS)的中重度慢阻肺病成人吸煙者或既往吸煙者中評價了達必妥?的療效和安全性。
研究顯示,達必妥?(每兩周一次)顯著降低急性加重,改善了肺功能,并提升了與健康相關的生活質量。
在療效方面與安慰劑聯合最佳標準吸入治療(三聯治療,如果存在 ICS 禁忌則允許使用二聯支氣管舒張劑)相比:
達必妥?組治療52周,慢阻肺病中重度急性加重年化率分別降低了30%和34%;在基線呼出氣一氧化氮較高的患者中,達必妥?相對于安慰劑組的中重度急性加重年化率降低和肺功能改善有更好的效果。
在安全性方面,兩項研究的安全性結果與達必妥?已獲批適應癥的已知安全性情況一致。
三、吸入療法優化:劑型創新與真實世界證據
3.1 噻托溴銨奧達特羅吸入噴霧劑
2025年8月1日,藥物臨床試驗登記與信息公示平臺數據顯示,浙江股份有限公司的噻托溴銨奧達特羅吸入噴霧劑在健康參與者中隨機、開放、兩制劑、兩周期交叉、空腹狀態下的生物等效性試驗已啟動。臨床試驗登記號為CTR20253032。[6]
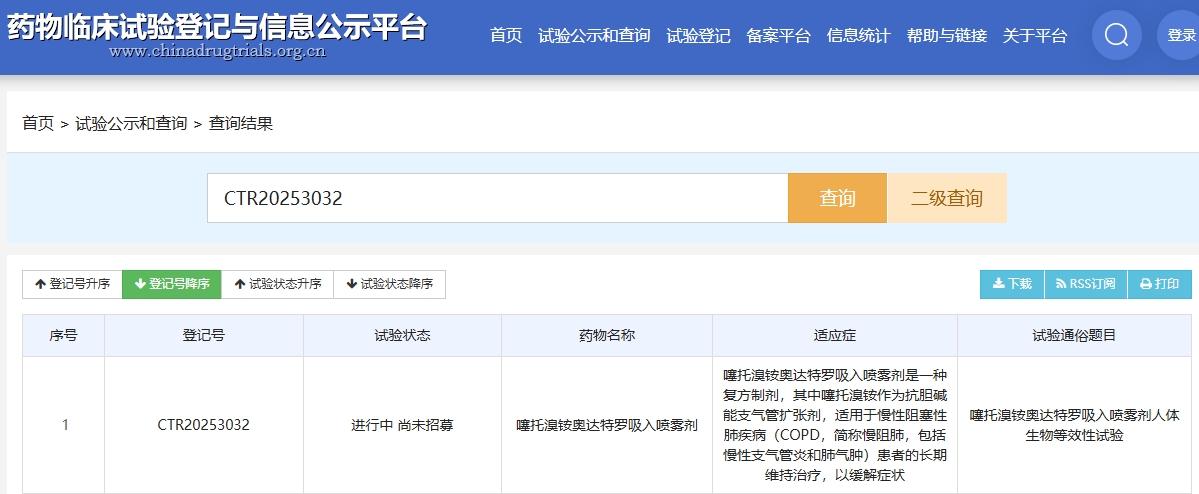
噻托溴銨奧達特羅吸入噴霧劑為化學藥物,適應癥為慢性阻塞性肺疾病。用法為成人每日1次,每次吸入2噴,每噴遞送劑量為噻托溴銨2.5μg和鹽酸奧達特羅2.5μg。本次試驗主要目的為評價兩種制劑在健康參與者體內的生物等效性;次要目的為觀察受試制劑和參比制劑在健康參與者中的安全性。
目前,該實驗狀態為進行中,目標入組人數36人。
3.2 三聯吸入療法
2025年3月25日,西班牙初級保健健康中心牽頭在《Medicina de Familia. SEMERGEN》期刊上發表了一篇名為《與雙吸入療法相比,三聯吸入療法對COPD患者心血管和全因死亡率的影響:系統評價和薈萃分析》的研究成果。[7]
通過一項證據綜合研究,評估了三聯吸入療法 (TT) 與雙聯吸入療法 (DT,包括LAMA/LABA或LABA/ICS) 相比對全因死亡率和心血管死亡率的影響。

本次研究納入了5項RCT。該研究納入5項隨機對照試驗,涉及7855例三聯吸入療法 (TT) 治療患者、7003例LABA/ICS治療患者和5059例LAMA/LABA治療患者,多數研究偏倚風險低或中等。
結果顯示,與LAMA/LABA相比,TT可使心血管死亡率降低48%、全因死亡率降低34%,差異均顯著;與LABA/ICS相比,TT能使心血管死亡率降低11%、全因死亡率降低10%,但差異不顯著。有效性排名中,TT 在心血管和全因死亡率改善上均居首。
結論指出,對于中度至重度且有加重史的COPD患者,三聯療法較雙聯療法能顯著降低心血管和全因死亡率。
四、臨床治療策略優化:個體化與精準分層
中國慢阻肺病患者的治療模式及三聯療法應用
2025年7月29日, 中南大學湘雅二醫院牽頭在《國際慢性阻塞性肺病雜志》上發表了一篇名為《中國慢性阻塞性肺病患者的治療模式及三聯療法應用:基于鄞州數據庫的真實世界數據分析》的研究成果。[8]

該回顧性研究納入7888例≥40歲的COPD患者,隨訪期間29.1%接受三聯療法(ICS+LABA+LAMA),中位治療持續 3.27個月;68.6%接受ICS+LABA雙聯療法,27.3%和23.3%分別接受ICS或LAMA單藥療法。
研究指出,三聯療法較雙聯或單藥療法可顯著降低中重度發作及后續住院風險,尤其適合有惡化史的高危患者。
與加拿大(71%)、西班牙(16.5%)、美國(9.6%)的應用率相比,我國三聯療法應用受固定劑量制劑推廣影響呈上升趨勢(從基線0.3%增至29.1%)。固定劑量三聯療法通過簡化給藥方案,有望提高患者依從性,惠及更廣泛患者群體。
五、再生醫學:干細胞療法的臨床應用
5.1 自體P63陽性肺前體細胞
P63陽性肺前體細胞是一種特定類型的干細胞,它們在肺部組織中起著重要的作用,參與肺部的再生和修復過程。
2024年2月14日,同濟大學醫學院附屬東方醫院左為教授團隊,與廣州醫科大學附屬第一醫院鐘南山院士、李時悅教授團隊,以及陸軍軍醫大學附屬西南醫院戴曉天教授合作,在全球頂級轉化醫學刊物《科學-轉化醫學》雜志發表了題為“移植自體P63陽性肺前體細胞用于慢性阻塞性肺病的治療”的研究論文。[9]

在這項研究中,科學家們將焦點對準了肺祖細胞,探索其在改善肺功能和氣體傳輸能力方面的潛力。實驗中共有28名處于Ⅱ~Ⅳ期的慢性阻塞性肺疾病患者參與,并被隨機分為兩組:干細胞治療組和對照組。結果顯示:
氣體傳輸能力顯著改善
在移植后的24周,與對照組相比,干細胞治療組的肺一氧化碳(DLCO)擴散能力在統計學上有了明顯的提升,其DLCO擴散能力相對于基線增加了18.2%,而對照組則下降了17.4%。
肺功能改善
在持續6分鐘的步行測試中,干細胞治療組的患者行走的距離增加了30米以上,這一變化表明他們的肺功能得到了明顯的提升。
無不良反應
在治療過程中及隨后的隨訪中,并未觀察到嚴重的不良反應,這進一步證明了P63+肺祖細胞移植的安全性和可行性,使其有望成為慢阻肺治療的一種新策略。
本研究是全世界第一個正式發表的基于肺臟再生機理的細胞治療臨床試驗,觀察到P63+ LPC細胞治療表現出遠超過傳統慢阻肺標準治療方法的潛力。試驗的成功為慢阻肺的治療提供了一種全新的策略,有望為全球數億慢阻肺患者帶來更有效的治療選擇。
5.2 間充質干細胞治療
2025年5月13日,我國科研人員在行業期刊《細胞療法》上發表了一篇關于《慢性阻塞性肺病的細胞療法》的研究成果。系統梳理了干細胞治療COPD的臨床試驗進展。[10]

早期研究中,巴西試驗首次驗證骨髓間充質干細胞(BM-MSC)靜脈輸注的安全性;后續隨機對照試驗顯示,同種異體 BM-MSC可降低C反應蛋白、減輕全身炎癥,肺功能和生活質量輕微改善,另有研究發現BM-MSC聯合肺減容手術可能促進肺內皮修復,但對FEV1提升有限。
創新療法方面,臨床表明支氣管內注射BM-MSC聯合單向支氣管瓣可顯著降低炎癥、改善生活質量;靜脈輸注自體脂肪干細胞能明顯改善生活質量評分,但缺乏肺功能數據;臍帶間充質干細胞(UC-MSC)對D期COPD患者療效優于C期,小樣本研究顯示其可能改善肺功能比值。
綜上所述,干細胞治療COPD的核心在于精準調控炎癥、促進肺組織修復及優化遞送策略。未來需結合類器官模型與多組學分析,解析干細胞作用機制,并探索聯合療法(如干細胞+抗炎藥物或基因編輯技術),推動其從“實驗性治療”向標準化臨床應用轉化。
相關閱讀:
慢阻肺如何治療?干細胞療法如何幫助慢阻肺患者喚醒肺部“新活力”?
突破呼吸困境!2025年干細胞治療慢阻肺全球臨床進展匯總!(截至5月)
六、無創呼吸支持治療:技術與應用進展
家庭高流量鼻導管氧療(HFNC)
2025年1月28日,荷蘭多德雷赫特阿爾伯特·史懷哲醫院在期刊《J. Clin. Med》上發表了一篇名為《家庭高流量鼻導管氧療對重度COPD和頻繁發作患者臨床療效的影響》的研究成果。[11]

在一項前瞻性概念驗證性介入多中心研究中,納入了40名GOLD III期和IV期COPD患者進行家庭高流量鼻導管氧療(HFNC)。
經1年的HFNC治療,27例患者進行評估。COPD急性加重率下降1.40,年入院次數減少0.96次,住院天數減少7.22天。毛細血管二氧化碳分壓下降0.02 kPa,CCQ評分下降0.06,MRC呼吸困難評分下降0.04,HADS焦慮評分下降了0.63。最后,HADS抑郁評分下降了0.32。正常碳酸血癥組和高碳酸血癥組在CCQ評分變化方面存在顯著差異。
因此對于疾病負擔重、COPD頻繁發作的嚴重COPD患者,無論他們是否患有高碳酸血癥,為期一年的HFNC治療都顯著降低了COPD發作率、住院時間和住院天數,并且只有高碳酸血癥組的HRQoL指標有所改善。
這可能意味著,疾病負擔重、COPD頻繁發作的嚴重COPD患者,無論是否患有高碳酸血癥,都適合接受家庭HFNC氧療治療。
結語
從雙靶點PDE抑制劑的協同作用、生物制劑的精準靶向,到三聯吸入療法的優化應用,再到干細胞療法的組織修復潛力和家庭無創呼吸支持的普及,COPD治療正邁向多維度、個體化的新時代。
這些進展不僅顯著改善了肺功能、減少了急性加重,更提升了患者的生活質量。未來,隨著技術的持續成熟和臨床策略的精準化,COPD患者將迎來更安全、高效的治療選擇,為控制疾病進展、降低負擔提供堅實支撐。
參考資料:
[1]https://bydrug.pharmcube.com/news/detail/55f957da727f3ee36b076db5aea49524
[2]https://www.prnewswire.com/apac/news-releases/nuance-pharma-announces-ensifentrine-meets-primary-endpoint-in-phase-3-enhance-china-trial-for-copd-302457563.html
[3]正大天晴慢阻肺1類新藥擬納入突破性治療品種|炎癥|抗炎|copd|免疫性疾病|中國生物制藥_網易訂閱
[4]Afrose D, Valizadeh M, Sivapalan P. Exacerbation control in chronic obstructive pulmonary disease with tezepelumab: insights from the COURSE trial. J Thorac Dis 2025;17(7):4379-4382. doi: 10.21037/jtd-2025-769
[5]https://news.qq.com/rain/a/20240927A06DJH00
[6]http://www.chinadrugtrials.org.cn/clinicaltrials.searchlist.dhtml
[7]A. Calderón-Montero, M. García Fernández, M.E. García-Velasco, M. Joshi, K. Khan, C. Calderón-Ferrer, M. Nú?ez-Nú?ez,Effect of triple inhaled therapy on cardiovascular and all-cause mortality compared with dual inhaled therapy in COPD: A systematic review and meta-analysis,Medicina de Familia. SEMERGEN,
Volume 51, Issue 5,2025,102478,ISSN 1138-3593,https://doi.org/10.1016/j.semerg.2025.102478.[8]https://www.tandfonline.com/doi/full/10.2147/COPD.S499783
[9]Yujia Wang et al.,Autologous transplantation of P63+ lung progenitor cells for chronic obstructive pulmonary disease therapy.Sci. Transl. Med.16,eadi3360(2024).DOI:10.1126/scitranslmed.adi3360
[10]Le, BP.T., Le, QD. (2025). Cell Therapy for Chronic Obstructive Pulmonary Disease. In: Liem, N.T., Forsyth, N.R., Heke, M. (eds) Cell Therapy. Springer, Singapore. https://doi.org/10.1007/978-981-96-1261-1_17
[11]Theunisse, C.; de Graaf, N.T.C.; Braam, A.W.E.; Vonk, G.C.; Baart, S.J.; Ponssen, H.H.; Cheung, D. The Effects of Home High-Flow Nasal Cannula Oxygen Therapy on Clinical Outcomes in Patients with Severe COPD and Frequent Exacerbations. J. Clin. Med. 2025, 14, 868. https://doi.org/10.3390/jcm14030868
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。




 掃碼添加微信
掃碼添加微信