腦癱 (CP) 包括一組影響運動、肌張力和/或姿勢的持續性非進行性疾病。CP患者一生中的全部經濟損失給全世界的此類患者及其家人帶來了沉重的經濟負擔;然而,仍然缺乏徹底的治愈方法。
引起腦癱的因素有哪些:通常,缺氧引起的腦損傷、遺傳因素、突變和其他幾種假設理論(包括感染/炎癥)可能導致腦組織發育不良,從而導致神經元功能喪失。
腦癱癥狀表現:據統計,腦癱患者除神經系統癥狀外,還有其他癥狀,如:疼痛(75%)、智力障礙(50%)、無法行走(33%)、無法說話(25%)、癲癇 (25%)、失禁 (25%) 和失明 (10%) 。

然而,目前仍然缺乏徹底的治愈方法。
干細胞已被用于許多實驗性CP動物模型并取得了良好的效果,這取決于兩個基本特性:自我更新(產生相同細胞的能力)和多能性(產生多種細胞類型的能力)。
治療腦癱新途徑:臍帶血干細胞移植治療腦癱的作用機制
基于臍帶血 (UCB) 的干預措施正在成為一種科學上合理的治療方法,并且可能治愈CP。干細胞已被用于許多實驗性CP動物模型并取得了良好的效果。根據動物模型和臨床試驗的發現,與其他類型的干細胞相比,UCB干細胞在治療安全性和有效性、倫理學、非腫瘤增殖、可及性、易于保存和免疫反應調節方面具有優勢。目前,由于UCB的成分復雜且具有不同的治療機制,因此基于UCB的CP干預措施的使用受到限制。這些可以分為三個方面:歸巢和神經再生、營養因子分泌和神經保護作用。
大連醫科大學第一附屬醫院干細胞臨床研究中心在一篇文章綜述中總結了臍帶血干細胞活性成分的特征及其治療腦癱的作用機制。這篇綜述重點介紹了有關臍帶血干細胞移植的當前研究結果和臨床證據,這些研究結果和臨床證據有助于提供治療建議、為治療干預決策提供信息,并有助于指導未來的研究。

臍帶血干細胞治療腦癱的機制
細胞治療研究中涉及的臍帶血干細胞成分顯示在表格1。與其他類型的干細胞相比,來自UCB的干細胞在CP治療安全性和有效性 、倫理學、非腫瘤增殖、可及性、易于保存和免疫反應調節等方面具有優勢,基于動物模型和臨床試驗的發現。
在動物研究中,臍帶血細胞療法取得了實質性進展(遷移至位點、改善功能喪失和預防白質損傷)。令人鼓舞的是,在臨床試驗中,臍帶血干細胞治療已被證明是一種安全、可行且潛在有效的CP治療方法,特別是在患者的運動功能恢復和急性期后新生兒腦損傷中。
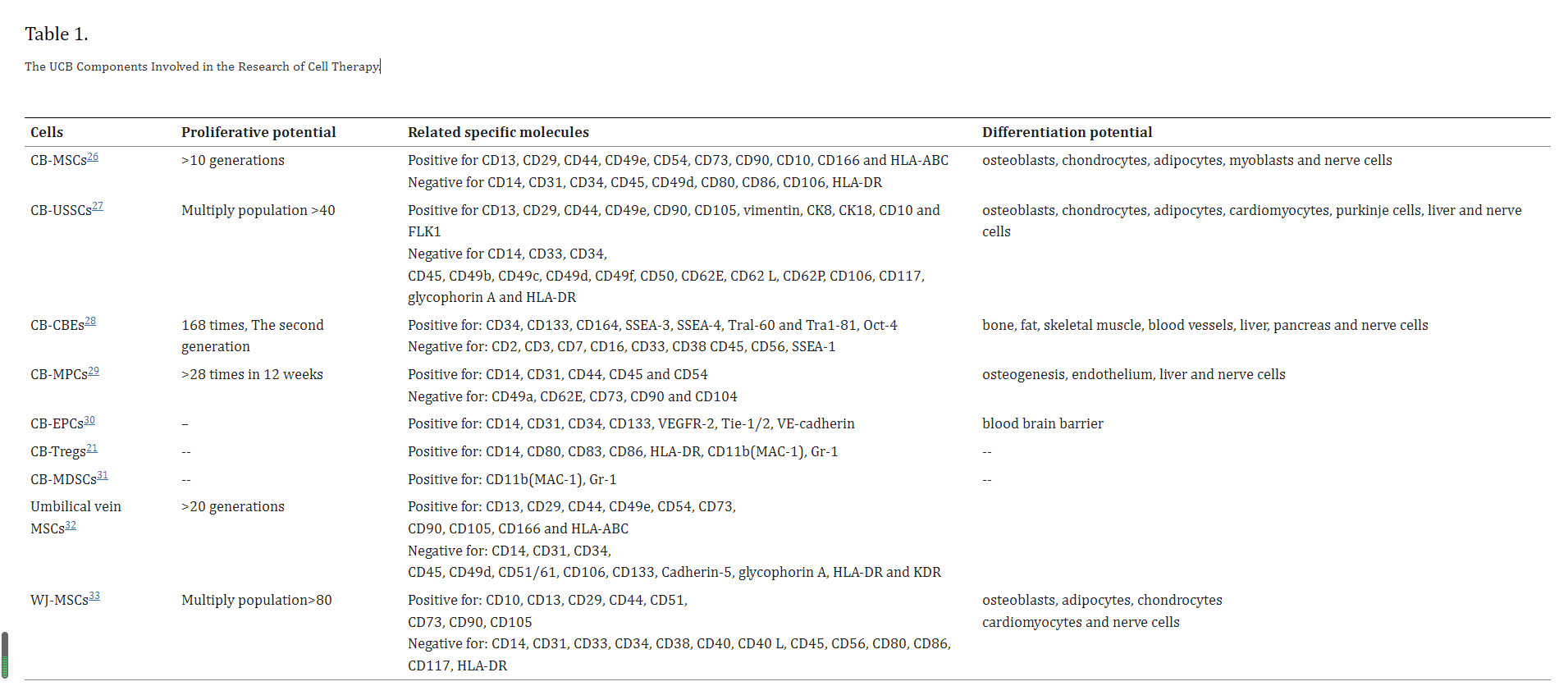
CB-MSCs:臍帶血間充質干細胞;CB-USSCs:臍帶血來源的非限制性成體干細胞;CB-CBEs:臍帶來源的胚胎樣干細胞;CB-MPCs:臍帶血來源的多能祖細胞;CB-EPCs:臍帶血來源的內皮祖細胞;CB-Tregs:臍帶血來源的T調節細胞;CB-MDSCs:臍靜脈間充質干細胞;WJ-MSCs:沃頓氏膠質間充質干細胞;SSEA:階段特異性胚胎抗原;HLA:人類白細胞抗原;VEGF:血管內皮生長因子;MAC-1:巨噬細胞-1抗原。
處理機制可歸納如下:
歸巢促進神經再生:干細胞的歸巢作用是活化的干細胞注入靶腦組織后,沿濃度梯度定向遷移,并發揮再生功能的全過程。
營養因子的分泌:普遍認為,歸巢后,干細胞以旁分泌方式分泌神經營養因子、細胞因子、免疫調節因子和血管生成因子;這些被認為是最重要的治療機制。
免疫調節和神經保護:UCB單核/全血細胞在圍產期缺血缺氧腦模型中可以降低炎癥反應以治療損傷。
必須指出的是,這三種作用機制在細胞治療過程中是密不可分的。歸巢細胞在受傷部位定居并參與神經元、神經膠質細胞、軸突和組織周圍血管的形成。
- 歸巢細胞以旁分泌方式釋放神經營養因子,促進神經元和血管再生,釋放炎癥和抗炎因子保護生長環境。早期炎癥是有益的,Treg調節對于再生至關重要。大多數非歸巢細胞還釋放大量可溶性分子或以EV細胞的形式傳遞血管生成因子、細胞因子甚至miRNA以促進再生。更多的組織再生放大了對修復損傷的影響(圖1)。為了詳細說明每個細胞或因子在UCB中的作用并找到合適的補充治療方案,我們分別描述這三種機制。
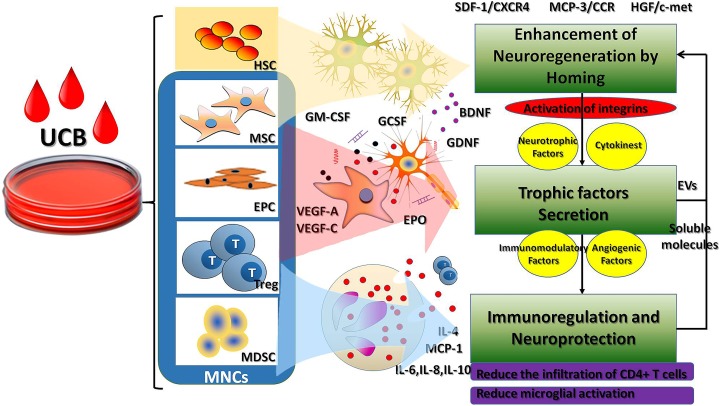
從采集的臍帶血中分離出五種常見成分(HSPs、MSCs、EPCs、Tregs、MDSCs),分別通過歸巢和神經再生、營養因子分泌、免疫調節和神經保護等機制實現治療效果。這三種治療機制也是相互關聯的。
結果和展望
臍帶血干細胞移植治療腦癱的臨床試驗
自2018年6月25日以來,共有18項使用臍帶血干細胞治療腦癱的臨床試驗已在clinicaltrials.gov注冊(表2)( NCT01486732和NCT03203941中未上傳的注冊數據),包括10項已完成的研究(不包括HIE)。然而,當麥克唐納等人。發表了他們的評論(2017年9月),CP的臨床試驗只有11項(僅完成了4項)。現在正在設計和完成更多的臨床試驗,表明UCB是CP的有效選擇。
表2:使用臍帶血治療腦癱的臨床試驗。從ClinicalTrials.gov獲得的信息。
| NCT Number | Title | Status | Interventions | Study type | Outcome measure | Population | Research purposes |
|---|---|---|---|---|---|---|---|
| 01639404 | Umbilical Cord Blood Therapy for Children With Cerebral Palsy | Complete | UCB+ Rehabilitation | Single Group; Open Label | Motor Performance; Standardized Gross Motor Function; Cognitive; Visual Perception Test; | Enrollment:17 (6M-12Y) | Neuroregeneration; Trophic secretion; |
| 01528436 | Umbilical Cord Blood Therapy for Cerebral Palsy | Complete | UCB+ Rehabilitation | Randomized; Parallel; Quadruple | Gross Motor Function; Cognitive; Visual Perception Test; Muscle Strength; Brain Glucose Metabolism; | Enrollment:37 (6M-20Y) | Neuroregeneration; Trophic secretion; |
| 01193660 | Allogenic Umbilical Cord Blood and Erythropoietin Combination Therapy for Cerebral Palsy | Complete | UCB+EPO+R/UCB/EPO | Randomized; Parallel; Quadruple | Gross Motor Function; Cognitive; MRI; Brain Glucose Metabolism; 18F-FDG; Muscle Strength | Enrollment:105 (10M-10Y) | Neuroregeneration; Trophic secretion; |
| 02599207 | Assessment of the Safety of Allogeneic Umbilical Cord Blood Infusions in Children With Cerebral Palsy | Active, not recruiting | Sibling UCB | Non-Randomized; Open Label | adverse events; gross motor function | Enrollment:15 (1Y-6Y) | Neuroregeneration; Trophic secretion; Neuroprotection |
| 02025972 | Allogeneic Umbilical Cord Blood Therapy in Children With CP | Complete | Allogeneic UCB | Single Group Assignment; Open Label; | Cytokine analysis; Gross Motor Function; Cognitive; | Enrollment:10 (up to 15Y) | Neuroregeneration; Trophic secretion; Neuroprotection |
| 01072370 | Safety and Effectiveness of Cord Blood Stem Cell Infusion for the Treatment of Cerebral Palsy in Children | Recruiting | Autologous UCB | Randomized; Crossover Assignment; Blind | Safety, follow-up over one year with clinical and laboratory evaluations; efficacy, Gross Motor Function | Enrollment:40 (1Y-12Y) | Neuroregeneration; Trophic secretion; |
| 01988584 | Safety and Effectiveness of Banked Cord Blood or Bone Morrow Stem Cells in Children With Cerebral Palsy (CP) | Complete | Autologous SC/ Saline | Randomized; Crossover Assignment; Triple | Safety Late functional outcome | Enrollment:20 (2Y-10Y) | Neuroregeneration; Trophic secretion; Neuroprotection |
| 03473301 | A Study of UCB and MSCs in Children With CP: ACCeNT-CP | Not yet recruiting | Allogeneic UCB; MSC | Randomized; Parallel; Single | GMFM-66 score Adverse Event | Enrollment:90 (24M-60 M) | Neuroregeneration; Trophic secretion; |
| 01147653 | A Randomized Study of Autologous Umbilical Cord Blood Reinfusion in Children With Cerebral Palsy | Complete | Autologous UCB; Placebo | Randomized; Crossover Assignment; Quadruple | (GMFM-66) Score; Peabody Gross Motor Quotient; CP-QOL Score; MRI; | Enrollment:63 (12M-6Y) | Neuroregeneration; Trophic secretion; |
| 02866331 | GCSF and Autologous Cord Blood Infusion in Cerebral Palsy | Recruiting | GCSF; CB; Placebo | Randomized; Parallel; Quadruple; | Safety; efficacy; | Enrollment:88 (2Y-10Y) | Neuroregeneration; Trophic secretion; Neuroprotection |
| 03130816 | Mechanism of Allogeneic UCB Therapy in Cerebral Palsy | Recruiting | Allogeneic CB | Single; Open Label | GMFM; mRNA assay; GMPM | Enrollment:90 (10M-20Y) | Neuroregeneration; Trophic secretion; Neuroprotection |
| 03087110 | Stem Cells in Umbilical Blood Infusion for CP | Active, not recruiting | sibling donor CB | Single; Open Label; | gross motor function; cognitive; | Enrollment:12 (1Y-16Y) | Neuroregeneration; Trophic secretion; |
| 01991145 | Allogeneic UCB Therapy With EPO in Children With CP | Complete | UCB+R/EPO | Randomized; Parallel; Quadruple; | Gross Motor Function; Cognitive; | Enrollment:92 (10M-6Y) | Neuroregeneration; Trophic secretion; |
| 02236065 | Combination Therapy of Cord Blood and GCSF for Patients With Brain Injury or Neurodegenerative Disorders | Complete | UCB+ GCSF | Single; Open Label; | Berg Balance Scale; Gross Motor Function; ALSFRS-R; UPDRS | Enrollment:10 (19Y-75Y) | Neuroregeneration; Trophic secretion; |
| 01506258 | Autologous Stem Cells in Newborns With Oxygen Deprivation | Unknown status | SC+ Observation | Non-Randomized; Parallel; Open Label; Prevention | Effects; | Enrollment:20 (37W-42 W) | Neuroregeneration; Trophic secretion; |
| 01929434 | Efficacy of Stem Cell Transplantation Compared to Rehabilitation Treatment of Patients With Cerebral Paralysis | Complete | SC+ rehabilitation | Randomized; Parallel; Single | Gross Motor Function; Routine Blood Test | Enrollment:300 (1Y-14Y) | Neuroregeneration; Trophic secretion; |
| 01147653 | A Randomized Study of autologous Umbilical Cord Blood Reinfusion in children with cerebral palsy | Complete | Autologous UCBs | Randomized, Double-blind; Crossover Assignment | Improvement of standardized measures of neurodevelopmental function at 2 years | Enrollment:63 (12M-6Y) | Neuroregeneration; Trophic secretion; |
治療效果和不良反應
在Rizk等人的文章中,12項UCB治療研究是針對CP患者的。九項研究的結果被認為可能有效(患者 201/276),其中四項研究設有對照組。67例患者出現不良反應:發熱(20/67)、惡心嘔吐(13/67)、皮疹(4/67)、癲癇發作(3/67)等(4/67)。關于細胞類型,31項研究是單核細胞,20項研究是間充質干細胞,11項研究是自體細胞。
NCT01193660,隨機平行分配,招募了105名10個月至10歲的參與者,為期6個月的觀察期。大約31/35CP 患者加入了細胞治療組(有核UCB細胞總數>3×107/kg靜注促紅細胞生成素,每周2次,連續4周,劑量為 500 IU/kg2次靜注,250IU/kg6次皮下注射,積極康復)。33/36和32/34患者被分為促紅細胞生成素和康復組和單純康復組。該研究表明,干細胞療法改善了兒童在大多數結果指標中的功能(運動表現、粗大運動功能、認知神經發育結果、運動神經發育結果;通過腦18F-FDGPET比較腦葡萄糖代謝的變化、日常活動中的功能獨立性、肌肉力量和手部功能)。這些在嚴重不良事件(肺炎、癲癇發作、流感、尿路感染、死亡)發生率方面沒有差異(UCB與促紅細胞生成素和康復組為3/35。
NCT01147653是一項針對1-6歲CP兒童的單次靜脈輸注1-5×107個總有核細胞/公斤自體臍帶血 (ACB)的雙盲、安慰劑對照、交叉研究,在ACB治療后1年的分析中,接受劑量≥2×107/kg的患者證明,適當劑量的 ACB輸注可改善大腦連接和粗大運動功能(粗大運動功能測量66 (GMFM-66) 分數顯著增加。值得注意的是,試驗中出現胃腸道疾病的人數(2/63,3.17%)遠少于試驗中的NCT01193660(27/35,77.14%),但呼吸道相關感染患兒數(9/63,14.28%)遠高于對照組(2/63,3.17%)。
總的來說,這些結果得出了幾個結論。UCB是CP臨床試驗中使用最多的細胞類型之一,具有可靠的安全性和有效性。大約72.8%的CP患者受益于UCB相關細胞療法。
在一項臨床前動物研究中,在初始損傷的前24小時后,UCB單核細胞療法作為早期干預在HIE模型中顯示出更大的益處。早期UCB干預主要發揮免疫調節和神經保護作用。目前自體臍帶血干細胞的療效和安全性均優于異體臍帶血干細胞。不同的藥物和細胞類型在臨床研究中顯示出有益效果,但組合策略可能是神經再生的未來。
潛在的細胞來源和劑量
在目前的18項試驗中,有六種使用不同來源(UCB+康復;UCB+EPO;自體UCB;同種異體(同胞或其他)UCB;GCSF)和三種不同劑量(超過10M/kg 體重;超過30M/kg 體重;未提及)。一般認為10M/kg體重是靜脈給藥的安全劑量。自體臍帶血細胞 (UCBC) 靜脈內給藥療法可能是最安全和最可行的,因為UCB已用于造血干細胞移植數十年。用于CP研究和試驗的同種異體細胞很容易獲得,主要來自私人和公共銀行的UCB單位,并且非侵入性損傷的治療很容易被接受。
最佳給藥途徑
目前報告的給藥途徑是腦室內、鞘內、鼻內、肌肉內、動脈內或靜脈內。腦室內和鞘內注射在理論上很簡單,但具有侵入性,其中的風險對兒童來說是不可接受的。常見的并發癥有惡心嘔吐等腦膜刺激征、腦室內出血、蛛網膜下腔出血等。
靜脈內途徑是最常用的非侵入性方案。示蹤劑方法表明,通過系統循環的大量細胞在肺部定植。靜脈和動脈給藥最嚴重的不良反應是肺栓塞,與給藥過快或劑量過大有關。全身通路有可能調節炎癥反應,但很大一部分仍存在于其他器官中,并且許多不能穿過血腦屏障。Jantzie等人考慮到局部給藥可能更可行,甚至在大腦內的注射位置也可能很重要。
結論
我們回顧了在臍帶干細胞治療腦癱中都有哪些干細胞類型及干細胞治療腦癱的作用機制。臍帶血干細胞有益于臨床應用,其潛在機制已得到研究,并且在臨床前設置和臨床試驗中均取得了有意義的進展。然而,將干細胞付諸實踐還存在幾個緊迫的問題:(1)尋找低成本、高純度的干細胞來源;(2) 選擇療效和安全性最佳的干細胞類型;(3)對干細胞治療機制的深入研究;(4) 確定給藥途徑和劑量;(五)統一有效的評價標準和后續工作。
結語
這些研究都證明了臍帶血干細胞在治療腦癱的潛力,隨著再生醫學的發展,干細胞移植被認為是未來治療腦癱的最優之選。隨著醫學技術的不斷進步,尤其是干細胞的發展,腦癱患兒終將會迎來春天。
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加微信
掃碼添加微信