近日,CBA球星郭艾倫在社交平臺更新了遠赴西班牙接受干細胞治療的最新動態,他透露已經為自己的腿部注射了干細胞,期待其能帶來積極效果。
此舉不僅引發了公眾對郭艾倫傷勢的關心,更使得“干細胞”這一關鍵詞迅速登上熱搜榜,激起了廣大網友的熱烈討論,即干細胞療法的效用、為何需要出國接受治療,以及干細胞治療是否僅限于富人群體等問題,紛紛成為討論的焦點。
何為干細胞療法?
干細胞,被譽為“萬用細胞”,具有自我更新和多向分化的潛能,在治療退行性疾病、自身免疫性疾病和遺傳性疾病方面展現出了巨大的潛力。從1968年造血干細胞首次應用于骨髓移植手術,到如今干細胞療法在心臟修復、肝臟修復、骨骼再生等領域廣泛應用,干細胞醫療技術的發展可謂日新月異。
- 1968 年,造血干細胞被應用于第一例骨髓移植手術開始,干細胞醫療技術應用便開始快速發展,
- 1999年,干細胞療法因其光明治療前景被 Science 列為當年十大科學成就之首,
- 2001年前后,美國等發達國家先后立法允許應用干細胞進行治療性克隆研究,引發了世界各國對干細胞產品的研發熱潮。
- 2006年,日本京都大學教授山中伸彌首次通過基因技術得到了誘導性多能干細胞(iPSC),不僅有望避開倫理問題,還因此獲得了諾貝爾獎。
干細胞療法發展至今,隨著基因編輯技術的突破,干細胞療法的精確性和效率得到了顯著提升,已逐步成為生物醫學領域的一大熱點,無數科學家爭先恐后扎堆其中。
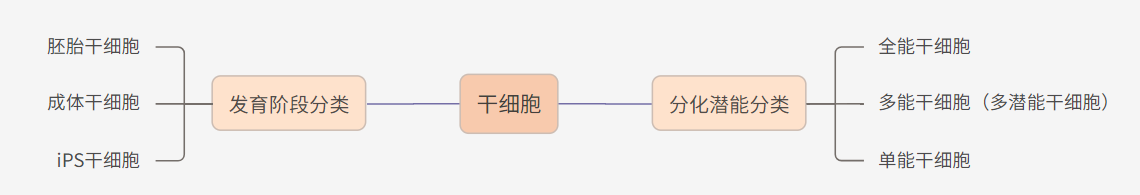
目前,根據發育階段來源可將干細胞分為胚胎干細胞、成體干細胞以及iPS干細胞三類,而根據分化潛能的大小,干細胞療法又可將其分為全能干細胞療法、多能干細胞療法(多潛能干細胞)和單能干細胞療法三類(上圖)。
全能干細胞
全能干細胞是指具備發育成完整個體的潛能或特性的一類細胞,目前主要應用于動物克隆和轉基因動物實驗等方面的研究,即通過對全能干細胞進行轉基因或基因編輯,可改良動物品種和生產藥物等。
目前在所有干細胞療法中,成品干細胞治療產品全球領域已有上市,但全能干細胞目前尚無任何一款新藥上市,且在臨床研究方面,全能干細胞療法也所有干細胞療法中數量最少的存在。
多能干細胞
由于多能干細胞與多潛能干細胞兩者均具有多向分化潛能,所以很多文獻與數據庫都將其放在一起討論,但其實兩者還是有較為明顯的區別。
多能干細胞方面,其主要包括間充質干細胞和造血干細胞,其是骨髓基質中具有較高分化潛能的存在,骨髓間充質干細胞、臍帶間充質干細胞、脂肪間充質干細胞療法是目前該領域最主流的研究方向之一。且由于間充質干細胞異體移植時發生免疫排斥的風險小,理論上也是干細胞治療的理想材料。
多潛能干細胞方面,由于其獲取上較大的倫理爭議,快速發展源于人工誘導方式出現,誘導性多能干細胞(iPSC)經體細胞重編程逆轉而來,具有多向分化潛能,對于干細胞的研究意義重大, 既避免了從胚胎中獲取多潛能干細胞的倫理問題。
單能干細胞
單能干細胞分化潛能較低,只能分化為一種細胞或是功能上密切相關、共同完成某一生理過程的幾種細胞。目前,研究較為深入的單能干細胞主要有神經干細胞和小腸干細胞。并且,單能干細胞相關新藥研究還是是干細胞療法中最主要的存在,占比超過了一半以上,而神經干細胞療法與小腸干細胞療法也是目前發展最為迅速的領域。
干細胞治療是否真的有用?
干細胞治療作為一種創新的醫療手段,在近年來顯示出了對多種疾病的治療潛力。例如,在心臟病治療中,干細胞可以被用來修復受損的心肌組織;在糖尿病治療中,可以利用干細胞生成胰島細胞以產生胰島素;在神經退行性疾病中,可以利用干細胞有恢復或替換受損的神經細胞。
隨著基因編輯技術,尤其是CRISPR-Cas9系統的興起,干細胞療法的精確性和效率得到了顯著提高。這項創新技術允許科學家們在分子層面上精確修改干細胞的遺傳信息,從而增強其治療效果。基因編輯不僅提升了干細胞的靶向治療能力,也為避免免疫排斥和提高細胞存活率提供了可能。
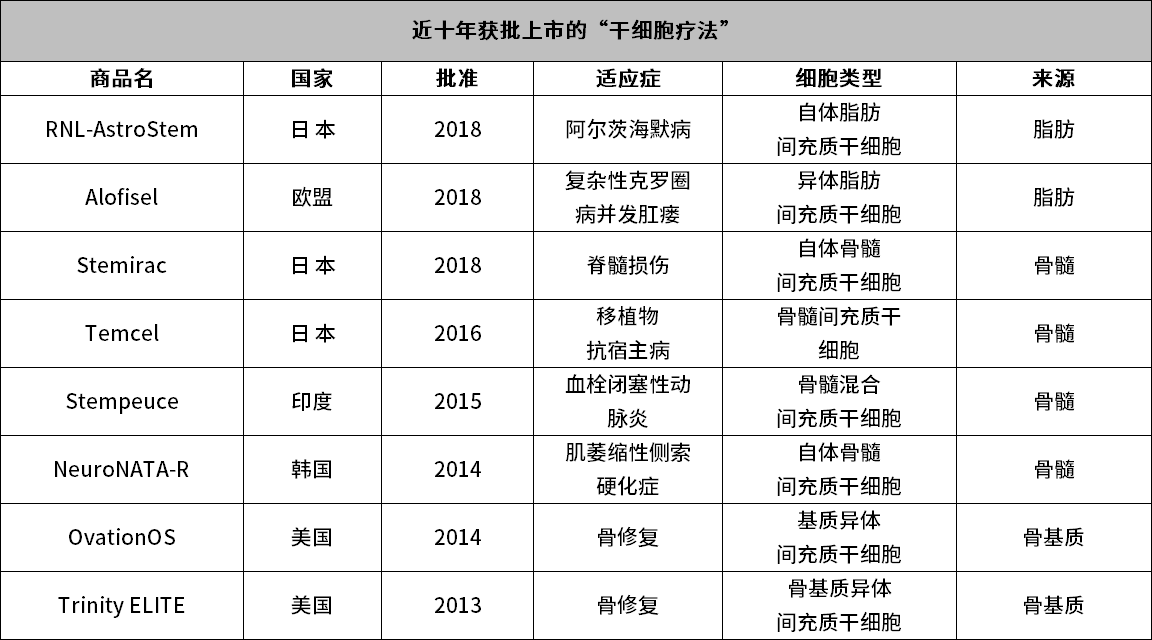
具體在藥物成果方面,據藥智數據不完全統計,全球已有18款干細胞療法獲批上市。而研究領域藥品數量則比之前更多,截至目前,全球注冊登記的干細胞臨床項目多達4000余項,涉及藥品管線近400余款。而其中,我國已有60余項間充質干細胞藥物臨床試驗,包括糖尿病足潰瘍、骨關節炎、類風濕關節炎、肺纖維化、克羅恩病等多種疾病。
為何遠赴西班牙治療?
雖說干細胞治療作為現階段前沿醫療重點手段之一,其差距相對其他領域反而更低,甚至部分機構表示中國干細胞技術已經國際領先,但其實就目前的干細胞治療領域的整體發展狀況來看,海內外差距仍然不小,這也是導致郭艾倫最終選擇遠赴西班牙進行干細胞治療的原因之一。
據有關數據顯示,目前全球在研項目主要集中于歐美地區,其中以美國、歐洲和日本的市場化應用最廣泛,已知391項干細胞新藥項目中,有105個項目屬于美國,中國項目僅次于美國,達58個,其次是韓國、英國、德國等一眾歐美國家。

另外,全球干細胞療法研究的主要玩家也多來源于海外,Mesoblast(MESO)、Osiris(OSIR)、Anterogen、Pharmicell等新銳企業也常年潛心于干細胞療法,并為干細胞療法產業做出了突出的貢獻,而中國尚無任何一款干細胞療法上市,多數已知臨床項目也多處早期。
而除了上述干細胞療法領域的研發實力差距外,國內外政策監管的不同,也是導致郭艾倫等患者遠赴海外治療的原因之一。
- 2007 年,我國將干細胞療法作為“醫療手段”而非 “藥物”來監管,造成了市場上干細胞產業混亂的局面,《自然》雜志先后三次對此亂象做出不利評論;
- 2011年,我國開始大肆對干細胞治療領域進行整頓,對2011年之前的干細胞臨床研究與治療領域頒布禁令,暫停了所有干細胞的臨床試驗與申請,我國干細胞產業進入了停滯期;
- 2015年,首個針對干細胞臨床研究管理的規范性文件《干細胞臨床研究管理辦法》發布,我國干細胞行業逐步開始走向規范化的道路。
- 2021年,國家藥品監督管理局批準進行臨床研究的干細胞制劑達16個,“雙軌制”監管之下,行業飛速發展。
而在此期間,美國干細胞療法的相關法規建立就相對順暢許多,2005年先后通過《干細胞研究促進法 案2005》《干細胞研究促進法案2007》,對干細胞研究的限制開始放松;2009年關于干細胞的總統行政令發布,宣告大力發展干細胞領域;之后幾年間,關于干細胞領域的19項法律法規進一步完善,美國也因此成為全球干細胞發展最快的地區。
國內干細胞“爆發”在即
近年來,我國干細胞臨床研究逐步進入規范化發展階段,取得了較大的進步與發展。干細胞備案項目和干細胞IND注冊受理項目數量成倍增長,通過新藥注冊申報途徑研發的干細胞臨床管線持續增加。
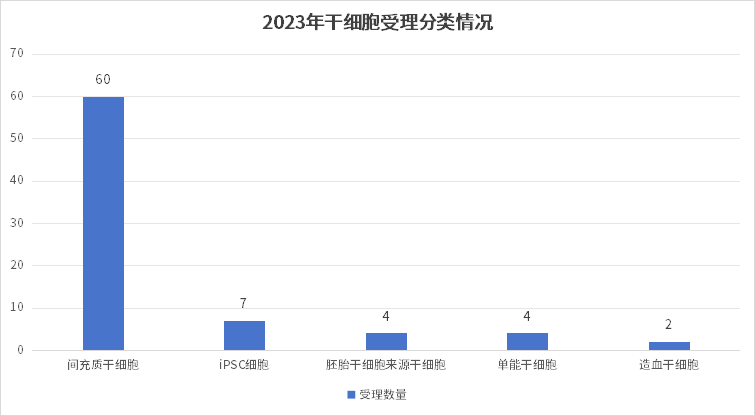
截至2023年12月,國內共有106項干細胞藥物臨床試驗申請獲得受理,其中2023年申報獲受理數量達到47個,較2022年度增長了近一倍,我國干細胞新藥研發速度明顯加快。
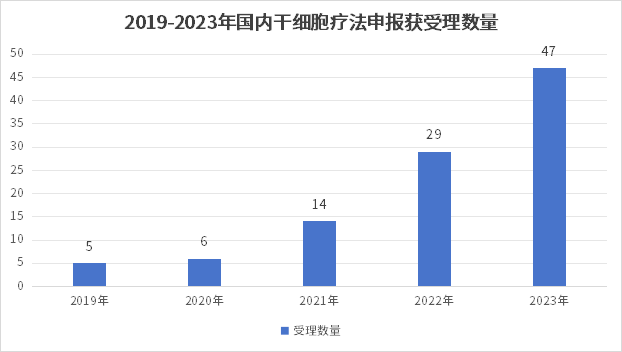
其中,從申報細胞類型來看,間充質干細胞藥物合計60款,占比75.9%,是目前我國干細胞藥物研發最主攻的細胞類型。誘導多能干細胞(iPsc)的功能細胞藥物也呈逐步增長趨勢,2023年里,共新增了4項iPSC分化的功能細胞藥物。
小 結
毫無疑問,對于現階段的干細胞療法而言,無論是全球還是國內領域,各階段的臨床管線數量都在呈現明顯的“井噴”趨勢,尤其是近2-3年間,這或許源于細胞領域的基礎研究水平上漲(畢竟隔壁CAR-T也是發展得風生水起)。
另外,干細胞技術細節方面,iPSC技術的出現對于干細胞研究實屬里程碑式的成果,但就現階段的干細胞治療的臨床研究而言,仍處于較為初級的階段,許多問題仍亟待解決。
而對于國內干細胞產業而言,在國家頂層設計持續加強、戰略層面宏觀統籌下,現階段也基本從探索階段轉向了有序發展階段,未來有望真正誕生登頂全球研發榜首的企業,我們拭目以待。
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請及時跟本公眾號聯系,我們將在第一時間處理。



 掃碼添加微信
掃碼添加微信