源自骨髓和臍帶血的單核細胞 (MNC) 因其獨特的生物學特性和多樣化的治療潛力,已成為再生醫學的熱門候選對象。
骨髓/臍帶血單個核細胞的:組成、作用機制、臨床應用、細胞劑量、給藥時機及途徑
首先,本章全面概述了這些MNC細胞群中的細胞成分,包括干細胞和祖細胞、免疫細胞以及構成其再生能力的各種亞群。
其次,本章還回顧了這些細胞發揮作用的潛在機制,重點闡述了它們在調節炎癥和免疫反應、增強血管生成、提供神經保護和促進神經發生以及促進組織修復方面的作用。
第三,本章重點介紹了骨髓和臍帶血來源的MNC的臨床應用,詳細介紹了適應癥、最佳細胞劑量、給藥時機、給藥途徑、潛在副作用和并發癥,以及其在治療神經系統、心血管、代謝和肺部疾病方面的療效。
第四,本章討論了利用這些細胞進行臨床應用的挑戰和未來方向,強調需要標準化協議和進一步研究以優化其在臨床環境中的功效和安全性。

1、骨髓來源的單個核細胞
細胞組成、分離方法
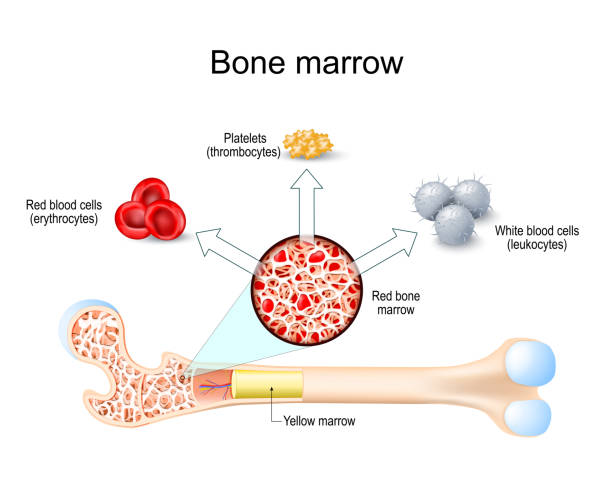
骨髓 (BM) 在十九世紀被認為是參與血細胞形成的重要組織,現在也是我們血液的主要來源。骨髓單核細胞 (BMMNC) 是一個異質性細胞群,包括造血干細胞 (HSC)、間充質干細胞/基質細胞 (MSC)、內皮祖細胞 (EPC)、極小的胚胎樣細胞以及免疫細胞,例如單核細胞、T細胞、B細胞和自然殺傷細胞。這些細胞類型的比例因個體及其健康狀況而異。由于BMMNC無需大量培養即可相對容易處理,因此已成為再生醫學中細胞療法的一種有吸引力的工具。
可通過密度梯度離心法分離骨髓多發性骨髓細胞(BMMNC),所用骨髓穿刺液通常取自髂后嵴和髂前嵴。穿刺骨髓的量取決于血液動力學,隨疾病狀態和供體的體重而變化,范圍從25毫升到200毫升。每毫升BMMNC的數量取決于性別,女性通常低于男性。據報道,BMMNC的數量和功能也會隨著年齡的增長而降低。在制備BMMNC以達到所需的細胞濃度和療效時,必須考慮所有這些因素。
骨髓單個核細胞(BMMNCs)的作用機制
BMMNCs的治療效應被認為通過多種機制協同介導,具體作用因細胞類型(尤其是其中的干細胞成分)而異。Nguyen等人的綜述指出,BMMNCs的主要機制包括血管生成、神經保護、免疫調節、歸巢與分化、線粒體轉移及細胞外囊泡介導的效應。
血管生成:BMMNCs通過上調血管內皮生長因子(VEGF)促進血管新生,并招募周細胞參與新血管形成。此外,BMMNCs分泌血管生成素-1(Angiopoietin-1)以穩定血管結構,并通過內皮祖細胞(EPCs)替換受損內皮細胞。
神經保護:BMMNCs釋放神經營養因子(如BDNF、NGF、NT-3等),促進神經再生;其上調抗凋亡因子Bcl-2可抑制caspase-3激活,減少神經元死亡。
免疫調節:BMMNCs降低促炎因子(IL-6、TNF-α、IL-1β)表達,增加抗炎因子(IL-4、IL-10),并抑制小膠質細胞/巨噬細胞活化。
歸巢與分化爭議:盡管實驗顯示BMMNCs可遷移至海馬、大腦皮層等靶區,但其分化能力仍存爭議。部分研究認為其可分化為神經膠質細胞或星形膠質細胞,但另一些研究指出其“轉分化”可能源于細胞融合(如與神經元或心肌細胞融合)而非內在分化潛能,或與神經前體細胞污染有關。
線粒體轉移:BMMNCs中的間充質干細胞(MSCs)及EPCs可通過轉移線粒體至內皮細胞,支持其能量代謝與屏障功能。脊髓損傷模型中,MSCs線粒體轉移可改善運動功能并減少膠質瘢痕。
細胞外囊泡(EVs):BMMNCs(尤其是MSCs)分泌的EVs具有免疫調節和抗炎特性,可促進組織修復、神經保護及血管生成。
骨髓單個核細胞(BMMNCs)在疾病治療中的臨床應用
BMMNCs的適應癥
BMMNCs已被研究用于多種疾病的治療,包括血液系統疾病、心血管疾病、骨科與肌肉骨骼疾病及神經系統疾病等。盡管臨床前研究和早期臨床試驗顯示其應用潛力,但具體適應癥仍需進一步探索。將研究成果轉化為廣泛臨床應用需通過嚴格的臨床試驗驗證安全性和有效性。此外,遺傳因素、疾病病因及分期等因素可能影響BMMNCs治療的療效,因此需謹慎評估適應癥選擇。
細胞劑量、給藥時機及途徑
BMMNCs的劑量因疾病類型和治療目標而異:
- ??神經系統疾病??:
- ??卒中??:10–500×10^6個細胞或1–10×10^6個細胞/千克體重
- ??腦性癱瘓(CP)??:15–120×10^6個細胞或1×10^6個細胞/千克體重
- ??脊髓損傷(SCI)??:10^6–1000×10^6個細胞
- ??創傷性腦損傷(TBI)??:平均128×10^6個細胞或6–12×10^6個細胞/千克體重
- ??肌萎縮側索硬化癥(ALS)??:80–460×10^6個細胞
- ??自閉癥譜系障礙(ASD)??:56–145×10^6個細胞或18–42×10^6個細胞/千克體重。
- ??心血管疾病??:
- ??急性心肌梗死??:早期(<11天)注射高劑量(≥10^8個細胞)可顯著降低住院風險;低劑量(<10^8個細胞)或晚期(≥11天)注射則無顯著差異。
- ??缺血性心臟病??:建議最低劑量為50×10^6個細胞。
??給藥時機??:目前自體BMMNCs的最佳治療時間窗尚未明確,需更多研究支持。
??給藥途徑??:給藥途徑因疾病而異。神經系統疾病的治療途徑包括靜脈注射、動脈注射、鞘內注射和局部注射。然而,鞘內注射途徑可能最適合神經系統疾病,因為它創傷性最小,且能最大程度地將輸注的細胞送達受損部位。
心血管疾病的治療主要采用四種途徑,包括冠狀動脈內注射、經心內膜注射、心外膜注射和靜脈注射。雖然每種方法都有其優缺點,但目前尚無足夠證據證明哪種方法更好。
副作用與并發癥
BMMNC療法在疾病治療中展現出良好的安全性,副作用極小,不良事件極少,并發癥也極少。由于BMMNC療法無需培養,分離后即可“即用”,因此可以避免長期細胞培養可能帶來的病毒和支原體污染。與其他細胞療法不同,BMMNC療法尚未報告細胞注射后出現血栓栓塞等重大不良事件。
雖然部分接受BMMNC輸注的患者可能會出現發熱、局部疼痛、頭痛、嘔吐、腹瀉或癲癇等輕微副作用,但這些癥狀通常會迅速緩解,不會影響患者的整體健康。
骨髓單個核細胞治療疾病的有效性如何?
骨髓單個核細胞治療神經系統疾病的有效性
BMMNCs已被證明在治療神經系統疾病(包括中風、腦癱、脊髓損傷、創傷性腦損傷、肌萎縮側索硬化和自閉癥譜系障礙)方面具有潛在療效。

中風方面:BMMNCs輸注可降低中風患者的美國國立衛生研究院卒中量表(NIHSS)和改良Rankin量表(mRS)評分,提高 Barthel指數(BI)評分;
腦癱方面:改善腦癱患者的功能獨立性測量(FIM)、巴特爾發育量表(BDI)、粗大運動功能測量(GMFM)和精細運動功能測量(FMFM)評分。
脊髓損傷方面:BMMNCs輸注可改善脊髓損傷患者的FIM、脊髓損傷步行指數(WISCI)、簡明損傷量表(AIS)、美國脊髓損傷協會(ASIA)評分、日常生活活動能力(ADL)和視覺模擬評分(VAS);
腦損傷方面:降低創傷性腦損傷患者的兒科治療強度水平(PILOT)、兒科器官功能障礙 logistic 評分(PELOD)并改善 FIM 評分。
肌萎縮側索硬化癥方面:BMMNCs治療可改善肌萎縮側索硬化患者的 ALS 功能評分量表(ALSFRS)和 6 分鐘步行測試表現,并降低 FIM 評分。
自閉癥方面:接受BMMNCs注射的自閉癥譜系障礙患者顯示正電子發射斷層掃描 – 計算機斷層掃描(PET-CT)、兒童自閉癥評定量表(CARS)、印度自閉癥評估量表(ISAA)、臨床總體印象量表(CGI)和兒童功能獨立性測量(WeeFIM)改善。
骨髓單個核細胞治療心臟病的有效性
BMMNCs是首批被納入心臟病治療的干細胞。
2002年,首次開展了使用BMMNCs治療急性心肌梗死的臨床試驗。對48項符合條件的隨機對照試驗(RCTs)(2602 例患者)數據的系統評價和薈萃分析顯示,骨髓細胞移植可縮小缺血性心臟病患者的梗死面積,改善左心室射血功能,并減輕心室重構。
2022年對RCTs的薈萃分析表明,BMMNCs可能降低心臟相關死亡率、再梗死率以及充血性心臟病住院的復合終點風險。盡管存在不確定性,但間充質干細胞(MSCs)在改善射血分數方面似乎優于BMMNCs。然而,Dolati等人指出,BMMNCs 治療在心血管疾病中的效果存在差異,需要更多試驗以得出準確結論。
2019年,薈萃分析顯示,自體BMMNCs對2型糖尿病具有有益作用。接受BMMNCs注射的患者顯示二期C肽水平改善,胰島素劑量需求顯著減少。
2020年,Aguia及其同事首次證明,對重癥哮喘患者靜脈注射BMMNCs是安全的。BMMNCs 治療不僅使三名患者中的一名右肺通氣量略有增加,還改善了所有三名患者的生活質量并穩定了肺功能。
2、臍帶血來源的單個核細胞
臍帶血來源的單個核細胞的細胞組成
自1988年進行首例臍帶血 (CB) 移植以來,CB造血移植的數量逐年增加。無論是陰道分娩還是剖宮產,都可以大量采集臍血 (UCB),足月嬰兒每次平均采集量為81ml,有核細胞計數范圍為3.89至15.68×108個細胞。即使在高危嬰兒中也可以采集UCB,包括胎齡低于30周的嬰兒,對于極度早產兒,至少可以采集9mlUCB。
此外,UCB細胞易于冷凍保存并儲存以備將來使用。這些細胞表現出免疫耐受性和對人類白細胞抗原 (HLA) 錯配的反應性較低,因此可以以同種異體的方式利用它們。
臍血來源的單核細胞 (UCB-MNC) 可通過梯度離心法輕松地從臍血中分離,并用于臨床常規治療,無需進一步的體外操作。UCB-MNC含有幾種細胞類型,包括造血干細胞 (HSC)、內皮祖細胞 (EPC)、淋巴細胞、單核細胞和間充質干細胞 (MSC)。但細胞類型的數量和比例因胎齡和分娩環境而異。造血干細胞在臍血中很常見。
與來自骨髓和外周血的造血干細胞相比,臍血來源的造血干細胞成熟度較低,但在細胞因子的作用下表現出強大的增殖能力。與成人骨髓單核細胞 (BMMNC) 相比,UCB-MNC具有更高的細胞活力,對細胞毒性T細胞和輔助性T細胞的反應性更低。
臍帶血來源的單個核細胞的潛在作用機制
證據表明,臍帶血單個核細胞(UCB-MNCs)可發揮抗炎和免疫調節作用。UCB-MNCs可通過減少小膠質細胞和星形膠質細胞的活化、增加抗炎細胞因子IL-10來減輕炎癥反應。此外,UCB-MNCs可調節中樞T細胞反應,并改變免疫細胞向神經組織的遷移。
移植的UCB-MNCs通過SDF-1/CXCL12介導歸巢至損傷部位,一旦到達損傷區域,它們可增殖并分化為神經元和神經膠質細胞以替代受損細胞,從而減輕腦損傷并促進神經和血管再生。
此外,UCB-MNCs移植可誘導損傷部位IL-8介導的血管生成。UCB-MNCs還可通過旁分泌效應發揮作用,例如分泌血管內皮生長因子(VEGF)以刺激血管生長和組織生成。在缺氧缺血性腦損傷模型中,UCB-MNCs可通過分泌神經營養因子(如膠質細胞源性神經營養因子(GDNF)、神經生長因子(NGF)、腦源性神經營養因子(BDNF))提供神經保護作用。
多項研究已證實 UCB-MNCs 的抗凋亡效應。給予UCB-MNCs可抑制凋亡基因(如 TNF-α、TNFR1、TNFR2、CD40 和 Fas)的表達,并減少表達凋亡標志物的細胞數量。腹腔注射UCB-MNCs可減少紋狀體中活化的半胱天冬酶-3(caspase-3)介導的細胞死亡,以及大腦皮層中小膠質細胞的活化,從而改善腦損傷。
臍帶血單個核細胞(UCB-MNCs)治療疾病的臨床應用
臍帶血單個核細胞的適應癥
臍帶血單個核細胞(UCB-MNCs)憑借無創獲取、倫理限制少及高可及性,廣泛應用于腦癱(CP)、自閉癥譜系障礙(ASD)、脊髓損傷(SCI)等疾病治療。相較于骨髓來源(BMMNCs),UCB-MNCs在兒科更具優勢,因其分離無痛且可異體使用,降低時間與成本。但異體治療需關注HLA匹配問題——研究顯示,HLA完全匹配或1個位點不匹配的CP患者運動功能改善更顯著,提示匹配度影響療效。此外,長期安全性仍需隨訪驗證。
細胞劑量、治療時機與給藥途徑
目前,UCB-MNCs的最佳細胞劑量和所需劑量次數因疾病或病癥而異,其最佳治療方案尚未完全闡明。
臨床前試驗中應用的UCB-MNCs數量范圍為 2×10?至 100×10?個細胞,臨床應用的最佳劑量尚未確定 [27]。現有證據表明,更高的細胞劑量可能帶來更大益處。
一項隨機對照試驗(RCT)顯示,接受自體UCB-MNCs劑量大于20×10?個細胞 / 千克體重的 CP 患兒,其運動功能改善程度優于低劑量組。臨床前和臨床研究建議,治療早產兒腦損傷時應靜脈注射至少 25×10?個自體UCB-MNCs/千克體重。
然而,對重度CP的年幼兒童(<10歲)單次鞘內注射20–30×10?個異體UCB-MNCs顯示不良事件風險增加。這一發現表明,鞘內輸注和治療起始年齡(≤10歲)可能與不良事件的發生相關。作者推測,對于免疫系統未成熟的年幼兒童(<10 歲),所應用的異體UCB-MNCs劑量可能過大。與此一致的是,接受 UCB-MNCs 治療時年齡 < 36 個月的 CP 患兒似乎比36個月后入組的年長患兒獲益更多。
細胞遞送時機也可能是決定UCB細胞治療有效性的重要因素。在早產兒缺氧缺血動物模型中,早期給藥(12小時)比晚期注射(5 天)更有效。此外,UCB-MNCs的多次給藥可能提高治療效果。Zarrabi等人提出,重復給藥是解決 UCB-MNCs在CP患者中短期效應的途徑。一項臨床前研究顯示,UCB細胞的重復給藥可改善新生大鼠腦損傷的長期恢復。
UCB-MNCs可通過全身途徑(靜脈、動脈、腹腔注射)或局部途徑(鞘內、心內、腦室內、腦內、鼻內)給藥。在圍產期腦損傷的臨床應用中,大多數臨床試驗采用靜脈注射UCB-MNCs。早期階段試驗表明,UCM-MNCs局部給藥途徑(鞘內和腦室內注射)在 CP 患者中的安全性與全身途徑相當,未觀察到安全性劣勢。需進一步研究探討UCB-MNCs局部給藥在各種病癥中的可行性、安全性和有效性。
副作用與并發癥
自體UCB-MNCs的安全性已在多種病癥中得到證實。 腦癱、自閉癥譜系障礙(ASD)、脊髓損傷(SCI)、缺氧缺血性腦病(HIE)和左心發育不良綜合征等疾病患者中,未觀察到與UCB-MNCs輸注相關的不良事件。
盡管人們對異體UCB-MNCs的應用存在擔憂,但初步證據表明這些細胞是安全的。迄今為止,尚無研究報道腫瘤形成或其他惡性病變。對非血液系統退行性疾病患者鞘內和靜脈注射1–3×10?個非匹配異體UCB-MNCs耐受性良好,4年隨訪后未觀察到不良事件、免疫反應或移植物抗宿主病(GVHD)。
2022年,一項對10項研究(361名參與者,至少442次輸注)的系統評價證實了異體UCB-MNCs在治療ASD、CP、中風、創傷性腦損傷(TBI)等神經系統疾病中的安全性,未報告嚴重不良事件或GVHD、畸胎瘤形成等潛在并發癥。
臍帶血單個核細胞治療的有效性
UCB-MNCs治療已被證明對神經系統疾病有效。
腦癱方面:靜脈輸注UCB-MNCs可增加CP患兒的腦連接性和粗大運動功能,改善運動和認知功能障礙(提高粗大運動表現測量(GMPM)和貝利嬰兒發展量表第二版—心理與運動量表評分)。鞘內注射異體UCB-MNCs在CP患者中安全有效(改善粗大運動功能、肌張力和殘疾評分)。
中風方面:UCB細胞輸注可改善中風患者的改良Rankin量表(mRS)和美國國立衛生研究院卒中量表(NIHSS)評分。
自閉癥方面:UCB-MNCs移植可改善ASD患者的兒童自閉癥評定量表(CARS)、臨床總體印象量表(CGI)和異常行為清單(ABC)評分,而UCB-MNCs與臍帶間充質干細胞(UC-MSCs)聯合應用效果更佳。
UCB-MNCs移植顯著改善多系統萎縮患者的癥狀和體征,并延緩疾病進展。全身注射非HLA匹配的異體UCB-MNCs在急性重度挫傷性SCI患者中安全且可改善運動功能。
UCB-MNCs已被用于多種新生兒疾病的治療研究。包括支氣管肺發育不良(BPD)、先天性心臟病(CHD)和圍產期腦損傷。

Ren等人(2020年)開展的單中心 II 期前瞻性非隨機安慰劑對照試驗顯示,對BPD早產兒靜脈注射UCB-MNCs可縮短機械通氣和氧療時間。Burkhat 等人(2019年)的I期研究表明,UCB-MNCs 在左心發育不良綜合征患者中安全可行。
類似地,Vincenti等人的I期試驗顯示,向左心發育不良綜合征嬰兒心肌直接注射1–3×10?個UCB-MNCs可改善體重、右心室面積變化分數和射血分數。UCB-MNCs治療圍產期腦損傷也被證明安全可行。2014年,Cotton等人開展了一項開放標簽 I 期試驗,對一名HIE嬰兒在出生后12、24、48和72小時靜脈輸注1–5×10?個細胞 / 千克體重(四次劑量),該干預安全可行,盡管未觀察到顯著差異,但改善了貝利- III量表評分。
日本一項對HIE新生兒在出生后24、48和72小時靜脈輸注1.4–10.9×10?個UCB-MNCs的研究也獲得了類似結果。
3、對比與總結
| 特征 | BMMNCs | UCB-MNCs |
|---|---|---|
| 來源 | 骨髓(需有創采集) | 臍帶血(無創采集,可凍存) |
| 適用人群 | 成人為主,自體治療 | 兒科為主,可自體或異體(異體成本低、便捷) |
| 倫理爭議 | 較低 | 極低(臍帶血為醫療廢棄物) |
| 主要優勢 | 心血管疾病證據較充分 | 新生兒 / 兒科疾病應用廣泛,免疫原性低 |
| 局限性 | 異體需 HLA 匹配,采集痛苦 | 細胞數量有限,需高劑量輸注 |
4、挑戰與未來方向
基于BMMNC和UCB-MNC的細胞療法因其可及性、安全性和潛在的治療效果,在再生醫學中展現出廣闊的前景(圖1)。盡管具有這些優勢,但仍存在一些挑戰需要解決。自體BMMNC給藥是一種常見方法,但存在一些局限性,可能會限制其在某些情況下的應用。
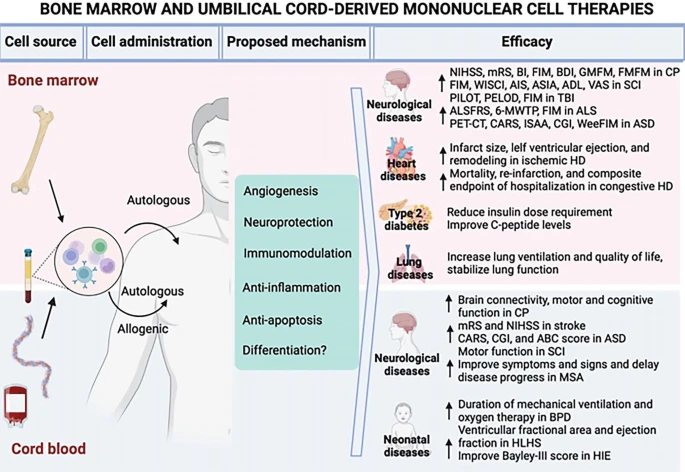
可以從BM和CB中分離單核細胞。通常,BM-MNC為自體給藥,而CB-MNC既可以自體給藥,也可以同種異體給藥。這些細胞通過多種機制發揮作用,包括血管生成、神經保護、免疫調節、抗炎、抗凋亡和分化。BM-MNC和CB-MNC均已用于治療各種疾病,例如神經系統疾病、心臟病、2型糖尿病、肺部疾病和新生兒疾病。箭頭表示療效改善。
年齡、健康狀況和影響骨髓功能的疾病等因素會影響所采集BMMNC的可用性、質量和活力,可能導致移植細胞不足。在自體BMMNC不切實際的情況下,同種異體BMMNC可以作為替代方案。然而,同種異體BMMNC治療是一個活躍的研究領域,在轉化為臨床應用之前,需要進一步進行臨床前試驗。
機制解析與新型策略探索:BMMNCs和UCB-MNCs的療效源于多種細胞類型(如HSCs、MSCs)的協同作用,但具體機制尚未闡明。當前研究轉向單一干細胞(如MSCs)或細胞外囊泡(EVs),以簡化治療策略并增強靶向性。未來需解析不同細胞成分的功能,并開發基于EVs的無細胞療法,以規避異體移植的免疫風險。
臨床轉化與標準化推進:盡管短期安全性數據積極,長期隨訪仍是評估BMMNCs和UCB-MNCs風險的關鍵。異體治療需結合HLA匹配與免疫抑制方案,同時關注供體特異性抗體產生。
此外,亟需通過大規模研究確定最佳劑量、時機及給藥途徑,并直接比較BMMNCs與UCB-MNCs在不同疾病中的療效差異,以建立精準治療框架。跨學科合作與技術創新將是突破現有瓶頸的核心驅動力。
參考資料:https://link.springer.com/chapter/10.1007/978-981-96-1261-1_1
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。




 掃碼添加微信
掃碼添加微信