近年來隨著生活壓力和生活方式的改變,女性朋友在40歲以前,本不該絕經的年齡發生卵巢功能衰竭,不來月經了或者月經減少,就是我們常說的“卵巢早衰”。
該疾病的發病機理錯綜復雜,涵蓋了心理、遺傳、免疫調節、酶代謝異常、感染性因素、環境因素以及醫源性因素等多個層面。更為復雜的是,多數卵巢早衰病例呈現出特發性特征,其確切的發病機制至今尚未完全明晰,導致傳統治療手段往往難以奏效。
在此背景下,干細胞移植作為一種新興且備受國內外學者關注的治療方法,已在多種疾病的治療領域內取得了顯著成效,為卵巢早衰的治療提供了新的希望與可能。
2025年1月至8月,干細胞治療卵巢早衰領域取得了多項重要進展,為這一困擾女性健康的疾病提供了新的治療思路和希望。以下將從臨床研究、治療機制、技術優化及未來展望等方面,系統梳理2025年1月至10月干細胞治療卵巢早衰的最新臨床進展。

2025年干細胞療法治療卵巢早衰最新臨床進展匯總(截至10月)
2025年1-10月干細胞治療卵巢早衰臨床進展匯總
2025年1月干細胞治療卵巢早衰最新臨床進展
1月初,中國人民解放軍聯勤保障部隊第940醫院在期刊《中國組織工程研究》上發表了一篇關于《人臍帶間充質干細胞聯合褪黑素對化療所致卵巢功能不全的治療作用及機制》的研究成果。[1]

本研究通過建立卵巢早衰模型大鼠,探討人臍帶間充質干細胞(hUCMSCs)聯合褪黑素對卵巢功能的修復機制。分為對照組、卵巢早衰模型組、干細胞治療組、褪黑素治療組及干細胞 + 褪黑素聯合治療組,通過注射干細胞(1×10?個/次,3次)和褪黑素(10mg/kg/天)后發現:
模型組大鼠出現體重下降、發情周期紊亂、卵巢萎縮,關鍵激素(雌二醇、抗苗勒氏管激素)水平降低,促卵泡激素等升高,卵巢細胞結構破壞,細胞自噬相關蛋白(LC3Ⅱ/Ⅰ)表達升高,PI3K/AKT/mTOR 信號通路活性降低。
各治療組體重、激素水平、卵巢結構均有改善,其中干細胞 + 褪黑素聯合治療效果最佳,能顯著恢復卵巢功能指標,抑制細胞自噬,激活 PI3K/AKT/mTOR 信號通路。
結論:干細胞聯合褪黑素可能通過調節細胞自噬信號通路,有效改善卵巢早衰癥狀,聯合療法效果優于單一治療。
2025年2月干細胞治療卵巢早衰最新臨床進展
2月25日,成都中醫藥大學醫學與生命科學學院牽頭在《中國優生與遺傳雜志》上發表了一篇關于《干細胞應用于卵巢早衰的研究現狀》的研究成果。[2]

研究發現干細胞治療卵巢早衰(POF)的潛力源于其歸巢能力和旁分泌作用,可通過減少顆粒細胞凋亡、促進血管生成、調節免疫及氧化應激等途徑恢復卵巢功能。目前應用的干細胞類型包括:
胚胎干細胞(ESCs):實驗發現,ESCs能分化為分泌雌激素的顆粒細胞樣細胞,其衍生的細胞外囊泡可恢復激素水平并增加卵泡數量,機制涉及PI3K/AKT通路激活和凋亡抑制。相比其他干細胞,ESCs衍生的MSCs增殖能力強,能有效減少卵泡凋亡。盡管存在倫理爭議,ESCs在POF治療中的應用仍具研究價值。
誘導多能干細胞(iPSCs):是將普通細胞轉化為類似胚胎干細胞的細胞,能分化為卵巢細胞等組織,為卵巢早衰(POF)治療提供新方案。研究表明,iPSCs可分化為功能性顆粒細胞和卵母細胞,恢復小鼠卵巢功能;其衍生的細胞外囊泡(EVs)通過調控信號通路改善卵泡數量和細胞凋亡。相比傳統胚胎干細胞,iPSCs避免倫理爭議和免疫排斥,未來有望成為POF治療的有效手段。
間充質干細胞(MSCs):來源廣泛(如臍帶、骨髓、脂肪等),其中臍帶間充質干細胞(hUC-MSCs)因低免疫原性和高安全性成為研究熱點,多項人體臨床研究顯示其可改善激素水平、恢復卵巢結構,部分患者月經恢復甚至成功妊娠。此外,月經血源性干細胞、羊水間充質干細胞等也展現出抗凋亡和修復潛力。
研究表明盡管存在細胞存活率、倫理等挑戰,干細胞療法已在改善卵巢功能和生育力方面取得顯著進展,未來有望成為POF的重要治療手段。
2025年3月干細胞治療卵巢早衰最新臨床進展
3月10日,濟寧醫學院生命科學學院牽頭在期刊《Scientific Reports》上發表了一篇關于《缺氧間充質干細胞來源的外泌體通過降低線粒體氧化應激改善卵巢功能不全》的研究成果。[3]

化療藥物環磷酰胺可能導致女性卵巢功能受損,影響生育。一項研究發現,從臍帶干細胞中提取的 “外泌體”能改善卵巢損傷,尤其在缺氧環境下 “訓練” 過的外泌體(HExos)效果更好。
給化療損傷的大鼠注射這些干細胞后,它們的卵巢重量、激素水平和排卵功能都有明顯改善,而且缺氧組效果比普通組更突出。在實驗室培養的卵巢細胞中,這些干細胞外泌體能被細胞吸收,減少細胞死亡,恢復細胞能量工廠(線粒體)的功能,減輕氧化損傷。
這項研究表明,缺氧預處理的臍帶干細胞外泌體,能通過激活細胞修復機制,有效減輕化療對卵巢的損傷,為保護女性生育力提供了新方法。
2025年4月干細胞治療卵巢早衰最新臨床進展
4月12日,國際期刊《Stem Cell Research & Therapy》上發表了一篇關于《卵巢內注射自體月經血來源的間充質基質細胞:一種安全且有前景的提高卵巢反應不佳者妊娠率的方法》的文章顯示:向卵巢注射間充質干細胞可改變患者的生育結局,在這項涉及105位患者的研究里,干細胞成功讓超過三分之一的女性懷孕,每次妊娠活產率高達74.42%。[4]

本次研究納入了包括2018年8月至2021年9月之間接受自體干細胞給藥的105位患者。接受注射時她們的平均年齡為37.91歲。
在接受隨訪期間(平均時間為3.72年),共有38人成功懷孕,其中27人自然受孕,占比為25.7%,概率是PRP療法的三倍以上!13人通過IVF受孕(兩人通過不同方式懷孕),自然受孕的中位時間為治療后3個月,IVF受孕的中位時間為注射后5.5個月,最終一共誕生了32名嬰兒(其中一例為雙胞胎),每次懷孕活產率高達74.42%,且未發現嬰兒先天性異常或死亡的情況。
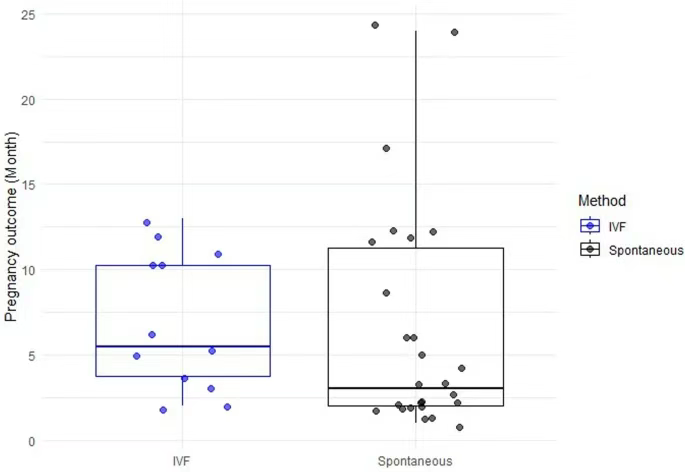
研究人員認為:年齡是其中的關鍵影響因素,在這100多位參與者當中,35歲以下的女性妊娠率為52.17%,35歲以上為31.7%。
安全性方面,近4年的隨訪時間里沒有發現明顯的長期問題,僅記錄了一例妊娠期間的卵巢囊腫,但未經干預就已經自行消退了,沒有發現子宮內膜異位癥、卵巢惡性腫瘤、扭轉、盆腔炎、異位妊娠或自身免疫性疾病的實例。這些發現表明,對于卵巢反應不佳的女性而言,向卵巢注射經血來源的干細胞可能是一種安全且有效的的治療選擇。
2025年5月干細胞治療卵巢早衰最新臨床進展
5月14日,國家藥監局藥品審評中心(CDE)公布,人臍帶間充質干細胞注射液(CXSL2500146)正式獲批開展治療卵巢早衰(無生育需求)的臨床試驗。這是我國首次明確針對卵巢早衰的臍帶干細胞藥物項目。[5]
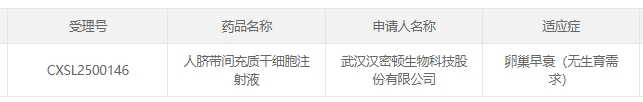
這意味著MSC治療卵巢早衰正式獲得法定身份,以Ⅰ類創新生物藥路徑進入臨床研究,未來將有望取得正式藥品批號,不再局限于“技術備案”范疇。此外,本次臨床試驗聚焦的是“無生育需求”的女性群體,更全面地瞄準圍絕經期女性的健康管理。
5月21日,《人羊膜上皮干細胞移植治療早發性卵巢功能不全的安全性和有效性:一項單中心、開放、隨機對照試驗》項目啟動會順利召開,標志著浙大婦院干細胞臨床研究開啟新篇章。該項目重點探索干細胞技術在生育力保護中的應用,旨在以科技創新護航女性健康。[6]

張丹教授說,激素替代治療是目前臨床治療POI患者的方法之一,但是難以重建POI患者的卵巢功能及生育能力。人羊膜上皮干細胞(hAESCs)是一種能向三個胚層組織分化,具有較強分化能力、良好的抗炎功能和免疫耐受能力。
前期動物試驗已經證實,hAESCs可以改善POI小鼠的卵巢功能,包括減少卵巢萎縮纖維化、改善卵巢內分泌功能以及卵巢相關標志物的表達,減少卵巢細胞的凋亡,恢復小鼠生育力等,并且在體內駐留期間無非預期分化發生,無不良事件發生。
我們希望基于動物模型的研究基礎上,在經過嚴格的倫理審查,并獲得注冊許可之后,積極探索人羊膜上皮干細胞對改善POI患者的卵巢功能和生育能力的有效性和安全性,為今后治療有生育要求的POI患者提供新型的治療方案參考。
2025年6月干細胞治療卵巢早衰最新臨床進展
6月27日,西班牙阿利坎特科研人員在《Aging (Albany NY)》雜志上發表了一篇名為《增強卵巢衰竭女性的卵母細胞活化:干細胞再生研究在現實世界實踐中使用G-CSF動員外周血干細胞和卵巢內注射富含干細胞因子的富血小板血漿的臨床結果》的研究成果。[7]

該研究評估了干細胞再生療法對卵巢衰竭女性卵母細胞激活的有效性和安全性,包括卵巢反應低下 (POR)、卵巢儲備減少 (DOR) 和卵巢功能不全 (POI) 等情況。
共145名女性參與:總體激活率為68.28%,其中7.07%自然妊娠,14.14%IVF妊娠。所有參與者的CD34+細胞動員均成功,平均采集到32.96個CD34+細胞/μl。未觀察到嚴重不良反應。
該研究得出結論,干細胞再生療法在現實生活中對卵巢功能衰竭女性的卵母細胞激活是有效且安全的。
2025年7月干細胞治療卵巢早衰最新臨床進展
7月24日,土耳其安卡拉大學干細胞實驗室牽頭在《Journal of Assisted Reproduction and Genetics》上發表了一篇名為《原發性卵巢功能不全和卵巢儲備功能低下的細胞療法:系統評價》的研究成果。[8]

研究檢索到的資料覆蓋到2025年5月,共有27項研究,合計694名接受隨訪的患者。總體來看,研究方法和給藥方式并不完全一致,但能看出一些趨勢。
在細胞來源與給藥途徑上,約37%的研究使用的是自體骨髓來源的間充質干細胞(MSCs);如果把同時聯合富血小板血漿(PRP)的研究也算上,這類聯合方案的占比上升到大約52%。
隨訪時間多集中在7到12個月這一區間(約41%)。在所有有對照組的研究中,約59%報告了妊娠結局的數據。
效果方面,在接受干細胞治療的522名患者中,共有60人妊娠,妊娠率約為11.7%;相比之下,對照組的172名患者中僅13人妊娠,妊娠率約為7.6%。在那些采用對照設計的研究里,有的報告顯示治療組的妊娠率更高——例如部分雙組研究里,治療組的妊娠率達到了22.6%(對應40例患者)。
月經恢復方面,接受治療的522例中有37例(月經恢復率約7.1%),而對照組的恢復率為5.1%。
2025年8月干細胞治療卵巢早衰最新臨床進展
8月1日,開羅大學理學院生物技術系在《Stem Cell Reviews and Reports》雜志上發表了一篇名為《間充質干細胞:恢復卵巢早衰生育力的治療方法》的研究成果。[9]
本綜述探討了MSC在卵巢功能恢復中的機制,評估了現有證據,并討論了POI治療臨床轉化面臨的挑戰。

研究表明,間充質干細胞(MSCs)在動物模型和多項早期臨床研究中都表現出積極信號:移植后常見的改善包括激素水平回升(如雌激素、AMH)、竇卵泡數增加、卵巢血流改善、月經部分恢復,甚至出現自然妊娠。其作用主要不是直接變成卵細胞,而是通過旁分泌釋放生長因子和miRNA、調節免疫炎癥、促進血管新生、抑制細胞凋亡以及可能的線粒體轉移等多重機制來改善卵巢微環境并激活休眠卵泡。
研究還發現,MSC來源多樣(骨髓、脂肪、臍帶、胎盤、月經血等),給藥方式包括局部卵巢注射或系統輸注;而MSC衍生的外泌體/外泌體療法作為“無細胞”替代,因更易保存、免疫原性低且安全性潛力更高,正成為熱門方向。
2025年9月干細胞治療卵巢早衰最新臨床進展
9月17日,我國科研人員在《婦產科與人類生殖雜志》上發表了一篇名為《間充質干細胞在治療卵巢早衰中的潛力和機制》的研究成果。[10]

研究表明,間充質干細胞(MSCs)在治療卵巢早衰(POF)中顯示出顯著療效和良好安全性。MSCs能夠通過抗細胞凋亡、促進血管生成、調節免疫反應和抗氧化等多種機制,改善受損卵巢組織的微環境,促進卵泡發育,恢復雌激素水平,并提升患者的生育潛能。
研究還指出,MSCs主要通過旁分泌作用發揮療效,而不依賴生成新的卵母細胞,這意味著即使卵巢功能部分喪失,殘余卵巢仍能受益。
與傳統激素替代療法相比,MSCs不僅能緩解癥狀,還可能改善卵巢自身功能,為POF患者提供了一種安全、可行且有前景的新型治療策略。
2025年10月干細胞治療卵巢早衰最新臨床進展
10月9日,南京醫科大學附屬南京鼓樓醫院牽頭在行業期刊《干細胞研究與治療》上發表了一篇名為《將臍帶間充質干細胞移植到卵巢可改善卵巢功能和卵巢早衰患者體外受精/卵胞漿內單精子注射周期的中期結局:一項臨床隊列研究》的臨床研究成果。[11]
研究納入了71例接受臍帶間充質干細胞(UC-MSC)卵巢組織注射或傳統體外受精/卵胞漿內單精子注射-冷凍胚胎移植(IVF/ICSI-FET)治療的卵巢早衰(POI)患者。

結果顯示,UC-MSC組治療后竇卵泡計數(AFC)顯著增加(3.86 ± 2.93 vs. 2.39 ± 1.66),首次控制性卵巢刺激(COS)周期的卵母細胞數量和冷凍胚胎數量均明顯高于對照組(卵母細胞:1.88 ± 1.00 vs. 1.39 ± 1.13,p = 0.034;冷凍胚胎:0.74 ± 0.82 vs. 0.14 ± 0.41,p < 0.001),且獲得冷凍胚胎的周期比例顯著提升(55.81% vs. 11.63%)。
此外基因集富集分析顯示,UC-MSC治療可上調卵巢激素和雌激素相關信號通路的基因表達。
研究表明,UC-MSC卵巢注射是一種有前景的治療策略,可改善POI女性體外受精周期的臨床結局,尤其為希望生育的患者提供新的選擇,但仍需更大規模、多中心試驗驗證其長期安全性與有效性。
2025年干細胞治療卵巢早衰最新臨床進展總結
綜上所述,2025年干細胞治療卵巢早衰的研究從機制探索到臨床轉化均取得顯著突破。研究表明,不同來源的干細胞(如臍帶、月經血、羊膜上皮等)通過抗凋亡、抗炎、促血管生成及調節氧化應激等多靶點機制,有效修復卵巢組織損傷、恢復激素平衡及生育功能,尤其在聯合療法(如干細胞+褪黑素)和新型遞送方式(如缺氧預處理外泌體)中展現出協同增效的優勢。
這些成果不僅深化了干細胞調控卵巢功能的分子機制認知,也為無生育需求女性的健康管理及有生育要求患者的生育力保護提供了創新方案。隨著首個臍帶干細胞藥物進入臨床試驗及規范化研究的推進,干細胞療法有望成為卵巢早衰治療的重要支柱,推動個體化醫療與再生醫學的融合發展。
未來展望
說到這里,也不能忽視存在的問題。干細胞來源(自體還是異體)、合適劑量、最優給藥路徑、長期安全性和療效持續性都還需要進一步明確;與此同時,標準化的生產流程、倫理審查和法律監管也還不夠完善。換句話說,現在的進展讓人期待,但還不足以把干細胞當成常規一線治療。
結語
展望未來,隨著更多大規模、多中心的隨機對照試驗完成,干細胞治療有望成為激素替代之外的重要選擇,甚至在某些情況下提供真正的組織修復方案。盡管仍需進一步研究和探索,但干細胞治療卵巢早衰的前景令人期待,有望為更多女性帶來福音。
參考資料:
[1]魏璐曉,黃炳學,杜靜,石栓霞,王吉田,王玲. 人臍帶間充質干細胞聯合褪黑素對化療所致卵巢功能不全的治療作用及機制研究[J]. 中國組織工程研究, 2025, 29(25): 5281-5288.
[2]鄒昀桓,丁顯平,鄭勇鳳.干細胞應用于卵巢早衰的研究現狀[J].中國優生與遺傳雜志,2025,33(02):471-477.DOI:10.13404/j.cnki.cjbhh.2025.02.026.
[3]Zhang, S., Zou, X., Feng, X. et al. Exosomes derived from hypoxic mesenchymal stem cell ameliorate premature ovarian insufficiency by reducing mitochondrial oxidative stress. Sci Rep 15, 8235 (2025). https://doi.org/10.1038/s41598-025-90879-3
[4]Zafardoust, S., Didar, H., Ganagard, M.G. et al. Intra-ovarian injection of autologous menstrual blood-derived-mesenchymal stromal cells: a safe and promising method to improve pregnancy rate in poor ovarian responders. Stem Cell Res Ther 16, 171 (2025). https://doi.org/10.1186/s13287-025-04278-6
[5]cde
[6]浙大婦院干細胞移植治療早發性卵巢功能不全的臨床研究項目正式啟動|浙江大學_新浪財經_新浪網
[7]Santamaria A, Ballester A, Mu?oz M. Enhancing oocyte activation in women with ovarian failure: clinical outcomes of the Stem Cell Regenera study using G-CSF mobilization of peripheral blood stem cells and intraovarian injection of stem cell factor-enriched platelet rich plasma in real-world-practice. Aging (Albany NY). 2025 Jun 27;17(6):1571-1580. doi: 10.18632/aging.206274. Epub 2025 Jun 27. PMID: 40587267; PMCID: PMC12245204.
[8]Seyihoglu, B., Gucuk, S. & Can, A. Cellular therapies in primary ovarian insufficiency and poor ovarian reserve: a systematic review. J Assist Reprod Genet (2025). https://doi.org/10.1007/s10815-025-03599-y
[9]Hassan, N., Hussein, D.M., Malak, F.A. et al. Mesenchymal Stem Cells: A Therapeutic Approach in Fertility Restoration in Premature Ovarian Insufficiency. Stem Cell Rev and Rep (2025). https://doi.org/10.1007/s12015-025-10944-2
[10]Jin WR, He SY, Mao XX, Li JY, Zhang XC, Liu QW. The potential and mechanism of mesenchymal stem cells in the treatment of premature ovarian failure. J Gynecol Obstet Hum Reprod. 2025 Sep 17;54(9):103031. doi: 10.1016/j.jogoh.2025.103031. Epub ahead of print. PMID: 40967164.
[11]Huang, C., Kong, N., Xue, P.?et al.?Transplantation of UC-MSCs in ovary improves ovarian function and intermediate outcomes in IVF/ICSI cycles of POI patients: a clinical cohort study.?Stem Cell Res Ther?16, 552 (2025). https://doi.org/10.1186/s13287-025-04680-0
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加微信
掃碼添加微信