脊髓損傷,這一嚴重的神經(jīng)系統(tǒng)創(chuàng)傷,如同無情的枷鎖,使患者身體機能嚴重受損,生活陷入困境。現(xiàn)有的手術(shù)、藥物、康復和神經(jīng)刺激等方法雖然能緩解癥狀、維持功能,但在修復受損脊髓、促進軸突再生方面效果有限,因此臨床上一直在尋求更有效的治療路徑。
2025年1月到10月期間,干細胞治療脊髓損傷領(lǐng)域取得了一系列令人矚目的最新臨床進展,為眾多患者點亮了希望之光。
本文結(jié)合全球最新研究動態(tài),系統(tǒng)梳理2025年1月到10月干細胞治療脊髓損傷核心技術(shù)突破以及臨床案例,為患者呈現(xiàn)最前沿科學動態(tài)與臨床突破。
2025年1-10月干細胞治療脊髓損傷最新進展:關(guān)鍵臨床數(shù)據(jù)盤點
2025年1-10月干細胞治療脊髓損傷臨床進展匯總
2025年1月干細胞治療脊髓損傷臨床進展
2025年1月28日,伊朗德黑蘭科研人員在行業(yè)期刊《細胞移植》上發(fā)表了一篇關(guān)于《鞘內(nèi)間充質(zhì)干細胞與雪旺細胞聯(lián)合移植對完全性脊髓損傷患者神經(jīng)性疼痛的療效:一項II期隨機陽性對照試驗》的臨床研究成果。本臨床試驗旨在探討鞘內(nèi)聯(lián)合注射雪旺細胞 (SC) 和骨髓間充質(zhì)干細胞 (BMSC) 對改善脊髓損傷引起的神經(jīng)性疼痛的療效。[1]

治療組和對照組分別有37名和30名患者接受了6個月的隨訪。
與對照組相比,治療組在注射后6個月的干擾項目平均評分顯著降低,包括日常活動、情緒和睡眠。同樣,與對照組相比,治療組在6個月后的疼痛頻率、平均和最差數(shù)字評定量表 (NRS) 疼痛強度評分也顯著降低。基于控制潛在混雜因素的多元回歸分析,發(fā)現(xiàn)研究期間所有結(jié)果指標的變化與治療組之間存在顯著關(guān)聯(lián)。
這項臨床試驗表明聯(lián)合細胞療法在改善完全性SCI患者的神經(jīng)性疼痛和生活質(zhì)量方面有效。未來的研究應評估該策略與其他現(xiàn)有療法聯(lián)合治療SCI引起的神經(jīng)性疼痛的效果。
2025年2月干細胞治療脊髓損傷臨床進展
2025年2月11日,日本再生醫(yī)學研究中心在國際權(quán)威期刊《Nature Medicine》上發(fā)表題為《人類脊髓損傷的干細胞療法:近期臨床研究進展與轉(zhuǎn)化路徑分析》的系統(tǒng)性綜述。[2]
該研究全面梳理了從2024年5月到12月內(nèi)全球17項干細胞治療脊髓損傷(SCI)的臨床試驗數(shù)據(jù),首次提出“細胞移植聯(lián)合康復干預”可顯著提升神經(jīng)功能恢復率,并強調(diào)干細胞療法已實現(xiàn)亞急性SCI患者運動功能改善達40%的突破性療效。

研究強調(diào),脊髓損傷(SCI)臨床研究在過去十年取得顯著進展,研究對象涵蓋胎兒源性NS/PC及多能干細胞(ES/iPSC)衍生NS/PC、間充質(zhì)干細胞(MSC)、嗅鞘細胞與施萬細胞等。亞急性SCI患者的臨床數(shù)據(jù)已顯示運動功能改善的積極信號。值得注意的是,同種異體NS/PC相較自體MSC具有更強的脊髓整合能力且可標準化生產(chǎn),適用于超急性期干預。誘導多能干細胞(iPSC)的基因編輯技術(shù)突破使其成為未來精準治療的關(guān)鍵方向,有望通過定制化細胞方案解決供體匹配與免疫排斥問題。
2025年3月干細胞治療脊髓損傷臨床進展
“國家兩委備案干細胞臨床研究·脊髓損傷患者招募”媒體發(fā)布會于2025年3月6日召開,西安醫(yī)院正式啟動了西北地區(qū)首個中樞神經(jīng)損傷干細胞項目。該項目旨在通過間充質(zhì)干細胞移植治療脊髓損傷,標志著從“不可逆”損傷到“功能重建”的重要臨床突破。[3]

在發(fā)布會上,院長詳細介紹了“間充質(zhì)干細胞移植治療脊髓損傷”項目的申報背景及過程。他指出,傳統(tǒng)治療方法如手術(shù)和藥物往往無法顯著改善患者的病情,特別是對于神經(jīng)信號通路的修復效果有限。基于此,賀院長帶領(lǐng)團隊開啟了干細胞療法的研究,希望通過精準的干細胞移植技術(shù),重建受損神經(jīng)系統(tǒng)的“通信網(wǎng)絡”,為患者提供新的治療途徑。
張偉主任在會上分享了項目的初步成果:參與臨床研究的6名脊髓損傷患者中,5例患者出現(xiàn)了神經(jīng)功能的改善,4例患者運動功能顯著提升,其中2例患者的恢復情況尤為突出。一位完全性損傷患者在接受治療后,已經(jīng)能夠在輔助下短暫站立,這表明細胞移植治療脊髓損傷具有可行性,并為進一步的臨床試驗提供了有力依據(jù)。
一名22歲的山西患者因高空墜落導致脊髓損傷,術(shù)后下肢肌肉逐漸恢復力量,現(xiàn)已能夠自行滾背和跪立;
另一位患者則在細胞移植術(shù)后一個月內(nèi)擺脫拐杖,實現(xiàn)了獨立行走。


3月24號,日本慶應義塾大學教授岡野秀之領(lǐng)導的研究小組宣布首個利用誘導多能干細胞在治療脊髓損傷方面取得重大突破。該研究結(jié)果發(fā)表在權(quán)威期刊雜志《nature》上。[4]

研究表明,在一項修復脊髓損傷的臨床研究中,接受特殊干細胞移植的四名患者中有兩名表現(xiàn)出運動功能恢復,并且沒有任何不良反應。
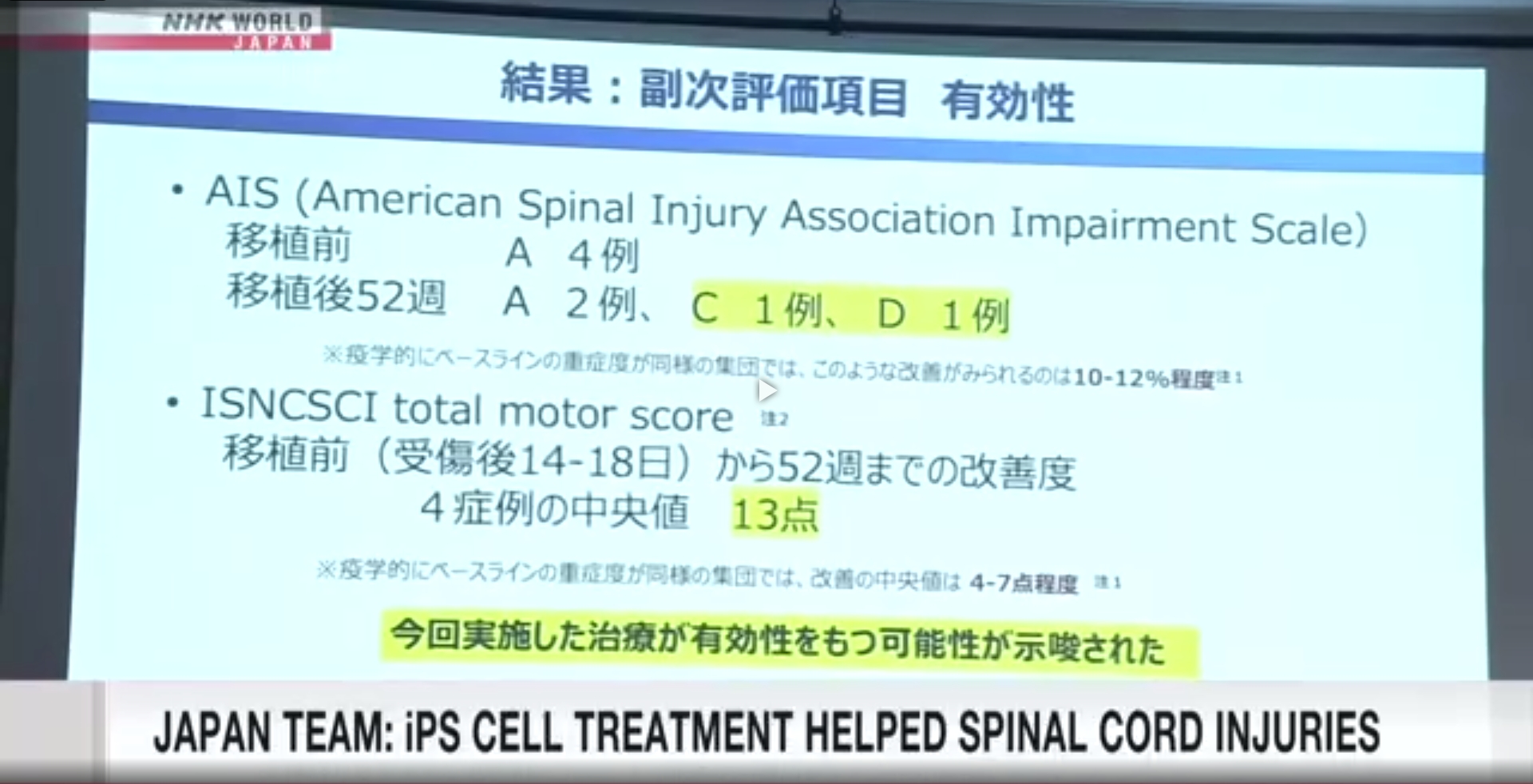
慶應義塾大學和其他機構(gòu)的研究人員周五表示,這是世界上首例利用源自誘導性多能干細胞(iPSC)的細胞進行治療,幫助改善脊髓損傷患者的癥狀的案例。
據(jù)報道,其中一名患者此前被歸類為完全癱瘓,現(xiàn)在他可以獨立站立,并開始進行行走鍛煉。另一名患者恢復了手臂和腿部的運動能力,而另外兩名患者沒有明顯改善。
患者均為成年男性,在受傷后的14至28天內(nèi)接受治療,即所謂的亞急性期。
為了再生丟失的神經(jīng)連接,每個人的受傷部位都被注射了兩百萬個神經(jīng)干細胞。盡管結(jié)果好壞參半,但標志著尋找有效脊髓損傷治療方法的道路上邁出了重要一步。
詳情請瀏覽:世界首例:iPS細胞治療恢復脊髓損傷患者的運動能
2025年4月干細胞治療脊髓損傷臨床進展
4月16日,國際期刊雜志《細胞神經(jīng)科學前沿》發(fā)表了一篇《間充質(zhì)干細胞治療脊髓損傷的評估:系統(tǒng)評價和網(wǎng)絡薈萃分析》的研究文章。該研究旨在通過網(wǎng)絡薈萃分析評估了18項研究,合計950例SCI患者。主要目的是探討間充質(zhì)干細胞(MSC)移植治療脊髓損傷(SCI)患者的臨床療效,并探討最佳移植治療策略。[5]

研究結(jié)果表明:間充質(zhì)干細胞(MSCs)顯著改善脊髓損傷(SCI)后患者的運動、感覺及日常生活活動能力。網(wǎng)絡薈萃分析顯示,臍帶間充質(zhì)干細胞(UCMSCs)是最有效的細胞來源,鞘內(nèi)注射(IT)是最佳的移植方式。
詳情請瀏覽:科學實證:間充質(zhì)干細胞對脊髓損傷患者功能恢復效果顯著
2025年5月干細胞治療脊髓損傷臨床進展
5月5日,伊朗德黑蘭科研人員在行業(yè)期刊《干細胞研究與治療》上發(fā)表了一篇名為《間充質(zhì)干細胞和雪旺細胞聯(lián)合治療脊髓損傷后的神經(jīng)系統(tǒng)、功能和生活質(zhì)量結(jié)果:9年經(jīng)驗》的臨床研究成果。[6]
本研究旨在評估經(jīng)鞘內(nèi)途徑聯(lián)合移植自體骨髓間充質(zhì)干細胞 (MSC) 和雪旺細胞 (SC) 對完全性脊髓損傷 (SCI) 患者的療效和安全性。評估了2013年8月至2022年9月期間接受聯(lián)合細胞療法治療的106例完全性脊髓損傷患者,并進行了隨訪。

1.對患者的神經(jīng)系統(tǒng)改善效果
研究顯示,干細胞治療使脊髓損傷患者在12個月內(nèi)神經(jīng)功能顯著改善。所有患者的運動、輕觸覺和針刺評分均提升,其中頸椎損傷患者的運動功能改善更明顯(從23.9增至29.3),而胸腰椎患者改善較小(從47.9增至49.3)。感覺功能(輕觸覺、針刺)在各組間無明顯差異。(見圖2 a-c)
無論是早期(損傷后14天-6個月)還是晚期(損傷后6個月以上)患者,神經(jīng)功能評分均顯著提高,但改善幅度在兩組間無明顯區(qū)別。
研究結(jié)論表明,干細胞治療對脊髓損傷具有普遍恢復效果,頸椎患者運動功能獲益更突出。
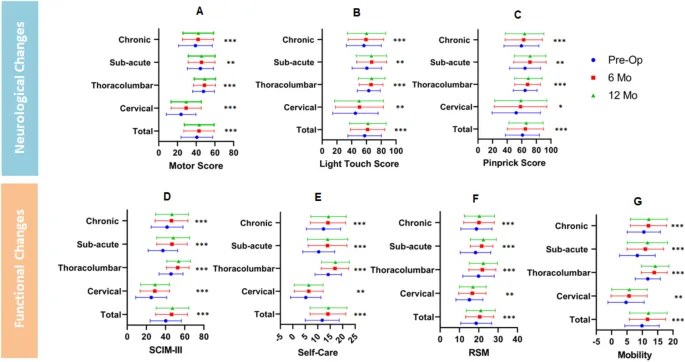
2.對患者功能性的改善效果
研究顯示,干細胞治療顯著提升了脊髓損傷患者的功能獨立性。12個月內(nèi),SCIM III總分從40.3(±16.3)升至47.2(±17.1),自我護理、呼吸/括約肌管理(RSM)和活動能力均顯著提高。(見圖2 d-g)
無論損傷部位(頸椎或胸腰椎),所有患者的SCIM III評分均改善。亞急性SCI患者(損傷后14天-6個月)在總分和活動能力上的提升幅度大于慢性患者(>6個月),但自我護理和RSM改善無明顯差異。
結(jié)果表明,干細胞治療在12個月內(nèi)有效增強功能恢復,且亞急性患者在活動能力方面獲益更明顯。
3.對患者生活質(zhì)量的改善
研究顯示,干細胞治療顯著提升了脊髓損傷患者的生活質(zhì)量。總體生活質(zhì)量感知(37.8→43.9),總體健康評分從23.8(±23.0)大幅提高至51.8(±31.8)。生理、心理、社會及環(huán)境領(lǐng)域均顯著改善。(見圖3)
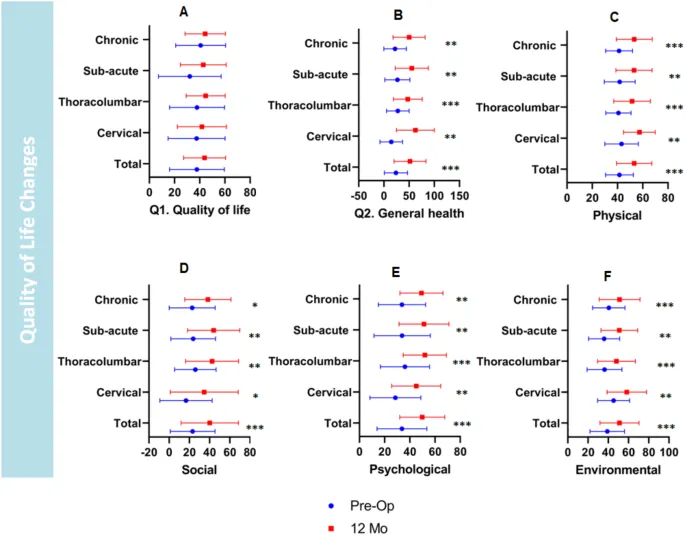
4.患者主觀報告的改善情況
根據(jù)患者主觀描述,12個月后患者自我報告的軀干運動、坐姿能力、坐姿平衡和站立平衡顯著改善,膀胱充盈感和自主控制能力也明顯提高。但直腸充盈感和肛門自主收縮能力未見顯著變化。(見圖3)
結(jié)果表明,干細胞治療在改善軀干和坐姿功能、膀胱控制方面效果顯著,但對腸道功能的提升有限。
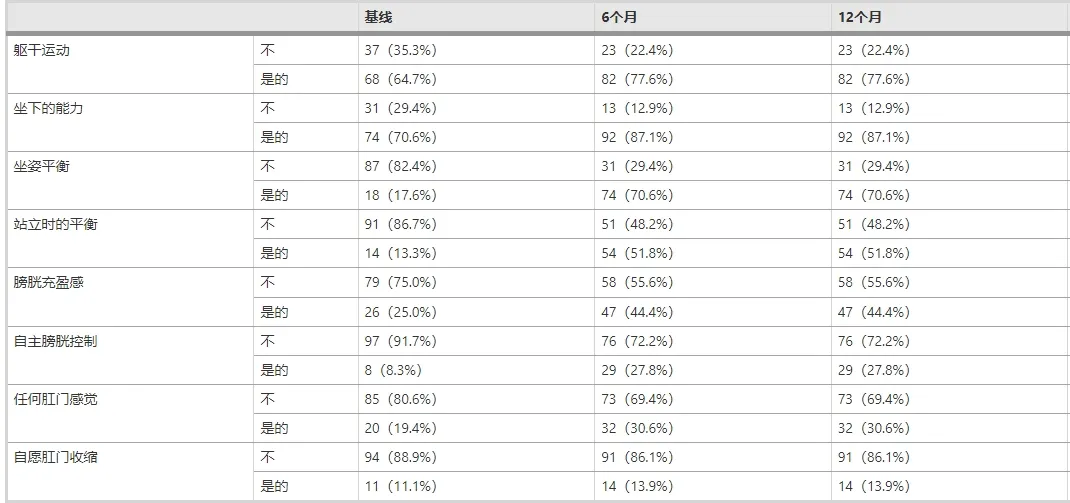
綜上所述,本研究表明,間充質(zhì)干細胞與雪旺細胞聯(lián)合療法在12個月內(nèi)顯著改善了完全性脊髓損傷患者的神經(jīng)功能、生活質(zhì)量和活動能力,尤其對頸椎損傷和亞急性期患者效果更佳。
詳情請瀏覽:間充質(zhì)干細胞+許旺細胞治療脊髓損傷:9年實證神經(jīng)與功能恢復
5月,美國食品藥品監(jiān)督管理局 (FDA) 和中國國家藥品監(jiān)督管理局 (NMPA) 批準了一項我國科研公司研發(fā)的誘導多能干細胞治療脊髓損傷 (SCI) 的全球臨床試驗。[7]
這是全球首個再生細胞療法針對脊髓損傷(SCI)的注冊I期臨床試驗,標志著這一領(lǐng)域迎來歷史性的里程碑。

作為“全球首個”再生脊髓區(qū)亞型特化神經(jīng)前體細胞新藥再生治療脊髓損傷的注冊臨床試驗,將由脊髓損傷診療領(lǐng)域頂級專家中山大學附屬第三醫(yī)院戎利民院長作為牽頭臨床中心及臨床總負責人,大連醫(yī)科大學附屬第一醫(yī)院黨委書記、大連干細胞與精準醫(yī)學創(chuàng)新研究院劉晶院長作為聯(lián)合臨床中心及臨床聯(lián)合負責人正式開展。
此次獲批的臨床試驗采用了誘導多能干細胞(iPSC)療法,這是一種具有革命性潛力的治療手段。iPSC技術(shù)通過將成體細胞重編程為類似于胚胎干細胞的狀態(tài),使其獲得無限增殖和分化的能力。在脊髓損傷治療中,iPSC 可以分化為神經(jīng)元和少突膠質(zhì)細胞等脊髓損傷修復所需的關(guān)鍵細胞類型,有望從根本上修復受損的神經(jīng)組織,重建神經(jīng)傳導通路。
1.技術(shù)原理:
iPSC技術(shù):將普通體細胞(如皮膚細胞)重編程為多能干細胞,再定向誘導分化為亞型特化神經(jīng)前體細胞,替代受損神經(jīng)元。
異體“現(xiàn)貨型”療法:無需從患者體內(nèi)提取細胞,實現(xiàn)標準化生產(chǎn),降低個體化治療成本與復雜性。
2.核心優(yōu)勢:
修復與再生雙重作用:替代死亡神經(jīng)元,重建神經(jīng)通路;分泌神經(jīng)營養(yǎng)因子(如BDNF、GDNF),抑制炎癥并促進內(nèi)源性修復。
低免疫排斥風險:通過篩選優(yōu)化的細胞亞型與免疫調(diào)節(jié)策略,顯著降低異體移植排斥反應。
規(guī)模化應用潛力:標準化生產(chǎn)流程可實現(xiàn)“現(xiàn)貨供應”,預計5-7年內(nèi)實現(xiàn)量產(chǎn)。
此次脊髓損傷iPSC療法不僅為全球患者提供首個可實現(xiàn)神經(jīng)修復的解決方案,更標志著再生醫(yī)學從“理論探索”邁向“臨床轉(zhuǎn)化”的關(guān)鍵轉(zhuǎn)折,更可能徹底改變神經(jīng)退行性疾病的治療模式。
2025年6月干細胞治療脊髓損傷臨床進展
6月初,伊朗德黑蘭神經(jīng)科學研究中心在《IBRO Neurosci Rep》期刊上發(fā)表了一篇名為《間充質(zhì)干細胞條件培養(yǎng)基與脊髓損傷:當前治療能力的回顧》的研究成果。[8]

研究結(jié)果表明,CM的修復作用通過多種細胞和分子機制發(fā)揮,例如降低炎癥因子(例如IL-2、TNF-α和IL-6),刺激巨噬細胞/小膠質(zhì)細胞M2極化,抑制巨噬細胞/小膠質(zhì)細胞M1極化,促進運動和感覺功能,減輕小膠質(zhì)細胞焦亡,增強軸突生長相關(guān)基因(FGF-2和GAP-43)的表達,以及增加少突膠質(zhì)細胞的總數(shù)。
因此,這種基于MSC的策略可能為SCI患者在臨床試驗中的應用帶來光明的前景。
2025年7月干細胞治療脊髓損傷臨床進展
7月18日,伊朗德黑蘭生理學研究中心在《Spinal Cord》期刊雜志上發(fā)表了一篇名為《干細胞療法對脊髓損傷運動功能恢復和神經(jīng)性疼痛緩解的影響:綜述和薈萃分析》的研究成果。[9]
本綜述和薈萃分析旨在評估干細胞療法對脊髓損傷 (SCI) 嚙齒動物模型中的運動恢復和神經(jīng)性疼痛緩解的功效。

研究納入了31篇系統(tǒng)綜述/薈萃分析,結(jié)果顯示:
各類干細胞都能在一定程度上促進運動功能恢復,其中臍帶間充質(zhì)干細胞(U-MSCs)和少突膠質(zhì)細胞祖細胞(OPCs)的效果最明顯;而骨髓間充質(zhì)干細胞(BM-MSCs)則在緩解機械性神經(jīng)性疼痛方面表現(xiàn)更好。研究還發(fā)現(xiàn),干細胞的療效會受到損傷類型、治療時間、細胞劑量以及是否使用抗生素或免疫抑制劑等因素的影響。
總體來說,如果在損傷后盡早、使用中低劑量U-MSC,運動功能的改善最為顯著;而BM-MSC在緩解疼痛方面則更有優(yōu)勢。這些結(jié)果為未來在臨床上優(yōu)化干細胞治療提供了有價值的參考,也提示需要在理想條件下進一步開展臨床研究以驗證效果。
2025年8月干細胞治療脊髓損傷臨床進展
8月初,《國際外科雜志》上發(fā)表了一篇名為《神經(jīng)干細胞移植在脊髓損傷臨床試驗中的應用及當前挑戰(zhàn)》的研究成果。[10]

臨床數(shù)據(jù)顯示,把神經(jīng)干細胞(如NSI-566)注入受損脊髓是可耐受的,短期和中期隨訪中很少見到嚴重不良事件。患者確實在感覺和運動上有實實在在的好轉(zhuǎn)——比如下肢對主動運動的反應增強、局部節(jié)段的感覺部分恢復,以及神經(jīng)性疼痛減輕。隨訪數(shù)年者也報告了穩(wěn)定的改善,影像學檢查沒有發(fā)現(xiàn)移植后腫瘤或明顯的結(jié)構(gòu)損害,整體安全性令人放心。
不過,療效并非在所有人身上都一樣。研究發(fā)現(xiàn)不同損傷類型、不同劑量和給藥策略會影響結(jié)果:中低劑量常能見到功能改善,而更高劑量不一定帶來更大收益。上肢力量、痙攣情況與疼痛評分多數(shù)呈改善或維持穩(wěn)定的趨勢。
總的來說,神經(jīng)干細胞移植在慢性與亞急性脊髓損傷中顯示出可行性與潛在療效。
2025年9月干細胞治療脊髓損傷臨床進展
9月8日,紐約醫(yī)學院大都會醫(yī)院在國際期刊《Tissue Engineering and Regenerative Medicine》上發(fā)表了一篇名為“干細胞療法在神經(jīng)創(chuàng)傷和神經(jīng)退行性疾病中的臨床療效:一項比較綜述”的研究成果。[11]
研究表示,目前利用細胞療法治療難治性脊髓損傷的研究已有數(shù)十篇,在頸椎、胸椎、腰椎脊髓損傷的病例中,應用自體間充質(zhì)干細胞(骨髓來源細胞、脂肪來源細胞)、同種異體間充質(zhì)干細胞、神經(jīng)干細胞、華通膠來源細胞、少突膠質(zhì)細胞祖細胞等。
| 干細胞類型 | 核心療效表現(xiàn) | 優(yōu)勢損傷節(jié)段 | 安全性特征 |
|---|---|---|---|
| 自體間充質(zhì)干細胞 | AIS 分級提升1-2 級,膀胱 /感覺/ 運動功能恢復 | 胸腰段為主 | 輕中度反應,無長期風險 |
| 同種異體 WJ-MSC | 胸椎損傷 AIS 提升(A→C/D 級),膀胱 / 肌力恢復 | 胸椎中下段 | 無嚴重并發(fā)癥,隨訪無不良事件 |
| 神經(jīng)干細胞(NSC) | 多節(jié)段感覺 / 運動評分改善(如 UEMS 提升 1.58 分) | 全節(jié)段 | 輕中度反應,無嚴重并發(fā)癥 |
| 少突膠質(zhì)細胞祖細胞(LCTOPC1) | 頸髓損傷后,21/22 例恢復至少 1 個節(jié)段神經(jīng)功能,7 例恢復≥2 個節(jié)段 | 頸髓(C4-C7) | 29起嚴重不良事件(腦脊液漏、細菌感染) |
1.自體間充質(zhì)干細胞:多來源有效,胸腰段為主
自體骨髓或脂肪來源的間充質(zhì)干細胞在多項小樣本研究和病例系列中顯示出對脊髓損傷(SCI)患者的潛在療效。
多數(shù)研究報告受試者AIS分級至少提高一級,部分患者出現(xiàn)兩級或更多改善,膀胱控制、感覺與運動功能也有恢復報道。
總體安全性良好,少數(shù)患者出現(xiàn)泌尿道感染、頭痛、惡心等輕中度不良反應;長期嚴重不良事件少見。
2.同種異體間充質(zhì)干細胞(WJ-MSC):胸椎損傷顯潛力
有兩份關(guān)于使用同種異體沃頓膠衍生的間充質(zhì)干細胞 (WJ-MSC) 治療胸椎SCI患者的病例報告。
有趣的是,這兩個病例都說明了WJ-MSC在較低水平胸椎SCI中的潛在治療作用。
Miczarek等人報告的臨床研究,患者AIS分級從A/B級改善至C/D級,感覺水平從T12胸椎下降至L3-L4腰椎,膀胱控制和肛門感覺恢復,左下肢肌力改善。病例作者報告,在18個月的隨訪中未出現(xiàn)并發(fā)癥。
與Miczarek等人的病例報告類似,在三個月的隨訪中,AIS分級改善為C,并且在整個22個月的研究過程中保持穩(wěn)定。
患者在三個月時恢復了自愿的肛門收縮,并在 12個月時恢復了部分排尿控制。在25個月的隨訪期間未報告與治療相關(guān)的嚴重不良反應。
3.神經(jīng)干細胞(NSC):多節(jié)段適用,評估標準待統(tǒng)一
神經(jīng)干細胞 (NSC) 已被證明可有效治療包括頸椎、胸椎和腰椎所有主要節(jié)段的慢性脊髓損傷,這在近十年的四項臨床試驗中得到了證實。
頸椎SCI:I、IIa期對照試驗發(fā)現(xiàn),在19名參與者中,5名患者的AIS得到改善,其中2名患者的AIS級別從A級提高到C級,1名患者的AIS級別提高到B級,2名患者的B級提高到D級。
胸部SCI:I/IIA期臨床試驗中,12名T2–T11胸部SCI參與者中有5名在至少第一年的隨訪中表現(xiàn)出感覺改善,7名AIS分級為A級的患者中有2名在病變以下出現(xiàn)了一些感覺。
四肢癱瘓的頸椎SCI:2期臨床試驗證實,6例 C5-C7治療后,與基線UEMS評分1.25相比,在9個月的隨訪中,UMES評分提高至2.83,GRASSP評分(力量、抓握能力和運動能力)分別提高了4.17分和1.08分。
可惜的是,盡管利用神經(jīng)干細胞治療各主要損傷層面脊髓損傷的研究取得了令人鼓舞的成果,但根據(jù)給藥途徑的不同,NSC 的標準化理想劑量尚未確定。
4.少突膠質(zhì)細胞祖細胞(LCTOPC1):頸髓損傷新方向
最近的一份報告表明,人類胚胎干細胞來源的少突膠質(zhì)細胞祖細胞 (以前稱為 APC-OPC1) 已被證明可用于治療頸髓損傷。
essler等人進行了一項開放標簽、劑量遞增、多中心臨床試驗,其中25名C4-C7節(jié)段以上頸髓損傷患者。在一年的隨訪中,22個意向治療組中有 21個恢復了身體至少一側(cè)一個或多個節(jié)段的神經(jīng)功能,22個組中有7個恢復了身體至少一側(cè)兩個或更多節(jié)段的神經(jīng)功能。
注意的是該細胞共報告了29起嚴重不良事件,包括腦脊液漏和細菌感染。
2025年干細胞治療脊髓損傷臨床進展總結(jié)
綜上所述,2025年,全球干細胞治療脊髓損傷(SCI)領(lǐng)域呈現(xiàn)多維度突破:
技術(shù)層面,誘導多能干細胞(iPSC)實現(xiàn)亞型特化神經(jīng)前體細胞的定向分化,異體“現(xiàn)貨型”療法推動標準化生產(chǎn);
療效層面,亞急性SCI患者運動功能改善率達40%,聯(lián)合康復干預顯著提升神經(jīng)功能恢復率;
策略優(yōu)化中,鞘內(nèi)注射臍帶間充質(zhì)干細胞(UCMSCs)被證實為最優(yōu)移植方式,雪旺細胞聯(lián)合療法在疼痛緩解和功能重建中展現(xiàn)協(xié)同效應;
臨床轉(zhuǎn)化上,全球首個異體iPSC療法進入I期臨床試驗,標志著再生醫(yī)學從“理論探索”邁向“臨床落地”。
2025年的進展表明,干細胞療法正重塑脊髓損傷治療格局。通過精準細胞類型選擇、標準化生產(chǎn)流程及聯(lián)合干預策略,干細胞不僅為神經(jīng)修復提供了生物學基礎,更在功能重建、疼痛管理及生活質(zhì)量提升方面展現(xiàn)綜合價值。這一突破性進展有望降低長期護理成本,減輕社會醫(yī)療負擔。
未來需進一步明確長期安全性、優(yōu)化細胞遞送技術(shù),并推動多學科協(xié)作以加速從實驗室到臨床的轉(zhuǎn)化,最終實現(xiàn)“不可逆損傷”向“可修復疾病”的歷史性轉(zhuǎn)變。
結(jié)語
2025年,干細胞治療脊髓損傷領(lǐng)域取得了顯著進展,為這一復雜且嚴重的神經(jīng)系統(tǒng)疾病提供了新的治療希望。無論是士澤生物的“現(xiàn)貨型”iPSC療法,還是日本的癱瘓患者站立案例,抑或全球多中心試驗的加速推進,都預示著再生醫(yī)學的黃金時代正在到來。然而,這一革命仍需科研界、產(chǎn)業(yè)界與政策制定者的持續(xù)努力——唯有突破技術(shù)、倫理與經(jīng)濟的多重壁壘,才能讓“重啟生命”的承諾真正惠及每一位患者。
參考資料:
[1]Akhlaghpasand M, Tavanaei R, Hosseinpoor M, et al. Effects of Combined Intrathecal Mesenchymal Stem Cells and Schwann Cells Transplantation on Neuropathic Pain in Complete Spinal Cord Injury: A Phase II Randomized Active-Controlled Trial. Cell Transplantation. 2025;34. doi:10.1177/09636897241298128
[2]Sugai K, Nakamura M, Okano H, Nagoshi N. Stem cell therapies for spinal cord injury in humans: A review of recent clinical research. Brain Spine. 2025 Feb 7;5:104207. doi: 10.1016/j.bas.2025.104207. PMID: 40027291; PMCID: PMC11870206.
[3]https://sn.ifeng.com/c/8hWQMQCB97U
[4]Mallapaty S. Paralysed man stands again after receiving ‘reprogrammed’ stem cells. Nature. 2025 Apr;640(8057):18-19. doi: 10.1038/d41586-025-00863-0. PMID: 40128427.
[5]Wang R, Wang Y, Yan F, Sun J and Zhang T (2025) Assessment of mesenchymal stem cells for the treatment of spinal cord injury: a systematic review and network meta-analysis. Front. Cell. Neurosci. 19:1532219. doi: 10.3389/fncel.2025.1532219
[6]Akhlaghpasand, M., Tavanaei, R., Hosseinpoor, M. et al. Neurological, functional, and quality of life outcomes following combined mesenchymal stem cell and Schwann cell therapy in spinal cord injury: a 9-year experience. Stem Cell Res Ther 16, 226 (2025). https://doi.org/10.1186/s13287-025-04312-7
[7]https://www.xellsmart.com/news9/329.html
[8]Conditioned medium derived from mesenchymal stem cells and spinal cord injury: A review of the current therapeutic capacitiesKaka, Gholam Reza et al.IBRO Neuroscience Reports, Volume 18, 293 – 299
[9]Azimi, A., Toloui, A., Mozafarybazargany, M. et al. Stem cell therapy for locomotion recovery and neuropathic pain alleviation in spinal cord injury: an umbrella review and meta-analysis. Spinal Cord 63, 393–409 (2025). https://doi.org/10.1038/s41393-025-01104-x
[10]Zhang, Wen-Jun PhDa; Zhang, Jun MDb,*. Application and current challenges of neural stem cells transplantation in clinical trials of spinal cord injury. International Journal of Surgery 111(8):p 5325-5336, August 2025. | DOI: 10.1097/JS9.0000000000002548
[11]Ku, J.B., Pak, R.J., Ku, S.S.?et al.?Clinical Efficacy of Stem Cell Therapy in Neurotraumatic and Neurodegenerative Conditions: A Comparative Review.?Tissue Eng Regen Med?(2025). https://doi.org/10.1007/s13770-025-00757-2
免責說明:本文僅用于傳播科普知識,分享行業(yè)觀點,不構(gòu)成任何臨床診斷建議!杭吉干細胞所發(fā)布的信息不能替代醫(yī)生或藥劑師的專業(yè)建議。如有版權(quán)等疑問,請隨時聯(lián)系我。




 掃碼添加微信
掃碼添加微信