腎臟疾病是全球范圍內威脅人類健康的重要慢性疾病,其高發(fā)病率、不可逆的器官損傷及有限的治療手段,使得患者面臨長期透析或移植的困境。傳統(tǒng)療法如免疫抑制劑或降壓藥物雖能延緩病情進展,卻難以修復已受損的腎組織或逆轉纖維化進程。在此背景下,干細胞治療作為再生醫(yī)學的前沿方向,憑借其獨特的修復與再生潛力,為腎病治療開辟了全新路徑。干細胞通過分化為腎細胞、抑制炎癥反應、促進血管新生等機制,為受損腎臟提供“再生動力”,成為臨床研究的熱點。
然而,這一創(chuàng)新療法的臨床轉化面臨關鍵挑戰(zhàn):如何選擇最安全的給藥途徑?干細胞的注射方法(如靜脈注射、局部注射等)不僅影響治療靶向性,更直接關系到患者的安全性與療效。
本文將系統(tǒng)梳理干細胞不同注射方法治療腎病安全性特征,結合當前研究進展,探討其在腎病治療中的潛在價值與風險,并為未來優(yōu)化給藥策略提供參考。
干細胞治療腎病:靜脈、動脈、皮質注射哪種更安全?
一、干細胞主要輸注方式及其特點
1. 靜脈注射:靜脈注射是目前最廣泛使用的給藥方式,占臨床試驗的43%。通過外周靜脈將干細胞輸入全身循環(huán),操作簡便且創(chuàng)傷小,適用于系統(tǒng)性炎癥調控。
2.腎動脈內注射:通過腎動脈直接輸注干細胞可顯著提高病灶部位的干細胞濃度,但其操作風險和技術要求較高。
3.腎皮質注射:超聲或CT引導下多點穿刺注射可精準定位損傷區(qū)域,但一個注射點所能影響的組織范圍有限,若以治療為目的,通常需要在腎皮質上進行多點位的注射,進一步增加了難度。
4.聯(lián)合靜脈+局部注射:聯(lián)合途徑通過多靶點調節(jié)提升療效,但需動態(tài)監(jiān)測累積風險。

二、干細胞不同輸注方式的臨床安全性比較
2.1 靜脈注射
2023年,愛爾蘭戈爾韋大學醫(yī)學院牽頭在國際期刊《美國腎臟病學會雜志》上發(fā)表了一篇關于《間充質干細胞治療糖尿病腎病的安全性和初步療效》的一項隨機臨床試驗。

該研究在歐洲三個研究中心進行了一項最低劑量組,共16名參與者,按3:1的比例隨機分配接受間充質干細胞(80×106個細胞)或安慰劑靜脈輸注治療,并進行了18個月的隨訪。
早期安全監(jiān)測顯示:
- 輸注期間及8小時觀察期內:15名參與者未出現(xiàn)與細胞或安慰劑輸注相關的不良反應,生命體征(體溫、脈搏、呼吸、血壓、血氧飽和度)均保持穩(wěn)定。
- 唯一不良事件:1名接受安慰劑的參與者在輸注后不久出現(xiàn)中度支氣管痙攣,經(jīng)藥物治療后50分鐘內完全緩解,輸注后1個月內未再發(fā)生其他不良事件。
后期安全監(jiān)測(2-18個月隨訪):
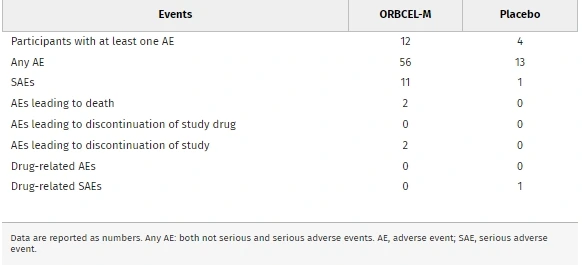
- 細胞治療組:4名參與者共報告11起嚴重不良事件(SAE),但均未被判定與干細胞試驗產(chǎn)品相關。
- 安慰劑組:未報告額外SAE,僅輸注時的支氣管痙攣1起與治療相關。(見圖1)
2.2 腎動脈內注射
2025年,日本細胞治療與再生醫(yī)學中心聯(lián)合湘南鐮倉綜合醫(yī)院在國際期刊《世界干細胞雜志》上發(fā)表了一篇關于《自體CD34+細胞療法改善慢性進行性腎病腎功能的初步證據(jù)》的臨床研究成果。本次研究于0個月和3個月時兩次經(jīng)雙側腎動脈直接注射CD34+細胞,并評估6個月的安全性和有效性。
CD34+細胞是是造血干細胞(HSC)和多系祖細胞的主要標志,能夠分化為紅細胞、白細胞、血小板等所有血細胞類型。

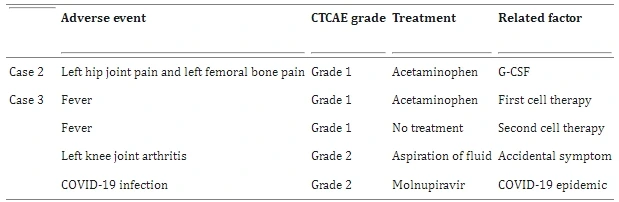
本研究中,所有不良事件(AE)均為輕度至中度且已完全恢復,未觀察到嚴重AE(CTCAE 3-5級)。具體表現(xiàn)如下:
患者2:在G-CSF動員期間出現(xiàn)左髖關節(jié)及股骨疼痛,經(jīng)對乙酰氨基酚治療后緩解,治療后一周疼痛完全消失。
患者3:
- 首次細胞治療后:出現(xiàn)短暫性發(fā)熱(≥38°C),持續(xù)數(shù)天,排除感染后自行緩解,未使用退熱藥物。
- 第二次細胞治療后:
- 再次出現(xiàn)短暫性發(fā)熱,同樣自行緩解;
- 一周后出現(xiàn)左膝關節(jié)疼痛伴腫脹,關節(jié)液抽吸提示焦磷酸鹽晶體性關節(jié)炎,經(jīng)抽吸處理后癥狀改善。
- 后續(xù)感染:第二次治療后3個月確診2019冠狀病毒病(COVID-19),表現(xiàn)為輕度咽痛和全身疲勞,接受莫努匹拉韋治療后康復。(見圖2)
隨訪結果:所有患者在6個月觀察期及研究結束后長達15個月的隨訪中,均未出現(xiàn)新的不良事件或并發(fā)癥。
2.3 腎皮質注射
2021年,北卡羅來納大學牽頭在《腎臟國際報告》中發(fā)表了一篇關于《新型經(jīng)皮局部注射腎細胞治療糖尿病慢性腎臟病的安全性和可行性》的研究成果。

2017年10月至2020年11月期間,研究人員對來自兩項II期臨床試驗的51名符合納入標準的2型糖尿病CKD 3-4期患者,使用20/25號同軸針系統(tǒng)進行了87次連續(xù)直接新型經(jīng)皮局部注射腎細胞注射分析。
安全性結果:所有患者在注射過程中均保持血流動力學穩(wěn)定,腎皮質靶向注射技術成功率達100%。未出現(xiàn)嚴重不良事件或并發(fā)癥,唯一1例REGEN-003組患者注射后出現(xiàn)輕微延遲性腎皮質包膜下血腫,需住院觀察但未輸血。
2.4 聯(lián)合輸注
2017年,印度尼西亞大學在醫(yī)學期刊《Journal of Medical Case Reports》上發(fā)表了一篇關于《人臍帶間充質干細胞治療慢性腎衰竭并胸段脊髓卡壓后腎功能改善一例》的臨床研究成果。

報告了一例62歲的印尼裔女性病例,此前診斷為胸椎脊髓卡壓,伴有截癱和慢性腎衰竭,需要血液透析。采用方案包括 6個周期的hUC-MSCs鞘內植入和靜脈聯(lián)合注射,時間間隔為3個月。
安全性結果:在整個治療周期(6個周期,間隔3個月)及術后隨訪期間,未觀察到與hUC-MSCs輸注相關的嚴重不良事件(如過敏反應、感染、免疫排斥或移植部位并發(fā)癥)。
此外,該研究強調,hUC-MSCs治療在該病例中展現(xiàn)了良好的耐受性,與其他類似研究的安全性結果一致。
三、不同輸注方式的安全性總結
綜上所述,靜脈注射在安全性表現(xiàn)上最為突出,研究顯示,糖尿病腎病患者接受間充質干細胞靜脈輸注后,僅1例安慰劑組出現(xiàn)短暫支氣管痙攣,干細胞組未報告與治療相關的嚴重不良事件(SAE),且后期隨訪中所有SAE均與治療無關,表明其具有高度安全性與耐受性。
腎動脈內注射雖技術復雜,但不良事件可控,日本研究中,患者出現(xiàn)的G-CSF動員期疼痛、短暫發(fā)熱及關節(jié)炎均通過藥物或對癥處理緩解,且未發(fā)生嚴重并發(fā)癥,但需注意操作風險及潛在感染關聯(lián)(如新冠感染)。
腎皮質注射作為局部侵入性方法,技術成功率可達可觀,但存在輕微并發(fā)癥風險,如包膜下血腫需住院觀察,但未引發(fā)嚴重后果。
聯(lián)合輸注則展現(xiàn)了良好的整體安全性,印度尼西亞病例中未出現(xiàn)免疫排斥或感染等嚴重反應,但需平衡多途徑操作的復雜性。
總體而言,靜脈注射因無創(chuàng)、低風險成為首選,而局部注射需嚴格操作規(guī)范以控制侵入性風險,聯(lián)合療法的安全性需更大樣本驗證,但現(xiàn)有數(shù)據(jù)支持其可行性。
四、影響安全性的共性因素
干細胞來源:
- 自體干細胞免疫排斥風險低,但采集過程可能引發(fā)骨髓抑制或感染。
- 異體干細胞需嚴格質量控制,避免病原體傳播,但其易獲取性使其成為主流選擇。
患者基線特征:
- 年齡與免疫狀態(tài)顯著影響安全性。例如,低齡患者因免疫耐受性強,不良事件發(fā)生率較成人低很多。
- 合并糖尿病或高血壓的患者需調整干細胞劑量,高劑量可能誘發(fā)細胞因子風暴。
相關閱讀:自體vs異體:不同來源的干細胞治療腎病患者的安全性有區(qū)別嗎?
結語
干細胞治療腎病的臨床安全性與輸注方式密切相關。靜脈注射因操作簡便、低風險且全身性調節(jié)效果顯著,成為最常用且安全性最高的選擇;局部注射(如腎動脈、腎皮質)雖能精準靶向病灶,但需嚴格操作規(guī)范以規(guī)避侵入性風險;聯(lián)合輸注(靜脈+局部)潛力初顯,但需更大樣本驗證其長期安全性。安全性受干細胞來源(自體或異體)、患者免疫狀態(tài)及合并癥等多重因素影響,未來需結合技術優(yōu)化與標準化流程,進一步提升治療的安全性與精準性,推動干細胞療法在腎病領域的臨床轉化。
相關閱讀:干細胞治療腎病的長期安全性如何?8年隨訪記錄告訴你答案
參考資料:
Perico, Norberto1; Remuzzi, Giuseppe1; Griffin, Matthew D.2; Cockwell, Paul3,4; Maxwell, Alexander P.5; Casiraghi, Federica1; Rubis, Nadia1; Peracchi, Tobia1; Villa, Alessandro1; Todeschini, Marta1; Carrara, Fabiola1; Magee, Bernadette A.6; Ruggenenti, Piero L.1,7; Rota, Stefano7; Cappelletti, Laura7; McInerney, Veronica2,8; Griffin, Tomás P.2; Islam, Md Nahidul2; Introna, Martino7; Pedrini, Olga7,9; Golay, Josée7; Finnerty, Andrew A.2,8,10; Smythe, Jon11; Fibbe, Willem E.12; Elliman, Stephen J.13; O’Brien, Timothy2; for the NEPHSTROM Trial Consortium. Safety and Preliminary Efficacy of Mesenchymal Stromal Cell (ORBCEL-M) Therapy in Diabetic Kidney Disease: A Randomized Clinical Trial (NEPHSTROM). Journal of the American Society of Nephrology 34(10):p 1733-1751, October 2023. | DOI: 10.1681/ASN.0000000000000189
Ohtake T, Sato T, Tsukiyama T, Muraoka S, Mitomo A, Maruyama H, Yamano M, Mochida Y, Ishioka K, Oka M, Moriya H, Hidaka S, Masuda H, Asahara T, Kobayashi S. Preliminary evidence of renal function improvement in chronic progressive kidney disease using autologous CD34+ cell therapy: A clinical trial. World J Stem Cells. 2024 Dec 26;16(12):1012-1021. doi: 10.4252/wjsc.v16.i12.1012. PMID: 39734483; PMCID: PMC11669983.
Hyeon Yu, Paul D. Sonntag, Peter R. Bream, Michael P. Lazarowicz, Francis S. Nowakowski, Gregory J. Woodhead, Charles T. Hennemeyer, Ryan D. Muller, Rakesh Navuluri, Elaine M. Caoili, Aaron C. Eifler, Brandon S. Tominna, Joseph M. Stavas,Safety and Feasibility of a Novel Percutaneous Locoregional Injection Technique of Renal Cellular Therapy for Chronic Kidney Disease of Diabetes,Kidney International Reports,Volume 6, Issue 9,2021,Pages 2486-2490,ISSN 2468-0249,https://doi.org/10.1016/j.ekir.2021.06.014.
Rahyussalim, A.J., Saleh, I., Kurniawati, T. et al. Improvement of renal function after human umbilical cord mesenchymal stem cell treatment on chronic renal failure and thoracic spinal cord entrapment: a case report. J Med Case Reports 11, 334 (2017). https://doi.org/10.1186/s13256-017-1489-7
免責說明:本文僅用于傳播科普知識,分享行業(yè)觀點,不構成任何臨床診斷建議!杭吉干細胞所發(fā)布的信息不能替代醫(yī)生或藥劑師的專業(yè)建議。如有版權等疑問,請隨時聯(lián)系我。



 掃碼添加微信
掃碼添加微信